

乳腺癌是导致全球女性癌症死亡的第二大原因[1]。乳腺癌是发生在乳腺上皮组织的恶性肿瘤,它是一种具有不同病理实体的异质性疾病,因此需要多种治疗措施。约10%~20%的浸润性乳腺癌是三阴性的肿瘤,其定义为缺乏雌激素受体、孕激素受体和人类表皮生长因子受体2 [2]。这种乳腺癌亚型与不良预后相关,并且与其他亚型相比,转移后的存活率更差。虽然相关研究开展多年,但由于缺乏有效的药物靶点,大部分三阴性乳腺癌患者依然不可治愈。再加上病患对现有药物的抗药性不断增强,促使人们必须寻找新的抗肿瘤药物及抗肿瘤辅助药物。中药抗肿瘤作用具有多靶点和多环节性的特征[3],同时中药抗肿瘤提取物还具有低毒性等优点。因此,具有抗肿瘤功能的中药材提取物的开发及利用,越来越受到人们的关注。
蒲公英(Taraxacum mongolicum Hand.-Mazz.),属于菊科,蒲公英属,多年生草本植物,具有极高的食用和药用价值,属于传统的中药材。近年来研究发现,蒲公英具有抗肿瘤、利胆、利尿、抗氧化、抗炎、保肝等特性[4]。报道显示,蒲公英在各种类型的恶性肿瘤中发挥着抗肿瘤作用,包括结直肠癌[5]、白血病[6]等。例如,蒲公英根提取物、根多糖等能诱导肿瘤细胞凋亡,抑制肿瘤细胞增殖,以及抑制肿瘤引起的炎症反应[7-8]。此外,蒲公英粗提物对人黑色素瘤细胞也具有一定的抑制作用[9]。但是,关于蒲公英根水提物对于三阴性乳腺癌细胞MDA-MB-231的影响还未见报道。因此,研究蒲公英根水提物促进三阴性乳腺癌细胞的凋亡具有重要意义。本文主要研究蒲公英根水提物对三阴性乳腺癌细胞的促凋亡作用,初步研究其促进三阴性乳腺癌细胞凋亡的分子机制,为后期活性成分的提取和新药开发提供实验依据和理论基础。
1 材料与方法 1.1 材料 1.1.1 细胞株人乳腺癌MDA-MB-231细胞、MDA-MB-436细胞、MCF-7细胞,以及人肝细胞L02,均购自上海中科院细胞库。
1.1.2 药物与试剂蒲公英采自徐州丰县田间,由专业人士鉴定;Alamar blue,美国Sigma公司;caspase-3、caspase-8、caspase-9、Bax、Bcl-2、p53、多聚ADP核糖聚合酶(poly ADP-ribose polymerase,PARP)、GAPDH抗体、caspase抑制剂,均购自美国Bioworld公司;PE Annexin V凋亡检测试剂盒,美国BD公司;细胞裂解液、DAPI试剂,均购自碧云天生物技术研究所;其余试剂均为国产分析纯。
1.1.3 仪器IBE2000显微镜(COIC公司);Leica DM 5000 B荧光显微镜(德国徕卡公司);CO2培养箱(日本三洋公司);SpectroMax M2荧光检测仪(Molecular Device公司);电泳仪及转膜仪(美国伯乐公司);超声波细胞破碎仪(美国SONICS公司);流式细胞仪(BD公司)。
1.2 方法 1.2.1 蒲公英水提物的制备将新鲜的蒲公英洗净后,晾干表面水分,取叶(包括叶柄)和根,分别置于家用榨汁机中榨成汁液,4 ℃、4 000 r·min-1离心30 min, 取上清液,于-80 ℃冰箱过夜冷冻,随后置于冷冻干燥机中冷冻干燥,用PBS配制成100 g·L-1的母液,用0.22 μm的无菌滤膜抽滤2次,然后用DMEM完全培养基稀释成不同浓度的蒲公英根水提物(0、1.5、3、7.5、15 g·L-1)。置于-20 ℃冰箱,备用。
1.2.2 细胞培养与体外抗肿瘤活性实验采用Alamar blue法,检测蒲公英根和叶水提物体外对正常细胞及肿瘤细胞的增殖抑制活性[10]。抑制率=(A对照-A样品)/(A对照-A空白)×100%,式中A对照代表阳性对照组的荧光值,A样品代表实验组的荧光值,A空白代表空白组的荧光值。
1.2.3 倒置显微镜观察细胞形态取对数生长期的MDA-MB-231细胞,用胰酶消化后,以2×108·L-1接种于6孔培养板,24 h细胞贴壁后,加入不同浓度的蒲公英根水提物(0、1.5、3、7.5、15 g·L-1)培养48 h后,用倒置显微镜观察形态并拍照。
1.2.4 DAPI染色分析细胞凋亡将MDA-MB-231细胞接种于6孔板中(2×108·L-1),待24 h细胞贴壁后,加入不同浓度蒲公英根水提物(0、1.5、3、7.5、15 g·L-1)处理。在5% CO2、37 ℃细胞培养箱中培养48 h后,4 000 r·min-1离心5 min收集细胞,用PBS重悬细胞,4 000 r·min-1离心5 min,去除PBS,向清洗后的细胞中每组加入1 mL 4%多聚甲醛,室温固定10 min,4 000 r·min-1离心5 min,去除多聚甲醛,再用PBS重悬细胞,4 000 r·min-1离心5 min,清洗4次,去除PBS后,再加入100 μL DAPI染色液轻轻吹匀,室温避光孵育10 min。去除DAPI染色液,用PBS洗涤3次,每次5 min。最后在荧光显微镜下观察并拍照。
1.2.5 流式细胞术检测MDA-MB-231细胞的凋亡实验步骤参照PE Annexin V凋亡检测试剂盒说明书。收集经过蒲公英根水提物(0、1.5、3、7.5、15 g·L-1)处理48 h的MDA-MB-231细胞,2 000 r·min-1离心5 min,弃上清,用冷PBS重悬细胞,2 000 r·min-1离心5 min,弃上清,然后以每100 μL含1×105个细胞的浓度重悬于Annexin V结合缓冲液中,再加入5 μL PE Annexin V和5 μL 7-AAD。轻轻重悬细胞,在室温(25 ℃)避光孵育15 min。最后向细胞悬液中加入400 μL Annexin V结合缓冲液。1 h内通过流式细胞仪检测。
1.2.6 Western blot检测凋亡相关蛋白的表达不同浓度的蒲公英根水提物(0、1.5、3、7.5、15 g·L-1)处理MDA-MB-231细胞48 h后,去除培养基,每孔加入2 mL PBS洗涤细胞,并转移至1.5 mL的离心管中,2 000 r·min-1离心10 min,弃上清,每孔加入100 μL细胞裂解液RIPA(含PMSF),冰上放置30 min,每隔10 min混匀1次,使细胞充分裂解。12 000 r·min-1离心30 min,取上清,-80 ℃保存备用。SDS-PAGE电泳,电泳结束后,将蛋白转移到PVDF膜上,5%脱脂奶粉封闭2 h,一抗(1:1 000)4 ℃封闭过夜,TBST清洗4次,每次5 min;二抗(1:1 000)封闭2 h,TBST清洗4次,每次5 min,利用化学发光系统进行显色拍照。
1.2.7 caspase-3、caspase-8和caspase-9抑制剂对蒲公英根水提物抗肿瘤活性的影响将MDA-MB-231细胞接种于96孔细胞培养板中,待24 h细胞贴壁后,加入100 μL 20 μmol·L-1 caspase-3抑制剂(Ac-DEVD-CHO)、caspas-8抑制剂(Z-IETD-FMK)和caspase-9抑制剂(Z-LEHD-FMK)孵育2 h后,加入100 μL不同浓度的蒲公英根水提物继续孵育48 h,Alamar blue法检测细胞活性。
1.2.8 统计学分析实验数据采用SPSS 16.0统计软件进行统计学处理,数据用x±s表示, 组间比较采用One-way ANOVA检验。
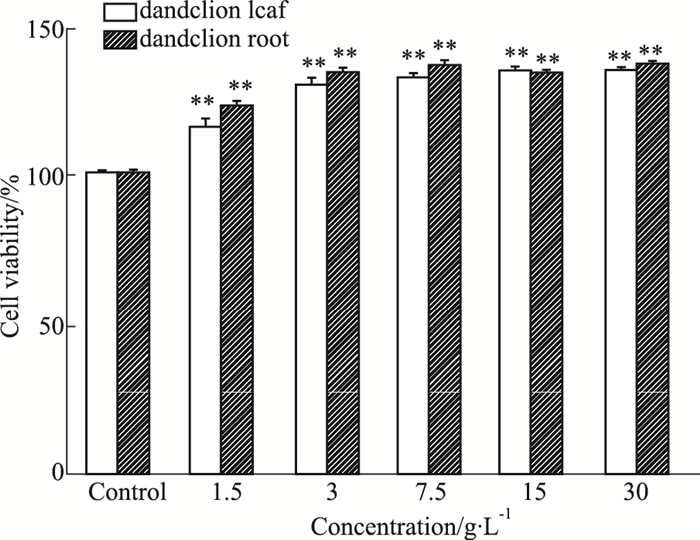
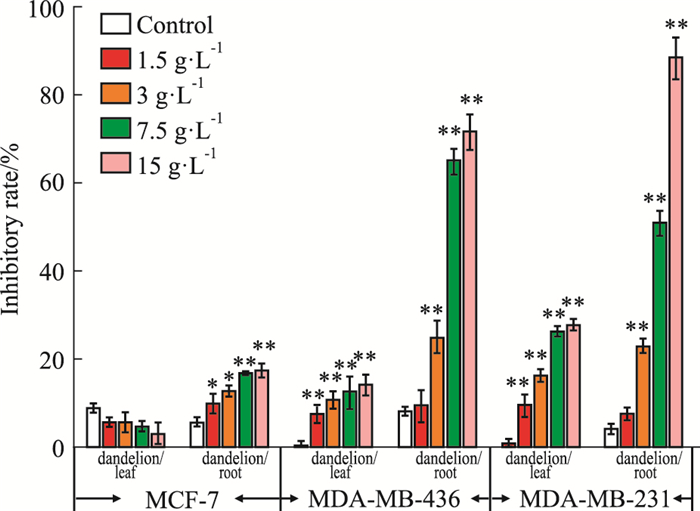
2 结果 2.1 蒲公英各部位水提物体外对正常细胞及乳腺癌细胞增殖的影响如Fig 1、2所示,不同浓度的蒲公英根和叶水提物0、1.5、3、7.5、15 g·L-1作用于人正常肝细胞L02和各乳腺癌细胞48 h后,对正常细胞的生长没有明显的抑制作用,但高浓度的蒲公英根水提物对人三阴性乳腺癌细胞MDA-MB-231和MDA-MB-436的生长具有明显的抑制作用,尤其是对MDA-MB-231细胞的抑制作用最为明显,且呈现一定的浓度依赖关系。接下来,选取MDA-MB-231细胞进行有关蒲公英根水提物影响三阴性乳腺癌细胞生长和活性的分子机制研究。
|
| Fig 1 Effect of water extracts from various parts of dandelion on viability of L02 cells (x±s, n=3) **P < 0.01 vs control |
|
| Fig 2 Inhibitory effect of water extracts from various parts of dandelion on proliferation of three different breast cancer cells (x±s, n=3) *P < 0.05, **P < 0.01 vs control |
不同浓度的蒲公英根水提物处理细胞48 h后,对照组生长状态良好、贴壁较牢固,且细胞间紧密相连。随着蒲公英根水提物浓度的增加,细胞间距逐渐变大,贴壁能力逐渐下降,部分细胞变圆、脱落,但细胞膜依然完整(Fig 3)。结果表明,蒲公英根水提物能够促进MDA- MB-231细胞凋亡。

|
| Fig 3 The cell morphology of MDA-MB-231 cells treated with water extract of dandelion root |
将不同浓度的蒲公英根水提物处理过的MDA-MB-231细胞,进行DAPI染色分析。如Fig 4所示,对照组细胞核形完整、大小均一,染色质比较均匀。随着蒲公英根水提物浓度的增加,细胞核逐渐解体,破裂成碎片,形成很多颗粒状物质。结果表明,随着蒲公英根水提物浓度的增加,细胞凋亡数量也逐渐增多。

|
| Fig 4 DAPI staining of apoptosis of MDA-MB-231 cells induced by water extract of dandelion root (×400) |
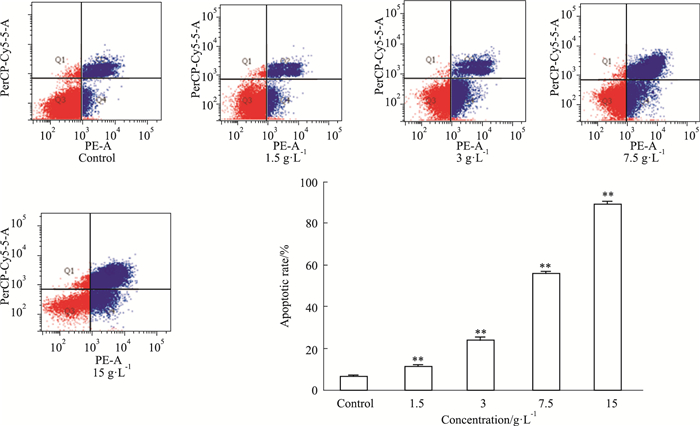
采用Annexin V-FITC/PI双染,通过流式细胞术检测MDA-MB-231细胞的凋亡情况。如Fig 5所示,阴性对照组和不同浓度蒲公英根水提物处理细胞48 h后,MDA-MB-231细胞的凋亡率随着蒲公英根水提物浓度的增加而明显增加。当蒲公英根水提物浓度达到15 g·L-1时,MDA-MB-231细胞的凋亡率约达到85%。该结果与DAPI荧光染色结果相一致,说明蒲公英根水提物确实能够促进MDA-MB-231细胞的凋亡,为今后新药的开发提供了一定的实验依据。
|
| Fig 5 Effect of water extract of dandelion root on cell apoptosis of MDA-MB-231 cells by flow cytometry (x±s, n=3) *P < 0.05, **P < 0.01 vs control |
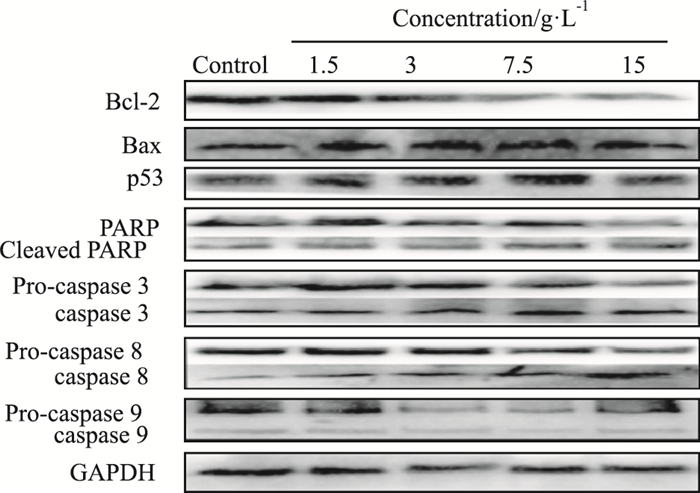
不同浓度蒲公英根水提物处理MDA-MB-231细胞48 h后,Fig 6的Western blot结果显示,细胞凋亡的末端效应蛋白酶cleaved PARP、cleaved caspase-3、cleaved caspase-8和cleaved caspase-9的蛋白水平随蒲公英根水提物浓度的增加而增加,同时促进凋亡相关蛋白(Bax、p53)的表达量也逐渐升高;而抑制凋亡蛋白Bcl-2的表达明显受到蒲公英根水提物的抑制,均呈明显的浓度依赖性。提示蒲公英根水提物可能是通过外源性细胞凋亡途径和内源性线粒体凋亡途径,共同作用于MDA-MB-231细胞,并诱发细胞凋亡。
|
| Fig 6 The protein expression of apoptosis-related factor in MDA-MB-231 cells treated with different concentrations of water extract of dandelion root |
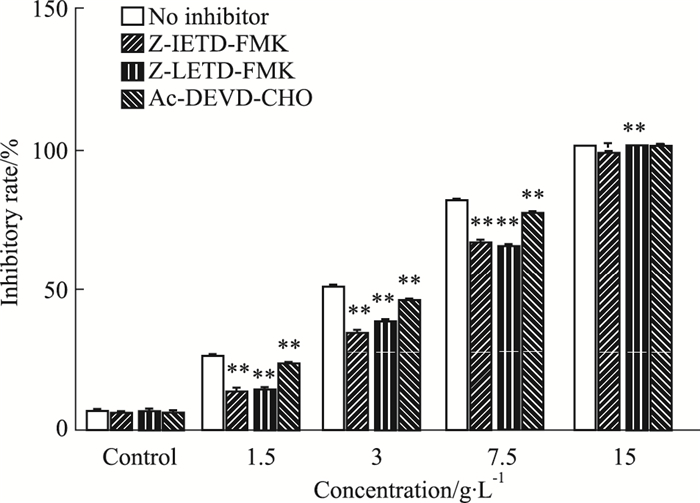
如Fig 7所示,caspase-8抑制剂Z-IETD-FMK、caspase-9抑制剂Z-LEHD-FMK和caspase-3抑制剂Ac-DEVD-CHO在蒲公英根水提物浓度为7.5 g·L-1以下时,能够明显提高各处理组中MDA-MB-231细胞的活性;在蒲公英根水提物浓度为15 g·L-1时,逆转细胞损伤效率较弱,可能是细胞在该浓度下发生了不可逆性损伤。
|
| Fig 7 Effect of caspase inhibitors on apoptosis induced by water extract of dandelion root (x±s, n=3) **P < 0.01 vs control |
蒲公英长期以来作为我国民间药食同源的植物,国内外大量实验都揭示了其广泛的药理作用,为后续的深入开发奠定了良好基础。之前有研究发现,蒲公英能够有效抑制肝癌细胞的增殖[11]。本文研究发现,蒲公英根水提物对三阴性乳腺癌细胞MDA-MB-231具有明显的抑制作用,且呈现一定的浓度依赖关系,这种现象可能与根部的某些化学成分有关。
本研究通过光学显微镜、DAPI荧光染色、流式细胞术均证实,蒲公英根水提物处理MDA-MB-231细胞后,均出现明显的凋亡现象。caspase-3的活化是诱导细胞凋亡的关键核心步骤,caspase-3的活化又离不开其上游因子caspase-8或caspase-9的激活。PARP是DNA修复酶,在细胞修复与凋亡的调控中起重要作用,是caspase-3的底物之一,可以被活化的caspase-3切割分解而失活,从而促使细胞凋亡[12]。Western blot结果显示,蒲公英根水提物处理MDA-MB-231细胞后,随着浓度的增加,caspase-3、caspase-8和caspase-9的活性明显增加。另一方面,线粒体在细胞凋亡中也处于重要位置,蒲公英根水提物抑制了线粒体膜上抗凋亡蛋白Bcl-2的表达,从而使Bcl-2/Bax的比值明显降低。它们都能阻止或促进线粒体内细胞色素C的释放,进而引发caspase级联反应,诱导细胞凋亡[13-14]。之前研究表明,活化的p53可以调节Bcl-2家族蛋白的表达[15]。本研究中,蒲公英根水提物处理MDA-MB-231细胞后,p53的含量也明显增加,这可能与p53在蒲公英根水提物诱导MDA-MB-231细胞凋亡过程中,是通过Bcl-2家族蛋白起作用有关。为了进一步验证蒲公英根水提物诱导MDA-MB-231细胞凋亡的信号通路,采用caspase抑制剂(Z-IETD-FMK、Z-LEHD-FMK、Ac-DEVD-CHO)处理细胞,结果显示,caspase抑制剂能够在一定程度上逆转蒲公英根水提物诱导MDA-MB-231细胞凋亡的作用。
综上所述,蒲公英根水提物对正常细胞几乎没有不利影响,而对三阴性乳腺癌细胞MDA-MB-231的生长具有明显的抑制作用,并能够促进MDA-MB-231细胞凋亡,为后期活性成分的提取和新药开发提供了实验依据和理论基础。
| [1] |
Torre L A, Bray F, Siegel R L, et al. Global cancer statistic, 2012[J]. CA Cancer J Clin, 2015, 65(2): 87-108. doi:10.3322/caac.21262 |
| [2] |
Kumar P, Aggarwal R. An overview of triple-negative breast cancer[J]. Arch Gynecol Obstet, 2016, 293(2): 247-69. doi:10.1007/s00404-015-3859-y |
| [3] |
胡人杰. 中药方剂抗肿瘤作用的药理学研究进展——动物模型建立与评价指标的选择[J]. 亚太传统医药, 2014, 10(5): 59-63. Hu R J. Advances in pharmacological research on antitumor effects of traditional chinese medicine formulas——selection of animal models and evaluation indexes[J]. Asia-Pacific Tradit Med, 2014, 10(5): 59-63. |
| [4] |
Mingarro D M, Plaza A, Galán A, et al. The effect of five Taraxacum species on in vitro and in vivo antioxidant and antiproliferative activity[J]. Food Funct, 2015, 6(8): 2787-2793. doi:10.1039/C5FO00645G |
| [5] |
Ovadje P, Ammar S, Guerrero J A, et al. Dandelion root extract affects colorectal cancer proliferation and survival through the activation of multiple death signalling pathways[J]. Oncotarget, 2016, 7(45): 73080-100. |
| [6] |
Ovadje P, Hamm C, Pandey S. Efficient induction of extrinsic cell death by Dandelion root extract in human chronic myelomonocytic leukemia (CMML) cells[J]. PLoS One, 2012, 7(2): e30604. doi:10.1371/journal.pone.0030604 |
| [7] |
Chungmu P, Hyunjoo Y, Chang H K, et al. TOP1 and 2, polysaccharides from Taraxacum officinale, attenuate CCl4-induced hepatic damage through the modulation of NF-κB and its regulatory mediators[J]. Food Chem Toxicol, 2010, 48(5): 1255-61. doi:10.1016/j.fct.2010.02.019 |
| [8] |
Jeon H J, Kang H J, Jung H J, et al. Anti-inflammatory activity oftaraxacum officinale[J]. J Ethnopharmacol, 2008, 115(1): 82-8. doi:10.1016/j.jep.2007.09.006 |
| [9] |
Hudec J, Burdová M, Kobida L, et al. Antioxidant capacity changes and phenolic profile of Echinacea purpurea, nettle (Urtica dioica L.), and dandelion (Taraxacum officinale) after application of polyamine and phenolic biosynthesis regulators[J]. J Agric Food Chem, 2007, 55(14): 5689-96. doi:10.1021/jf070777c |
| [10] |
Yang S, Liu J, Chen Y, et al. Reversal effect of Tween-20 on multidrug resistance in tumor cells in vitro[J]. Biomed Pharmacother, 2012, 66(3): 187-94. doi:10.1016/j.biopha.2011.10.007 |
| [11] |
Koo H N, Hong S H, Song B K, et al. Taraxacum officinale induces cytotoxicity through TNF-alpha and IL-1alpha secretion in HepG2 cells[J]. Life Sci, 2004, 74(9): 1149-57. doi:10.1016/j.lfs.2003.07.030 |
| [12] |
王婷婷, 赵丽, 李晓丹, 等. 胡黄连苷Ⅱ对脑缺血损伤后神经细胞凋亡和超微结构的影响[J]. 中国药理学通报, 2015, 31(3): 400-6. Wang T T, Zhao L, Li X D, et al. Effect of picroside Ⅱ on neuronal apoptosis and ultrastructure in cerebral ischemic injury in rats[J]. Chin Pharmacol Bull, 2015, 31(3): 400-6. doi:10.3969/j.issn.1001-1978.2015.03.021 |
| [13] |
张红艳, 翟丽, 王婷婷, 等. 胡黄连苷Ⅱ通过抑制cyto C/caspase-9/caspase-3通路发挥神经保护作用[J]. 中国药理学通报, 2017, 33(5): 668-74. Zhang H Y, Zhai L, Wang T T, et al. Picroside Ⅱ plays a neuroprotective effect by inhibiting cyto C/caspase-9/caspase-3 signal pathway following ischemia/reperfusion injury in rats[J]. Chin Pharmacol Bull, 2017, 33(5): 668-74. doi:10.3969/j.issn.1001-1978.2017.05.016 |
| [14] |
张贝贝, 刘文洪, 李俊峰, 叶志青. 铁皮石斛多糖对高糖诱导的血管内皮细胞Bax、Bcl-2表达的影响[J]. 中国药理学通报, 2015, 31(1): 64-70. Zhang B B, Liu W H, Li J F, Ye Z Q. Effects of Dendrobium candidum polysaccharide on the expression of Bax and Bcl-2 in vascular endothelial cells induced by high glucose[J]. Chin Pharmacol Bull, 2015, 31(1): 64-70. doi:10.3969/j.issn.1001-1978.2015.01.015 |
| [15] |
Schuler M, Green D R. Mechanisms of p53-dependent apoptosis[J]. Biochem Soc Trans, 2001, 29(6): 684-8. doi:10.1042/bst0290684 |

