铁皮石斛(Dendrobium officinale Kimura et Migo,DOP)是我国传统名贵中药材,具有益胃生津、滋阴清热等功效,多糖是其主要活性成分[1]。研究发现,铁皮石斛多糖体外能促进脾细胞增殖,增加自然杀伤性细胞和巨噬细胞活性[2];体内具有免疫调节活性,且不同分子量的多糖具有不同的免疫调节活性[3],促进干燥症病人唾液分泌[4],促进毛发生长[5]等作用。有文献报道,铁皮石斛多糖对高糖诱导的血管内皮细胞NF-κB因子的过量表达有较好的抑制作用,提示其可能对糖尿病血管病变具有保护作用[6]。
糖尿病对机体的危害源于糖尿病并发症,尤其是糖尿病血管并发症[7],糖尿病血管并发症是人类致死、致残的重要原因。内皮细胞受损被认为是血管病变的首要步骤。近年来国内外研究都证实高糖可以诱导内皮细胞凋亡[8],促发活性氧自由基(ROS)的生成[9],影响Bax,Bcl-2等基因表达,诱导细胞凋亡[10]。
铁皮石斛的市场需求持续旺盛,但其野生资源有限,加之铁皮石斛生活环境不断遭受破坏,导致铁皮石斛野生资源濒临灭绝,无法满足市场需求。因此,提高铁皮石斛多糖提取率,充分利用现有的药材,是值得关注的,故本试验采用响应曲面法探讨铁皮石斛多糖的最佳提取工艺条件,以期从工艺上提高药材的使用效率。同时,铁皮石斛已经成为一种广受关注的保健用品,探讨其对一些疾病,尤其是慢性病的作用机制具有较好的研究价值,实验采用细胞培养及分子生物学技术,研究铁皮石斛多糖对高糖诱导的人脐静脉血管内皮细胞增殖的影响及其Bax、Bcl-2的表达干预情况,从体外实验的角度探讨铁皮石斛多糖防治糖尿病血管病变的机制。
1 材料与方法 1.1 材料铁皮石斛原球茎,由浙江中医药大学生命科学学院提供;人脐静脉内皮细胞系HUVEC由浙江中医药大学生物与制药工程实验中心惠赠。
1.2 主要试剂葡萄糖、苯酚、浓硫酸、DMEM高糖培养基(Gibco,批号:H2387)、胰蛋白酶(1 ∶ 250,Gibco,批号:2750018)、胎牛血清(杭州四季青公司)、TRIzol(Invitrogen公司)、RT-PCR试剂盒(北京鼎国昌盛生物技术有限责任公司)。其余试剂为国产分析纯。
1.3 实验分组共分6组。A组(空白组):新鲜DMEM培养基;B组(高糖刺激组):新鲜DMEM培养液+葡萄糖22 mmol·L-1;C组(正常血糖组):新鲜DMEM培养液+葡萄糖5.6 mmol·L-1;D组(铁皮石斛多糖低剂量组):含50 mg·L-1铁皮石斛多糖的DMEM培养液+葡萄糖22 mmol·L-1;E组(铁皮石斛多糖中剂量组):含300 mg·L-1铁皮石斛多糖的的DMEM培养液+葡萄糖22 mmol·L-1;F组(铁皮石斛多糖高剂量组):含500 mg·L-1铁皮石斛多糖的DMEM培养液+葡萄糖22 mmol·L-1。
1.4 铁皮石斛多糖的提取的工艺优化 1.4.1 多糖标准曲线的制定采用苯酚-硫酸法[11]测定多糖。精密量取对照品溶液(0.6 g·L-1)0.5、1.0、1.5、2.0、2.5 mL,分别置50 mL容量瓶中,各加水至刻度,摇匀。分别精密量取上述溶液2 mL,置具塞试管中,各加4%苯酚溶液1 mL,混匀,迅速加入硫酸7.0 mL,摇匀,置40℃水浴中保温30 min,取出后置冰水浴中放置5 min,取出,以相应试剂为空白。照分光光度法,在490 nm的波长处测定吸光度,以吸光度为纵坐标,浓度为横坐标,绘制标准曲线(Fig1)。

|
| Fig 1 Standard curve of polysaccharides |
采用绘制标准法相同的方法,根据多糖标准曲线得出供试品溶液中铁皮石斛多糖的重量(mg),计算提取率。多糖提取率按下式计算:多糖提取率/%=多糖含量/药材质量×100%。
1.4.3 工艺流程原球茎60 ℃烘干→粉碎→热水浸提→离心→浓缩→85%乙醇沉淀→离心分离→沉淀物无水乙醇抽洗3次,乙醚抽洗2次→铁皮石斛原球茎多糖→水溶解→Sevage法去蛋白→再用85%乙醇沉淀为粗品多糖。
1.4.4 单因素试验以多糖提取的初始工艺为基础(液料比10 ∶ 1,提取时间为3 h,提取次数3次),以铁皮石斛多糖提取率为指标分别考察提取时间、提取次数、液料比3个因素对铁皮石斛多糖提取的影响,每个因素设定5个梯度,各因素水平如下:液料比为5 ∶ 1、10 ∶ 1、15 ∶ 1、20 ∶ 1、25 ∶ 1,提取时间为1、2、3、4、5 h,提取次数为1、2、3、4、5次。分析各因素对铁皮石斛多糖提取的影响,确定影响因素水平。
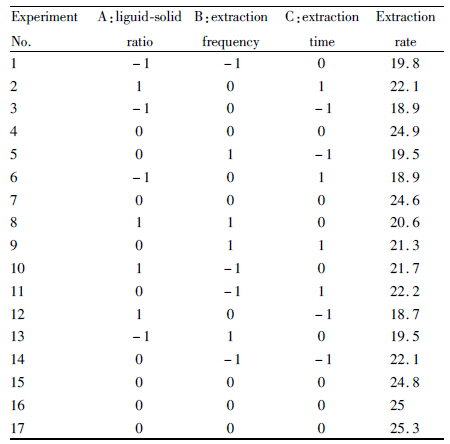
1.4.5 响应面法优化提取工艺根据中心组合实验设计原理,综合单因素试验所得结果,选取液料比、提取时间、提取次数3个对多糖提取率影响显著的因素,采用三因素三水平的响应面分析方法优化铁皮石斛多糖提取工艺(Tab1)。并利用统计软件design-expert对试验数据进行回归分析,预测铁皮石斛多糖提取的最佳工艺参数)。
取指数生长期1×108·L-1细胞接种于96孔细胞培养板中,待细胞融合度达85%以上,A和B对照组及C、D、E、F铁皮石斛多糖处理组,加入相应剂量的铁皮石斛多糖,每个实验组设置6个平行孔。培养24或48 h后,将带有药物的培养液移除,加入MTT作用4 h后,吸出MTT,加入DMSO震荡10 min,测570 nm波长处吸光度(A)值,按照以下公式计算细胞增殖抑制率:细胞增殖抑制率/%=(1-处理组OD570值/空白对照组OD570值)×100%。
1.6 RT-PCR法检测Bax、Bcl-2 mRNA的表达 1.6.1 细胞总RNA的提取收集刺激后的细胞,用PBS洗2次,加入1 mL TRIzol,反复吹打,室温孵育5 min后,转移至1.5 mL离心管中,加入200 μL氯仿,大力摇晃15 s,冰上孵育5 min,4 ℃,12 000 r·min-1离心15 min(下同)。将上相转移至另1.5 mL离心管中,加入500 μL异丙醇,振荡混匀后室温孵育10 min,12 000 r·min-1离心15 min,弃上清。加入1 mL 75%乙醇,振荡混匀,12 000 r·min-1离心15 min,弃去上清。自然干燥5~10 min,加入适量0.1% DEPC水,-80℃保存备用。
1.6.2 RT-PCRβ-actin、Bcl-2和Bax基因引物均根据Primer 5.0引物设计软件自行设计,再由上海生物工程公司合成:β-actin F:5′- TCCTGGGTGAGTGGAGACTG-3′;R:5′-ATGCCTGAGAGGGAAATGAGG-3′,扩增产物大小为105 bp。Bcl-2 F:5′- GAAGCACAGATGGTTGATGG-3′;R:5′-CAGCCTCACAAGGTTCCAAT-3′,扩增产物大小为496 bp。Bax F:5 ′-CACAACTCAGCGCAAACATT-3′;R:5′-ACAGCCATCTCTCTCCATGC-3′,扩增产物大小为519 bp。
cDNA合成体系(30 μL):15 μL细胞总RNA,5×RT Buffer 6 μL,dNTP Mixture(10 mmol·L-1)3 μL,Oligo-dT 1.5 μL,RNase inhibitor(40 U/μL)1.5 μL,AMV Reverse Transcriptase 1.5 μL,RNase free H2O 1.5 μL。反应条件:室温放置10 min,55 ℃45 min,95 ℃ 5 min,冰浴5 min。
PCR扩增体系(50 μL):cDNA2 μL,Premix Taq (LA TaqVersion 2.0) 25 μL,Bcl-2F、Bcl-2R、β-actinF、β-actinR各1 μL(浓度均为20 nmol·L-1),无菌水21 μL。反应条件:95 ℃ 2 min,95 ℃ 30 s,52 ℃ 30 s,72 ℃ 30 s,36个循环,72 ℃ 10 min,4 ℃ 5min。Bax基因扩增条件同Bcl-2,退火温度改为54 ℃。1%琼脂糖凝胶电泳检测PCR扩增产物,使用凝胶图像分析软件测定目的条带和β-actin的灰度值,以两者的比值表示RT-PCR目的产物的相对表达量。
1.7 统计学处理灰度值分析采用Image J2x软件,数据处理应用SPSS15.0统计软件,数据采用 ± s表示。RT-PCR数据,采用方差分析作统计学检验。
± s表示。RT-PCR数据,采用方差分析作统计学检验。
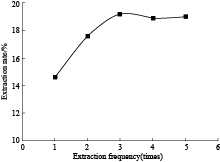
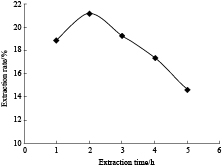
实验结果显示,铁皮石斛多糖随着各因素的变化而变化,提取次数大于3次以后,多糖提取率基本保持不变(Fig2);铁皮石斛多糖提取率随着液料比的增加而增加,当液料比大于15 ∶ 1时,多糖提取率反而下降(Fig3);提取时间为2.0 h时,提取率最大,此后,不增反减(Fig4)。实验结果说明,提取次数为3次,液料比为15 ∶ 1,提取时间为2.0 h是铁皮石斛多糖提取的最佳工艺水平。
|
| Fig 2 Impact of extraction frequency on extraction of DOP |

|
| Fig 3 Impact of solid-liquid ratio on extraction of DOP |
|
| Fig 4 Impact of extraction time on extraction of DOP |
对铁皮石斛多糖提取工艺的结果进行响应面分析,采用Design-Expert 8.0.6软件对对铁皮石斛多糖提取工艺的结果进行多元回归拟合,可得铁皮石斛多糖提取率化率(Y)对液料比(A)、提取时间(B)、提取次数(C)的二元多次回归模型为:Y=24.92+0.75A-0.61B+0.66C-0.20AB+0.85AC+0.43BC-3.07A2-1.45B2-2.20C2
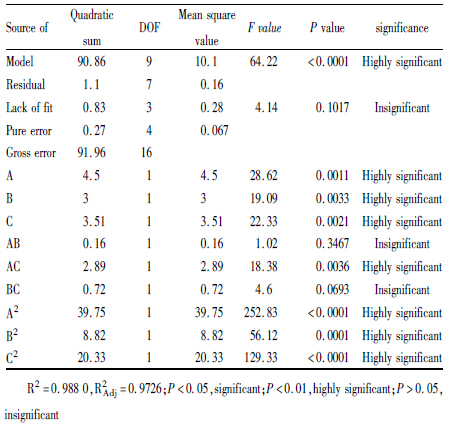
由Tab3可以看出:失拟项P=0.101 7>0.05,模型的P<0.0001,表明二次多元回归模型回归效果差异有统计学意义,不同处理之间的差异极大;软件分析的复相关系数R2=0.988 0,校正后的R2Adj=0.972 6,说明此模型与实际试验拟合较好,实验误差较小,因此可用该模型来分析和预测铁皮石斛多糖的提取率。对模型回归方程系数的显著性实验表明,一次项A、B、C差异有统计学意义;二次项全部影响极显著;交互项AC的P值大于0.001,差异有统计学意义,交互项AB和BC大于0.05,差异有统计学意义。可见,实验各因素铁皮石斛多糖提取率的影响不是简单的线性关系,影响铁皮石斛多糖提取率的主要因素次序是A>C>B。(Tab3)
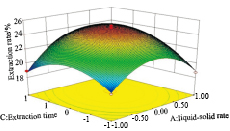
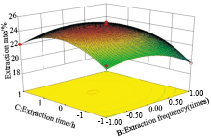
根据以上得到的回归方程来绘制分析图,考察所拟合的响应曲面的形状,Fig5、6、7直观地给出各个因素交互作用的响应面的3D图。图的分析结果表明,液料比和提取时间锌之间的交互关系非常明显,表现为曲面较陡,等高线为椭圆形(Fig6);液料比和提取次数、提取次数和提取时间交互关系差异无统计学意义,表现为曲面平缓,等高线为圆形(Fig5、7)。这与方差分析结果一致。从响应面图可以看出此试验模型都能够达到极值点。

|
| Fig 5 Effect of liquid-solid ration and extraction times on yield of DOP |
|
| Fig 6 Effect of liquid-solid ration and extraction time on yield of DOP |
|
| Fig 7 Effect of extraction times and extraction time on yield of DOP |
通过回归模型预测的铁皮石斛多糖提取的最佳工艺条件为:液料比15.75,提取次数为2.8次,提取时间为2 h在此条件下,多糖提取率理论上可达25.1%。在响应面分析法求得的最佳条件下对铁皮石斛多糖提取3次,多糖提取率平均为24.9%,验证值与回归方程所预测值相吻合得很好,验证了此响应面分析方法的可行性。
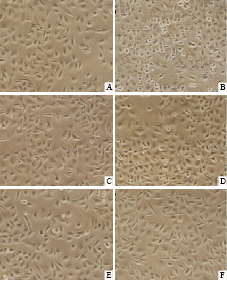
2.3 不同浓度的铁皮石斛多糖对细胞形态的影响作用24 h后,不同给药组细胞完全贴壁。在倒置显微镜下观察,发现A和C组细胞正常生长,为短梭形或扁平多角形(Fig8A、C);B组细胞变圆,丧失原有的细胞形态,变得不均一,排列不规则,出现大量的细胞凋亡现象(Fig8B);随着铁皮石斛多糖浓度的增加,HUVEC细胞形态逐渐恢复。D组细胞变圆,但是细胞凋亡较少(Fig8D),E组总体细胞形态规则,趋向于正常细胞,但仍有少数的不规则圆形细胞(Fig8E);F组细胞轮廓清楚,细胞与正常组细胞无差异(Fig8F)。实验结果说明,高糖诱导下,铁皮石斛多糖能够促进细胞的生长,抑制细胞的凋亡。
|
| Fig 8 The growth condition of different administration groups of cells A:blank control B:high sugar stimulation C:normal blood sugar D:low dose drug E:middle dose drug F:high dose drug. |
实验结果显示,不同浓度铁皮石斛多糖作用于HUVEC细胞24 h和48 h后,与正常血糖组A相比,B组细胞明显受到抑制,差异有显著性(P<0.01);同一时间,不同浓度处理组之间差异有统计学意义(P<0.05或P<0.01),且随着剂量的增加,抑制率降低;同一浓度,随作用时间延长,抑制率升高(Tab4)。实验结果说明,通过高糖诱导,铁皮石斛多糖呈剂量依赖性抑制HUVEC细胞的凋亡,时间依赖性促进细胞的凋亡。
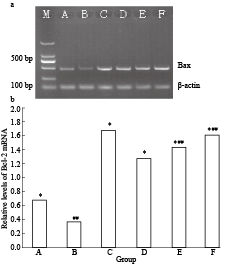
不同浓度的铁皮石斛多糖处理刺激HUVEC 24 h后,实验结果显示,与空白对照组和正常血糖组比较,高糖刺激组Bcl-2 mRNA表达量降低;高糖(22 mmol·L-1)诱导下,Bcl-2 mRNA表达量随着铁皮石斛的浓度增加而增加(Fig9-a)。条带的灰度值统计学分析结果显示,与B组比较,A、C组Bcl-2/β-actin灰度比值降低,不同剂量的多糖组Bcl-2/β-actin灰度比值,差异均有统计学意义(P<0.05);随着铁皮石斛多糖的铁皮石斛多糖浓度增加,Bcl-2/β-actin灰度比值逐渐增大,差异有统计学意义(P<0.05)(Fig9-b)。实验结果表明,高糖诱导下,铁皮石斛多糖能够抑制人脐静脉内皮细胞的凋亡,铁皮石斛多糖提取液对Bcl-2 mRNA表达上调作用存在剂量依赖关系。
|
| Fig 9 Effects of each group on expression of BCL-2 mRNA induced by high sugar M:2.0 kb marker;A:blank control B:high sugar stimulation C:normal blood sugar;D:low dose drug E:middle dose drug F:high dose drug.*P<0.05 vs B;##P<0.01 vs D. |
实验结果显示高糖(22 mmol·L-1)刺激HUVEC 24 h后,可增加Bax mRNA表达量,而在铁皮石斛多糖的作用下,可抑制高糖诱导的Bax mRNA表达,且随着铁皮石斛活性成分浓度的增加,抑制作用增强(Fig10A)。条带的灰度值统计学分析结果显示,与B组比较,A和C组Bax/β-actin灰度比值降低,铁皮石斛低、中和高剂量组Bax/β-actin灰度比值降低,差异均有统计学意义(P<0.05);与D组比较,Bax/β-actin灰度比值逐渐降低,差异均有显著性(P<0.05)(图10B)。实验结果表明,高糖诱导下,铁皮石斛多糖能够抑制人脐静脉内皮细胞的凋亡,铁皮石斛多糖提取液对Bax mRNA表达下调作用存在剂量依赖关系。

|
| Fig 10 Effects of each group on expression of Bax mRNA in HUNEC induced by high sugar M:2.0 kb marker;A:blank control B:high sugar stimulation C:normal blood sugar;D:low dose drug E:middle dose drug F:high dose drug.**P<0.01 vs B;##P<0.01 vs D. |
铁皮石斛是珍贵的药用植物,早在上世纪80年代野生铁皮石斛被国家列为重点保护的珍惜濒危药用植物,具有极高的药用价值。铁皮石斛能够保持胃张力,提高生产的体液和缓解症状(如喉咙干渴与视力模糊干涩[12])。现代临床和药理研究证明,铁皮石斛具有抗衰老、抗肿瘤、降低血糖和提高免疫 等作用,对恶性肿瘤的辅助治疗,对慢性胃炎、糖尿病、慢性咽炎和久病体虚免疫功能低下等方面都有广泛的应用[13]。铁皮石斛主要活性成分多糖具有明显的抗肿瘤活性和免疫调节功能,研究表明,多糖类物质不仅能够提高免疫系统功能,而且具有较好的抗癌[14]、抗氧化[15]等生物活性。
实验通过单因素和响应面优化铁皮石斛多糖的提取工艺,实验发现,当提取次数为2.8次,液料比15.75 ∶ 1,提取时间2 h时,铁皮石斛的提取率达到最大,此时提取率为25.1%,影响铁皮石斛多糖提取的因素顺序依次为:液料比>提取次数>提取时间;体外细胞培养观察和细胞活性的检测结果说明,铁皮石斛多糖呈剂量依赖性抑制HUVEC的凋亡,时间依赖性促进细胞的凋亡,而在高糖诱导下,铁皮石斛多糖促进细胞增殖,抑制细胞的凋亡;RT-PCR结果发现,当药物刺激作用24 h时,铁皮石斛多糖可以不同程度的抑制高糖诱导的Bax基因表达,增强Bcl-2基因表达,并呈剂量依赖性。研究结果说明,铁皮石斛提取物可能从基因水平抑制高糖诱导的人脐静脉内皮细胞Bax mRNA表达,增强Bcl-2 mRNA表达,抑制血管内皮细胞凋亡,这可为铁皮石斛及其活性物质在临床应用及产品开发提供实验依据,为防治糖尿病血管病变提供参考。
| [1] | 国家药典委员会.中华人民共和国药典[M].一部.北京:中国医药科技出版社,2010:265.Chinese Pharmacopoeia Commission.Pharmacopoeia of the People's Republic of China[M].Part1.Beijing:the medicine science and technology press of China,2010:265. |
| [2] | Xia L J,Liu X F,Guo H Y,et al.Partial character-ization and immunomodulatory activity of polysaccharides from the stem of Dendrobium officinale in vitro[J].J Funct Foods,2012,4:294. |
| [3] | 刘亚娟,王诗豪,张铭.铁皮石斛多糖抗癌及免疫活性研究[J].广州化工,2014,42(10):58-65.Liu Y J,Wang S H,Zhang M.Study on immune and antitumor activity of dendrobium officinale polysaccharides[J].Guangzhou Chem Ind,2014,42(10):58-65. |
| [4] | Lin X,Tzi B N,Yi B F.Dendrobium candidum extract increases the expression of aquaporin-5 in labia glands from patients with Sjgren′s syndrome[J].Phytomedicine,2011,18:194-8. |
| [5] | 陈健,戚辉,李金标,等.铁皮石斛多糖促进毛发生长的实验研究[J].中国中药杂志,2014,39(2):291-4.Chen J,Qi H,Li J B,et al.Experimental study on Dendrobium candidum polysaccharides on promotion of hair growth[J].China J Chin Mat Med,2014,39(2):291-4. |
| [6] | 陈泳荪,刘文洪.铁皮石斛多糖提取工艺及其对高糖诱导血管内皮细胞NF-κB表达干预的研究[J].山西中医学院学报,2011,12(2):28.Chen Y S,Liu W H.Optimal extraction procedure of polysaccharides from candidum dendrobium and effects of polysaccharides on overexpression of NF-κB agent in vascular endothelial cells reduced by high glucose[J]. J Shanxi Coll Tradit Chin Med,2011,12(2):28. |
| [7] | 刘开平,沈国清,周晓芳.老年糖尿病与中青年糖尿病并发症对比分析[J].现代诊断与治疗,2012,23(1):48-9.Liu K P,Shen G Q,Zhou X F.Contrust analysis of complications between middle-aged diabetic and elderly diabetic[J].Mod Diagn Treat,2012,23(1):48-9. |
| [8] | Chen G,Chen Y,Chen H,et al.The effect of NF-κB pathway on proliferation and apoptosis of human umbilical vein endothelial cells induced by intermittent high glucose[J].Mol Cell Biochem,2011,347(1/2):127-33. |
| [9] | Devi T S,Hosoya K,Terasaki T,et al.The critical role of TX-the NIP in oxidative stress and DNA damage and retinal pericy teapoptosis under high glucose:implications for diabetic reti-nopathy[J].J Exp Cell Res,2013,319:1001-12. |
| [10] | Hwang H H,Moon P G,Lee J E,et al.Identification of the target proteina of rosiglitazone in 3T3-L1 adipocytes through proteomic analysis of cytosolic and secreted proteins[J].Molcells,2011,31(3):239-46. |
| [11] | 池源,王丽波.苯酚-硫酸法测定南瓜籽多糖含量的条件优化[J].食品与机械,2014,30(1):89-92.Chi Y,Wang L B.Study on phenol-sulfuric acid method for determination of polysaccharide content in pumpkin seeds[J].Food Machinery,2014,30(1):89-92. |
| [12] | Ng T B,Liu J,Wong J H,et al.Review of research on Dendrobium aprized folk medicine[J].Appl Microb Biot,2012,93(5):1795-803. |
| [13] | 李桂锋,李进进,许继勇,等.铁皮石斛研究综述[J].中药材,2010,33(1):150-3.Li G F,Li J J,Xu J Y,et al.The research summarizes of Dendrobium officinale[J].J Chin Med Mat,2010,33(1):150-3. |
| [14] | Zong A Z,Cao H Z,Wang F S,et al.Anticancer polysaccharides from natural resources:a review of recent research[J].Carbohyd Polym,2012,90:1395. |
| [15] | 张娥珍,辛明,苏燕竹,等.铁皮石斛超微粉体外抗氧化性研究[J].食品科技,2014,39(01):84-97.Zhang E Z,Xin M,Su Y Z,et al.Antioxidant effect of Dendrobium candidum in vitro experiments[J].Food Sci Technol,2014,39(01):84-97. |