


2. 中医脑病重点实验室,江苏 南京 210023
 ,
TAO Wei-wei1,2
,
TAO Wei-wei1,2 ,
CHAI Yi1,2,
LI Shou-xue1,2,
WANG Xing1,2,
ZHANG Yu-xuan1,2,
CHEN Li1,2,
XIA Bao-mei1,2,
WU Hao-xing1,2,
CHEN Gang1,2
,
CHAI Yi1,2,
LI Shou-xue1,2,
WANG Xing1,2,
ZHANG Yu-xuan1,2,
CHEN Li1,2,
XIA Bao-mei1,2,
WU Hao-xing1,2,
CHEN Gang1,2

2. Key Laboratory of Integrative Biomedicine of Brain Diseases, Nanjing University of Chinese Medicine, Nanjing 210023, China
随着社会竞争的日益激烈,抑郁症的发病率也在逐年增加。据世界卫生组织统计,抑郁症已成为世界第四大疾患,预计到2020年,可能成为仅次于冠心病的第二大疾病[1]。目前主流抗抑郁药起效缓慢、首次用药有效率低、不良反应多等局限性,降低了患者用药的依从性,不利于重症抑郁患者自杀风险的防范。因此,临床迫切需要寻找和研制起效快、疗效好以及副作用小的抗抑郁药物[2]。
栀子来源于茜草科Rubiaceae植物栀子Cape jasmine的干燥成熟果实。 中医谓其“性寒味苦,归心肺三焦经,具有泄火除烦,清热利尿,凉血解毒之功效”。以栀子为主要药物组分的复方研究中发现其有明显的抗抑郁作用[3]。本实验室前期的研究发现传统中药方剂越鞠丸具有快速起效抗抑郁作用[4],确认了其石油醚部位具有快速起效抗抑郁潜力[5],并发现在越鞠丸快速起效抗抑郁中起关键作用的药物组分为栀子[6]。在此基础上,对栀子下分部位进行的研究发现,栀子石油醚部位具有快速起效抗抑郁作用,其机制与BDNF及其特异性受体TrkB的激活相关[7]。本实验进一步对栀子石油醚的下分部位进行了研究,以明确其快速起效时程及探讨其相关生物学机制,从而为快速起效抗抑郁药物的新药研发提供临床前依据。
1 材料与方法 1.1 实验动物健康昆明种小鼠160只,体质量20~25 g,♂,由常州卡文斯实验动物有限公司提供,动物合格证号:SCXK(苏)2011-0003。动物房室温25℃,湿度45%,昼夜交替12 h,动物自由饮食进水。
1.2 实验药物栀子石油醚有效部位(689.9 g)经硅胶柱色谱分离,石油醚-乙酸乙酯梯度洗脱(100 ∶0~50 ∶50)得到4个组分(GJ-PE1、GJ-PE2、GJ-PE3、GJ-PE4),各组分别采用1L旋转蒸发仪(河南巩义予华仪器设备有限责任公司,产品型号:501)浓缩得到浸膏,各部位浸膏均采用1%的吐温-80溶解。盐酸氯胺酮(ketamine)注射液为福建古田制药厂生产(批号:20140301)。使用时用0.9%生理盐水配成30 g·L-1的药液。
2 方法 2.1 分组与给药160只小鼠分3批实验进行。首先进行栀子石油醚4个部位给药后24 h的快速抗抑郁筛药测试,以确定具有快速抗抑郁潜力的栀子石油醚下分部位。之后分别进行30 min和2 h的行为测试,以确定具有快速起效抗抑郁潜力的栀子石油醚有效部位的初始起效时间。
24 h测试:60只♂小鼠分为空白组、GJ-PE的4个部位(按照栀子石油醚部位[7]有效剂量折算):GJ-PE1组(0.07 g·kg-1)、GJ-PE2组(0.08 g·kg-1)、GJ-PE3组(0.01 g·kg-1)、GJ-PE4组(0.5 g·kg-1)以及氯胺酮组(30 mg·kg-1)。灌胃24 h后依次进行小鼠悬尾实验、强迫游泳实验和陌生环境摄食。
30 min测试:50只♂小鼠分为空白组、GJ-PE的3个部位组以及氯胺酮组(30 mg·kg-1)。灌胃,30 min后进行小鼠悬尾实验。
2 h测试:50只♂小鼠分为空白组与GJ-PE的3个部位组以及氯胺酮组(30 mg·kg-1)。灌胃,2 h后进行小鼠强迫游泳实验。
2.2 行为学测试 2.2.1 小鼠悬尾实验(TST)将单个小鼠尾端用胶布粘在悬挂钩上面,尾尖距胶布约1 cm。将小鼠放入通用隔音行为箱内,使其成倒挂状态,头部离箱底20 cm。小鼠为了克服不正常体位而挣扎活动,活动一段时间后出现间断性不动,显示绝望状态。小鼠悬尾视频分析系统3.0版(上海吉量软件公司)记录6 min内小鼠的活动情况,前2 min为小鼠的悬尾适应期,分析后4 min内小鼠的不动时间[5]。
2.2.2 小鼠强迫游泳(FST)实验前1 h空调调整行为房温度至26℃,将3L水灌入5 L(直径18 cm×高25 cm)的玻璃烧杯中,水温调至24℃~26℃。之后将小鼠依次放入隔音行为箱中,强迫游泳视频分析系统3.0版(上海吉量软件公司)记录小鼠6 min内的活动。前2 min为小鼠的游泳适应期,分析后4 min内小鼠游泳的总不动时间,即小鼠在水中停止挣扎,或呈漂浮状态,仅有细小的肢体运动[8]。
2.2.3 新奇抑制摄食实验(novelty suppressed feeding test,NSFT)小鼠禁食24 h后,依次从固定角落被放入一个新的空鼠笼内,中心放置已称重的粮食。放入后,检测小鼠首次进食的潜伏时间。小鼠进食标准为开始咀嚼食物,而不仅仅嗅食或摆弄食物。以吃食的潜伏期和消耗食物的重量为观测指标[8]。单位时间摄食量计算公式为:单位时间摄食量/g=10 min内消耗粮食重量(g)/小鼠体重(g)
2.3 Westernblot Western blot检测BDNF、p-eEF2、eEF2水平: 24 h及2 h行为实验结束后,分别处死两批小鼠中的空白组、GJ-PE1组及氯胺酮组,冰上取脑,并提取小鼠海马蛋白,用Nanodrop测定样品中蛋白浓度。根据BDNF、p-eEF2 、eEF2的分子量选择SDS-PAGE胶(分别为15%、8%、8%的胶)电泳(Bio-Rad电泳系统)分离蛋白质,300 mA恒流冰浴转膜,将蛋白转移至聚偏二氟乙烯(PVDF)膜上。将裁剪好的PVDF膜分别放入1%的BSA中室温摇床震荡1h,然后将膜分别放入加有BDNF(Santa Cruz,sc-546,1 ∶200)、p-eEF2(CellSignaling Technology,货号:2331S)、eEF2(Cell Signaling Technology,货号:2332S)、β-tubulin (Proteintech,10094-1-AP,1:2000)抗体的抗体盒中,4℃冰箱摇床过夜。次日TBST缓冲液漂洗3次后,将PVDF膜分别放入加有羊抗兔二抗(Proteintech,SA00001-2,1 ∶2 000)的抗体盒中,室温孵育1h,ECL(康为世纪,货号:CW0048C)显影。凝胶成像及分析系统(Tannon)采集BDNF、p-eEF2、eEF2及Tubulin条带灰度值,分析各样本BDNF、p-eEF2、eEF2与Tubulin的灰度值。
2.4 统计学方法实验结果以x±s表示,采用SPSS 17.0统计分析软件对多组间数据进行单因素方差分析。
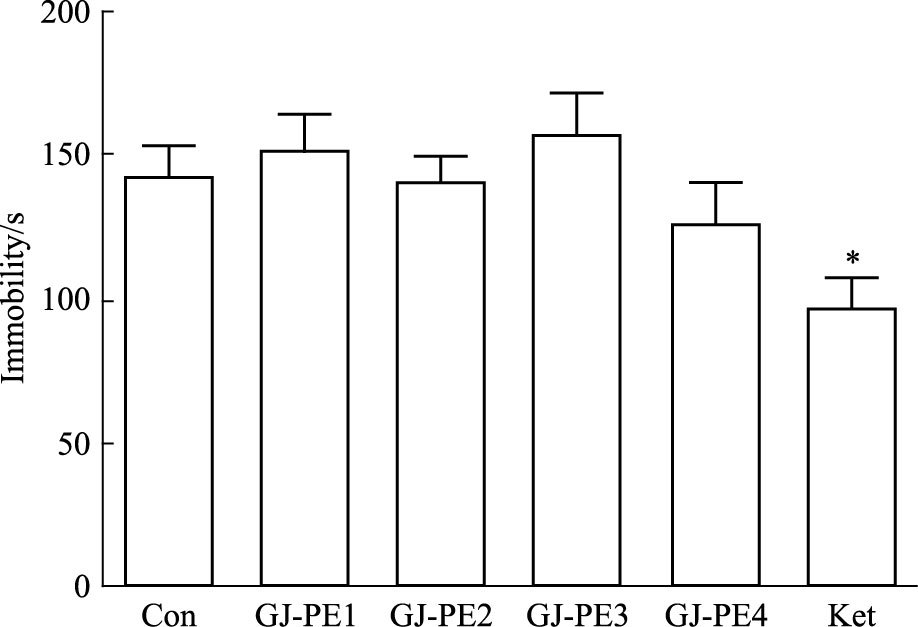
3 结果 3.1 给予栀子石油醚4个部位24h后对小鼠悬尾实验的影响给药24 h后,栀子石油醚4个部位组在小鼠悬尾上不动时间与空白组相比差异均无显著性(P >0.05)。Ket组与空白组相比不动时间明显缩短(P<0.05),见Fig 1。
|
| 图 1 Immobility time in tail suspension test at 24 h after a single treatment of four fractions(n=10) *P<0.05 vs control |
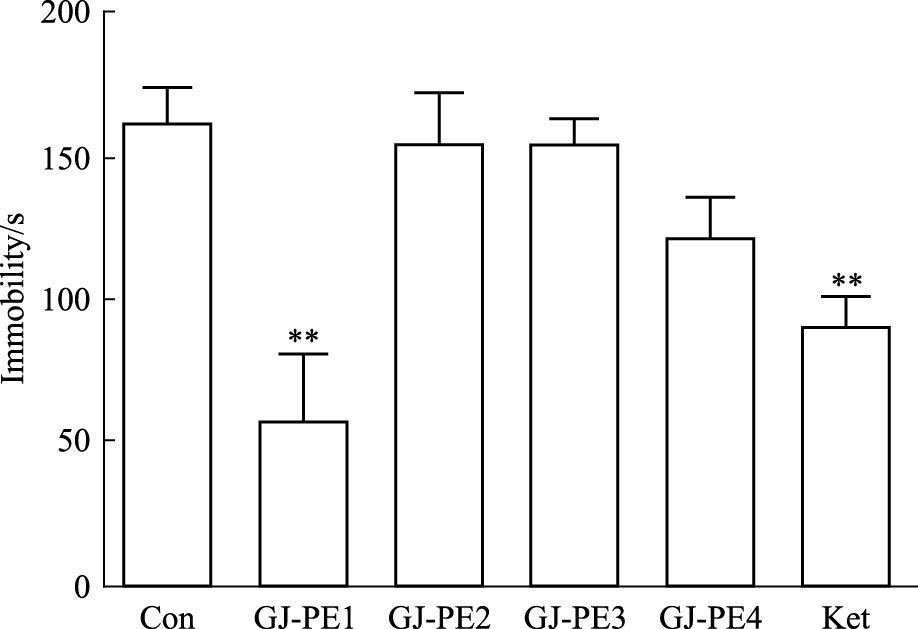
给药24 h后,与空白组相比,GJ-PE1组及Ket组在强迫游泳上不动时间明显降低(P<0.01),其余3个部位组差异无显著性(P >0.05),见Fig 2。
|
| 图 2 Immobility time in forced swimming test at 24 h after a single treatment of four fractions(n=10) **P<0.01 vs control |
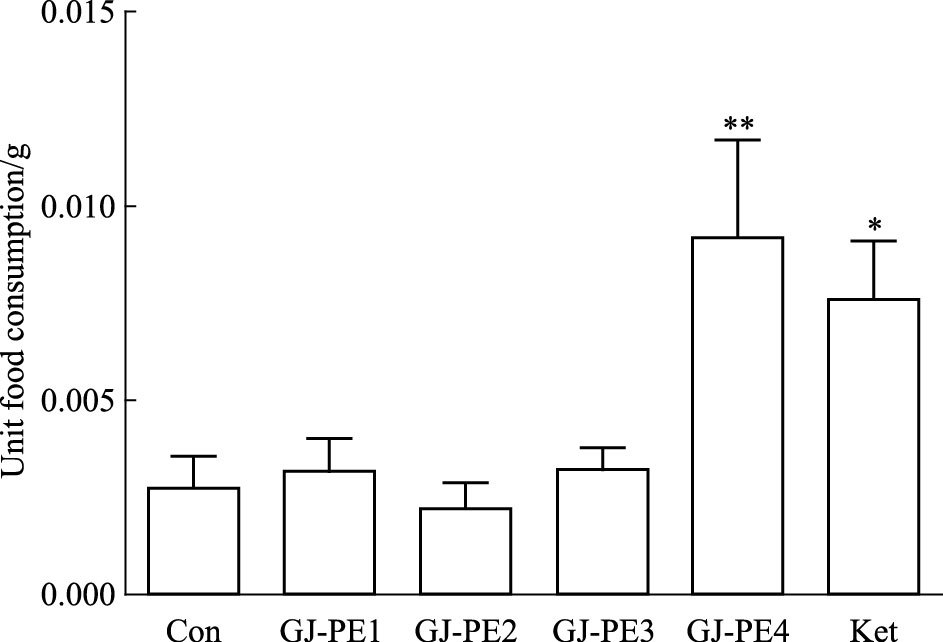
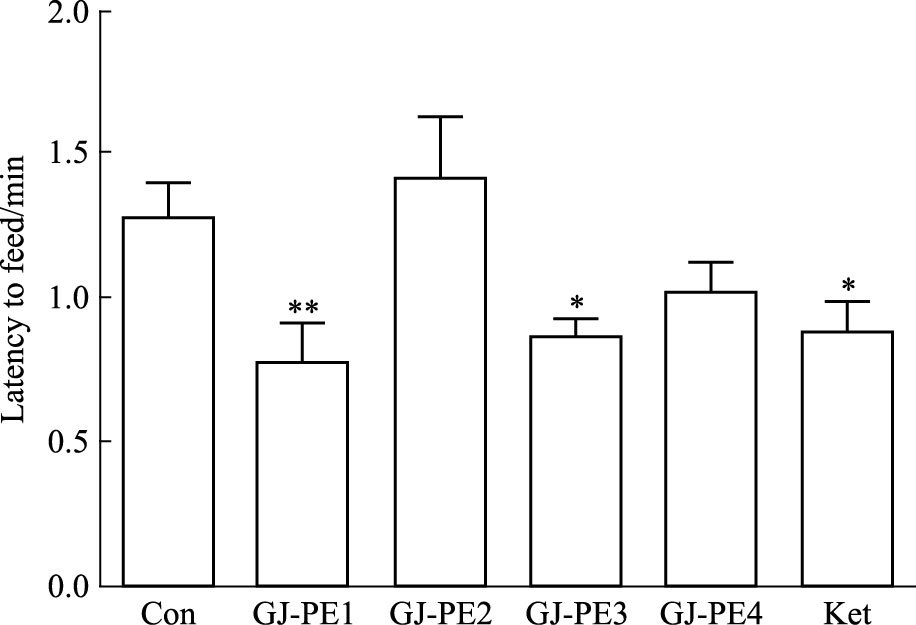
给药24 h后,与空白组相比,GJ-PE4组和Ket组在陌生环境中的单位时间摄食量明显增加(P<0.01,P<0.05),其余各部位组与空白组相比差异无显著性(P >0.05)。与空白组相比,GJ-PE1、GJ-PE3和Ket组在陌生环境中的摄食潜伏期明显缩短(P<0.01,P<0.05,P<0.05),GJ-PE2、GJ-PE4组差异无显著性(P >0.05),见Fig 3,4。
|
| 图 3 Unit food comsumptions in novelty suppressed-feeding test at 24 h after a single treatment of four fractions(n=10) *P<0.05,**P<0.01 vs control |
|
| 图 4 Latency time at 24 h after a single treatment of four fractions(n=10) *P<0.05,**P<0.01 vs control |
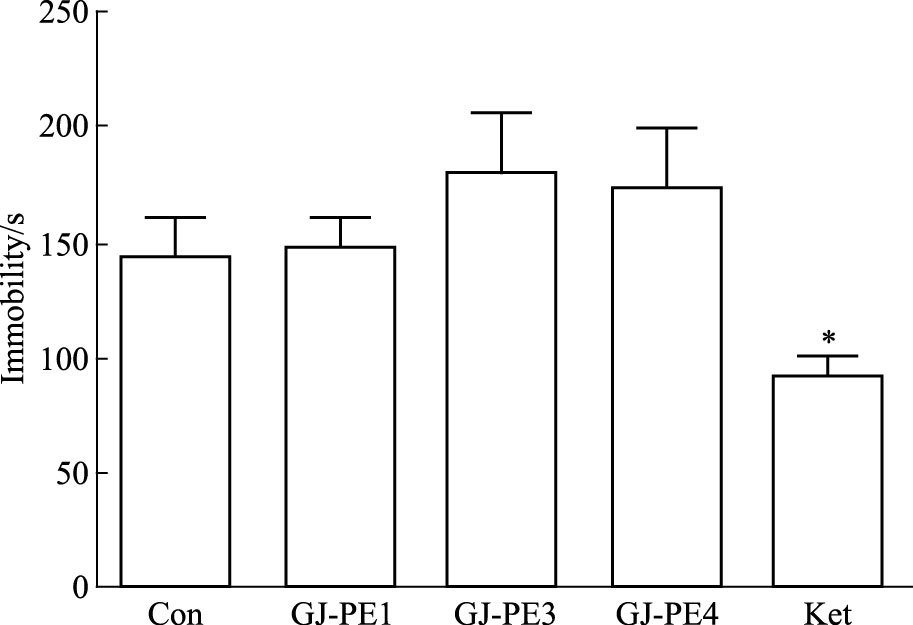
给药30 min后,与空白组相比,栀子石油醚3个部位在小鼠悬尾上不动时间均差异无显著性(P >0.05),Ket组在小鼠悬尾实验上不动时间明显降低(P<0.05),见Fig 5。
|
| 图 5 Immobility time in tail suspension test at 30 min after a single treatment of three fractions(n=10) *P<0.05 vs control |
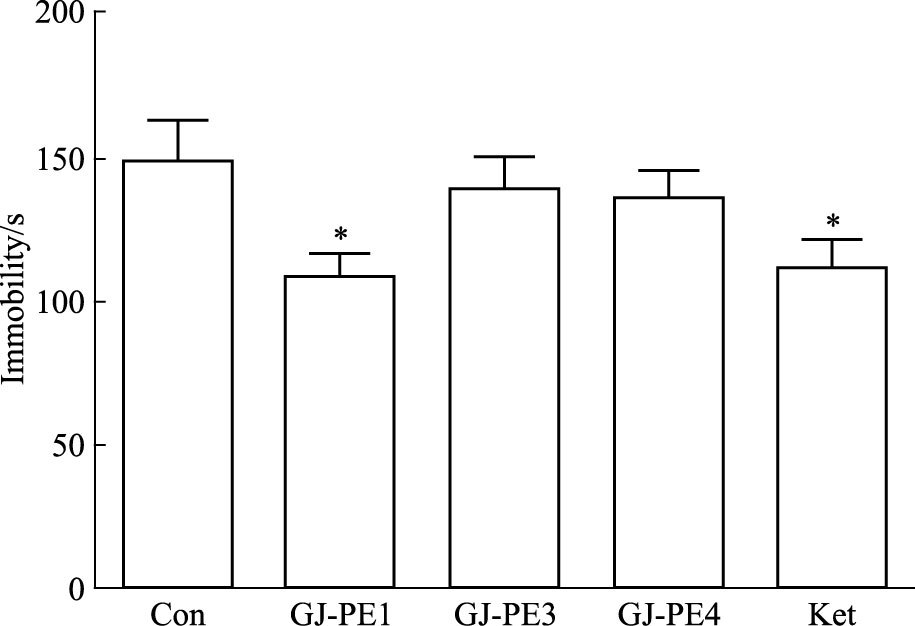
给药2 h后,与空白组相比,GJ-PE1和Ket组在小鼠强迫游泳实验上不动时间明显降低(P<0.05),其余部位组与空白组相比差异无显著性(P >0.05),见Fig 6。
|
| 图 6 Immobility time in forced swimming test at 2 h after a single treatment of three fractions(n=10) *P<0.05 vs control |
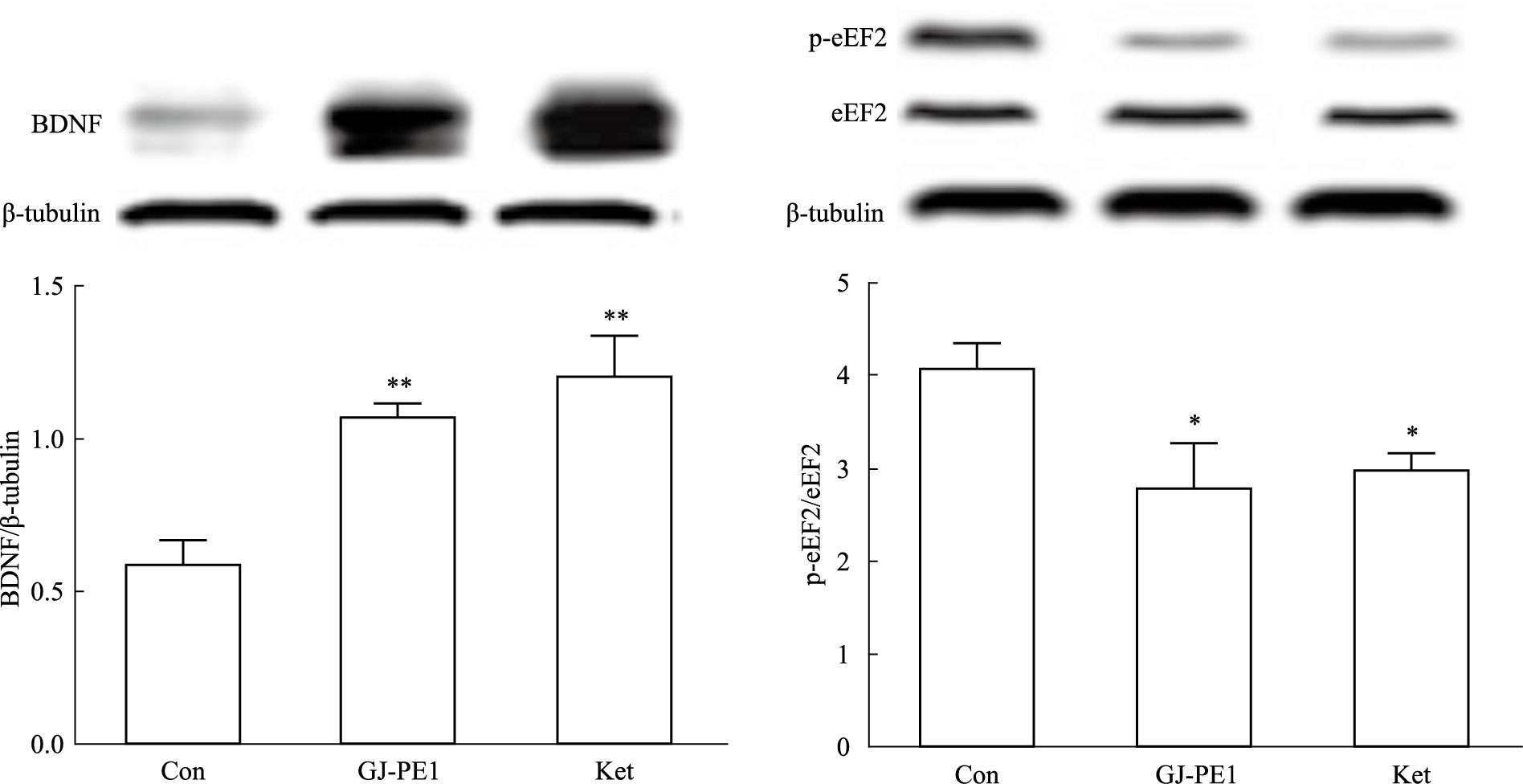
给药2 h后,与空白组相比,GJ-PE1组和Ket组小鼠海马BDNF的表达均明显升高,差异有统计学意义(P<0.01);与空白组相比,栀子石油醚有效部位组和Ket组小鼠海马p-eEF2的表达均明显降低,差异有统计学意义(P<0.05),见Fig 7。
|
| 图 7 BDNF and p-eEF2 expressions in hippocampus at 2 h after GJ-PE1 treatment(n=7) *P <0.05,**P<0.01 vs control |
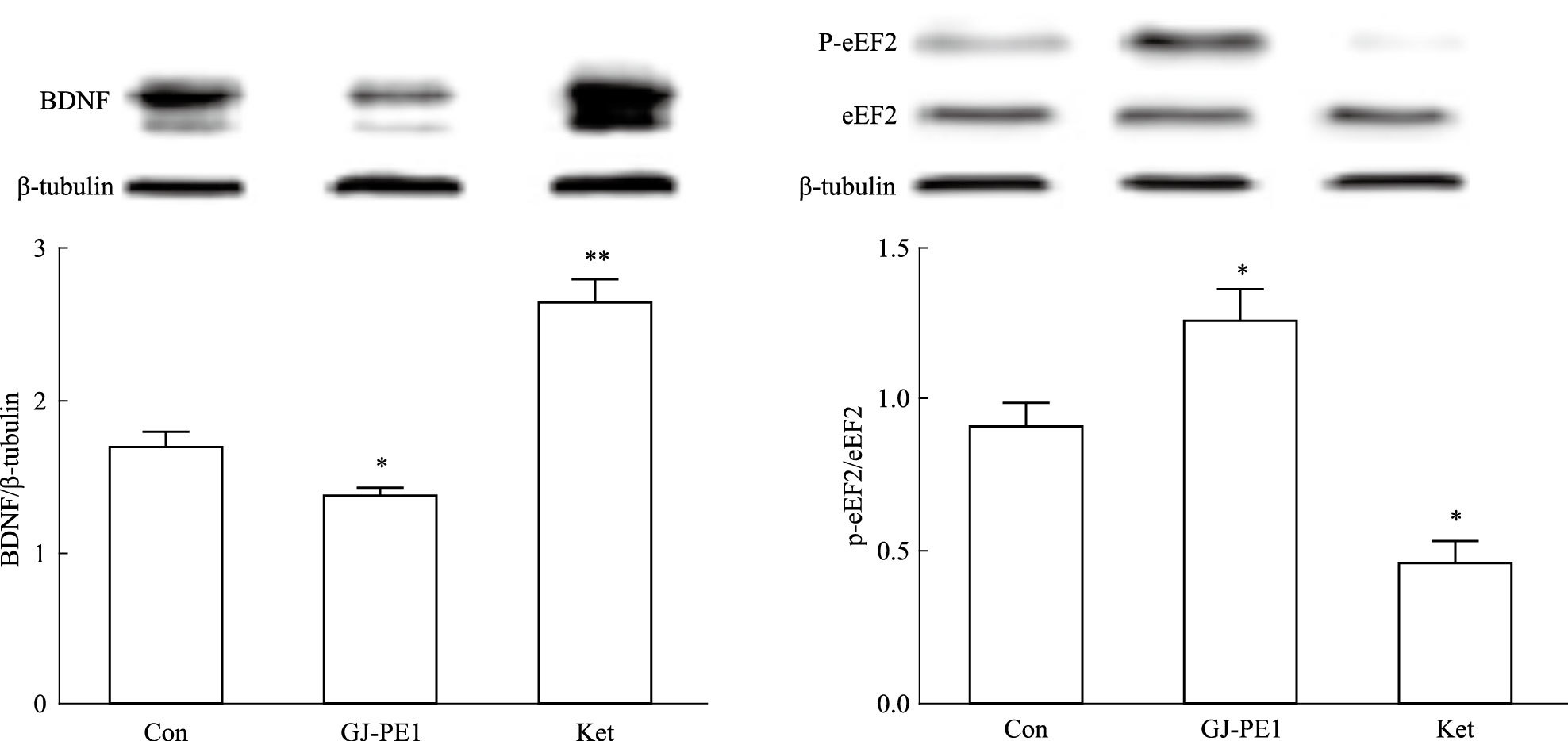
给药24 h后,与空白组相比,GJ-PE1组小鼠海马BDNF的表达明显降低(P<0.05),Ket组小鼠海马BDNF的表达明显升高(P<0.01);与空白组相比,GJ-PE1组小鼠海马的p-eEF2表达明显升高而Ket组小鼠海马的p-eEF2表达明显降低(P<0.05),见Fig 8。
|
| 图 8 BDNF and p-eEF2 expressions in hippocampus at 24 h after GJ-PE1 treatment(n=7) *P<0.05,**P<0.01 vs control |
谷氨酸受体N-甲基-D-天冬氨酸受体(N-methyl-D-aspartic acid receptor,NMDAR )的拮抗剂氯胺酮为公认的具有快速起效抗抑郁作用的药物,它同时也是快速起效抗抑郁研究的原型药[9]。临床研究发现,低剂量氯胺酮在给药30~40 min后开始起效[10]。虽然氯胺酮的体内代谢半衰期只有3 h[11],其单次给药后的抗抑郁效果却能持续7 d[10]。本实验室前期的动物实验研究发现,与氯胺酮类似,单次给予栀子石油醚部位能够减轻动物的抑郁样症状[7],而常规单胺类药物在此模型上至少需要7 d以上才能发挥作用[12],体现出栀子石油醚部位具有快速抗抑郁特性。
小鼠悬尾和强迫游泳实验是两种对抗抑郁药敏感的行为绝望模型,常用于抗抑郁药的初筛。两个实验中小鼠不动时间的延长模拟了人类抑郁症中的“绝望”状态。新奇抑制摄食实验是根据测量在一个新环境中动物的抑郁潜伏期和食物消耗量的减退情况来模拟出一个长期的抑郁模型[13]。本研究采用这3种小鼠抑郁行为实验来筛选栀子石油醚4个下分部位中最具有快速抗抑郁潜力的部位,并进一步探讨其初始起效时间。
脑源性神经营养因子(brain derived neurotrophic factor,BDNF)是目前研究较多的与抑郁症发病及抗抑郁作用相关的蛋白[14]。抑郁症的发生与神经可塑性的损伤密切相关。BDNF能促进神经发生及调节神经可塑性。临床研究发现抑郁症患者海马部位及前额叶皮层部位BDNF水平明显减少[15]。动物实验也证实,诱发抑郁症的压力应激会导致动物海马部位BDNF mRNA表达减少[16]。而抗抑郁药物治疗能够导致动物海马部位BDNF水平升高[17]。真核细胞肽链延伸因子-2激酶(eukaryotic elongation factor 2 kinase,eEF2K) 是一类钙离子/钙调蛋白依赖的丝氨酸/苏氨酸激酶,并在调控蛋白质翻译的延长过程中发挥重要作用[18]。eEF2K目前已知的唯一底物是eEF-2(真核生物肽链延伸因子-2)。eEF2通过诱导肽基转运RNA从核糖体A位到P位的移位而使肽链进一步延伸。eEF2激酶通过磷酸化eEF-2上的苏氨酸56位点降低其与核糖体的亲和力从而终止肽链延伸[19]。研究发现给予氯胺酮30 min至2 h内,eEF2的磷酸化水平迅速降低,表明了其活性的增加[2]。Autry等[20]报道快速抗抑郁药物氯胺酮可能通过快速降低eEF2磷酸化水平,从而对BDNF的翻译去抑制,以达到快速增加BDNF合成,增强突触应答来实现快速抗抑郁作用。
本研究将3批动物分为3个时间点进行测试。研究首先分别对给予栀子石油醚4个部位后24 h的小鼠进行了悬尾、强迫游泳和新奇抑制摄食实验。结果显示,GJ-PE1给药后24 h明显缩短了小鼠的游泳不动时间,同时减少了小鼠在新奇抑制摄食实验的潜伏时间。GJ-PE3仅减少了24 h后小鼠在新奇抑制摄食实验的潜伏时间。GJ-PE4仅增加了给药24 h后小鼠新奇抑制摄食实验的单位时间摄食量。而GJ-PE2给药24 h后在3种行为测试中均未表现出抗抑郁作用。因此我们认为GJ-PE2不具有快速起效抗抑郁潜力。在初始起效时间点实验中我们排除了GJ-PE2,仅对GJ-PE1、GJ-PE3、GJ-PE4 3个部位进行测试。给药30 min后的小鼠悬尾测试结果显示,栀子石油醚的这3个部位在给药后30 min均未显示出抗抑郁作用。我们又选取了栀子快速抗抑郁初始起效时间点2 h作为测试时程[6]。结果显示GJ-PE1在给药后2 h明显缩短了小鼠的游泳不动时间。行为学研究结果表明GJ-PE1、GJ-PE3、GJ-PE4均具有快速起效抗抑郁潜力,其中GJ-PE1具有快速起效,抗抑郁的潜力最大,且其最快起效时间为给药后2 h。GJ-PE2不具有快速抗抑郁潜力。
分子机制研究中,与前期越鞠丸实验结果类似[4],GJ-PE1降低了给药24 h后小鼠海马中BDNF的表达,增加了磷酸化eEF2的表达。这表明给药后24 h,GJ-PE1激活了eEF2,并导致了BDNF的翻译抑制。与越鞠丸[4]及越鞠丸石油醚部位研究[5]结果不同,而与栀子快速起效抗抑郁研究结果[6]相同的是,GJ-PE1在给药后2h,而非30 min才表现出快速抗抑郁作用。其给药后2 h上调了BDNF并下调了磷酸化eEF2,提示其在2 h这一时间点的快速起效抗抑郁机制可能与氯胺酮快速起效抗抑郁机制类似。越鞠丸及越鞠丸石油醚部位给药后30 min显示出抗抑郁样作用,同时引起了小鼠海马BDNF表达的上调。而栀子、栀子石油醚部位及栀子石油醚有效部位GJ-PE1均在给药后2 h才开始显示出抗抑郁样作用。这表明越鞠丸及越鞠丸石油醚部位30 min的抗抑郁作用可能是栀子与其它药物组分共同作用的结果。在目前的研究中,我们发现了栀子石油醚3个有效部位具有快速抗抑郁潜力,筛选出了GJ-PE1具有的快速抗抑郁潜力最大,并发现这种快速起效抗抑郁潜力的起效时间为给药后2 h,其机制与BDNF的上调及p-eEF2的下调相关。而给药后24 h,GJ-PE1的快速抗抑郁作用则可能并非BDNF的作用。影响其抗抑郁持久性方面的生物学机制值得进一步探讨。越鞠丸中给药30 min后发挥快速抗抑郁作用的物质基础,同样值得后期的进一步研究,以期为快速起效抗抑郁药物的研发提供思路。
( 致谢: 本文实验在南京中医药大学基础医学院转化系统生物学与神经科学研究中心与中医脑病校重点实验室完成,特此致谢! )
| [1] | 刘佳莉, 苑玉和, 陈乃宏. 抑郁症的治疗研究进展[J]. 中国药理学通报, 2011, 27 (9) : 1193-6 . Liu J L, Yuan Y H, Chen N H. Research progress in treatment of depression[J]. Chin Pharmacol Bull, 2011, 27 (9) : 1193-6 . |
| [2] | 徐凌志, 李素霞, 邓佳惠, 等. 快速抗抑郁机制研究进展[J]. 脑与神经疾病杂志, 2014, 22 (4) : 317-21 . Xu L Z, Li S X, Deng J H, et al. A review of mechanism of rapid antidepressant[J]. J Brain Nerv Dis, 2014, 22 (4) : 317-21 . |
| [3] | 高 芳.栀子豉汤治疗抑郁症的实验研究[D].福建:福建中医药大学,2007:1-36. Gao F. Experimental study on treating the depression with decoction of capejasmine and fermented soybean[D].Fujian: Fujian university of Traditional Chinese Medicine,2007:1-36. |
| [4] | Xue W D, Zhou X, Yi N, et al. Yueju pill rapidly induces antidepressant-like effects and acutely enhances BDNF expression in mouse brain[J]. Evid Based Complement Alternat Med, 2013, 2013 : 184367 . |
| [5] | 任荔, 陶伟伟, 薛文达, 等. 越鞠丸石油醚部位潜在的快速抗抑郁作用与BDNF、TrkB的上调相关[J]. 中国药理学通报, 2015, 31 (12) : 1754-9 . Ren L, Tao W W, Xue W D, et al. The potent rapid antidepressant effects of petroleum ether fraction of Yueju Pill are associated with BDNF and TrkB Up-regulation[J]. Chin Pharmacol Bull, 2015, 31 (12) : 1754-9 . |
| [6] | Zhang H L, Xue W D, Wu R J, et al. Rapid antidepressant activity of ethanol extract of Gardenia jasminoides Ellis is associated with upregulation of BDNF expression in the hippocampus[J]. Evid Based Complement Alternat Med, 2015, 2015 : 761238 . |
| [7] | Ren L, Tao W W, Zhang H L, et al. Two standardized fractions of Gardenia jasminoides Ellis with rapid antidepressant effects are differentially associated with BDNF up-regulation in the hippocampus[J]. J Ethnopharmacol, 2016, 187 (2016) : 66-73 . |
| [8] | 夏宝妹, 张海楼, 薛文达, 等. 产后抑郁小鼠模型的构建及越鞠甘麦大枣汤对其抑郁样行为的影响[J]. 中国药理学通报, 2015, 31 (9) : 1324-8 . Xia B M, Zhang H L, Xue W D, et al. Postpartum depression animal model in mice and effect of Yuejuganmaidazaotang on PPD model[J]. Chin Pharmacol Bull, 2015, 31 (9) : 1324-8 . |
| [9] | Abdallah C G, Sanacora G, Duman R S, et al. Ketamine and rapid-acting antidepressants: a window into a new neurobiology for mood disorder therapeutics[J]. Annual Rev Med, 2015, 66 : 509-23 doi:10.1146/annurev-med-053013-062946. |
| [10] | Zarate C, Singh J, Manji H K. Cellular plasticity cascades: targets for the development of novel therapeutics for bipolar disorder[J]. Biol Psychiatry, 2006, 59 (11) : 1006-20 doi:10.1016/j.biopsych.2005.10.021. |
| [11] | Clemens J, Nimmo W S, Grant I S. Bioavailability, pharmacokinetics, and analgesic activity of ketamine in humans[J]. J Pharm Sci, 1982, 71 (5) : 539-42 doi:10.1002/jps.2600710516. |
| [12] | Duman R S, Li N, Liu R J, et al. Signaling pathways underlying the rapid antidepressant actions of ketamine[J]. Neuropharmacology, 2012, 62 (1) : 35-41 doi:10.1016/j.neuropharm.2011.08.044. |
| [13] | 陈湘, 窦建卫, 胡亚丽. 抑郁症动物模型的应用及研究进展[J]. 中国组织工程研究与临床康复, 2008, 12 (28) : 5521-4 . Chen X, Dou J W, Hu Y L. Application and progress of animal models of depression[J]. J Clin Rehabil Tissue Eng Res, 2008, 12 (28) : 5521-4 . |
| [14] | 乔卉, 安书成, 徐畅. BDNF与抑郁症的研究现状及进展[J]. 生理科学进展, 2011, 42 (3) : 195-200 . Qiao H, An S C, Xu C. Research progress of BDNF and depression[J]. Progr Physiol Sci, 2011, 42 (3) : 195-200 . |
| [15] | Taliaz D, Stall N, Dar D E, Zangen A. Knockdown of brain-derived neurotrophic factor in specific brain sites precipitates behaviors associated with depression and reduces neurogenesis[J]. Mol Psychiatry, 2010, 15 (1) : 80-92 doi:10.1038/mp.2009.67. |
| [16] | Yogesh D. Brain-derived neurotrophic factor: role in depression and suicide[J]. Neuropsychiatr Dis Treat, 2009, 5 (1) : 433-49 . |
| [17] | Fani L, Gisela B, Sonia T, et al. Neurotrophins role in depression neurobiology: A review of basic and clinical evidence[J]. Curr Neuropharmacol, 2011, 9 (4) : 530-52 doi:10.2174/157015911798376262. |
| [18] | Ryazanov A G. Elongation factor-2 kinase and its newly discovered relatives[J]. FEBS Lett, 2002, 514 (1) : 26-9 doi:10.1016/S0014-5793(02)02299-8. |
| [19] | 刘晓媛.eEF-2激酶抑制剂对恶性脑胶质瘤治疗的增效作用及其机制研究[D].江苏:苏州大学,2012:1-89. Liu X Y. Inhibition of eEF-2 kinase augments the antitumor activity of temozolomide against Glioma[D].Jiangsu: Soochow university, 2012:1-89. |
| [20] | Autry A E, Adachi M, Nosyreva E, et al. NMDA receptor blockade at rest triggers rapid behavioural antidepressant responses[J]. Nature, 2011, 475 (7354) : 91-5 doi:10.1038/nature10130. |