


2. 南京中医药大学中医脑病重点实验室, 江苏 南京 210023
陶伟伟(1984-),男,博士,助理研究员,研究方向:中医药的药效物质基础,E-mail:tw845@163.com
2. Key Laboratory of Integrative Biomedicine of Brain Diseases, School of Basic Biomedical Science, Nanjing University of Chinese Medicine, Nanjing 210023, China
抑郁症以情绪低落、悲观、睡眠障碍,严重者常伴有自杀念头或行为特点的情志疾病[1]。世界卫生组织联合中国精神疾病防治协会研究表明,在我国抑郁症患病人数超过6 100万,成为国民疾病负担第二的疾病,具有极高的致残性和致死性,严重危害国民健康[2]。然而由于本病的复杂性,至今仍不能完整全面的阐释其发病机制,且一线西医药物的局限性和副作用都很突出。目前临床上以5-羟色胺(5-hydroxytryptamine,5-HT)重摄取抑制剂为代表的单胺增强类药物是主流抗抑郁药物,但据统计,三分之一病人对各种单胺增强类药物没有反应性,而有反应性的病人中有50%的人群临床症状改善后会复发。除此以外,这些常规抗抑郁药还有起效缓慢的缺点,通常需要服用3-6个星期的时间后才能显示出效果[3]。显效迟滞性导致抑郁症病人服药的依从性低,往往提前中断用药,也会因此推迟服用其他或许有效的抗抑郁药物,尤其不利于治疗有高自杀风险的抑郁症病人[4, 5]。因此,快速有效地缓解抑郁症状成为抑郁症治疗中一个迫切需要解决的重要问题。
传统中药方剂越鞠丸,功用行气解郁,主治郁证。始载于元代著名医家朱震亨《丹溪心法》中: “越鞠丸,解诸郁”。方由苍术、香附、川芎、神曲、栀子五味药组成。能解气、血、湿、热、食、痰等诸郁。越鞠丸在现当代也多被用于抑郁症的治疗。Xue等[6]的研究发现,醇提越鞠丸具有快速抗抑郁的作用。Wei等[7]的研究发现越鞠丸石油醚部位为包含了越鞠丸活性成分的部位,并认为该部位具有抗抑郁作用。然而之前的研究并未解释越鞠丸石油醚部位是否为越鞠丸的快速起效抗抑郁部位。本研究试图解答越鞠丸石油醚部位是否具有快速抗抑郁的潜力,并对其生物学机制进行相应探讨,为之后具有快速抗抑郁作用的相关中医药开发打下初步的基础。
1 材料与方法 1.1 实验动物健康昆明种小鼠68只,体质量20~25 g,♂,由中国军事医学科学院提供,动物合格证号:SCXK-(军)2012-0004。动物房室温25℃,湿度45%,昼夜交替12 h,动物自由饮食进水。
1.2 实验药物越鞠丸全方由香附、栀子、川芎、苍术、神曲5药组成,按1 ∶1 ∶1 ∶1 ∶1比例配伍。实验用中药材购于南京中医药大学国医堂门诊。取5种药材粉碎1 kg,过100目筛,等量混合后浸泡在95%乙醇中(6倍体积)24 h,期间不停搅拌。静置后取上清,同样过程重复2次,收集3次的上清液后过滤,减压浓缩至无乙醇。浓缩浸膏采用水混悬,用石油醚萃取5次,合并石油醚萃取液并减压回收至干,得到石油醚萃取部位。盐酸氯胺酮(ketamine,Ket)注射液为福建古田制药厂生产(批号:20140301)。使用时用0.9%生理盐水配成30 g·L-1的药液[6]。
1.3 实验试剂和仪器主要仪器:旋转蒸发仪(河南巩义矛华仪器设备有限公司),摄像机(Panasonic),小鼠悬尾视频分析系统(上海吉量软件公司),Nanodrop 2000(Thermo),蛋白电泳及转膜系统(Bio-Rad);凝胶成像及分析系统(Tannon)
主要试剂:RIPA裂解液:Beyotime,货号:P0013B;蛋白酶抑制剂Cocktail: CellSignaling Technology,货号:#5871S;蛋白Marker:货号:Thermo,批号:00222891;一抗:均为兔抗小鼠,BDNF (Santa Cruz,sc-546,1 ∶200),TrkB (Cell Signaling Technology,4603P,1 ∶1 000),β-tubulin (Epitomics,1879-1,1 ∶2 000);二抗:中杉金桥羊抗兔,批号:109525;ECL显色液:康为世纪,批号:2514K。
2 方法 2.1 小鼠悬尾实验(TST) 2.1.1 分组与给药30 min测试:44只♂小鼠均分为空白组与YJ-PE高、中(即越鞠丸醇提物有效剂量[6])、低剂量(20、13.5、6.75 g·kg-1)组以及氯胺酮组(30 mg·kg-1)。灌胃,30 min给药结束后进行小鼠悬尾实验。
24 h测试:24只♂小鼠均分为空白组与YJ-PE低剂量组(6.75 g·kg-1)以及氯胺酮组(30 mg·kg-1)。灌胃,24 h给药结束后进行小鼠悬尾实验。
2.1.2 行为学测试将单个小鼠尾端(距尾1 cm处) 用胶布粘在悬挂钩上面,放入通用隔音箱内,使其成倒挂状态,头部离箱底20 cm。小鼠为了克服不正常体位而挣扎活动,但活动一段时间出现间断性不动,显示绝望状态。观察6 min,记录后4 min 内小鼠不动时间为绝望时间。
2.2 Western blot Westernblot检测BDNF及TrkB水平,提取小鼠海马蛋白,用Nanodrop测定样品中蛋白浓度。根据BDNF和TrkB的分子量选择SDS-PAGE胶(分别为15%和8%的胶)电泳分离蛋白质,然后转移至聚偏二氟乙烯(PVDF)膜上,将PVDF膜放入一抗封闭缓冲液中室温摇床震荡1h,然后分别加有BDNF、TrkB、Tubulin抗体的抗体盒中,4℃过夜。TBST缓冲液漂洗3次,将PVDF膜分别放入加有羊抗兔二抗的抗体盒中,室温孵育1h,ECL显影。采集BDNF、TrkB及Tubulin条带灰度值,得到各样本BDNF、TrkB与Tubulin的灰度比值。
2.3 统计学方法实验结果以 ± s表示,采用SPSS 17.0统计分析软件对多组间数据进行单因素方差分析。
± s表示,采用SPSS 17.0统计分析软件对多组间数据进行单因素方差分析。
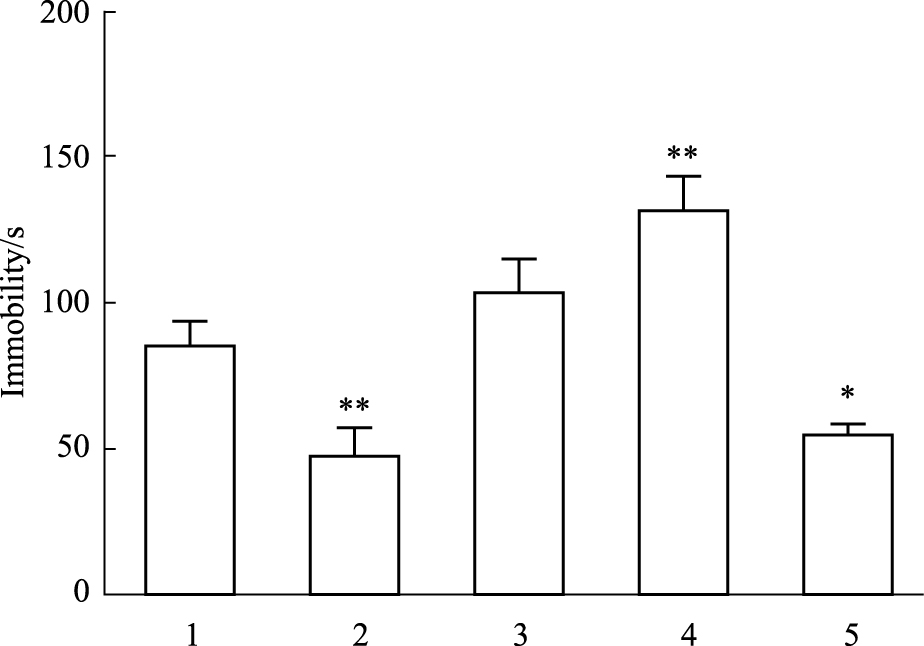
给药30 min后YJ-PE低剂量组在小鼠悬尾上不动时间与空白组相比明显降低(P < 0.01); YJ-PE中剂量组与空白组相比差异无显著性;YJ-PE高剂量组与空白组相比不动时间明显延长(P < 0.01)。Ket与空白组相比不动时间明显降低(P < 0.05)。YJ-PE低剂量组与Ket相比差异无显著性,见Fig1。
|
| Fig 1 Immobility time of mice in tail suspension test(n=8-9) 1:Control; 2:YJ-PE 6.75 g·kg-1; 3: YJ-PE 13.5 g·kg-1; 4:YJ-PE 20 g·kg-1; 5:Ket 30 mg·kg-1,*P < 0.05,**P < 0.01 vs control |
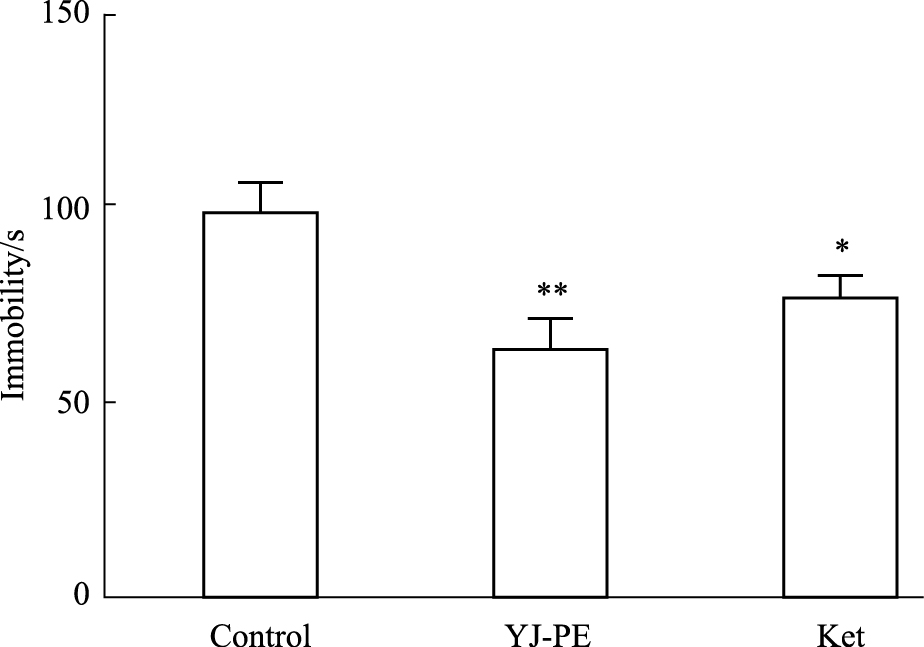
给药24 h后,YJ-PE低剂量组在 小鼠悬尾上不动时间与空白组相比明显降低(P < 0.01);Ket组与空白组相比明显降低(P < 0.05),见Fig2。
|
| Fig 2 Immobility time of mice in forced swimming test(n=8) *P < 0.05, **P < 0.01 vs control |
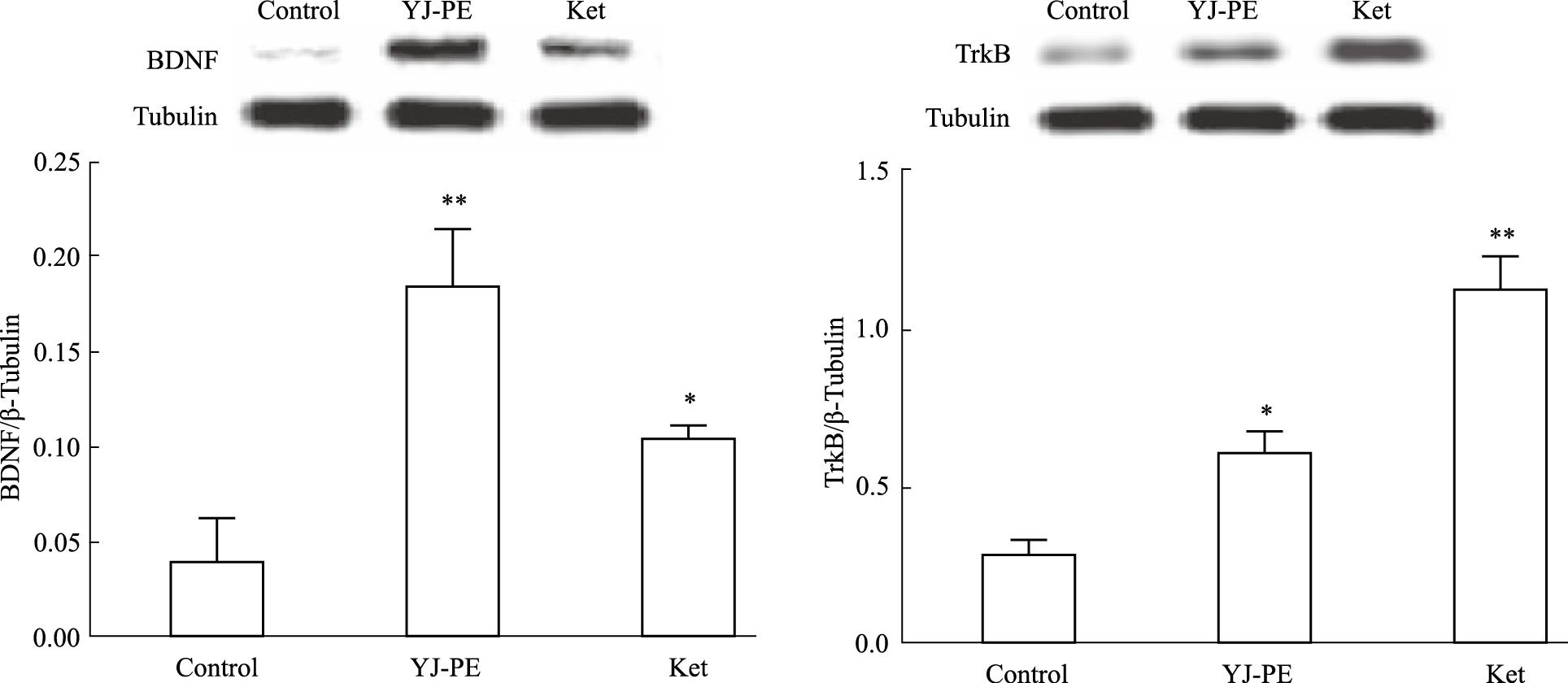
给药30 min后,YJ-PE组和Ket与空白组相比,小鼠海马BDNF的表达均明显升高,差异有统计学意义(P < 0.01,P < 0.05);与空白组相比,YJ-PE组和Ket组小鼠海马TrkB的表达均明显升高,差异有统计学意义(P < 0.05,20151220),见Fig3。
|
| Fig 3 BDNF and TrkB expressions at 30min(n=7) *P < 0.05, **P < 0.01 vs control |
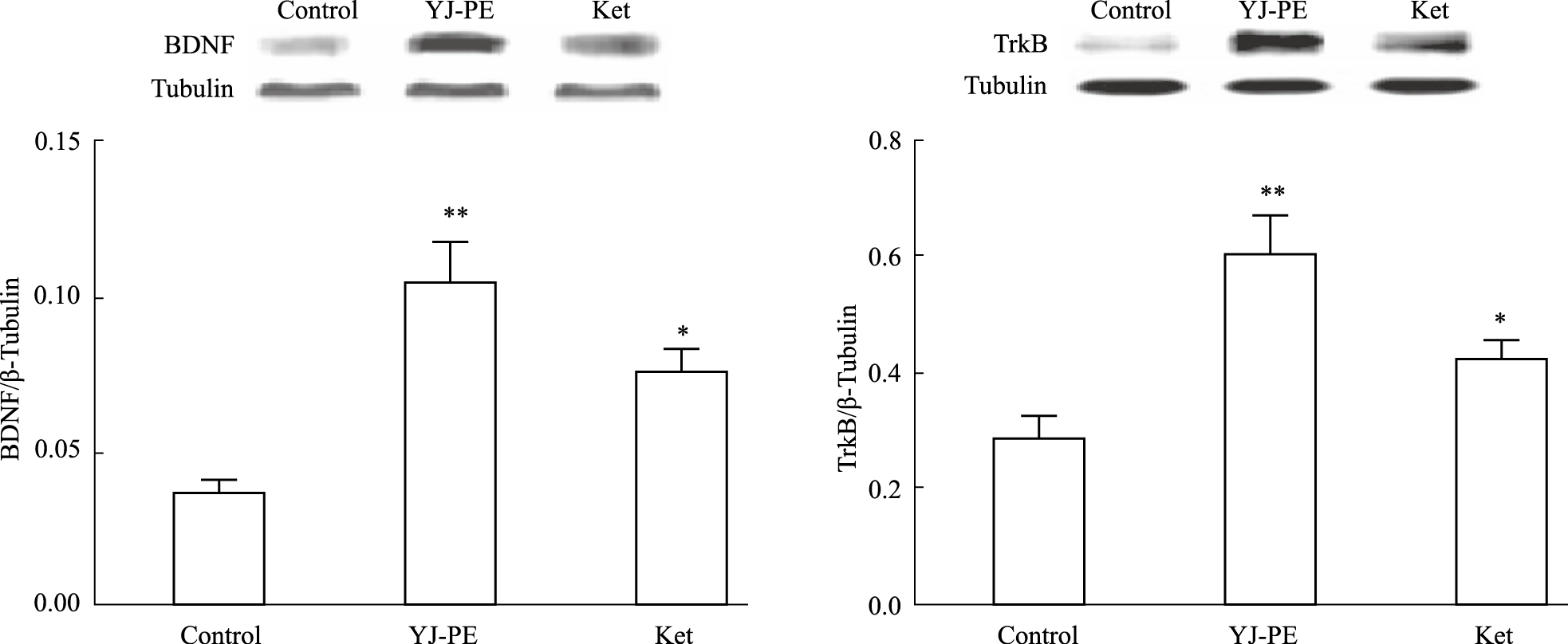
给药24 h后,YJ-PE组和Ket与空白组相比,小鼠海马BDNF的表达均明显升高,差异有统计学意义(P < 0.01,P < 0.05);与空白组相比,YJ-PE组和Ket组小鼠海马TrkB的表达均明显升高,差异有统计学意义(P < 0.01,P < 0.05),见Fig4。
|
| Fig 4 BDNF and TrkB expressions at 24h(n=7) *P < 0.05, **P < 0.01 vs control |
相对于传统的SSRI而言,快速抗抑郁药物能短时间内对抑郁症病人产生抗抑郁的效果。而氯胺酮为目前研究较多的快速抗抑郁药物。在临床上及动物模型中都显示出快速性。氯胺酮是脑内主要的兴奋性神经递质谷氨酸受体N-甲基-D-天冬氨酸受体(NMDAR)的拮抗剂。临床研究发现,单次注射小剂量氯胺酮,可对超过七成病人起到快速抗抑郁作用,同时超过35%的病人反映其抗抑郁作用可以维持两周[8]。动物实验研究也发现,单次低剂量的氯胺酮导致快速持久的抗抑郁作用[9, 10]。快速抗抑郁药物使用的检验模型与传统抗抑郁模型一致,包括悬尾实验(tail suspension test,TST)和强迫游泳实验(forced swimming test,FST)等行为绝望、在习得性无助(learned helplessness,LH)上的失败逃脱次数和慢性不可预知轻微应激(chronic unpredictable mild Stress,CUMS)造模后形成的糖偏好,陌生环境摄食(novelty suppressed-feeding,NSF)等抑郁样行为 [11],但强调单次给药后产生的抗抑郁作用包括其作用的持久性。虽然氯胺酮具有快速抗抑郁作用,然而成瘾性、肝毒性、神经毒性等副作用限制了其临床应用范围[12, 13]。目前临床尚没有具有快速抗抑郁效果,且毒副作用较低的西药。
中医治疗情志病历史悠久,有关“郁证”的临床表现与现代抑郁症十分相似。其中越鞠丸是治疗郁证的经典方剂。著名医家蒲辅周先生曾云:“郁之为病,人多忽视,多以郁为虚,惟丹溪首创五郁六郁之治,越鞠丸最好”。有若干中医临床案例报道提示越鞠丸具有较快起效抗抑郁作用[14, 15, 16]。虽然部分报道尚缺乏系统性研究,但共同提示越鞠丸具有临床快速起效抗抑郁的作用。我们前期使用快速抗抑郁的研究方法,也揭示了越鞠丸作为中药复方的快速抗抑郁作用[6, 17]。
Wei等[7]在越鞠丸中提取出石油醚部位、正丁醇部位、乙酸乙酯部位及水部位4个部位来筛选出越鞠丸中抗抑郁的主要活性成分,发现越鞠丸的主要活性成分包含在石油醚部位和正丁醇部位2个部位中。其中石油醚部位的抗抑郁活性要高于正丁醇部位。本研究中小鼠悬尾实验的结果支持越鞠丸石油醚部位具有快速起效抗抑郁潜力。小鼠悬尾实验是常用的筛选抗抑郁药物的评价模型[18]。小鼠被置于不可逃脱的环境中时,会出现拼命挣扎,试图逃脱的行为,在经过努力仍不能摆脱困境后,小鼠会表现出间断性不动的“行为绝望”状态。这种状态被认为某种程度模拟了抑郁症的表现[19]。绝大多数的抗抑郁药物均可缩短小鼠的不动时间[20]。本研究发现,单次给药30 min后,与空白组相比,低剂量YJ-PE明显缩短小鼠的悬尾不动时间,高剂量YJ-PE明显延长了小鼠的悬尾不动时间,而中剂量YJ-PE的小鼠悬尾不动时间差异无显著性。24 h后再次使用低剂量YJ-PE进行小鼠悬尾测试,其抗抑郁作用依然存在,表明该剂量的持久抗抑郁作用,也与越鞠丸醇提物的效应相似[6]。这表明低剂量YJ-PE给药可能具有快速抗抑郁潜力,中剂量YJ-PE给药则没有快速抗抑郁作用,而高剂量YJ-PE给药反而可能导致抑郁样反应。高剂量YJ-PE的致抑郁样反应,可能与越鞠丸中一些药物成分在大剂量给药时出现的较为明显的镇静催眠作用有关[21, 22]。
大量的文献表明脑源性神经营养因子(brain-derived neurotrophic factor,BDNF)及其受体酪氨酸蛋白激酶B(Tropomyosin receptor kinase B,TrkB)在抑郁症的发病中扮演着相当重要的角色。BDNF及其特异性受体TrkB广泛分布于大脑皮质及海马区域,对神经元的生存、生长、分化维持神经元功能和再生修复等多方面具有重要影响[23]。有研究表明,海马BDNF mRNA和蛋白水平的降低与抑郁症的发病密切相关[24]。而BDNF通过与TrkB的特异结合,激活海马内一系列细胞内信号,从而发挥其抗抑郁效应[25]。Autry等[26]的研究发现氯胺酮可能通过快速降低eEF2 磷酸化水平,去除对BDNF翻译的抑制,快速增加BDNF合成,增强突触应答来实现快速抗抑郁作用。有报道认为[27, 28],BDNF和TrkB同样参与了快速抗抑郁药物氯胺酮的快速起效作用机制。本研究发现急性给药YJ-PE 30 min和24 h后,昆明小鼠海马中的BDNF和TrkB蛋白表达明显升高。神经营养因子表达的增加可通过提高神经可塑性而产生抗抑郁作用[29]。因此,YJ-PE可能通过快速增加BDNF及其特异性受体TrkB的表达来快速增加神经营养以及神经可塑性,从而起到快速抗抑郁的作用。
本研究结果提示,YJ-PE快速抗抑郁的量效关系可能与越鞠丸醇提物相似,具有一个较为狭窄的快速抗抑郁有效剂量范围[6]。但其有效剂量范围有所不同。这种特殊的有效剂量依赖性背后的物质基础和机制值得进一步研究,以拓展该方剂的临床应用,夯实后续药物开发的基础。
(致谢:本文实验在南京中医药大学基础医学院转化系统生物学与神经科学研究中心与中医脑病重点实验室完成,特此致谢。)
| [1] | 中华医学会.抑郁障碍防治指南(2007)[B].北京大学医学出版社,2007,6:3-5,11-24. Chinese Medical Association. Guidelines for the prevention and treatment of depressive disorder (2007)[B].Peking University Press.2007,6:3-5,11-24.10-15 |
| [2] | Kessler R C, Berglund P, Demler O, et al. The epidemiology of major depressive disorder:results from the National Comorbidity Survey Replication (NCS-R)[J]. Jama, 2003,289(23):3095-105. |
| [3] | Trivedi M H, Rush A J, Wisniewski S R, et al. Evaluation of outcomes with citalopram for depression using measurement-based care in STAR* D:implications for clinical practice[J]. American J Psychiatry, 2006,163(1):28-40. |
| [4] | Brunoni A R, Teng C T, Correa C, et al. Neuromodulation approaches for the treatment of major depression:challenges and recommendations from a working group meeting[J]. Arq Neuro Psiquiatr, 2010,68(3):433-51. |
| [5] | Fava M. Diagnosis and definition of treatment-resistant depression[J]. Biological Psychiatry, 2003,53(8):649-59. |
| [6] | Xue W, Zhou X, Yi N, et al. Yueju pill rapidly induces antidepressant-like effects and acutely enhances BDNF expression in mouse brain[J]. Evid Based Complement Alternat Med, 2013,2013:184367. |
| [7] | Wei X H, Cheng X M, Shen J S, et al. Antidepressant effect of Yueju-Wan ethanol extract and its fractions in mice models of despair[J]. J Ethnopharmacol, 2008,117(2):339-44. |
| [8] | 张若曦,朱维莉,陆林.氯胺酮抗抑郁作用快速起效机制及发展前景[J].中国药物依赖性杂志, 2012,21(4):249-52.Zhang R X,Zhu W L,Lu L.The develoment prospects and rapid antidepressant mechanism of ketamine[J].Chin J Drug Depend, 2012,21(4):249-52. |
| [9] | Autry A E, Adachi M, Nosyreva E, et al. NMDA receptor blockade at rest triggers rapid behavioural antidepressant responses[J]. Nature, 2011,475(7354):91-5. |
| [10] | Li N, Lee B, Liu R J, et al. mTOR-dependent synapse formation underlies the rapid antidepressant effects of NMDA antagonists[J]. Science, 2010,329(5994):959-64. |
| [11] | Duman R S, Li N, Liu R J, et al. Signaling pathways underlying the rapid antidepressant actions of ketamine[J]. Neuropharmacology, 2012,62(1):35-41. |
| [12] | Wang C, Zheng D, Xu J, et al. Brain damages in ketamine addicts as revealed by magnetic resonance imaging[J]. Front Neuroanat, 2013,7:23. |
| [13] | Kalsi S S, Wood D M, Dargan P I. The epidemiology and patterns of acute and chronic toxicity associated with recreational ketamine use[J]. Emerg Health Threats,2011,4:7107. |
| [14] | 李志文.越鞠丸的临床应用[J].吉林中医药,1984,(3):22-3. Li Z W. The clinical usage of Yueju pill[J].Jilin J Tradit Chin Med,1984,(3):22-3. |
| [15] | 何健纯.古方越鞠丸之临床运用[J].吉林中医药,1995,(3):32. He J C. The clinical applications of an ancient formula,Yueju pill[J].Jilin J Tradit Chin Med, 1995,(3):32. |
| [16] | 吴登山. 高辉远.活用越鞠丸的临床经验[J].中国中医药信息杂志, 2001,8(3):71-71. Wu D S,Gao H Y. The clinical experience of applicating Yueju pill[J]. Chin J Inform TCM, 2001,8(3):71-71. |
| [17] | 夏宝妹,张海楼,薛文达,等. 产后抑郁小鼠模型的构建及越鞠甘麦大枣汤对其抑郁样行为的影响[J].中国药理学通报,2015,31(9):1324-8. Xia B M, Zhang H L,Xue W D, et al.Postpartum depression animal model in mice and effect of Yuejuganmaidazaotang on PPD model[J]. Chin Pharmacol Bull, 2015,31(9):1324-8. |
| [18] | Cryan J F, Mombereau C,Vassout A.The tail suspension test as a model for assessing antidepressant activity:review of pharmacological and genetic studies in mice[J], Neurosc Biobeh Rev, 2005,29(4-5):571-625. |
| [19] | Cryan J F, Holmes A. The ascent of mouse:advances in modelling human depression and anxiety[J]. Nat Rev Drug Discov,2005, 4(9):775-90. |
| [20] | 孙秀萍,李腾飞,石哲,等.人参总皂苷和远志总苷配伍对小鼠抗抑郁作用[J].中国比较医学杂志,2012,22(6):30-6. Sun X P,Li T F,Shi Z,et al.Study of antidepressant-like effects of combination of ginseng total saponins and polygala tenuifolia total glycosiders in mice[J]. Chin J Compar Med, 2012,22(6):30-6. |
| [21] | 李宝莉, 陈雅慧, 杨暄, 等. 栀子油的提取和对中枢神经系统的作用[J].第四军医大学学报, 2008,29(23):2152-5. Li B L,Chen Y H,Yang X,et al.Extraction technology of gardenia oil and its effect on central nerve system[J].J Fourth Mil Med Univ,2008,29(23):2152-5. |
| [22] | 郑琴,伍振峰,邱玲玲,等.大川芎方中川芎提取纯化工艺及其镇静镇痛作用[J].中国实验方剂学杂志,2011,17(15):6-9 Zhang Q F,Wu Z F,Qiu L L,et al.Analgesic effect and extraction,purification procedure of ligusticum chuanxiong from dachuanxiong fang[J].Chin J ETMF,2011,17(15):6-9. |
| [23] | 邓颖,张春虎,张海男,等.柴胡疏肝散对抑郁模型大鼠海马、杏仁核、额叶BDNF及其受体TrKB的影响[J].中国中西医结合杂志,2011,31(10):1373-8. Deng Y,Zhang C H,Zhang H N, et al.Effects of chaihu shugan power on the behavior and expression of BDNF and TrkB in the hippocampus,amygdala,and the frontal lobe in rat model of depression[J].Chin J Integr Med, 2011,31(10):1373-8. |
| [24] | Jacobsen J P, Mork A. The effect of escitalopram, desipramine, electroconvulsive seizures and lithium on brain-derived neurotrophic factor mRNA and protein expression in the rat brain and the correlation to 5-HT and 5-HIAA levels[J].Brain Res,2004,1024(1-2):183-92. |
| [25] | 李岩,陈俊逾,伊琦忠.抑郁症大鼠模型海马区及前额叶组织BDNF因子、Trkb蛋白表达的实验研究[J].中国医药导刊, 2015, 17(1):94-8. Li Y,Chen J Y,Yi Q Z.Experiments study on expression of BDNF factor and protein Trkb in hippocampus and prefrontal cortex tissue of depression in model rats[J].Chin J Med Guide, 2015,17(1):94-8. |
| [26] | Autry A E,Adachi M,Nosyreva E,et al.NMDA receptor blockade at rest triggers rapid behavioural antidepressant responses[J].Nature, 2011,475:91-5. |
| [27] | Autry A E, Monteggia L M. Brain-derived neurotrophic factor and neuropsychiatric disorders[J].Pharmacol Rev,2012,64(2):238-58. |
| [28] | Duman R S, Aghajanian G K. Neurobiology of rapid acting antidepressants:role of BDNF and GSK-3β[J].Neuropsychopharmacology,2014,39(1):233. |
| [29] | 奚耕思,张武会.抑郁症发生机制研究进展[J].陕西师范大学学报, 2011,39(6):64-71. Xi G S,Zhang W H. Research advances on mechanisms of depression[J].J Shaanxi Normal Univ, 2011,39(6):64-71. |

