安全壳作为核电站辐射防护的最后一道屏障,对核电站附近环境及人员安全至关重要。在核电站发生严重事故情况下,安全壳过滤排放系统能够保障安全壳的完整性,从而避免放射性物质对核电站周围环境及人员造成的危害。在过滤排放系统中应用的鼓泡技术能够有效去除放射性气体和气溶胶颗粒。尤其对较难去除的甲基碘气体,鼓泡式过滤器具有较高的过滤效率[1-2]。安全壳过滤排放系统中鼓泡技术的应用条件与其他行业有所不同,滞留在液相中的放射性物质所产生的衰变热会使气泡表面液相出现蒸发现象。在鼓泡式过滤器内,当待过滤的放射性气体从气泡内部向液相环境迁移时,需穿过因气泡表面蒸发而向气泡内部扩散的蒸汽,因此会影响对放射性气体的去除。温济铭等[3-4]实验研究结果表明,蒸发过程具有降低鼓泡除甲基碘去除效率的效果。孙长贵等[5]采用准稳态方法对热液相介质中气泡内的传热和传质过程构建了数学模型,并分析气泡表面液膜蒸发对溶质结晶现象的影响。聂永丰等[6]从分子动力学角度构建高温废气导致蒸发过程的传热传质模型,并分析蒸发现象对气泡尺寸、气泡上升速度等特征参数的影响。Colombet等[7]通过数值求解N-S方程、对流扩散方程及连续性方程,分析Re和Pe对气泡内气体向液相迁移速率的影响。关于气泡表面液相蒸发的研究主要关于伴随蒸发的传热过程及蒸汽组分的传质过程,而针对气泡表面蒸发现象同鼓泡除气过程关系的研究未见公开报道。
放射性甲基碘气体对人体的危害较大且与水洗液反应速率缓慢而难于去除[8-9],本文将甲基碘气体选为鼓泡除气对象进行建模研究。由于气泡表面液膜蒸发及气泡内气体温度的下降,气泡尺寸时刻在变化,因而对鼓泡除气过程的数值计算属于非固定计算域的求解问题。本文对鼓泡除气和蒸发过程的控制方程进行无量纲处理,并根据数值计算结果分析蒸发现象对气泡尺寸、气泡表面处甲基碘浓度、气泡收缩速度的影响,进而分析蒸发对鼓泡除气效率的影响规律及影响机理。
1 理论模型及网格无关性验证为了便于计算,本文作如下假设:1)气泡形状为球形,气泡内部无循环流动;2)初始时刻,气泡内不存在甲基碘浓度梯度及温度梯度;3)初始时刻,气泡表面处的气体温度与液相温度相同;4)气泡内气体压力与周围液相压力相同。
在上述假设基础上,参考Lage等[10]及Lage[11]的研究结果,建立气泡中多组分混合气体的质量、能量、各组份浓度守恒方程和相应的边界条件。为实现对气泡动边界问题进行求解,本文采用与Lage等[11]相近的无量纲化方法对控制方程和边界条件进行处理。
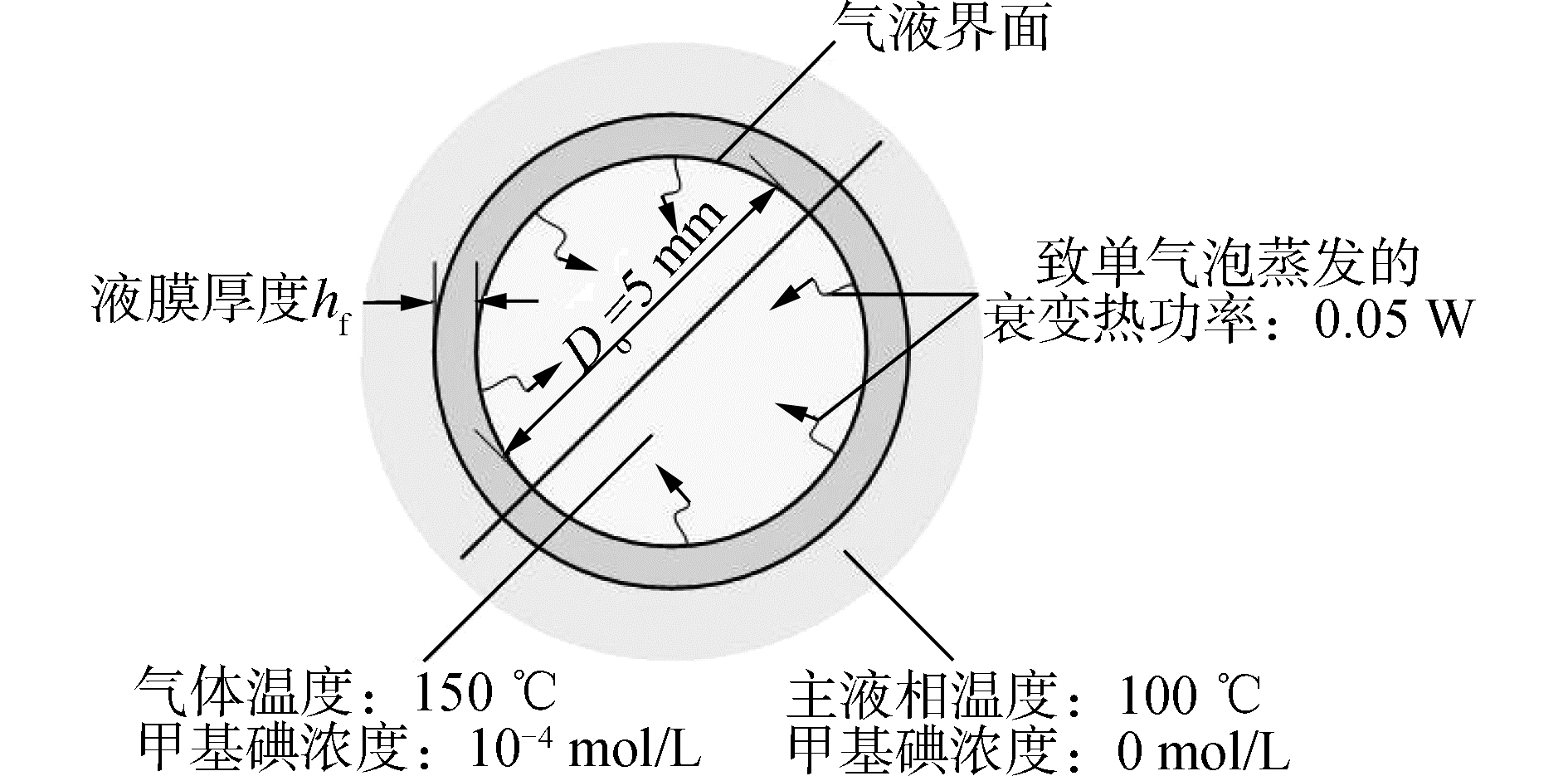
计算模型中气泡初始时刻状态如图 1所示,根据鼓泡式过滤器应用条件[1, 12]和Sauter平均直径、含气率等参数的计算关系式[13-14],气泡的初始直径设定为5 mm,所对应的衰变热功率为0.05 W。安全壳过滤排放系统投入运行的绝对压强为0.6 MPa左右,相应的排放气体初始温度为150 ℃[12]。为避免溶液中甲基碘与其他溶质的化学反应速率变化对除气过程产生干扰,将主液相中甲基碘浓度按0 mol/L处理。由于实际应用中甲基碘浓度较小[1],初始时刻气泡内甲基碘浓度为1×10-4 mol/L,并忽略甲基碘气体对混合气体物性参数的影响。
|
Download:
|
| 图 1 初始参数设定示意图 Fig. 1 The sketch map of setting initial parameters | |
采用IAPWS IF-97模型计算蒸汽物性参数,使用理想气体状态方程计算空气密度。由气体的比定压热容的直线关系式可以得到空气定压比热容Cp随温度的变化关系如式(1)所示。
| $ {\mathit{C}_\mathit{p}}{\rm{ = 99}}{\rm{.56 + 0}}{\rm{.093}}\mathit{t} $ | (1) |
利用线性回归方法对已有的空气导热系数λ进行拟合,得到拟合公式(2)。
| $ \lambda = 0.000\;067t + 0.025\;581 $ | (2) |
在80~300 ℃范围内,式(1)、式(2)拟合精度较高。
甲基碘在液相中的扩散系数由WILKE-CHANG式[15-16]计算得到:
| $ {D_1} = 7.4 \times {10^{ - 8}}{\left( {\beta {M_3}} \right)^{1/2}}T/\left( {{\mu _3}V_1^\prime } \right) $ | (3) |
式中:β为缔合因子;T为液相温度;μ3为液相动力粘度;V1为甲基碘在正常测点下的分子体积;M3为分子量。
甲基碘和蒸汽在气相中的扩散系数采用FULLER关联式计算[17]:
| $ {D_2} = \frac{{{{10}^{ - 7}}{T^{1.75}}\left( {1/{M_1} + 1/{M_2}} \right)}}{{p{{\left[ {{{\left( {\mathit{\Sigma }{V_1}} \right)}^{1/3}} + {{\left( {\mathit{\Sigma }{V_2}} \right)}^{1/3}}} \right]}^2}}} $ | (4) |
式中:M1、M2为甲基碘气体蒸汽的分子量;P为气体总压强。
甲基碘从气泡内部向液相迁移的过程中在气液界面发生溶解,由于甲基碘在液相中的溶解浓度较低,因而甲基碘溶液属于稀溶液,符合亨利定律使用条件。Adachi等[18]得到亨利系数和温度的关系为:
| $ {K_c} = 1.69 \times {10^{ - 5}}\exp \left( {\frac{{7\;200}}{{RT}}} \right) $ | (5) |
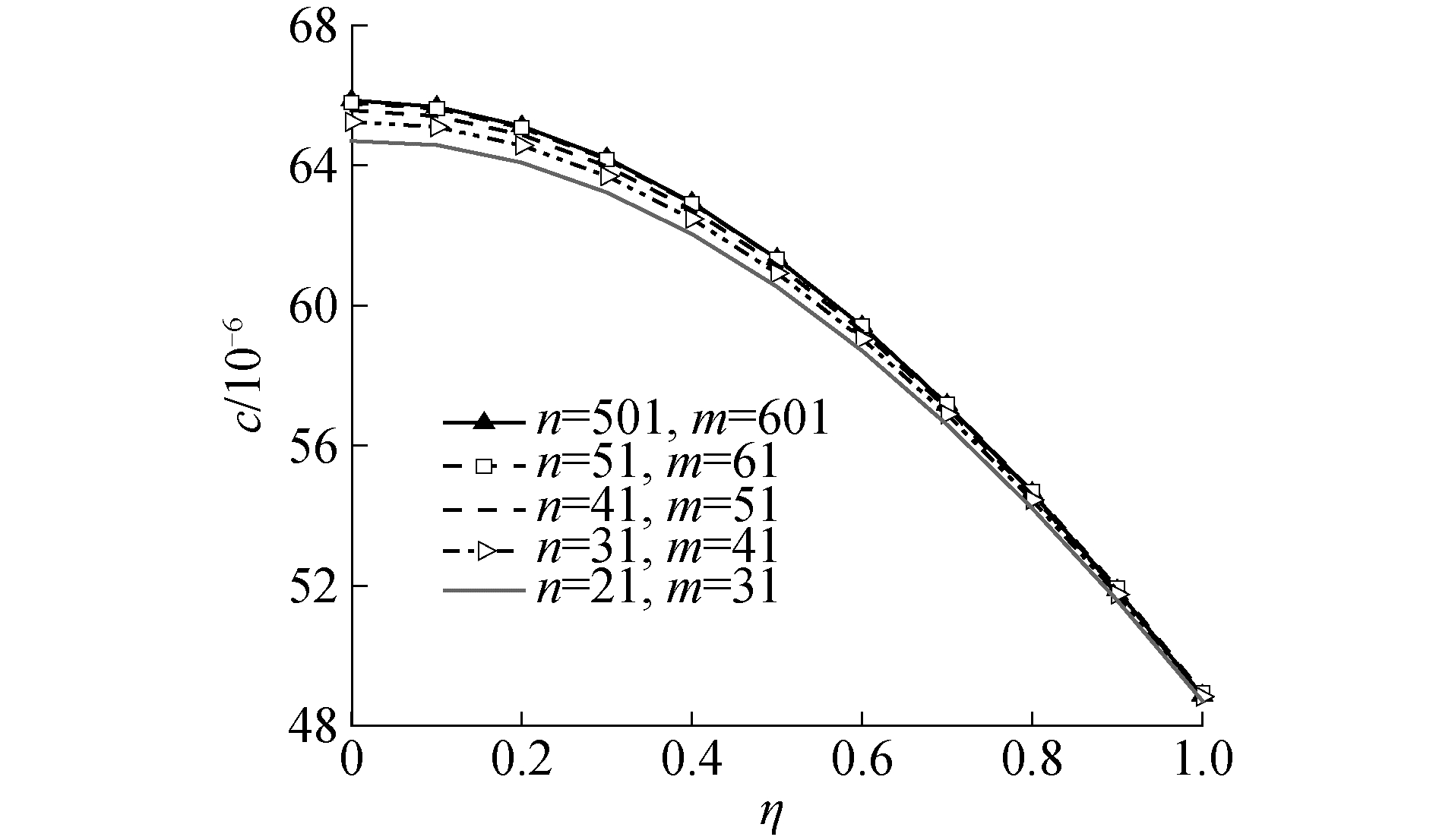
图 2为模型网格无关性验证结果,将气泡生成时间为1.5 s时的甲基碘浓度场c作为分析对象,η为无量纲径向位置。如图 2所示,当空间节点数目和时间步长数目分别达到500和600时,空间网格疏密程度和时间步长大小对计算结果基本没有影响。
|
Download:
|
| 图 2 网格无关性验证结果 Fig. 2 The results of independence verification on grids | |
本文使用去除因子表征鼓泡除气效率,即τ时刻气泡去除因子e(τ)定义为初始时刻气泡内甲基碘的总量ct与该时刻气泡内甲基碘的总量ct(τ)之比:
| $ e(\tau ) = \frac{{{c_t}}}{{{c_t}(\tau )}} $ | (6) |
根据模型计算结果分析蒸发过程对甲基碘去除因子的影响,如图 3所示,随着气泡在液相中的滞留时间增加,气泡内甲基碘含量逐渐降低,鼓泡除气的去除因子随之增加。存在蒸发过程的鼓泡去除因子明显低于不存在蒸发过程的鼓泡去除因子。

|
Download:
|
| 图 3 蒸发对甲基碘去除因子影响 Fig. 3 The influence of methyl iodide on the decontamination factor for methyl iodide | |
气泡内气体在由气相向液相迁移过程中,气泡表面附近存在液相浓度边界层。浓度边界层内的传质速率主要由边界层两侧浓度差值及边界层厚度决定,而浓度边界层厚度受液相粘性、气泡上升速度hf等因素影响。浓度边界层厚度与气泡的上升速度和气泡尺寸相关,一般认为该厚度与Pe-1/2dvs成正比且远小于气泡表面的液相速度边界层[19-20],但目前尚未有计算浓度边界层厚度的关系式。如图 4所示,甲基碘去除因子随着液膜厚度减薄而明显提升。在对其他因素进行计算分析时,将浓度边界层厚度统一为10 μm。

|
Download:
|
| 图 4 甲基碘去除因子与液膜厚度的关系 Fig. 4 The relationship of decontamination factor for methyl iodide and liquid film thickness | |
如图 5所示,当气泡在液相中的滞留时间相同时,含有液膜蒸发现象的气泡内剩余的甲基碘总量要明显高于不存在蒸发现象的气泡内剩余的甲基碘总量。随着气泡在液相中滞留时间增加,有无蒸发过程所导致气泡内甲基碘浓度分布的差值逐渐增大。导致该现象出现的原因主要有2个:首先,气泡表面蒸发产生的蒸汽向气泡内部的迁移过程与甲基碘气体向气泡表面迁移过程方向相反,蒸汽迁移过程增加了甲基碘气体向气泡表面迁移过程的阻力,从而导致气泡表面附近的甲基碘浓度沿径向的下降速度加快;其次,气泡表面蒸发产生的蒸汽稀释了气泡表面处的甲基碘气体浓度,降低了气液界面处甲基碘的饱和溶解浓度,进而造成液膜两侧浓度差值的下降。

|
Download:
|
| 图 5 蒸发对甲基碘浓度场分布影响 Fig. 5 The influence of evaporation on methyl iodide concentration distribution | |
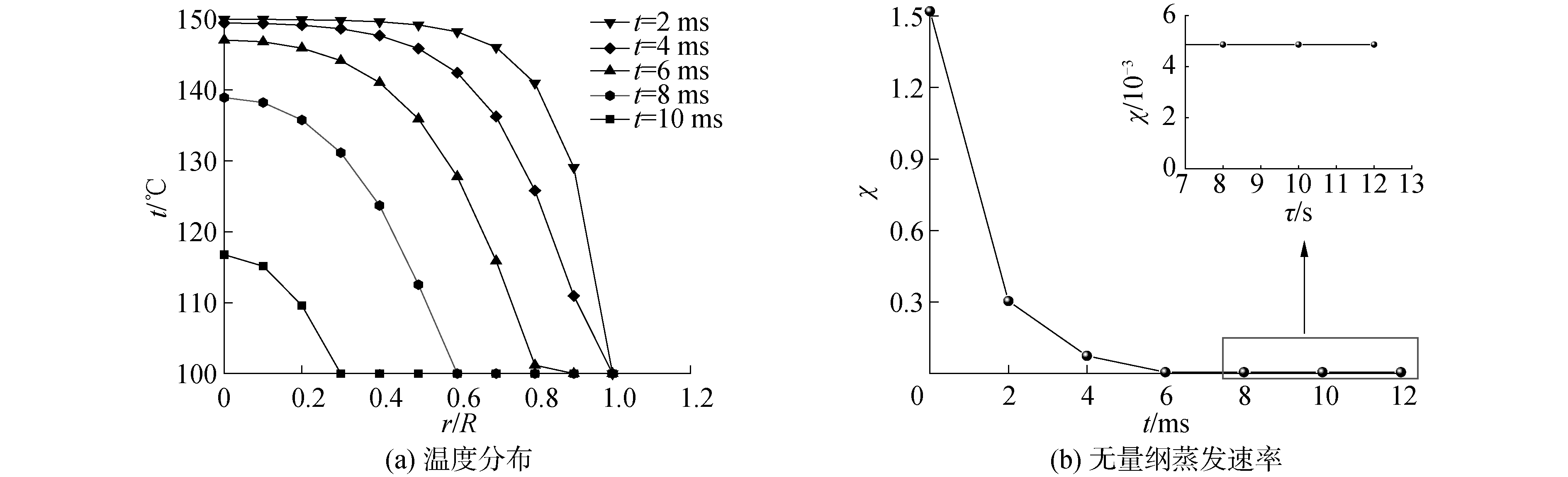
蒸发过程对气泡表面处甲基碘浓度的影响主要是蒸发产生的蒸汽会改变原有的气体组分份额。图 6所示为气泡温度分布随气泡滞留时间的变化关系,气泡刚生成时,气泡内主体温度基本与初始温度相同,仅在气泡边界处附近存在较明显的温度下降。当气泡生成0.01 s后,气泡内大部分区域温度与液相温度达到平衡。如图 7所示,在气泡刚形成的时刻,衰变热和气体显热共同产生的蒸汽会大量聚集在气泡边界,并形成较高的蒸汽份额。随着气体温度的快速下降,气泡表面的蒸发速率也随之迅速下降并稳定在一个较低水平上。
|
Download:
|
| 图 6 各特征参数随气泡生成时间的变化 Fig. 6 Variation of different parameters with bubble formation time | |

|
Download:
|
| 图 7 气泡边界处的蒸汽份额随气泡生成时间的变化 Fig. 7 Variation of evaporation concentration at bubble surface with bubble formation time | |
如图 7所示,气泡表面的蒸汽份额与气体温度和蒸发速率随时间的变化相对应。在气泡形成的初始阶段,气温较高,蒸发速率较大,蒸汽份额快速升高。随着蒸发速率快速降低,蒸发产生蒸汽的速率低于蒸汽向气泡内部迁移的速率,气泡表面的蒸汽份额也快速降低。在液膜蒸发速率稳定后,近气泡表面处的蒸汽份额开缓慢增加。
由以上分析可知,气泡显热仅在气泡刚生成的极短时间内对气泡表面处的甲基碘浓度产生影响,进而对鼓泡除气效率产生影响。当气泡温度与液相温度达到平衡后,液膜蒸发速率所需热量均是由衰变热提供。因此,衰变热所致的蒸发会对气泡除气过程有长期的影响。
由衰变热产生的蒸汽会降低甲基碘浓度,气液界面液膜侧的平衡浓度也会随之减小。从而导致气泡表面液膜两侧的甲基碘浓度差值降低,鼓泡去除因子减小。因此,蒸发速率大小会对鼓泡除气过程产生影响。如图 8所示,随着衰变热功率增大鼓泡除气效率降低。随着气泡在液相停留时间的增加,衰变热功率的影响变得更加明显。

|
Download:
|
| 图 8 衰变热功率对甲基碘去除因子影响 Fig. 8 The influence of decay heat power on the decontamination factor for methyl iodide | |
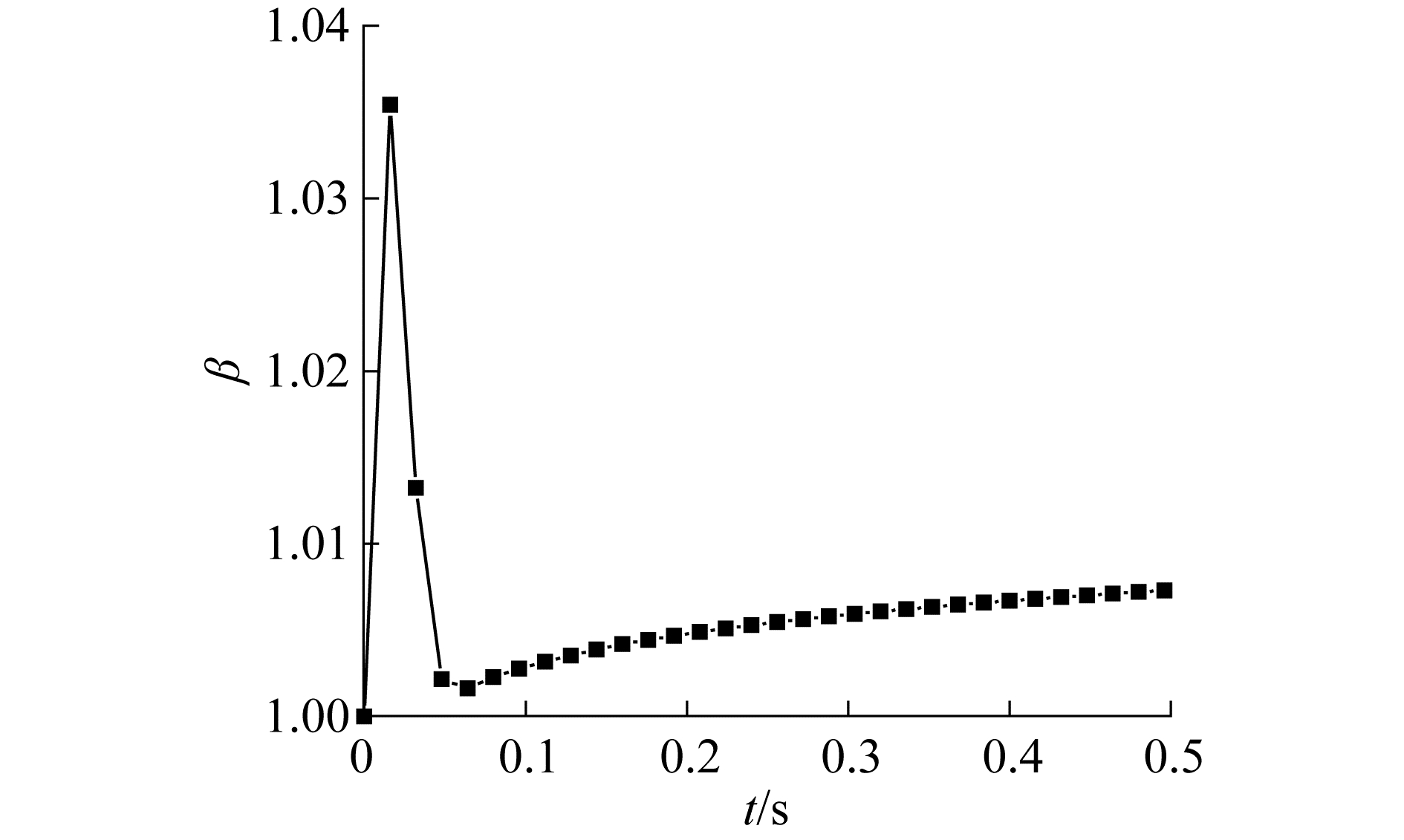
气泡尺寸决定了气泡传质面积相对于气泡体积的比值,同等气量下,小气泡能够提供更多的气液交界面面积[13]。图 9所示为气泡尺寸β和时间的关系,在气泡刚生成时,气体显热导致蒸发产生的蒸汽会使得气泡尺寸有所增加。随着气体温度下降,气泡收缩,气泡体积减小。在气泡内温度与液相温度达到平衡后,衰变热导致的蒸发现象使气泡尺寸增长。整体而言,气泡尺寸在一个很小的范围内发生变化,因而可以忽略由蒸发导致的气泡尺寸变化对鼓泡除气效率的影响。
|
Download:
|
| 图 9 气泡无量纲直径随气泡生成时间的变化 Fig. 9 Variation of dimensionless bubble diameter with bubble formation time | |
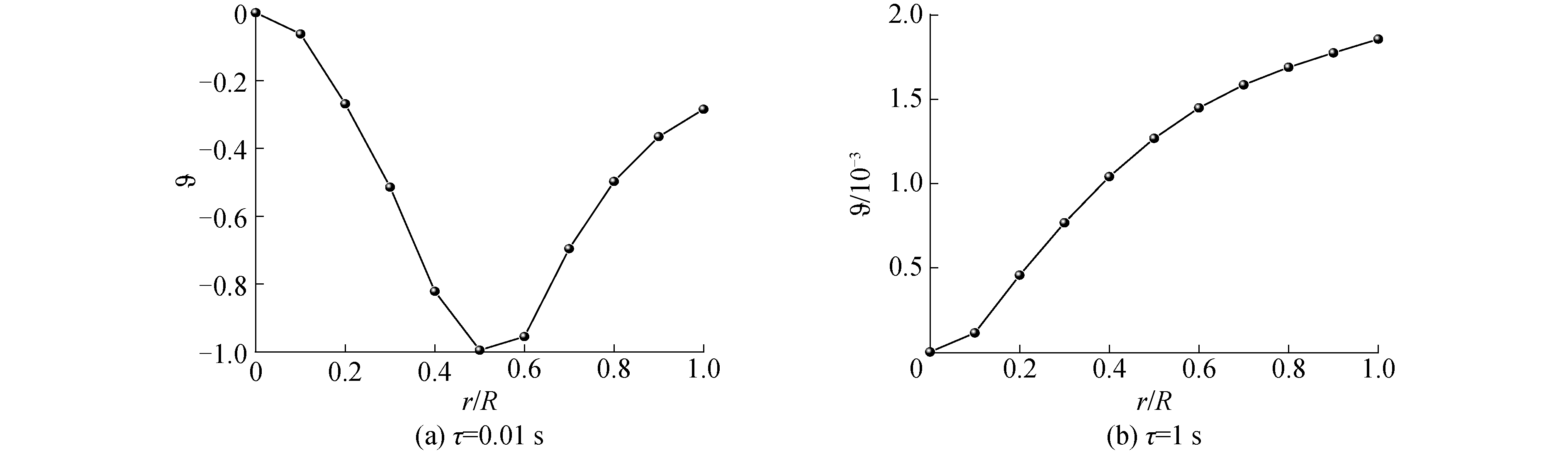
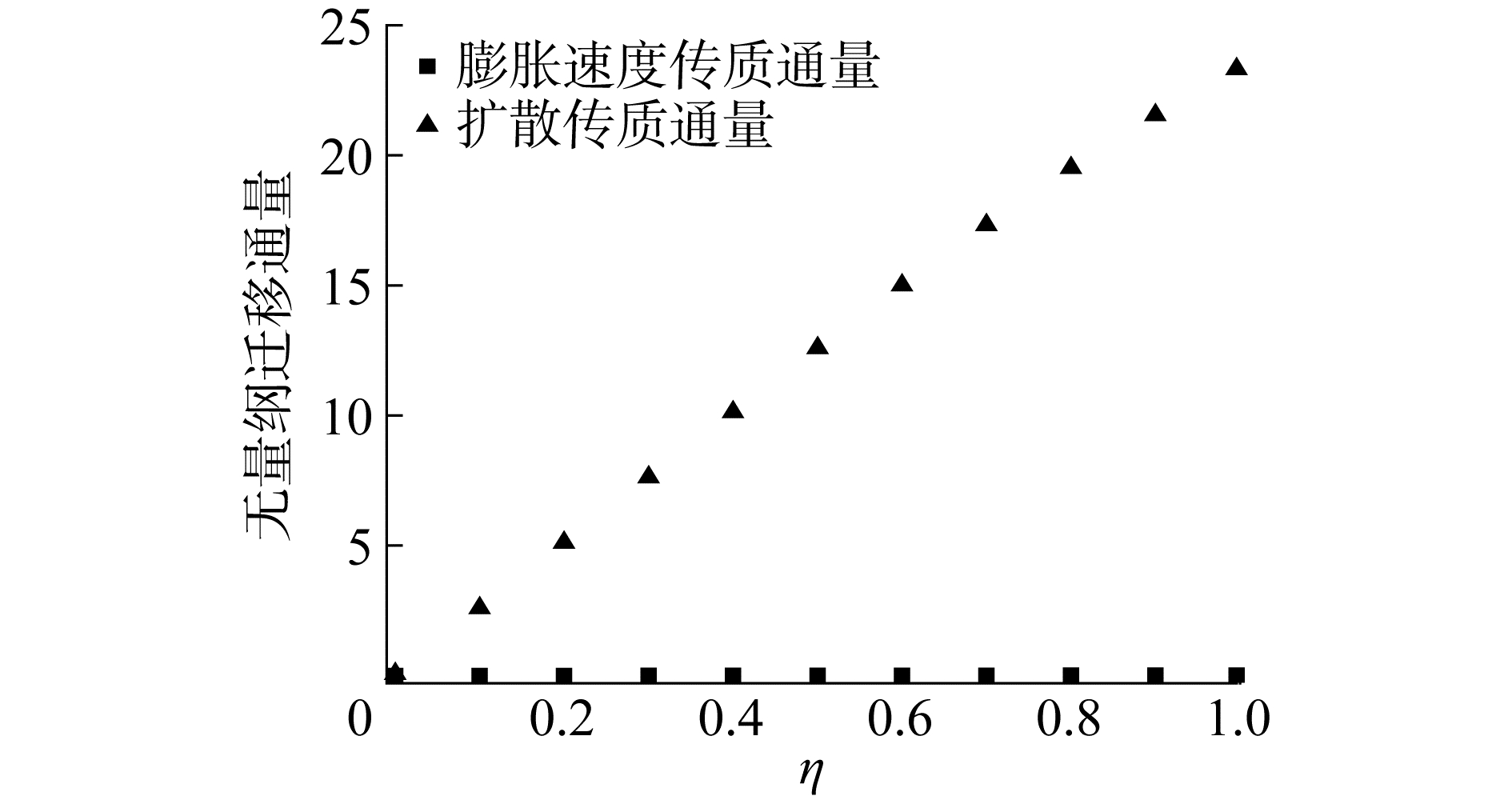
气泡膨胀(收缩)速度会对甲基碘气体由气泡内部向气泡表面处的迁移过程产生影响。如图 10所示,气泡内温度刚同液相温度达到平衡时,气体降温造成的气泡收缩过程还在继续。此时,气泡收缩速度具有从中心到表面的累积效应,因而气泡收缩速度从中心向表面逐渐增大。但液膜蒸发产生的蒸汽延缓了气泡的收缩趋势。所以收缩速度的极大值出现在气泡中心和表面之间的位置。当τ=1 ms时,由气泡降温引起的气泡收缩过程已结束,气泡表面的持续蒸发导致气泡开始膨胀。当无量纲速度g为正时,气泡膨胀过程与扩散过程对甲基碘气体由气泡内部向气泡表面处的迁移均起到促进作用。但从图 11可以看出,η带来的甲基碘迁移通量远小于扩散过程所造成的迁移通量,二者相差2个量级。因此,可以忽略气泡膨胀对鼓泡除气过程的促进作用。
|
Download:
|
| 图 10 不同时刻下气泡无量纲速度分布 Fig. 10 The dimensionless bubble velocity distribution at different bubble formation times | |
|
Download:
|
| 图 11 甲基碘无量纲迁移通量径向分布 Fig. 11 The radial distribution of dimensionless migration flux | |
1) 气泡表面液膜蒸发过程会明显降低鼓泡式过滤器对甲基碘的去除因子,且蒸发对鼓泡去除因子的影响随着气泡在液相滞留时间的增长而变大。
2) 液膜蒸发由气体显热和衰变热所导致,气泡内的气体显热仅在气泡刚生成的0.1 s内对液膜蒸发具有贡献作用。因此,减弱鼓泡除气效果的蒸发过程主要为由衰变热引起的蒸发过程。
3) 气体由气泡内部向液相迁移的主要阻力在气泡表面的液膜侧,蒸发过程削弱鼓泡除气能力的主要原因是蒸发产生的蒸汽稀释了气泡表面处的甲基碘气体浓度,从而减小了气泡表面液膜内的甲基碘平衡浓度。
4) 由于蒸发导致气泡尺寸增加的幅度较小,可以忽略蒸发现象所导致的气泡直径增大对鼓泡去污因子的影响。衰变热导致的蒸发会造成气泡持续膨胀,相比于扩散传质过程,气泡膨胀对由气泡内部向气泡表面的气体迁移通量的影响可以忽略。
| [1] |
OECD/NEA/CSNI. Status report on filtered containment venting[R]. Paris: OECD/NEA/CSNI, 2014.
(  0) 0)
|
| [2] |
汤华鹏, 温济铭, 谷海峰. 基于高速摄影测量气泡体积的图像处理技术研究[J]. 应用科技, 2019, 46(2): 108-115. TANG Huapeng, WEN Jiming, GU Haifeng. Study on image processing technique for bubble volume based on high speed camera[J]. Applied science and technology, 2019, 46(2): 108-115. (  0) 0)
|
| [3] |
WEN Jiming, SUN Zhongning, GU Haifeng, et al. Experimental study on decontamination factor of methyl iodide by bubbling[C]//Proceedings of 2016 International Conference on Nuclear Engineering. Charlotte, North Carolina, USA, 2016: V004T11A006.
(  0) 0)
|
| [4] |
WEN Jiming, GU Haifeng, SUN Zhongning, et al. A theoretical model and experiment validation on filtration characteristics of methyl iodide in bubble column[J]. International journal of heat and mass transfer, 2017, 114: 1263-1273. DOI:10.1016/j.ijheatmasstransfer.2017.07.023 (  0) 0)
|
| [5] |
孙长贵, 徐维勤, 沈自求. 气泡在热液相介质中上升时的传热与传质[J]. 高校化学工程学报, 1992, 6(2): 139-146. SUN Changgui, XU Weiqin, SHEN Ziqiu. Heat and mass transfer of rising bubble in hot liquid medium[J]. Journal of chemical engineering of Chinese universities, 1992, 6(2): 139-146. (  0) 0)
|
| [6] |
聂永丰, 岳东北, 许玉东, 等. 浸没燃烧蒸发过程单个气泡传热传质模型[J]. 清华大学学报(自然科学版), 2005, 45(9): 1221-1224. NIE Yongfeng, YUE Dongbei, XU Yudong, et al. Heat and mass transfer modeling of a single bubble during submerged combustion evaporation[J]. Journal of Tsinghua University (science and technology), 2005, 45(9): 1221-1224. (  0) 0)
|
| [7] |
COLOMBET D, LEGENDRE D, COCKX A, et al. Mass or heat transfer inside a spherical gas bubble at low to moderate Reynolds number[J]. International journal of heat and mass transfer, 2013, 67: 1096-1105. DOI:10.1016/j.ijheatmasstransfer.2013.08.069 (  0) 0)
|
| [8] |
刘兆年, 谷海峰. 核电厂退役中低放废物量估算方法研究[J]. 应用科技, 2017, 44(3): 78-81. LIU Zhaonian, GU Haifeng. Method study of computing low-intermediate level radwaste during NPP decommissioning[J]. Applied science and technology, 2017, 44(3): 78-81. (  0) 0)
|
| [9] |
BRUCHERTSEIFER G, VENZ H, WALLIMANN F. A novel process for efficient retention of volatile iodine species in aqueous solutions during reactor accidents. 2009.
(  0) 0)
|
| [10] |
KUO K K Y. Principles of combustion[M]. New York: Wiley, 1986.
(  0) 0)
|
| [11] |
CAMPOS F B, LAGE P L C. Simultaneous heat and mass transfer during the ascension of superheated bubbles[J]. International journal of heat and mass transfer, 2000, 43(2): 179-189. DOI:10.1016/S0017-9310(99)00143-X (  0) 0)
|
| [12] |
NA Y S, HA K S, PARK R J, et al. Thermal hydraulic issues of containment filtered venting system for a long operating time[J]. Nuclear engineering and technology, 2014, 46(6): 797-802. DOI:10.5516/NET.02.2014.031 (  0) 0)
|
| [13] |
AKITA K, YOSHIDA F. Bubble size, interfacial area, and liquid-phase mass transfer coefficient in bubble columns[J]. Industrial & engineering chemistry process design and development, 1974, 13(1): 84-91. (  0) 0)
|
| [14] |
AKITA K, YOSHIDA F. Gas holdup and volumetric mass transfer coefficient in bubble columns. Effects of liquid properties[J]. Industrial & engineering chemistry process design and development, 1973, 12(1): 76-80. (  0) 0)
|
| [15] |
ISOGAI K M A R. Estimation of molecular diffusivity in liquid phase systems by the Wilke-Chang equation[J]. Journal of chromatography A, 2011(38): 6639-6645. (  0) 0)
|
| [16] |
MIYABE K, ISOGAI R. Estimation of molecular diffusivity in liquid phase systems by the Wilke-Chang equation[J]. Journal of chromatography A, 2011, 1218(38): 6639-6645. DOI:10.1016/j.chroma.2011.07.018 (  0) 0)
|
| [17] |
MIYABE K. Estimation of molecular diffusivity in aqueous solution of acetonitrile by the Wilke-Chang equation[J]. Journal of separation science, 2011, 34(19): 2674-2679. DOI:10.1002/jssc.201100385 (  0) 0)
|
| [18] |
FULLER E N, SCHETTLER P D, GIDDINGS J C. New method for prediction of binary gas-phase diffusion coefficients[J]. Industrial & engineering chemistry, 1966, 58(5): 18-27. (  0) 0)
|
| [19] |
ADACHI M, EGUCHI W, HAOKA T. Dissolution of gaseous methyl iodide into aqueous sodium hydroxide solutions[J]. Journal of nuclear science and technology, 1977, 14(5): 370-375. DOI:10.1080/18811248.1977.9730771 (  0) 0)
|
| [20] |
TAKEMURA F, YABE A. Gas dissolution process of spherical rising gas bubbles[J]. Chemical engineering science, 1998, 53(15): 2691-2699. DOI:10.1016/S0009-2509(98)00094-3 (  0) 0)
|
 2019, Vol. 40
2019, Vol. 40


