扩展功能
文章信息
- 张楠, 刘鹏, 李宗智, 孟德怀, 滕丽微, 刘振生
- ZHANG Nan, LIU Peng, LI Zongzhi, MENG Dehuai, TENG Liwei, LIU Zhensheng
- 基于红外相机技术的贺兰山阿拉善马鹿集群行为研究
- Study on Group Behavior of Cervus elaphus alashanicus in Helan Mountains Based on Infrared Cameras
- 四川动物, 2021, 40(6): 632-639
- Sichuan Journal of Zoology, 2021, 40(6): 632-639
- 10.11984/j.issn.1000-7083.20210039
-
文章历史
- 收稿日期: 2021-02-01
- 接受日期: 2021-08-03
2. 成都大熊猫繁育研究基地, 四川省濒危野生动物保护生物学重点实验室, 成都 610086;
3. 国家林业和草原局野生动物保护学重点实验室, 哈尔滨 150040
2. Chengdu Research Base of Giant Panda, Key Laboratory of Endangered Wildlife Conservation Biology of Sichuan Province, Chengdu 610086, China;
3. Key Laboratory of Wildlife Conservation, State Forestry and Grassland Administration, Harbin 150040, China
集群行为受到国内外学者关注,在生态学研究中扮演着越来越重要的角色(Jarman,1974)。有研究表明,集群行为是指当个体受到环境气候影响、面临捕食风险、食物资源不足,以及个体繁殖期特殊活动等因素影响时,在环境应对、集群大小、资源分配以及繁衍生态等方面表现出不同特征的过程(胡磊,2013)。集群行为对动物的生存繁衍具有重要意义和价值,了解其集群行为可以更好地保护动物。
马鹿Cervus elaphus属鲸偶蹄目Cetartiodactyla鹿科Cervidae鹿属(魏辅文等,2021),广泛分布于北非西北部、欧洲、亚洲和北美(Nowak,1999;张明春等,2012;高惠等,2017),国内分布于黑龙江、内蒙古、河北、新疆等地(高行宜,姚军,2007;刘振生,2009),为我国二级重点保护野生动物(刘振生,2009),国内现存8个亚种(王应祥,2003;李顺才等,2008)。本研究中的马鹿阿拉善亚种Cervus elaphus alashanicus是一个隔离种群(张明春等,2012),在各亚种中分布范围最小、数量最少,仅分布在宁夏自治区贺兰山中部(盛和林,1992;靳勇超,张明海,2012;高惠等,2017),是贺兰山地区主要分布的有蹄类动物(骆颖,2011),也是该地区主要的食草动物,在贺兰山生态系统中具有重要地位。因此,对马鹿阿拉善亚种的保护管理与研究具有重要意义。
目前,红外相机技术是一种广泛运用于野生动物研究的技术(Carthew & Mslater,1991;Cutler & Swann,1999;Swann et al., 2004;Kucera & Barrett,2011),与传统方法(直接观察法、无线电项圈法)相比具有明显优势。因此,本研究利用红外相机技术对贺兰山马鹿阿拉善亚种进行监测,通过监测数据对其集群行为进行研究。
1 研究地概况宁夏贺兰山国家级自然保护区位于宁夏平原与阿拉善高原交界处,以山脊为界,东西坡分属于宁夏回族自治区、内蒙古自治区,海拔一般2 000~3 000 m,最高峰海拔3 556.1 m,位于主分水岭西侧(牛达生,2005)。保护区处于温带半干旱、干旱地区,灾害天气频繁,气温年较差26.0 ℃,年均气温-0.9 ℃,为典型的大陆性气候;年均降水量418.1 mm,季节性变化大。保护区处于我国荒漠区与温带草原区的过渡地带,受自然和社会多重因素的影响,形成了丰富的山地植被类型和地区自然条件,涵盖了多种生境类型。由贺兰山麓到主峰可划分为4个植被垂直带类型:山地草原带(1 400~1 600 m),优势植物为灌木亚菊Ajania fruticulosa与短花针茅Stipa breviflora;山地疏林草原带(1 600~2 000 m),大面积生长着蒙古扁桃Prunus monglica灌丛,大量蒙古草原区系植物与稀疏分布的灰榆Ulmus pumila伴随生长;山地针叶林带(1 900~3 100 m),主要分为油松Pinus tabulaeformis林亚带(1 900~2 350 m)和青海云杉Pinus crassiflia林亚带(2 350~ 3 100 m);亚高山灌丛和草甸带(3 100~3 556 m)位于主峰周围地带,鬼箭锦鸡儿Caragana jubata与毛蕊杯腺柳Salix cupularis等为优势种(狄维忠,1987;郑敬刚,张景光,2006;刘振生等,2009;昶野,2010)。贺兰山动植物资源丰富,是我国北方地区仅有的生物多样性中心,也为我国八大生物多样性中心之一(骆颖,2011)。
2 研究方法 2.1 红外相机架设2014年10月—2015年10月在贺兰山区森林生境内布设红外相机(型号:Ltl Acorn-6210MC)。
利用地理信息系统将贺兰山区划分成1 km×1 km的网格,其中,森林生境占389个网格,按每个网格布设1台的密度布设红外相机。
相机布设前进行充分调查确定相机布设地点,在考虑均匀性原则、海拔梯度因素的基础上,重点在有马鹿活动痕迹的范围内布设(常见痕迹如粪便、足迹、躺卧痕迹、遗落毛发等,常见区域如兽径、饮水点等)。相机间距>300 m,避免重复拍摄。
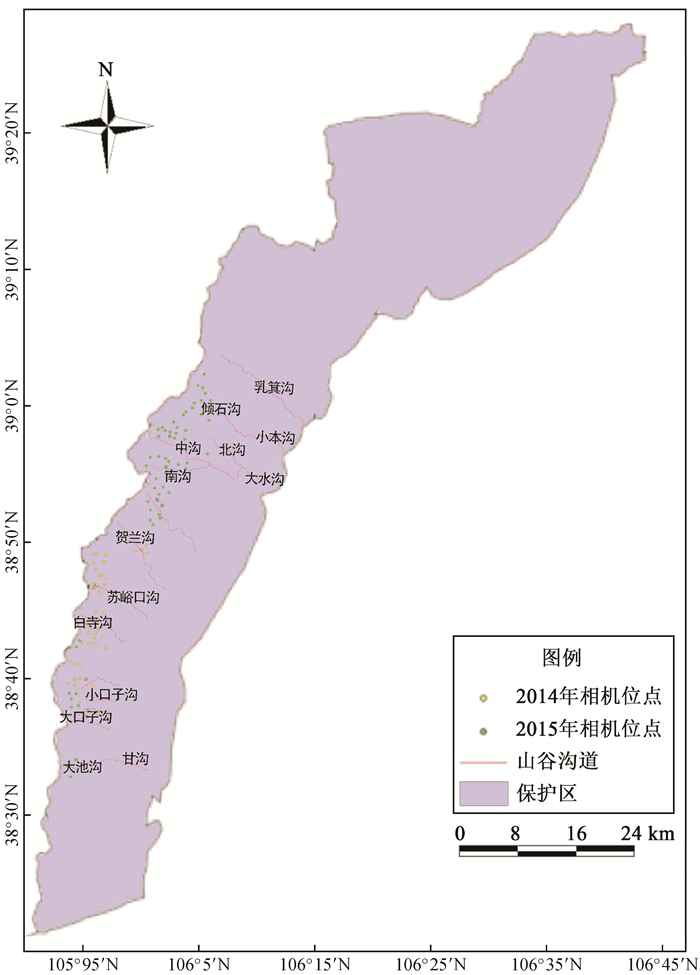
按照抽样强度10%以上的原则,共选择120个红外相机布设位点(图 1),2014年10—12月47台,2015年1—4月18台,4—10月55台,抽样强度30.8%。其中山地草原带20台、山地疏林草原带29台、山地针叶林带54台、亚高山灌丛和草甸带17台。
|
| 图 1 贺兰山国家级自然保护区内的红外相机位点 Fig. 1 Locations of infrared cameras in the Helan Mountains National Nature Reserve |
| |
相机拍摄参数设置为灵敏度中档,24 h工作,设置为每隔1 min拍照2张,录制视频15 s。放置主要位置是树干,距地面50~80 cm,镜头主要对准马鹿活动痕迹的方向,且平行于地面。
相机放置好后,记录相关数据(GPS位点、红外相机的编号、植被类型、架设的时间等)。研究期间,每3个月检查一次相机工作状况,更换电池和内存卡,回收数据,并记录编号。
2.2 数据分析根据贺兰山的气候特征和马鹿食物资源的季节变化特点,将1年分为冷暖2季(4月11日— 10月10日为暖季,10月11日至次年4月10日为冷季)。
仔细筛选所收集视频、图片,首先对个体进行识别,通过角的形态和大小、体型、毛发、有无斑纹等对个体进行划分(表 1)。
| 个体 | 体型 | 鹿角 | 其他划分标准 |
| 成年雄性 | 较大 | 有且明显分叉,脱落后有明显脱落痕迹 | 雄性生殖器 |
| 成年雌性 | 较大 | 无 | 常伴有幼崽 |
| 亚成年 | 较成年小 | 雄性角纤细而不分叉,雌性无 | 无 |
| 幼体 | 小 | 无 | 常跟随雌鹿,当年生的身体两侧有斑状花纹 |
在个体识别基础上,对集群、性别比例进行统计,最后对其集群类型进行划分,根据视频和图片观察结果划分马鹿集群活动(表 2)。
| 集群类型 | 个体数量 | 雌雄分布 | 是否携带幼崽 |
| 单个雄性群 | 1 | 雄性 | 否 |
| 单个雌性群 | 1 | 雌性 | 否 |
| 母仔群 | 1 | 雌性 | 是 |
| 雌性混合群 | 同一样点活动数量≥2 | 雌性 | 否 |
| 雄性混合群 | 同一样点活动数量≥2 | 雄性 | 否 |
| 雌雄混合群 | 同一样点活动数量均≥1 | 雌性、雄性 | 否 |
对相同和相似特征的目标动物只做一次统计(在同一时间段出现的马鹿,根据特征仔细对比,避免重复),对无法区分性别、成幼的数据不作统计。
使用SPSS 20.0对数据进行分析处理及绘图,采用卡方检验检测不同集群类型出现的频次差异以及频次的季节差异、不同集群类型集群平均大小的季节差异,采用K个独立样本的Kruskal-Wallis H检验对不同集群大小的季节差异和不同集群类型大小的季节差异进行分析。
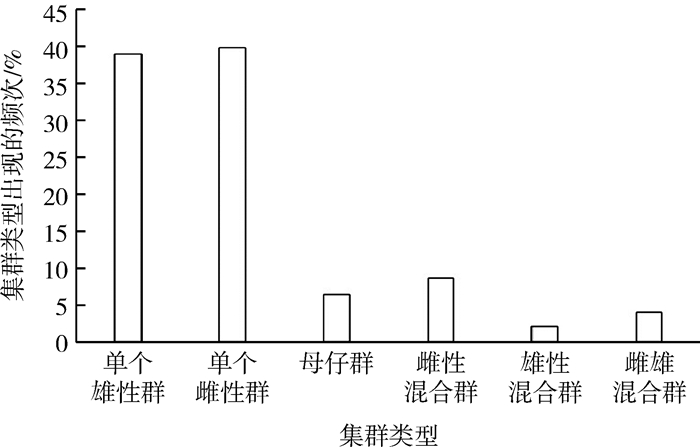
3 研究结果 3.1 集群类型出现频次的分布红外相机监测数据共筛选出可识别的马鹿图像579群次,810只次,平均集群数量为1.40只±1.04只,最大集群数量为11只。对马鹿群体类型进行划分:单个雄性群226群(39.03%),226只次;单个雌性群231群(39.90%),231只次;母仔群37群(6.39%),92只次;雌性混合群50群(8.64%),139只次;雄性混合群12群(2.07%),44只次;雌雄混合群23群(3.97%),78只次(图 2)。卡方检验表明,不同集群类型出现的频次差异极显著(χ2=550.32,df=5,P < 0.001)。
|
| 图 2 马鹿阿拉善亚种不同集群类型出现频次的变化 Fig. 2 Frequency variation of different group types of Cervus elaphus alashanicus |
| |
不同集群类型出现频次的季节变化分析显示(图 3),暖季单个雌性群出现频次最高,冷季单个雄性群最高,2个季节单个雄性群、单个雄性群出现的频次都要高于其他集群类型。雄性混合群在2个季节出现的频次均最低。母仔群、雌性混合群的出现频次在冷季均高于暖季,雌雄混合群、雄性混合群的出现频次在暖季均高于冷季。卡方检验表明,不同集群类型出现频次的季节间差异极显著(χ2=22.96,df=5,P < 0.001)。

|
| 图 3 马鹿阿拉善亚种不同集群类型频次的季节变化 Fig. 3 Seasonal variation of the frequency of different group types of Cervus elaphus alashanicus |
| |
冷季共识别出马鹿292群次,群平均大小1.35只±0.92只(1~7只);暖季287群,群平均大小1.45只±1.15只(1~11只)。集群大小多为1~2只,出现的频次可占到各季节集群总数的90%(图 4)。Kruskal-Wallis H检验表明,不同季节的集群大小差异显著(χ2=4.94,df=1,P < 0.05)。

|
| 图 4 马鹿阿拉善亚种不同集群大小频次的季节变化 Fig. 4 Seasonal variation of group size frequency of Cervus elaphus alashanicus |
| |
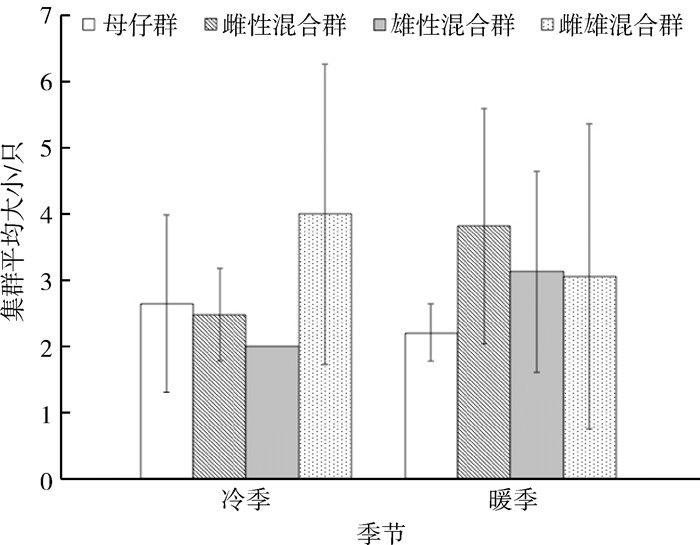
母仔群的集群平均大小在冷季(2.65只± 1.34只)较暖季(2.21只±0.43只)大;雌性混合群在冷季(2.48只±0.70只)较暖季(3.82只±1.78只)小;雄性混合群在冷季仅被拍摄到一次(2只),暖季为3.13只±1.52只。雌雄混合群在冷季(4.00只±2.27只)较暖季(3.06只±2.31只) 大。卡方检验表明,不同集群类型的集群平均大小无显著的季节差异(χ2=0.022,df=1,P=0.881)(图 5)。
|
| 图 5 马鹿阿拉善亚种不同集群类型集群平均大小的季节变化 Fig. 5 Seasonal variation of group size in different population types of Cervus elaphus alashanicus |
| |
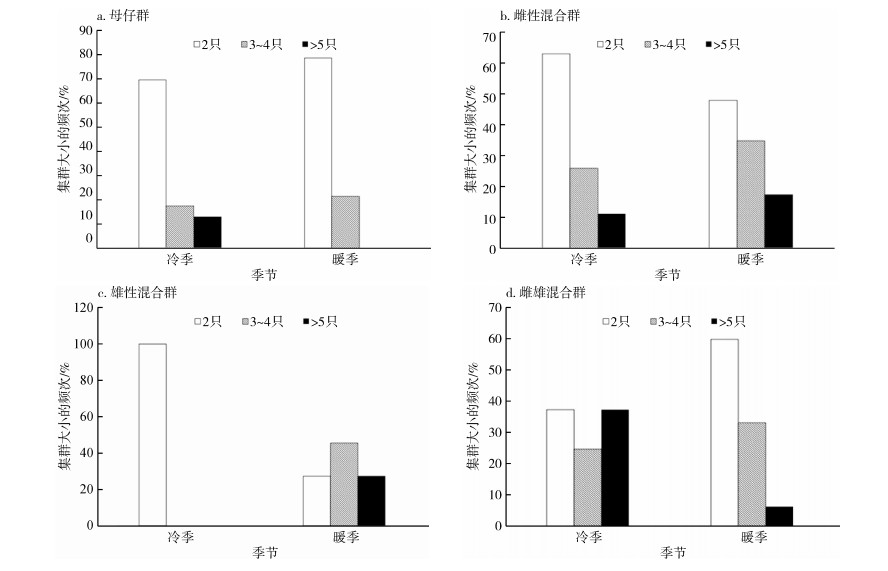
母仔群在冷暖季多为2只,集群大小的季节差异不显著(χ2=0.586,df=1,P=0.444)(图 6:a);雌性混合群在冷暖季以2只为主,在冷季的出现频次大于暖季,集群大小无显著季节性差异(χ2=1.144,df=1,P=0.285)(图 6:b);雄性混合群在冷季全为2只,在暖季多为3~4只,5只以上的出现频次与2只的持平,集群大小的季节差异不显著(χ2=1.524,df=1,P=0.217)(图 6:c);雌雄混合群在暖季多为2只,在冷季5只以上与2只持平,均高于3~4只,集群大小的季节差异不显著(χ2=2.018,df=1,P=0.155)(图 6:d)。
|
| 图 6 马鹿阿拉善亚种不同群集类型的集群大小频次的季节变化 Fig. 6 Seasonal variation of cluster size frequency in different group types of Cervus elaphus alashanicus |
| |
本研究通过红外相机对贺兰山阿拉善马鹿集群行为进行研究,通过数据采集和分析,共得到马鹿图像579群次,810只次。平均集群数量为1.40只±1.04只,最大集群数量为11只。6种不同集群类型出现的频次间差异极显著,单个雌性群最高,单个雄性群次之,最低的为雌雄混合群。贺兰山马鹿集群类型多为单个雌性群、单个雄性群,这与天敌捕食压力、食物资源、种内竞争有密切的关系(Elgar,1989;Dehn,1990;McNamara & Houston,1992;Lima,1995;Roberts,1995;Burger et al., 2000;孙儒泳,2001)。目前贺兰山缺乏大型捕食动物,马鹿的天敌如狼Canis lupus、雪豹Panthera uncia、猞猁Lynx lynx等在20世纪80年代已灭绝(骆颖,2011)。马鹿的被捕食风险很低,不需要跟其他个体集群抵御天敌。此外,贺兰山马鹿的适宜生境狭窄(高惠等,2017),食物资源也不够丰富,为减少种群内个体之间的食物竞争,马鹿个体多为单独活动。雄性混合群的出现频次最低,可能是由于雄性个体具有较强的领域意识,雄性个体之间存在的竞争较大。
本研究发现,不同集群类型出现频次存在极显著的季节性差异。冷季单个雄性群、母仔群、雌性混合群的出现频次均高于暖季,而暖季单个雌性群、雄性混合群、雌雄混合群的出现频次均高于冷季。在冷季单个雄性群出现频次高,主要是由于在冷季(繁殖期:9—11月)成年雄性个体活动活跃,存在频繁的繁殖行为(如占域、巡视领域)以及个体之间的激烈竞争。母仔群在冷季的出现频次高于暖季,原因可能有2点:第一,幼鹿需要母鹿的照顾才能在贺兰山漫长而寒冷的冷季中生存,Franklin和Dole(1975)、张明海等(1992)的研究指出幼鹿严重依赖成年母鹿,尤其在冬季;第二,产仔期(5—7月)为暖季,怀孕雌鹿会选择在一个隐蔽而安全的地方产崽,从而导致母仔群的出现频次较低。雌性混合群在冷季的出现频次较高,原因可能是雌性个体为提高其自身繁殖的成功率,而增加与雄性的遇见率。怀孕雌鹿需要在暖季产崽,驱赶亚成体,从而导致单独活动的雌性个体增加,故单个雌性群的出现频次在暖季高于冷季。在暖季(非繁殖期)雄性个体之间的竞争不激烈,食物资源较丰富,因此雄性混合群在暖季的出现频次较高。雌雄混合群在暖季较高,原因尚未清楚,还需要进一步验证。总体而言,马鹿不同集群类型的季节性差异显著,是由于其繁殖周期的变化而引起的。其他相关研究认为有蹄类动物集群类型的季节性变化是对生理(繁殖)周期、食物资源等条件的适应响应(Wang & Schaller,1996;李新庆,2006;李忠秋,蒋志刚,2006;龙帅等,2009;封托等,2010;O'Connell et al., 2010;胡磊,2013;黄沛琳等,2015)。
关于集群规模,本研究发现马鹿的集群大小、不同集群的集群平均大小和集群大小没有明显的季节性变化,其集群规模较小,多为1~ 2只。推测这主要与天敌威胁、生境类型、适宜生境狭小有关。有蹄类动物被捕食的风险会影响其集群大小,目前在贺兰山没有捕食马鹿的大型捕食动物(骆颖,2011),因此不需要通过增加集群大小来提高警戒并躲避捕食者。马鹿集小群与生境类型有关。许多研究表明,在不同生境中马鹿的集群类型不同,在开阔的草原生境中的集群规模大于在灌丛生境中的,林间生境不适合大量马鹿(体型大)集群取食(Franklin & Dole,1975;张明海等,1992;胡磊,2013)。本研究中3只以上的马鹿集群主要出现在开阔的林缘地带中,也支持了这一观点。本研究中马鹿的集群平均大小(1.40只±1.04只)小于张明春等(2012)的研究(3.50只±2.76只),这是因为前者是在森林生境中进行调查的,而后者包括整个贺兰山(以荒漠、草原等开阔的生境为主)。适宜生境狭小可能也是贺兰山马鹿集群规模较小的重要原因,贺兰山马鹿是马鹿阿拉善亚种唯一幸存的有效种群,且种群数量一直处于较低水平(骆颖,2011),高惠等(2017)研究发现其适宜生境面积仅为667.87 km2(占贺兰山总面积的18.2%)。由于栖息地面积和适宜生境狭小,为减轻个体之间的食物竞争,马鹿集群规模也较小。
本次集群行为研究是基于红外相机技术进行的,虽然跟传统方法相比具有明显优势,如客观性强、调查周期长、无人为干扰、全天候、受环境干扰小等,但也存在一定的局限性:红外相机的感应半径与灵敏度仅在一定范围内起作用,当群体中个体不在相机感应区活动时,就会造成漏拍(胡磊,2013;薛亚东等,2014;胡亮,2015;黄沛琳等,2015)。
昶野. 2010. 贺兰山岩羊食性分析[D]. 哈尔滨: 东北林业大学.
|
狄维忠. 1987. 贺兰山维管植物[M]. 西安: 西北大学出版社.
|
封托, 王静, 张洪峰, 等. 2010. 自动照相系统在野生动物调查中的应用[J]. 野生动物, 31(3): 161-163. DOI:10.3969/j.issn.1000-0127.2010.03.013 |
高惠, 滕丽微, 汪洋, 等. 2017. 阿拉善马鹿(Cervus alashanicus)生境适宜性评价[J]. 生态学报, 37(11): 3926-3931. |
高行宜, 姚军. 2007. 北天山喀拉乌成山的马鹿资源调查[J]. 地方病通报, 22(2): 6-7. |
胡磊. 2013. 基于红外自动相机技术的马鹿和狍活动节律与马鹿集群行为[D]. 北京: 北京林业大学.
|
胡亮. 2015. 基于红外相机技术的北山羊(Capra ibex)活动节律与集群行为的研究[D]. 新疆: 石河子大学.
|
黄沛琳, 肖文宏, 杨海涛, 等. 2015. 东北梅花鹿种群活动节律和集群行为研究[J]. 北京师范大学学报(自然科学版), (5): 498-503. |
靳勇超, 张明海. 2012. 基于粪便分子生物学技术的中国马鹿分子生态学研究进展[J]. 野生动物, 33(3): 152-157, 169. DOI:10.3969/j.issn.1000-0127.2012.03.012 |
李顺才, 杜利强, 安瑞永. 2008. 中国野生马鹿资源的保护与利用[J]. 草业科学, 25(4): 82-85. |
李新庆. 2006. 贺兰山岩羊集群特征[D]. 上海: 华东师范大学.
|
李忠秋, 蒋志刚. 2006. 青海布哈河上游地区同域分布的普氏原羚与藏原羚草青期的集群比较[J]. 动物学研究, (4): 396-402. DOI:10.3321/j.issn:0254-5853.2006.04.010 |
刘振生, 张明明, 李志刚, 等. 2009. 贺兰山马鹿冬季取食和卧息生境选择[J]. 兽类学报, (2): 133-141. |
刘振生. 2009. 贺兰山脊椎动物[M]. 银川: 宁夏人民出版社.
|
龙帅, 周材权, 王维奎, 等. 2009. 矮岩羊夏季活动节律、时间分配和集群行为[J]. 动物学研究, 30(6): 687-693. |
骆颖. 2011. 贺兰山岩羊(Pseudois nayaur)和马鹿(Cervus elaphus alxaicus)的食性及生境选择比较研究[D]. 哈尔滨: 东北林业大学.
|
牛达生. 2005. 贺兰山概况及其在西夏以前的情况[J]. 宁夏史志, (3): 37-40. |
盛和林. 1992. 中国鹿类动物[M]. 上海: 华东师范大学出版社.
|
孙儒泳. 2001. 动物生态学原理(第三版)[M]. 北京: 北京师范大学出版社.
|
王应祥. 2003. 中国哺乳动物种和亚种分类名录与分布大全[M]. 北京: 中国林业出版社.
|
魏辅文, 杨奇森, 吴毅, 等. 2021. 中国兽类名录(2021版)[J]. 兽类学报, 41(5): 487-501. |
薛亚东, 刘芳, 张于光, 等. 2014. 利用红外相机视频数据进行库姆塔格沙漠地区野骆驼集群行为研究的可行性[J]. 生物多样性, 22(6): 746-751. |
张明春, 李志刚, 胡天华, 等. 2012. 宁夏贺兰山国家级自然保护区马鹿分布及集群特征的初步研究[J]. 兽类学报, 32(4): 318-324. |
张明海, 钟立成, 关国生, 等. 1992. 黑龙江东部马鹿集群行为的初步观察[J]. 兽类学报, 12(4): 243-247. |
郑敬刚, 张景光. 2006. 试论贺兰山植物多样性的若干特点[J]. 干旱区地理, 28(4): 526-530. |
Burger J, Safina C, Gochfeld M. 2000. Factors affecting vigilance in springbok: importance of vegetative cover, location in herd, and herd size[J]. Acta Ethologica, 2(2): 97-104. |
Carthew S, MSlater E. 1991. Monitoring animal activity with automated photography[J]. Journal Wildlife Management, 55: 689-692. |
Cutler TL, Swann DE. 1999. Using remote photography in wildlife ecology: a review[J]. Wildlife Society Bulletin, 27(3): 571-581. |
Dehn MM. 1990. Vigilance for predators: detection and dilution effects[J]. Behavioral Ecology and Sociobiology, 26: 337-342. |
Elgar MA. 1989. Predator vigilance and group size in mammals and birds: a critical review of the empirical evidence[J]. Biological Reviews, 64: 13-33. |
Franklin WL, Dole M. 1975. Social organization and home range of Roosevelt elk[J]. Journal of Mammalogy, 56(1): 102-118. |
Jarman RJ. 1974. The social organization of antelope in relation to their ecology[J]. Behaviour, 48: 215-267. |
Kucera TE, Barrett RH. 2011. A history of camera trapping[M]//Nichols JD, O'Connell AF, Karanth KU. Camera traps in animal ecology. Tokyo: Springer Japan.
|
Lima SL. 1995. Back to the basics of antipredatory vigilance: the group size effect[J]. Animal Behaviour, 49: 11-20. |
McNamara JM, Houston AI. 1992. Evolutionarily stable levels of vigilance as a function of group size[J]. Animal Behaviour, 43: 641-658. |
Nowak RM. 1999. Walker's mammals of the world[M]. 6th ed. Baltimore and London: The Johns Hopkins University Press.
|
O'Connell AF, Nichols JD, Karanth KU. 2010. Camera traps in animal ecology: methods and analyses[M]. Tokyo: Springer Science, Business Media.
|
Roberts G. 1995. A realtime response of vigilance behaviour to changes in group size[J]. Animal Behaviour, 50: 1371-1374. |
Swann DE, Hass CC, Dalton DC, et al. 2004. Infrared-triggered cameras for detecting wildlife: an evaluation and review[J]. Wildlife Society Bulletin, 32: 357-365. |
Wang XM, Schaller GB. 1996. Status of large animals in Inner Mongolia, China[J]. East China Normal University (special issue of mammals), 6: 94-104. |
 2021, Vol. 40
2021, Vol. 40




