扩展功能
文章信息
- 沈载芸, 曹成全, 王向积, 刘方庆, 杨香宇
- SHEN Zaiyun, CAO Chengquan, WANG Xiangji, LIU Fangqing, YANG Xiangyu
- 2种斑鱼蛉(广翅目:齿蛉科:鱼蛉亚科)幼虫和蛹的分类鉴定及形态描述
- Identification and Morphological Description of the Larvae and Pupae of Two Species of Neochauliodes (Megaloptera: Corydalidae: Chauliodinae)
- 四川动物, 2021, 40(5): 532-542
- Sichuan Journal of Zoology, 2021, 40(5): 532-542
- 10.11984/j.issn.1000-7083.20200395
-
文章历史
- 收稿日期: 2020-10-16
- 接受日期: 2021-05-21
2. 山东省青岛市城阳区农业农村局, 山东青岛 266109
2. Agricultural and Rural Bureau of Chengyang District, Qingdao, Shandong Province 266109, China
鱼蛉亚科Chauliodinae隶属于广翅目Megaloptera齿龄科Corydalidae,在齿蛉科中,鱼蛉亚科较齿蛉亚科Corydalinae的属级分化更明显(刘星月,2008),该亚科世界己知15属130余种,世界性分布,呈现明显的间断分布格局(刘星月,2008;杨定,刘星月,2010)。斑鱼蛉属Neochauliodes是鱼蛉亚科中最大的属,世界已知38种及2亚种,分布广泛,从远东一直延伸到东南亚(刘星月,2008;王付彬,2010;杨定,刘星月,2010),其中,《中国动物志昆虫纲(第五十一卷广翅目)》(杨定,刘星月,2010)中的东方斑鱼蛉Neochauliodes orientalis和越南斑鱼蛉Neochauliodes tonkinensis为同物异名。
在中国乃至世界的广翅目昆虫分类研究中,成虫的分类学研究较为完善(刘星月,2008;杨定,刘星月,2010),但其余虫态的分类研究却很薄弱。世界上多个现存广翅目幼虫形态特征已被描述,包括:马达鱼蛉属Madachauliodes(Paulian,1951)、鱼蛉属Chauliodes和黑鱼蛉属Nigronia(Cuyler, 1958, 1965)、帝鱼蛉属Dysmicohermes、新鱼蛉属Neohermes和山鱼蛉属Orohermes(Evans,1972)、原泥蛉属Protosialis(Flint,1973)、丽鱼蛉属Chloronia(Penny & Flint,1982)、宽头齿蛉属Platyneuromus(Contreras-Ramos & Harris,1998)、异鱼蛉属Apochauliodes、始鱼蛉属Archichauliodes、原鱼蛉属Protochauliodes、澳泥蛉属Austrosialis和细泥蛉属Stenosialis(Theischinger,2000)、星齿蛉属Protohermes、斑鱼蛉属、准鱼蛉属Parachauliodes、日泥蛉属Nipponosialis和泥蛉属Sialis(Hayashi,2005)、新齿蛉属Corydalus(Azevêdo & Hamada, 2006, 2007)、宽鱼蛉属Platychauliodes和梯鱼蛉属Taeniochauliodes(Liu et al., 2011, 2013)、纤泥蛉属Leptosialis(Price et al., 2012)、巨齿蛉属Acanthacorydalis(Cao & Liu,2013)和齿蛉属Neoneuromus(Cao et al., 2016, 2018)等,斑鱼蛉属的小碎斑鱼蛉N. sparsus(王付彬,2011)和台湾斑鱼蛉N. formosanus(Sang & Yeon,2015)的形态也被描述过。
仅有少数属的蛹形态特征被描述过:星齿蛉属和斑鱼蛉属(王付彬,2011)、巨齿蛉属和齿蛉属(Cao & Liu,2013; Cao et al., 2016, 2018)。
本文利用分子数据和成虫形态特征双重证据对双齿斑鱼蛉Neochauliodes bicuspidatus和越南斑鱼蛉的末龄幼虫和蛹进行了分类鉴定,并对其形态特征进行了详细描述。
1 材料与方法 1.1 试虫采集及处理试验所用末龄幼虫于2019年3月和2020年3月采自四川省凉山彝族自治州会理县南阁乡凉桥村(102°17′42″E,26°36′58″N,海拔1 900 m),2种斑鱼蛉生活在一起而常被同时采集到,均采集于山林一条流速缓慢的小河沟中,常居于石头下,在无石头区域的厚积腐叶下也采集到少量。
每个种类采集50~100只,将采集回的活虫按照相关技术进行养殖(曹成全等, 2018a, 2018b),将试虫养至蛹和成虫。
1.2 幼虫和蛹的形态学研究将处理干净的鲜活完整幼虫和蛹置于有盖的培养皿中,0 ℃保存1 d以上冷冻休眠,取出置于空气中0.5 h左右,使其肢体自然伸展,调整标本姿势,在LY-WN-YH全自由度超景深系统(成都励扬精密机电有限公司)下拍摄, 并用校准的卡尺测量数据,体长从唇基到腹部末端测量,头部长度从唇基到头后测量(0.01 cm)。将拍摄好的试虫进行标注,并用Photoshop CS6处理。
1.3 试虫物种鉴定 1.3.1 成虫形态学鉴定将试虫养殖至成虫后,按照杨定和刘星月(2010)中的方法进行形态学鉴定。
1.3.2 幼虫和蛹的分子鉴定DNA提取:剪取样本胸腹部肌肉,取完后用消毒后的小剪刀剪碎,再采用基因组DNA试剂盒(北京天根生物科技)提取总的基因组DNA。
PCR扩增以及测序:COⅠ序列通用引物为C1-J-2183(5’-CAACATTTATTTTGATTTTTTGG-3’)和TL2-N-3014 (5’-TCCATTGCACTAATCTGCCAT-ATTA-3’)(张杰,2017)。PCR反应体系为25 μL,包括2×ES TaqMasterMix(cye) 12.5 μL,引物各1.0 μL(0.4 μmol),ddH2O 8.5 μL,样品2 μL。扩增程序为94 ℃ 1 min;94 ℃ 0.1 min,55 ℃ 0.5 min,72 ℃ 1 min,20个循环;94 ℃ 0.5 min,45 ℃ 0.5 min,72 ℃ 1 min,20个循环;72 ℃ 10 min,4 ℃ ∞,1个循环。经1%琼脂糖凝胶电泳检测后,PCR产物送生工生物技术(上海)公司成都生工测序部进行纯化和双向测序。
数据处理:测序后先在GenBank上对比,然后再上传获得GenBank登录号;同时,将所得序列与其他物种建立系统聚类树以比较遗传距离:外类群和其他内类群的DNA序列下载自GenBank,包括栉角鱼蛉Chauliodes pectinicornis(KR148304.1)、污翅斑鱼蛉N. fraternus(KF785799.1)、缘点斑鱼蛉N. bowringi(JQ351950.1)、圆端斑鱼蛉N. rotundatus(KF771894.1)、散斑鱼蛉N. punctatolosus(JX110703.1)和碎斑鱼蛉N. parasparsus(AQU14296.1),利用DNAman程序打开序列,与峰图软件(Chromas)对齐以及与BioEdit进行序列比对,检查变异序列并剪掉不必要的序列,然后保存为.pir文件,再将此文件导入DanSP 5.0中,生成.nex单倍型文件。再使用Primer,与从GenBank上获得的CO Ⅰ序列重新命名,在PAUP 4.10中运行NJ树,设置重复1 000代,得到的树文件(.tre) 通过FigTree 1.4.4进行可视化和树的美化,同时利用bootstrap(1 000次重复)检验各分支的支持率,物种两两之间的遗传距离通过MEGA 6.0(Tamura et al., 2013)中的P-distance遗传距离方法计算。
2 结果与分析 2.1 试虫物种鉴定试虫养殖至成虫后,通过形态鉴定,确定为双齿斑鱼蛉和越南斑鱼蛉。2种试虫的幼虫和蛹的CO Ⅰ序列GenBank登录号分别为:MW560981和MW560982。
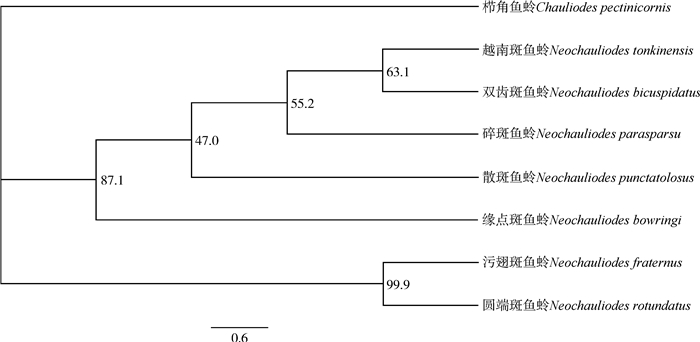
7种斑鱼蛉的CO Ⅰ种间遗传差异为0.089~0.210(表 1),双齿斑鱼蛉和越南斑鱼蛉与斑鱼蛉属其他物种的种间遗传距离范围分别为0.111~0.190和0.099~0.176。在NJ系统发育树中,双齿斑鱼蛉和越南斑鱼蛉分别形成了单独的分支(图 1),支持率为63.1%,与碎斑鱼蛉聚在一起形成姐妹群,支持率为55.2%,污翅斑鱼蛉和圆端斑鱼蛉聚集在一起,支持率为99.9%。
| 1. 双齿斑鱼蛉 N. bicuspidatus |
2. 越南斑鱼蛉 N. tonkinensis |
3. 碎斑鱼蛉 N. parasparsus |
4. 散斑鱼蛉 N. punctatolosus |
5. 缘点斑鱼蛉 N. bowringi |
6. 污翅斑鱼蛉 N. fraternus |
7. 圆端斑鱼蛉 N. rotundatus |
|
| 2 | 0.089 | ||||||
| 3 | 0.111 | 0.099 | |||||
| 4 | 0.116 | 0.108 | 0.123 | ||||
| 5 | 0.144 | 0.128 | 0.144 | 0.159 | |||
| 6 | 0.181 | 0.170 | 0.172 | 0.172 | 0.204 | ||
| 7 | 0.190 | 0.176 | 0.170 | 0.197 | 0.210 | 0.134 |
|
| 图 1 基于邻接法建立的斑鱼蛉属部分物种之间的系统发育树 Fig. 1 Phylogenetic tree of some Neochauliodes species based on Neighbour-Joining 节点数字为支持率 The node numbers are support rates |
| |
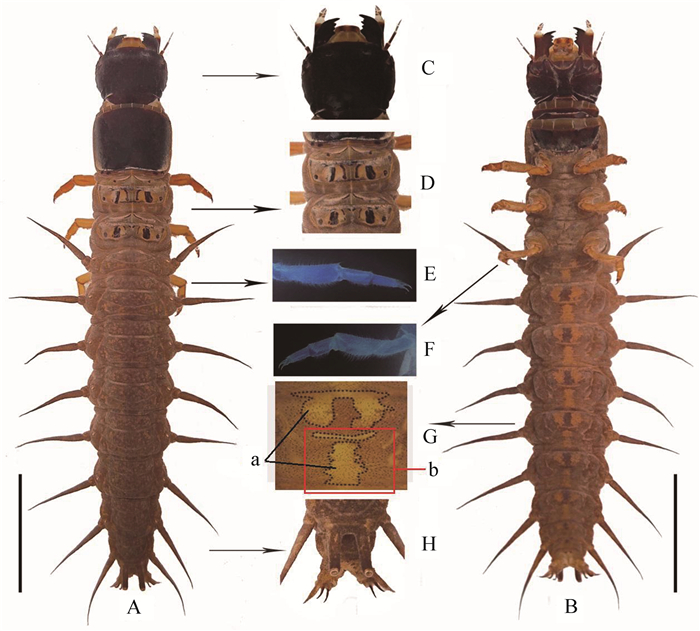
体长5.10 cm±0.01 cm,体宽0.75 cm±0.05 cm(n=10)(表 2),身体较为粗壮,头和前胸背板为黑色或黑棕色且基本无花纹,通体呈棕色或棕褐色(图 2:A、B)。
| 参数 Parameters/cm |
双齿斑鱼蛉 N.bicuspidatus (n=10) |
越南斑鱼蛉 N.tonkinensis (n=10) |
| 体长(不包括大颚) | 5.10±0.01 | 5.15±0.15 |
| 体宽 | 0.75±0.05 | 0.59±0.01 |
| 头长 | 0.55±0.05 | 0.48±0.03 |
| 头宽 | 0.55±0.15 | 0.45±0.05 |
| 前胸背板长 | 0.60±0.01 | 0.53±0.03 |
| 前胸背板宽 | 0.70±0.01 | 0.45±0.05 |
| 中后胸背板长 | 0.60±0.01 | 0.50±0.01 |
| 中后胸背板宽 | 0.65±0.05 | 0.50±0.01 |
| 腹长 | 3.12±0.01 | 3.50±0.01 |
| 呼吸管长 | 0.20±0.03 | 0.18±0.05 |
|
| 图 2 双齿斑鱼蛉末龄幼虫 Fig. 2 The final-instar larva of Neochauliodes bicuspidatus A. 背面, B. 腹面, C. 头部背面, D. 中后胸背板, E. 后足背面, F. 后足腹面, G. 腹部腹面花纹, a. "∵"形斑点,b. "T"型区域,H. 腹部末端背面; 标尺=10 mm A. dorsal view of the whole body, B. ventral view of the whole body, C. dorsal view of the head, D. the mesothorax and metathorax, E. dorsal view of the back foot, F. ventral view of the back foot, G. the patterns of the ventral abdomen, a. '∵ 'shaped mark, b. "T"mark, H. dorsal view of the end of the abdomen; scale bars=10 mm |
| |
头部:长0.55 cm±0.05 cm,宽0.55 cm± 0.15 cm。上唇圆形,淡黄色,中部具有2个暗褐色斑纹和几根刚毛。上颚黑色且光滑,骨化明显。外颚叶黄白相间且上面被毛,下颚棕色。触角长0.21 cm±0.01 cm,4节,棕色,第2节最长,第2节约是第4节的1.80倍,触角的近似比例为4∶ 9∶ 3∶ 5。头部腹面无明显的花纹,多凹点(图 2:C)。
胸部:前胸宽0.70 cm±0.01 cm,长0.60 cm±0.01 cm,中后胸长宽基本一致。前胸背板黑色或黑棕色,光滑,两侧具细长刚毛,前胸背板腹面前缘有4道黄色竖线,中上部有1个半月牙形红棕色骨化片;中后胸背板具有较复杂且左右对称的黑色花纹。足棕色,每个足末端各有2个小爪子,足两侧密被刚毛,每只足腹面的前侧毛少于后侧毛且长毛和短毛间隔排列(图 2:D、E、F)。
腹部:长3.12 cm±0.10 cm,10节,腹节宽度呈递减趋势,与相应呼吸鳃比例近似为1.14∶ 1.15∶ 1.15∶ 0.94∶ 0.88∶ 0.97∶ 0.69∶ 0.56(表 3)。虫体表面密被短钝刚毛,每一腹节有明显的居中横状无毛区;腹面比背面颜色鲜艳,每一腹节都有"∵ "形(图 2:G,图 3:A、B、C)的大黄斑点,因体色、体型的差异,颜色和大小存在细微不同。斑点中央具1个短粗黑斑,腹节中部长短不一的横状无毛区与下方斑点组成类似"T"型的区域,但两者并未直接相连(图 2:G)。腹节左右两侧有对称的3、4条短线无毛区。第8腹节后缘有1对呼吸管,呼吸管长0.20 mm±0.03 mm,第10腹节尾端两侧各有1对骨化的钩子(图 2:H),其基部棕黄色,顶端棕黑色。第6腹节的宽度和气管鳃长度变化明显。背面棕色,表面斑点可能被覆盖(图 3:D),少数为棕褐色,表面具有细碎黄色斑点(图 3:E、F)。
| 参数 Parameters/cm |
双齿斑鱼蛉 N. bicuspidatus (n=10) |
腹节与对应气管鳃比例关系 Approximate ratio of abdominal sections to tracheal gills |
越南斑鱼蛉 N. tonkinensis (n=10) |
腹节与对应气管鳃比例关系 Approximate ratio of abdominal sections to tracheal gills |
| 第1腹节宽 | 0.80±0.01 | 1.14±0.03 | 0.65±0.05 | 0.93±0.10 |
| 第1腹节气管腮长 | 0.70±0.01 | 0.70±0.02 | ||
| 第2腹节宽 | 0.80±0.03 | 1.15±0.05 | 0.71±0.04 | 0.89±0.06 |
| 第2腹节气管腮长 | 0.70±0.01 | 0.80±0.01 | ||
| 第3腹节宽 | 0.80±0.04 | 1.15±0.08 | 0.72±0.04 | 0.89±0.05 |
| 第3腹节气管腮长 | 0.70±0.01 | 0.80±0.01 | ||
| 第4腹节宽 | 0.75±0.05 | 0.94±0.08 | 0.70±0.05 | 0.94±0.07 |
| 第4腹节气管腮长 | 0.80±0.02 | 0.75±0.01 | ||
| 第5腹节宽 | 0.70±0.05 | 0.88±0.08 | 0.63±0.03 | 0.79±0.05 |
| 第5腹节气管腮长 | 0.80±0.02 | 0.80±0.01 | ||
| 第6腹节宽 | 0.68±0.02 | 0.97±0.04 | 0.58±0.05 | 0.71±0.08 |
| 第6腹节气管腮长 | 0.70±0.01 | 0.83±0.03 | ||
| 第7腹节宽 | 0.55±0.05 | 0.69±0.07 | 0.50±0.05 | 0.56±0.08 |
| 第7腹节气管腮长 | 0.80±0.02 | 0.90±0.03 | ||
| 第8腹节宽 | 0.39±0.04 | 0.56±0.07 | 0.30±0.04 | 0.34±0.06 |
| 第8腹节气管腮长 | 0.70±0.02 | 0.90±0.04 |

|
| 图 3 双齿斑鱼蛉末龄腹部部分花纹 Fig. 3 Part patterns of the abdomen of the final-instar larva Neochauliodes bicuspidatus A~C. 腹部腹面花纹, D~F. 腹部背面花纹 A-C. the patterns of the ventral abdomen, D-F. the patterns of the dorsal abdomen |
| |
越南斑鱼蛉末龄幼虫与双齿斑鱼蛉末龄幼虫整体较相似(图 4:A、B),前者除整体体色略淡外,其他不同之处如下:

|
| 图 4 越南斑鱼蛉末龄幼虫 Fig. 4 The final-instar larva of Neochauliodes tonkinensis A.背面, B. 腹面, C. 头部背面, D. 前胸背板, E. 中后胸背板, F. 后足背面, G. 后足腹面, H. 腹部背面花纹, I. 腹节腹面, J. 腹部末端背面; 标尺=10 mm A. dorsal view of the whole body, B. ventral view of the whole body, C. dorsal view of the head, D. dorsal view of pronotum, E. the mesothorax and metathorax, F. dorsal view of the back foot, G. ventral view of the back foot, H. the patterns of the dorsal abdomen, I. the patterns of the ventral abdomen, J. dorsal view of the end of the abdomen; scale bars=10 mm |
| |
体长5.15 cm±0.15 cm,体宽0.59 cm±0.01 cm (n=10),身体较为纤细,额部具有明显"∵ "形淡黄色单眼(图 4:C),前胸背板具有复杂花纹(图 4:D),光滑,身体附有密集、大小不等的黄色斑点,腹面斑纹存在变异。
头部:长0.48 cm±0.03 cm,宽0.45 cm±0.05 cm,头部红棕色或棕黑色,额部有可见的"∵ "形淡黄色单眼(图 4:C)。触角长0.20 cm±0.01 cm,4节,棕色,第2节和第4节最长,第2节约是第4节的1.50倍,触角的近似比例为3∶ 9∶ 2∶ 6。
胸部:前胸背板长0.53 cm±0.03 cm,宽0.45 cm±0.05 cm,红棕色或棕黑色,具有复杂花纹(图 4:D),两侧具有细长纤毛,中后胸长宽几乎相等,近方形,具有复杂对称的花纹(图 4:E),足端的2个小钩及跗节部分上的毛明显少于双齿斑鱼蛉(图 4:F、G)。
腹部:长度3.50 cm±0.01 cm,灰褐色或棕色,腹节宽度先略增后减少,呼吸鳃明显修长,尤其第6~8节,每个腹节与对应呼吸鳃的长度比例关系为0.93∶ 0.89∶ 0.89∶ 0.94∶ 0.79∶ 0.71∶ 0.56∶ 0.34(表 3)。背面具有密集、大小不等的黄色斑点(图 4:H),且每一腹节前后各有1对由细碎小斑点聚集成的较大黄色斑点(图 4:H)和明显的横线和斜线(图 4:H)。腹面每节两侧有2条弯曲的线条(图 4:I)。腹部第8节后缘有1对呼吸管(图 4:J),呼吸管长0.18 cm±0.05 cm。
腹部腹面斑纹存在一定的变异,经统计共有2种斑型(n=20):Ⅰ型约25%,Ⅱ型约60%,约15%的个体兼具2种斑型。Ⅰ型斑纹a、b两者近似平行(图 5:A、B),ⅠA型斑纹的a、b、c部分大小近似相等,比ⅠB型斑纹的相应部分略宽且d区域较窄;Ⅱ型斑纹a、b两者成分开趋势(图 5:C、D),ⅡA型斑纹的c部分比ⅡB型斑纹的宽。

|
| 图 5 越南斑鱼蛉末龄幼虫腹面斑纹 Fig. 5 The patterns of the ventral final-instar larva of Neochauliodes tonkinensis A. ⅠA型斑纹, B. ⅠB型斑纹, C. ⅡA型斑纹, D. ⅡB型斑纹 A. type ⅠA, B. type ⅠB, C. type ⅡA, D. type ⅡB |
| |
在自然状态下,蛹呈"C"形弯曲,体色根据时间而变化:刚化蛹1 d时头部、触角、胸背板及2对翅芽嫩黄色,腹部黑褐色,3~4 d时体色几乎变为黑色(图 6:A、B、C),直至快羽化时体色会再加深。头部较短粗,近与前胸等宽,头顶近三角形,有一些长的刚毛;触角丝状,弯曲到头部的腹面。复眼卵球形,突出。唇短于头部,大颚与末龄幼虫相似,前半部分黑色,后半部分棕红色,有黑色斑点(图 6:B、D)。前胸长度稍短于宽度,中胸和后胸较为健壮,有黑色无规则的斑点,表面被附有较多细毛;2对翅芽健硕;腹部饱满粗壮,腹面可见类似其末龄幼虫的斑纹,腹部第9节背腹面具有细长密集的毛(图 6:E、F),生殖器发育完全。

|
| 图 6 双齿斑鱼蛉雌蛹 Fig. 6 Female pupa of Neochauliodes bicuspidatus A.背面, B. 腹面, C. 自然状态下的蛹, D. 头部背面, E. 腹部末端背面, F. 腹部末端腹面; 标尺=10 mm A. dorsal view with stretched abdomen, B. ventral view with stretched abdomen, C. lateral view in natural condition, D. dorsal view of the head, E. dorsal view of the end of abdomen, F. ventral view of the end of abdomen; scale bars=10 mm |
| |
越南斑鱼蛉蛹与双齿斑鱼蛉蛹整体较相似,后者除整体体色略深、体色变化较快外,其他不同之处如下:
前额凹陷明显;复眼卵球形,棕褐色;大颚棕色,与其末龄幼虫相似;腹部腹面有较清晰的斑纹,且每个腹节两侧的下角处有黑点状斑纹,背面有明显、细碎、大小不一的黄色斑块(图 7:A、B、E);生殖器发育健全,腹面饱满、光滑无毛(图 7:F、G、H)。

|
| 图 7 越南斑鱼蛉雌蛹 Fig. 7 Female pupa of Neochauliodes tonkinensis A.背面, B. 腹面, C. 化蛹1 d时自然状态下的侧面, D. 羽化前1~2 d自然状态下的侧面, E. 头部背面, F. 腹部末端腹面, G. 腹部末端侧面; H. 腹部末端背面; 标尺=10 mm A. dorsal view with stretched abdomen, B. ventral view with stretched abdomen, C. lateral view in natural condition after pupating for 1 day, D. lateral view in natural condition 1 day or 2 days before eclosion, E. dorsal view of the head, F. ventral view of the end of abdomen, G. lateral view of the end of abdomen, H. dorsal view of the end of abdomen; scale bars=10 mm |
| |
根据发育时间,蛹期体色从嫩黄色(图 7:C)到金黄色(图 7:A、B)再到黑色(图 7:D),翅芽变化尤其明显。
3 结论双齿斑鱼蛉末龄幼虫除了体色上略有差异,总体特征相对稳定,而越南斑鱼蛉末龄幼虫种内形态特征差异较大。两者之间较为稳定的形态特征差异见表 4。
| 参数Parameters | 双齿斑鱼蛉N. bicuspidatus | 越南斑鱼蛉N.tonkinensis |
| 体型 | 粗壮 | 纤细 |
| 头部及前胸背板颜色 | 黑色或偏棕色 | 棕色或棕黑色 |
| 头部及前胸背板花纹 | 无 | 有 |
| 腹部背面花纹 | 花纹细碎不明显,无规律 | 花纹明显且有规律 |
| 腹部体表刚毛 | 明显、密集 | 不明显 |
| T区 | 上下分隔,大小、形状稳定 | 上下直接相连,大小、形状不稳定 |
| 腹部斑纹 | 有"∵"形的大黄斑点及1个短粗黑斑,形状、大小稳定 | 腹面斑纹存在2种类型,少数个体兼具2种斑纹,其中Ⅰ型与双齿斑鱼蛉斑纹十分相似,但后者的中央短粗黑斑宽度较前者小 |
2种蛹的形态特征总体上差异不大,具体差异为:前者蛹体色较深,随时间体色变化大,后者即便是羽化前1~2 d也只是2对翅芽颜色加深近黑色,头、触角及胸背板部分变棕黑色;前者的腹部第9节背腹面有密集纤长的刚毛,而后者相同部位光滑,几乎无毛。
形态上的差异性状对于2种斑鱼蛉幼虫和蛹的鉴别具有一定的参考价值,但幼虫的花纹和体色变异较大,不易作为稳定的鉴别特征,且蛹的体色会随时间而不断改变。
4 讨论本研究形态学结果显示,双齿斑鱼蛉和越南斑鱼蛉与其他物种存在明显的差异;系统发育分析也表明,双齿斑鱼蛉和越南斑鱼蛉在系统发育树中分别形成了2个单独的分支,因此认为两者很可能为2个独立的物种;然而,由于样本获取难度大,双齿斑鱼蛉和越南斑鱼蛉样本较少,本研究中分子生物学数据较为单薄,不排除后期研究中在获取更多样本后,系统发育树结果与形态学结果不一致的情况,即双齿斑鱼蛉种群和越南斑鱼蛉种群聚在一起,形成一个大的分支,表明两者形态学的差异是由于个体变异导致。例如,双齿斑鱼蛉末龄幼虫的足和一些呼吸鳃末端具有黑色斑点,是因受伤导致,或者受环境尤其是水质的影响。因此,在后期研究中将进一步补充更多的样本,对现有结果进行验证,以明确双齿斑鱼蛉和越南斑鱼蛉的分类和系统发育地位。
致谢: 感谢中国农业大学刘星月教授协助鉴定物种并对论文撰写提出宝贵意见,感谢沈华瑞、何绪康、沈载富等在标本采集和养殖过程中的协助和支持。
曹成全, 童超, 陈申芝, 等. 2018a. 爬沙虫幼虫和蛹的室内规模化养殖方法: 中国, ZL201610155499.2[P]. 2018-05-11.
|
曹成全, 童超, 陈申芝, 等. 2018b. 一种爬沙虫的采集、运输和养殖装置: 中国, ZL201820353109.7[P]. 2018-03-15.
|
刘星月. 2008. 中国广翅目系统分类研究(昆虫纲: 脉翅总目)[D]. 北京: 中国农业大学.
|
王付彬. 2011. 泰山区域小碎斑鱼蛉生物学研究及其资源价值评价[D]. 山东: 山东农业大学.
|
杨定, 刘星月. 2010. 中国动物志昆虫纲(第五十一卷广翅目)[M]. 北京: 科学出版社.
|
张杰. 2017. 蚁蛉科幼虫形态与分子鉴定研究(脉翅目: 蚁蛉科)[D]. 北京: 中国农业大学.
|
Azevêdo CAS, Hamada N. 2006. Description of last-instar larva of Corydalus nubilus Erichson, 1848 (Megaloptera: Corydalidae) and notes on its bionomics[J]. Zootaxa, 1177: 57-68. DOI:10.11646/zootaxa.1177.1.6 |
Azevêdo CAS, Hamada N. 2007. Description of the larvae of Corydalus batesii McLachlan and C. ignotus Contreras Ramos (Megaloptera: Corydalidae) with notes on life history and behavior[J]. Zootaxa, 1631: 33-45. DOI:10.11646/zootaxa.1631.1.2 |
Cao CQ, Liu FQ, Tong C, et al. 2018. Description of the final-instar larva and pupa of Neoneuromus ignobilis Navás, 1932 (Megaloptera: Corydalidae)[J]. Zootaxa, 4378(4): 581-588. DOI:10.11646/zootaxa.4378.4.9 |
Cao CQ, Liu XY. 2013. Description of the final-instar larva and pupa of Acanthacorydalis orientalis (McLachlan, 1899)(Megaloptera: Corydalidae) with some life history notes[J]. Zootaxa, 3691(1): 145-152. DOI:10.11646/zootaxa.3691.1.5 |
Cao CQ, Tong C, Chen SZ, et al. 2016. First description and bionomic notes for the final-instar larva and pupa of an Oriental dobsonfly species, Neoneuromus sikkimmensis (van der Weele, 1907)(Megaloptera: Corydalidae)[J]. Zootaxa, 4179(2): 288-294. DOI:10.11646/zootaxa.4179.2.9 |
Contreras-Ramos A, Harris SC. 1998. The immature stages of Platyneuromus (Corydalidae), with a key to the genera of larval Megaloptera of Mexico[J]. Journal of the North American Benthological Society, 17: 489-517. DOI:10.2307/1468368 |
Cuyler RD. 1958. The larvae of Chauliodes Latreille (Megaloptera: Corydalidae)[J]. Annals of the Entomological Society of America, 51(6): 582-586. DOI:10.1093/aesa/51.6.582 |
Cuyler RD. 1965. The larva of Nigronia fasciatus Walker (Megaloptera: Corydalidae)[J]. Entomological News, 76: 192-195. |
Evans ED. 1972. A study of the Megaloptera of the Pacific coastal region of the United States[D]. Corvollis: Oreon States University.
|
Flint OS Jr. 1973. The Megaloptera of Chile (Neuroptera)[J]. Revista Chilena de Entomologia, 7: 31-45. |
Hayashi F. 2005. Megaloptera[M]//Kawai T, Tanida K. Aquatic insects of Japan: mannual with keys and illustrations. Kanagawa: Tokai University Press.
|
Liu XY, Price B, Hayashi F, et al. 2013. Systematic revision reveals underestimated diversity of the South African endemic fishfly genus Taeniochauliodes Esben-Petersen (Megaloptera: Corydalidaez[J]. Systematic Entomology, 38: 543-560. DOI:10.1111/syen.12009 |
Liu XY, Price BW, Hayashi F, et al. 2011. Revision of the fishfly genus Platychauliodes Esben-Petersen (Megaloptera: Corydalidae) endemic to South Africa[J]. Zootaxa, 2909: 1-13. DOI:10.11646/zootaxa.2909.1.1 |
Paulian R. 1951. Fauna des eaux douces de Madagascar. 1951. Plécoptères et Mégaloptères[J]. Mémoires de l'Institut Scientifique de Madagascar, 6(A): 53-61. |
Penny ND, Flint OS Jr. 1982. A revision of the genus Chloronia (Neuroptera: Corydalidae)[J]. Smithsonian Contributions to Zoology, 348: 1-27. |
Price BW, Liu XY, de Moor F, et al. 2012. A review of the alderfly genus Leptosialis Esben-Petersen (Megaloptera: Sialidae) with description of a new species from South Africa[J]. ZooKeys, 201: 27-41. DOI:10.3897/zookeys.201.2623 |
Sang WJ, Yeon JB. 2015. DNA-based identification of South Korean Megaloptera larvae with taxonomic notes[J]. The Canadian Entomologist, 148(2): 123-139. |
Tamura K, Stecher G, Peterson D, et al. 2013. MEGA 6:molecular evolutionary genetics analysis version 6.0[J]. Molecular Biology and Evolution, 30(12): 2725-2729. DOI:10.1093/molbev/mst197 |
Theischinger G. 2000. Australian alderfly larvae and adults (Insecta: Megaloptera): a preliminary guide to the identification of larvae and survey of adults of Australian alderflies[M]. Albury: Murray Darling Freshwater Research Centre.
|
 2021, Vol. 40
2021, Vol. 40




