扩展功能
文章信息
- 刘凯凯, 袁廷柱, 唐君玮, 宋静静, 刘洪军, 迟雯丹, 盖珊珊, 于道德
- LIU Kaikai, YUAN Tingzhu, TANG Junwei, SONG Jingjing, LIU Hongjun, CHI Wendan, GE Shanshan, YU Daode
- 温度对海水青鳉胚胎发育的影响
- Effect of Temperature on the Embryonic Development of Oryzias melastigma
- 四川动物, 2020, 39(6): 658-663
- Sichuan Journal of Zoology, 2020, 39(6): 658-663
- 10.11984/j.issn.1000-7083.20200268
-
文章历史
- 收稿日期: 2020-07-13
- 接受日期: 2020-08-24
2. 长岛海洋生态文明综合试验区海洋经济促进中心,山东烟台 265800
2. Marine Economic Promotion Center of Chang Island Marine Ecological Civilization Comprehensive Test Zone, Yantai, Shandong Province 265800, China
海水青鳉Oryzias melastigma隶属于辐鳍亚纲Actinopterygii鳉形目Cypernodontiformes青鳉属,原产于印度、巴基斯坦、缅甸和泰国沿海及淡水水域(Dong et al., 2014)。海水青鳉是小型的热带鱼种,全年产卵,具有性别易区分、产卵率高、世代周期短、盐度适应范围广等特点,已逐渐成为一种理想的海洋模式鱼种(Kong et al., 2008;Chen et al., 2009;Dong et al., 2014)。由于对水质和环境中各种污染物干预敏感,海水青鳉已被广泛应用于海洋生态毒理学研究(Bao et al., 2011;穆景利等,2011;Tian et al., 2011),被国际生命科学学会健康和环境科学研究所(HESI)认定为毒理学研究的重要工具(伍辛泷等,2012)。
环境因子对于鱼类的生长发育、摄食、繁殖等起着重要作用。鱼类的生长发育易受温度、pH、溶解氧、盐度及光照强度等外界环境因素的影响。其中,温度是影响鱼类生存、生长的重要环境因子,影响鱼类胚胎发育时间、卵黄利用率、孵化后仔鱼的大小以及关键组织和结构的形成与功能(Kamler,1992;Saka et al., 2004;Gabillard et al., 2005)。不同鱼类对温度的适应范围有很大差异,同种鱼类的不同生态类群,其适温范围亦可能不同。确定鱼类胚胎发育的适宜温度范围,是进行人工繁育的关键。有关温度对鱼类胚胎发育影响的研究,国内外已有很多报道(Petereit et al., 2008;柴学军等,2011;Guillen et al., 2014),然而,不同温度下海水青鳉胚胎发育的相关研究尚处于空白。本文研究了温度对海水青鳉胚胎发育的影响,旨在探索海水青鳉胚胎发育的最佳温度范围,以期为海水青鳉的基础生物学积累资料,并为提高孵化率提供数据参考。
1 材料与方法 1.1 试验材料选取实验室世代培养的3月龄性成熟海水青鳉(10雌×10雄)作为亲鱼,暂养于玻璃缸中,体长28 mm±2 mm。每天定时投喂2次初孵卤虫的无节幼体。实验用水为青岛沙子口过滤海水,温度为27 ℃±1 ℃,盐度为32‰,光照周期为14 h: 10 h(光照:黑暗)。亲鱼产卵受精后,用塑料吸管小心地将受精卵从玻璃缸底部吸出,放入盛满海水的培养皿中,通过解剖镜观察挑选出发育正常且处于同一发育时期的受精卵(囊胚期)用于温度试验。
1.2 试验方法试验设置19 ℃、22 ℃、25 ℃、28 ℃、31 ℃和34 ℃共6个温度梯度。试验容器为200 mL烧杯,实验用水为红海盐(Israel)与超纯水配制而成的人工海水,盐度27‰。每个温度组设置2个平行,每个烧杯放入30粒挑选好的受精卵。将试验容器放入玻璃缸中,使用恒温加热棒控制水温,每天3次记录水体实际温度,计算平均值。采取逐渐升降温的方法,以每小时升(降)0.5 ℃的速度逐渐升(降)温度,达到预定温度后恒温孵化。每天使用等温水体换水1/3,保证受精卵孵化水体的新鲜。
定期使用奥林巴斯SZ61解剖镜观察受精卵的发育情况,并使用Zeiss Stereo Discovery V12体视显微镜拍照记录。在仔鱼半数出膜时计算孵化时间,仔鱼全部出膜后计算孵化率和畸形率,畸形主要指卵黄囊水肿和脊柱弯曲,结果取2组平行数据的平均值。
1.3 数据处理使用SPSS 17.0和Excel 2016处理数据、制作图表并对变化趋势作相应回归分析。生物学零度(C)与有效积温(K)是研究鱼类胚胎发育的指标,对人工育苗生产有重要的参考价值。胚胎发育速度的温度系数(Q10)可以定量表示某一温度范围内温度变化对胚胎发育速度的影响。生物学零度、有效积温和温度系数按以下公式计算:

|
式中,t为胚胎完成发育所需要的时间,V为胚胎发育所需时间的倒数(1/t),n为试验设计的温度梯度的个数,T表示胚胎发育的平均温度。
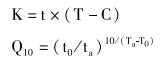
|
式中,T0表示胚胎发育的起始温度,t0表示孵化温度为T0时的孵化时间,ta表示孵化温度为Ta时的孵化时间。
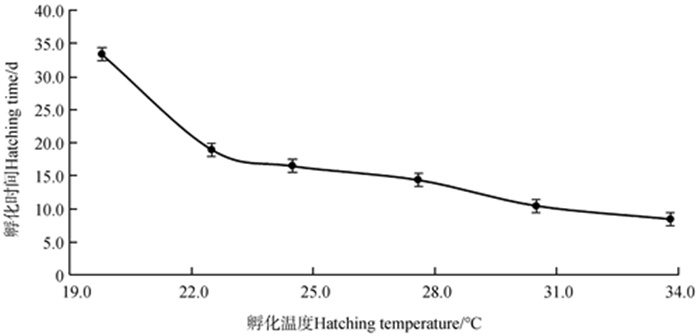
2 实验结果 2.1 温度与胚胎孵化时间的关系海水青鳉的孵化时间随孵化温度升高而缩短。水温为19.8 ℃时,孵化时间为33.4 d,水温为33.8 ℃时,孵化时间仅为8.5 d。在试验温度范围内,孵化时间(y)与孵化温度(x)呈负相关:y=0.147 4x2-9.445 1x+160.4,R2=0.933 6(P < 0.01)(图 1)。
|
| 图 1 海水青鳉Oryzias melastigma孵化时间与孵化温度的关系 Fig. 1 Relationship between hatching time and hatching temperature of Oryzias melastigma |
| |
19.8~33.8 ℃都可孵化出仔鱼。其中,27.6 ℃的孵化率最高,为63.33%,而19.8 ℃和33.8 ℃的孵化率较低,分别为10%和33.33%。在试验温度范围内,孵化率(y)随着孵化温度(x)的升高,呈现先升高后降低的趋势(图 2),其关系大致符合y=-0.725 6x2+40.192x-500.2,R2=0.886 6(P < 0.01)。在解剖镜下观察发现,28.0 ℃时胚胎畸形率最低(图 3)。孵化的正常仔鱼形态特征正常、活力旺盛(图 3:a);19.8 ℃孵化的部分仔鱼身体消瘦,脊椎弯曲呈V形(图 3:b);33.8 ℃孵化的部分仔鱼卵黄囊出现水肿(图 3:c);30.5 ℃鱼卵更易粘附脏污,滋生霉菌(图 3:d);仔鱼通过尾部破膜的形式出卵(图 3:e)。

|
| 图 2 海水青鳉孵化率、畸形率与孵化温度的关系 Fig. 2 Relationship between hatching temperature and hatching rate and deformity rate of Oryzias melastigma |
| |

|
| 图 3 孵化温度对海水青鳉初孵仔鱼发育的影响 Fig. 3 Effects of hatching temperature on the development of newly-hatched larvae of Oryzias melastigma a.正常发育的仔鱼,b. 19.8 ℃下仔鱼身体消瘦,脊椎呈V形,c. 33.8 ℃下仔鱼卵黄囊水肿,d. 30.5 ℃下鱼卵滋生霉菌,e.仔鱼尾部破膜出卵 a. normally developed larvae, b. the larval body was thin and the spine was V-shaped at 19.8 ℃, c. egg yolk sac edema of larvae at 33.8 ℃, d. fish eggs breed mold at 30.5 ℃, e. the tail of the larva breaks through the membrane and produces eggs |
| |
试验结果显示,海水青鳉胚胎发育的生物学零度和平均有效积温分别为14.89 ℃和3 919.04 ℃·h(表 1)。
| 设定温度 Set temperature/℃ |
平均温度 Average temperature/℃ |
有效积温 Effective accumulative temperature/(℃·h) |
| 19 | 19.80 | 3 935.76 |
| 22 | 22.50 | 3 470.16 |
| 25 | 24.80 | 3 924.36 |
| 28 | 27.60 | 4 392.58 |
| 31 | 30.50 | 3 933.72 |
| 34 | 33.80 | 3 857.64 |
不同孵化温度范围内海水青鳉胚胎发育速度的温度系数显示,海水青鳉在温度22.5~33.8 ℃的Q10接近2(2.04)(表 2)。
| 起始温度 Ta/℃ |
孵化时间 Ha/d |
孵化温度 T0/℃ |
孵化时间 H0/d |
温度差 Ta-T0/℃ |
温度系数 Q10 |
| 33.8 | 8.5 | 30.5 | 10.5 | 3.3 | 1.90 |
| 33.8 | 8.5 | 27.6 | 14.4 | 6.2 | 2.34 |
| 33.8 | 8.5 | 24.8 | 16.5 | 9.0 | 2.09 |
| 33.8 | 8.5 | 22.5 | 19.0 | 11.3 | 2.04 |
| 33.8 | 8.5 | 19.8 | 33.4 | 14.0 | 2.66 |
| 30.5 | 10.5 | 27.6 | 14.4 | 2.9 | 2.97 |
| 30.5 | 10.5 | 24.8 | 16.5 | 5.7 | 2.21 |
| 30.5 | 10.5 | 22.5 | 19.0 | 8.0 | 2.10 |
| 30.5 | 10.5 | 19.8 | 33.4 | 10.7 | 2.95 |
| 27.6 | 14.4 | 24.8 | 16.5 | 2.8 | 1.63 |
| 27.6 | 14.4 | 22.5 | 19.0 | 5.1 | 1.72 |
| 27.6 | 14.4 | 19.8 | 33.4 | 7.8 | 2.94 |
| 24.8 | 16.5 | 22.5 | 19.0 | 2.3 | 1.85 |
| 24.8 | 16.5 | 19.8 | 33.4 | 5.0 | 4.10 |
| 22.5 | 19.0 | 19.8 | 33.4 | 2.7 | 8.08 |
鱼类的胚胎发育容易受到外界环境因素的影响,其中温度的影响最大(Korwin-Kossakowski,2012)。本研究发现海水青鳉胚胎发育过程对温度比较敏感,孵化温度过高或过低会加速或抑制胚胎发育进程。在19.8~33.8 ℃温度范围内,海水青鳉都能孵化出膜,且随孵化温度的升高,孵化历时逐渐缩短。李岑等(2011)、Ahn等(2012)和黄贤克等(2017)分别研究了温度与泰国斗鱼Betta splendens、日本鳗鲡Anguilla japonica和黄姑鱼Nibea albiflora胚胎发育的关系,发现胚胎发育时间与温度呈负相关,本研究结果与上述结果一致。
鱼类胚胎的孵化出膜主要靠胚体的运动和孵化酶的作用(肖枫,康怀彬,2007)。温度主要通过影响孵化酶的分泌及其活性而控制仔鱼的孵出,同时影响胚胎的孵化率和孵化进程(樊廷俊,史振平,2002)。在33.8 ℃下,海水青鳉胚胎的孵化时间仅为8.5 d。可以推测,孵化温度升高可能提高了孵化酶的活性,代谢过程比低温时发生得更快,使得卵内胚胎的发育比低温时更活跃,从而加速了孵化进程。而在19.8 ℃下,海水青鳉孵化时间为33.4 d,为33.8 ℃下孵化时长的3.9倍。解剖镜下观察发现,胚胎心跳和血流速度迟缓,发育速度缓慢。低温环境降低了胚胎发育过程中孵化酶的活性,鱼卵内的新陈代谢活动受到抑制,卵黄的消耗速度降低,最终导致孵化时间延长。
升高孵化温度虽然可以加速孵化,但对鱼类的生长发育并非一定有利。高温可能具有致畸作用或引起肌肉细胞的长期改变(Finn,2007)。本实验中,孵化温度升高,初孵仔鱼出现卵黄囊水肿,畸形率增加。卵黄囊是仔鱼逐步从内源性营养阶段转入外源性营养阶段的重要营养物质来源(殷名称,1995)。鱼类卵黄囊的消耗速度取决于周围水温(Petereit et al., 2008)。高温下初孵仔鱼孵化历时短,能够提前进入外源性营养阶段,消耗的营养物质较少,导致卵黄囊体积较大。同样,温度降低,初孵仔鱼畸形率也会增加,其表现为身体消瘦、脊椎弯曲。
温度升高还会影响鱼卵表面细菌和真菌的生长(Cook et al., 2005)。海水青鳉鱼卵为沉性卵,表面附有短绒毛和长纤维丝,具有黏性(王友红等,2017)。本研究发现,与其他试验温度相比,在30.5 ℃下,鱼卵表面更容易吸附脏污,推测此温度可能适宜某种霉菌的生长。海水青鳉通过尾部摆动破膜出卵,此胚胎观察结果与陈漪等(2016)的结果一致。仔鱼尾部破膜后,头部何时出卵取决于仔鱼的力量和活力(Korwin-Kossakowski,2012)。霉菌的附着导致仔鱼孵化出卵的能耗增加,甚至造成仔鱼无法破膜而死亡,这是孵化率降低的原因之一。33.8 ℃并非海水青鳉孵化临界温度的上限。由孵化温度与孵化率的曲线方程推算出海水青鳉胚胎孵化的理论上限温度为36.51 ℃,真实的临界温度的上限需要设置更高的温度梯度进行试验。
当胚胎发育的温度系数Q10值约为2时,这一温度范围就可以确定为鱼类胚胎发育的最适温度范围(谢仰杰等,2001)。本研究显示,温度为22.5~33.8 ℃时,Q10值最接近2,综合考虑孵化率、孵化时间,可以得出海水青鳉胚胎的适宜孵化温度为24.8~30.5 ℃,最适温度在28 ℃左右。本实验所用亲鱼已繁殖3代以上,驯化温度为27 ℃±1 ℃,此温度范围内海水青鳉摄食及游动行为活跃(王润萍等,2019),与胚胎最适孵化温度相同,此实验结果与花尾胡椒鲷Plectorhinchus cinctus(谢仰杰等,2001)和斑鳜Siniperca scherzeri(胡振禧等,2014)的相关研究一致。胚胎的孵化受亲鱼质量等多种因素的影响,海水青鳉的驯化温度是否是影响胚胎发育最适温度的因素需要进一步的实验验证。
4 总结本研究设置6个温度梯度(19 ℃、22 ℃、25 ℃、28 ℃、31 ℃和34 ℃)探究了不同温度对海水青鳉胚胎发育的影响。结果表明:海水青鳉胚胎发育最适温度在28℃左右,升高或降低温度,都会导致孵化率降低,畸形率增加;胚胎发育时间与温度呈负相关;胚胎发育的生物学零度为14.89 ℃,平均有效积温为3 919.04 ℃·h。本研究为海水青鳉的胚胎发育研究提供了数据参考。
柴学军, 孙敏, 许源剑. 2011. 温度和盐度对日本黄姑鱼胚胎发育的影响[J]. 南方水产科学, 7(5): 43-49. |
陈漪, 王晓杰, 冉皓宇, 等. 2016. 海水模式种青鳉鱼(Oryzias melastigma)的胚胎发育观察[J]. 海洋与湖沼, 47(1): 71-82. |
樊廷俊, 史振平. 2002. 鱼类孵化酶的研究进展及其应用前景[J]. 海洋湖沼通报, 1: 48-56. |
胡振禧, 黄洪贵, 吴妹英, 等. 2014. 温度对斑鳜胚胎发育的影响[J]. 淡水渔业, 44(3): 104-107. |
黄贤克, 单乐州, 闫茂仓, 等. 2017. 黄姑鱼胚胎发育及其与温度和盐度的关系[J]. 海洋科学, 41(7): 44-50. |
李岑, 姜志强, 刘庆坤, 等. 2011. 泰国斗鱼的胚胎发育及温度对胚胎发育的影响[J]. 大连海洋大学学报, 26(5): 402-406. |
穆景利, 王莹, 王新红, 等. 2011. Cd2+、Hg2+、Cr6+和Pb2+对黑点青鳉(Oryzias melastigma)早期生活阶段的毒性效应研究[J]. 生态毒理学报, 6(4): 352-360. |
王润萍, 戴铃灵, 陈雅飞, 等. 2019. 短期温度、盐度胁迫对海洋青鳉鱼(Oryzias melastigma)摄食行为及抗氧化的影响[J]. 海洋与湖沼, 50(2): 378-387. |
王友红, 刘洪军, 于道德, 等. 2017. 海水青鳉胚胎发育的观察[J]. 海洋科学, 41(6): 18-25. |
伍辛泷, 黄乾生, 方超, 等. 2012. 新兴海洋生态毒理学模式生物——海洋青鳉鱼(Oryzias melastigma)[J]. 生态毒理学报, 7(4): 345-353. |
肖枫, 康怀彬. 2007. 环境胁迫对水产动物胚胎及幼苗发育影响的研究概况[J]. 生物学通报, 42(2): 19-20. |
谢仰杰, 翁朝红, 管延华, 等. 2001. 温度对花尾胡椒鲷胚胎发育的影响[J]. 集美大学学报(自然科学版), 6(2): 138-143. |
殷名称. 1995. 鱼类生态学[M]. 北京: 中国农业出版社.
|
Ahn H, Yamada Y, Okamura A, et al. 2012. Effect of water temperature on embryonic development and hatching time of the Japanese eel Anguilla japonica[J]. Aquaculture, 330: 100-105. |
Bao VWW, Leung KMY, Qiu JW, et al. 2011. Acute toxicities of five commonly used antifouling booster biocides to selected subtropical and cosmopolitan marine species[J]. Marine Pollution Bulletin, 62(5): 1147-1151. DOI:10.1016/j.marpolbul.2011.02.041 |
Chen XP, Li L, Wong CK, et al. 2009. Rapid adaptation of molecular resources from zebrafish and medaka to develop an estuarine/marine model[J]. Comparative Biochemistry & Physiology Part C, 149(4): 647-655. |
Cook MA, Guthrie KM, Rust MB, et al. 2005. Effects of salinity and temperature during incubation on hatching and development of lingcod Ophiodon elongatus Girard, embryos[J]. Aquaculture Research, 36(13): 1298-1303. DOI:10.1111/j.1365-2109.2005.01346.x |
Dong SJ, Kang M, Wu XL, et al. 2014. Development of a promising fish model (Oryzias melastigma) for assessing multiple responses to stresses in the marine environment[J/OL]. Biomed Research International, 2014: 563131[2020-02-10]. https://doi.org/10.1155/2014/563131.
|
Finn RN. 2007. The physiology and toxicology of salmonid eggs and larvae in relation to water quality criteria[J]. Aquatic Toxicology, 81(4): 337-354. DOI:10.1016/j.aquatox.2006.12.021 |
Gabillard JC, Weil C, Rescan PY, et al. 2005. Does the GH/IGF system mediate the effect of water temperature on fish growth? A review[J]. Cybium, 29(2): 107-117. |
Guillen A, Honryo T, Ibarra J, et al. 2014. Effect of water temperature on embryonic development of yellowfin tuna Thunnus albacares inhabiting the Eastern Pacific Ocean[J]. Aquaculture Science, 62(3): 319-322. |
Kamler E. 1992. Early life history of fish, an energetics approach[J]. Reviews in Fish Biology and Fisheries, 2(4): 348-349. DOI:10.1007/BF00043528 |
Kong RYC, Giesy JP, Wu RSS, et al. 2008. Development of a marine fish model for studying in vivo molecular responses in ecotoxicology[J]. Aquatic Toxicology, 86(2): 131-141. DOI:10.1016/j.aquatox.2007.10.011 |
Korwin-Kossakowski M. 2012. Fish hatching strategies: a review[J]. Reviews in Fish Biology and Fisheries, 22(1): 225-240. DOI:10.1007/s11160-011-9233-7 |
Petereit C, Haslob H, Kraus G, et al. 2008. The influence of temperature on the development of Baltic Sea sprat (Sprattus sprattus) eggs and yolk sac larvae[J]. Marine Biology, 154(2): 295-306. DOI:10.1007/s00227-008-0923-1 |
Saka S, Firat K, Çoban D. 2004. Development of the common dentex (Dentex dentex) eggs in relation to temperature[J]. Aquaculture Research, 35(3): 224-231. DOI:10.1111/j.1365-2109.2004.00986.x |
Tian L, Wang M, Li X, et al. 2011. Proteomic modification in gills and brains of medaka fish (Oryzias melastigma) after exposure to a sodium channel activator neurotoxin, brevetoxin-1[J]. Aquatic Toxicology, 104(3-4): 211-217. DOI:10.1016/j.aquatox.2011.04.019 |
 2020, Vol. 39
2020, Vol. 39




