扩展功能
文章信息
- 梁思倩, 杨坤, 黎树, 王小东, 宋昭彬
- LIANG Siqian, YANG Kun, LI Shu, WANG Xiaodong, SONG Zhaobin
- 不同水系松潘裸鲤的形态特征分析
- Multivariate Morphometric Analysis of Gymnocypris potanini in Different River Drainages
- 四川动物, 2020, 39(5): 500-507
- Sichuan Journal of Zoology, 2020, 39(5): 500-507
- 10.11984/j.issn.1000-7083.20200031
-
文章历史
- 收稿日期: 2020-01-24
- 接受日期: 2020-06-22
2. 西华师范大学生态研究院, 四川南充 637009
2. Institute of Ecology, China West Normal University, Nanchong, Sichuan Province 637009, China
松潘裸鲤 Gymnocypris potanini Herzenstein隶属鲤形目Cypriniformes鲤科Cyprinidae裂腹鱼亚科Schizothoracinae, 分布于岷江上游的干流及支流、金沙江水系和澜沧江水系(武云飞, 吴翠珍, 1992;丁瑞华, 1994;乐佩琦, 2000)。资源调查显示, 松潘裸鲤在雅砻江水系(茹辉军等, 2016;Cai et al., 2019;Ma et al., 2019)、大渡河(雷毅, 2017;Zhou et al., 2018)也有分布。因背鳍末根不分枝鳍条较硬, 其后缘下半部具细小锯齿, 具有发达的臀鳞, 其行列的前端一般达到或接近腹鳍基部等特征, 金沙江水系的松潘裸鲤被命名为硬刺松潘裸鲤 G. potanini firmispinatus Wu & Wu, 在雅砻江水系采集的样本也通常被鉴定为该亚种(Hu et al., 2016;Cai et al., 2019)。本实验室对雅砻江支流安宁河、大渡河支流南垭河采集的松潘裸鲤样本进行形态鉴定时发现, 其鳃耙数、背鳍不分枝鳍条的硬度及臀鳞发达程度等与金沙江水系的硬刺松潘裸鲤有一定差异, 似介于岷江样本和金沙江样本之间。目前松潘裸鲤的形态比较研究仅见于胡佳祥(2016)的报道, 对采自雅砻江一级支流安宁河的硬刺松潘裸鲤和岷江上游黑水河的松潘裸鲤样本的分析表明, 种与亚种的主要形态学差异在背鳍末根不分枝鳍条硬度和臀鳞行列长:硬刺松潘裸鲤的背鳍末根不分枝鳍条硬度较大, 且臀鳞行列前端一般达到或接近腹鳍基部。随着松潘裸鲤在较大范围被调查采集, 为进一步了解不同水系样本的异同并进行准确的物种及亚种鉴定, 有必要系统比较其形态特征, 并探讨雅砻江、大渡河水系种群与岷江种群和金沙江硬刺松潘裸鲤亚种间的关系。本研究采用常规形态学和多变量形态度量学方法, 通过主成分分析、判别分析、聚类分析和形态差异系数分析等比较了采自岷江、金沙江、大渡河、雅砻江水系的8个松潘裸鲤种群的形态差异, 以期为其分类研究积累基础资料, 为不同水系样本的物种鉴定提供一定参考。
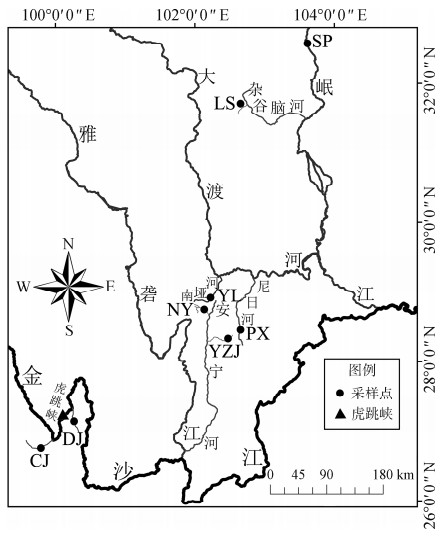
1 材料与方法 1.1 样本采集松潘裸鲤样本分别于2016年、2017年采自岷江上游干流及支流杂谷脑河, 大渡河中游支流南垭河和普雄河, 雅砻江下游支流安宁河支流孙水河和依兹觉河, 以及金沙江上游支流冲江河和大具河(表 1, 图 1), 所有样本均用95%乙醇保存。
| 种群 Population |
采集地 Sampling site |
水系 River drainage |
样本量 Sample size |
体长 Body length/mm |
体质量 Body mass/g |
采集时间 Sampling time |
| 松潘(SP) | 松潘县 | 岷江干流 | 22 | 89.88±19.10 | 10.86±7.43 | 2017-11-16 |
| 来苏(LS) | 来苏河 | 岷江支流 杂谷脑河 |
26 | 107.69±18.68 | 14.83±6.88 | 2016-09-29 |
| 冶勒(YL) | 冶勒乡 | 大渡河支流 南垭河 |
30 | 98.48±15.58 | 17.29±11.55 | 2017-05-21 |
| 普雄(PX) | 普雄镇 | 大渡河支流 尼日河上游普雄河 |
18 | 92.96±14.23 | 9.37±4.03 | 2017-05-21 |
| 宁源(NY) | 宁源乡 | 安宁河支流 孙水河 |
20 | 50.79±6.90 | 2.11±0.91 | 2016-10-24 |
| 依兹觉(YZJ) | 依兹觉乡 | 安宁河支流 依兹觉河 |
30 | 87.91±21.72 | 13.21±9.92 | 2016-10-23 |
| 冲江(CJ) | 冲江河 | 金沙江支流 | 30 | 64.07±9.44 | 3.75±1.76 | 2016-11-07 |
| 大具(DJ) | 大具河 | 金沙江支流 | 30 | 94.37±9.75 | 13.20±4.24 | 2016-11-07 |
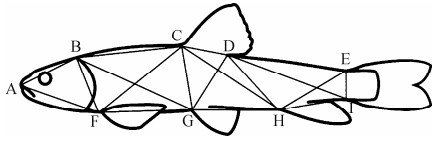
对每个样本的背鳍、左胸鳍、左腹鳍和臀鳍鳍条数进行计数, 并使用解剖剪和镊子打开样本的鳃盖, 取下第一鳃弓放置于解剖镜下, 观察并记录第一鳃弓外侧鳃耙数。采用电子天平称量所有样本的体质量(精度为0.01 g), 用数显游标卡尺(精度为0.01 mm)测量可量性状, 常规性状包括全长、体长、体高、头长、吻长、眼径长、眼间距、尾长、尾柄长、尾柄高、臀鳞行列长(裂腹鱼亚科鱼类的肛门和臀鳍基部间两侧特化的大型鳞片的排列长度)共11项, 框架度量采用9个形态解剖学坐标点(图 2), 共计18个框架数据。
|
| 图 2 松潘裸鲤框架特征 Fig. 2 Truss network of distance measurements of Gymnocypris potanini A.吻端, B.头背部末端, C.背鳍起点, D.背鳍基部末端, E.尾鳍背部起点, F.胸鳍起点, G.腹鳍起点, H.臀鳍起点, I.尾鳍腹部起点 A. snout tip, B. posterior point of occipital, C. origin of dorsal fin, D. posterior end of dorsal fin base, E. dorsal origin of caudal fin, F. origin of pectoral fin, G. origin of pelvic fin, H. origin of anal fin, I. ventral origin of caudal fin |
| |
对每个种群的5项可数性状进行卡方检验。整合统计所有样本的8个常规测量性状与18个框架性状, 使用SPSS 24.0和Microsoft Excel 2003进行数据处理, 参照杨琴等(2019)的方法进行KMO和Barttlett球度检验、主成分、聚类和判别分析。为消除鱼体大小对形态参数的影响, 将头部性状参数除以头长, 臀鳞行列长除以腹鳍基部至臀鳍基部的距离(GH), 其他参数除以体长予以标准化处理。根据Mayr等(1953)划分亚种的方法, 计算各种群间的形态差异系数(coefficient of difference, CD )。
2 结果 2.1 可数性状8个种群的可数性状结果表明, 不同水系松潘裸鲤的背鳍(3, 7)、臀鳍鳍条数(3, 5)相同, 胸鳍和腹鳍分枝鳍条数、第一鳃弓外侧鳃耙数存在一定的变异(表 2)。岷江种群(SP、LS)的第一鳃弓外侧鳃耙数较少, 范围为6~9和6~8, 众数均为8, 平均值分别为7.45和7.23。金沙江种群的第一鳃弓外侧鳃耙数相比岷江种群稍多, 范围均为7~10, CJ种群的众数为7和8, 平均值为8.17, DJ种群的众数为9, 平均值为8.73。大渡河(YL、PX)和安宁河(NY、YZJ)4个种群的众数分别为7、8、7和10, 均值分别为7.48、8.28、7.52和9.27。各种群间的第一鳃弓外侧鳃耙数、胸鳍和腹鳍分枝鳍条数之间的差异均无统计学意义(χ 2检验: P >0.05)。此外, 大渡河PX和安宁河YZJ种群中部分较大个体的下颌具有很细窄的角质前缘, 出现比例分别为44.4%和30.0%, 角质宽度分别为4.638 mm±0.976 mm和5.037 mm±1.342 mm, 角质厚度分别为0.798 mm±0.114 mm和0.797 mm±0.098 mm。
| 种群 Population |
水系 River drainage |
第一鳃弓外侧鳃耙数 Number of outer gill rakers of the first gill arch |
胸鳍分枝鳍条数 Branched ray number of pectoral fin |
腹鳍分枝鳍条数 Branched ray number of pelvic fin |
||||||||||
| 6 | 7 | 8 | 9 | 10 | 平均值 | 16 | 17 | 18 | 平均值 | 8 | 9 | 平均值 | ||
| 松潘(SP) | 岷江 | 4 | 7 | 9 | 2 | 0 | 7.45 | 11 | 8 | 3 | 16.64 | 17 | 5 | 8.23 |
| 来苏(LS) | 岷江 | 6 | 8 | 12 | 0 | 0 | 7.23 | 14 | 10 | 2 | 16.54 | 19 | 7 | 8.27 |
| 冶勒(YL) | 大渡河 | 4 | 13 | 7 | 6 | 0 | 7.48 | 22 | 8 | 0 | 16.27 | 27 | 3 | 8.10 |
| 普雄(PX) | 大渡河 | 0 | 3 | 9 | 4 | 2 | 8.28 | 10 | 7 | 1 | 16.50 | 13 | 5 | 8.28 |
| 宁源(NY) | 安宁河 | 2 | 9 | 6 | 3 | 0 | 7.52 | 16 | 4 | 0 | 16.20 | 13 | 7 | 8.35 |
| 依兹觉(YZJ) | 安宁河 | 1 | 0 | 4 | 10 | 15 | 9.27 | 15 | 7 | 8 | 16.77 | 19 | 11 | 8.37 |
| 冲江(CJ) | 金沙江 | 0 | 10 | 10 | 5 | 5 | 8.17 | 18 | 10 | 2 | 16.47 | 21 | 9 | 8.30 |
| 大具(DJ) | 金沙江 | 0 | 2 | 9 | 14 | 5 | 8.73 | 15 | 8 | 7 | 16.73 | 18 | 12 | 8.40 |
| 注:各种群的数字(除平均值外)为对应鳃耙或鳍条数的样本数量 Note:The values of the different populations (excluding the averages) refer to the specimen numbers corresponding to the numbers of gill rakers or fin |
||||||||||||||
共测量了206尾松潘裸鲤的5 356个形态学数据。所选形态参数的KMO值为0.823, Barttlett球度检验被拒绝(P < 0.05), 表明所选变量适合做因子分析。所有松潘裸鲤的26个形态参数中共提取了7个主成分, 其中前3个主成分解释形态性状的累计贡献率为45.269%(表 3), 对第一主成分起主要作用的是AF/体长、AB/体长、头长/体长、EH/体长、HI/体长等鱼体头部和尾部特征值;对第二主成分影响较大的是DG/体长、EI/体长、尾柄高/体长、CG/体长、FG/体长等特征值;对第三主成分起主要作用的是DH/体长、DE/体长、CH/体长、DI/体长、GH/体长等特征值。
| 性状 Character |
第一主成分 PC1 |
第二主成分 PC2 |
第三主成分 PC3 |
性状 Character |
第一主成分 PC1 |
第二主成分 PC2 |
第三主成分 PC3 |
| 头长/体长 | 0.710* | 0.315 | 0.120 | CG/体长 | 0.169 | 0.669* | -0.089 |
| 体高/体长 | 0.276 | 0.654* | 0.216 | CH/体长 | 0.053 | 0.290 | 0.677* |
| 吻长/头长 | 0.167 | 0.219 | -0.095 | CD/体长 | 0.586 | 0.137 | 0.049 |
| 眼径/头长 | 0.443 | -0.337 | -0.177 | DG/体长 | 0.047 | 0.817* | 0.055 |
| 眼间距/头长 | -0.138 | 0.069 | -0.018 | DH/体长 | -0.115 | 0.216 | 0.805* |
| 臀鳞行列长/GH | 0.066 | 0.144 | 0.136 | DI/体长 | 0.387 | 0.010 | 0.643* |
| 尾柄长/体长 | -0.056 | -0.138 | -0.062 | DE/体长 | 0.442 | -0.052 | 0.731* |
| 尾柄高/体长 | 0.323 | 0.690* | 0.136 | EH/体长 | 0.643* | 0.136 | 0.155 |
| AB/体长 | 0.733* | 0.244 | 0.084 | EI/体长 | 0.236 | 0.705* | 0.306 |
| AF/体长 | 0.824* | 0.228 | 0.098 | FG/体长 | 0.169 | 0.669* | -0.089 |
| BC/体长 | 0.133 | 0.112 | 0.156 | GH/体长 | -0.072 | 0.161 | 0.453 |
| BF/体长 | 0.512 | 0.324 | 0.169 | HI/体长 | 0.631* | 0.024 | 0.015 |
| BG/体长 | 0.208 | 0.351 | 0.325 | 贡献率/% | 26.390 | 10.984 | 7.931 |
| CF/体长 | -0.022 | 0.273 | 0.193 | 累计贡献率/% | 26.390 | 37.338 | 45.269 |
| 注:*有主要贡献的变量;性状中的缩写见图 2 Note:* Variables that have a major contribution;abbreviations see Fig. 2 |
|||||||
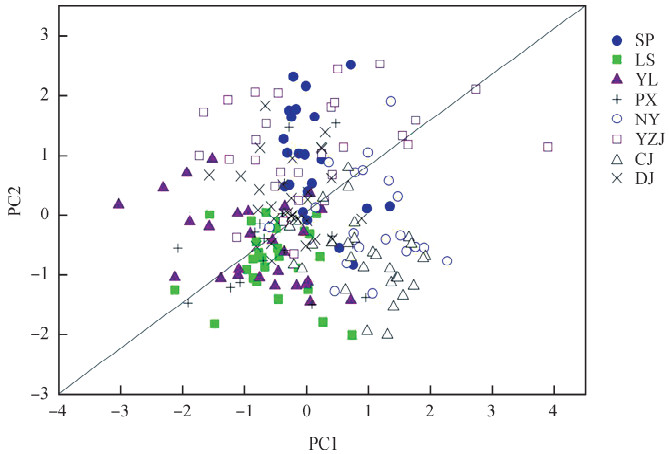
第一、第二主成分分析图可看出, 不同水系的松潘裸鲤种群间均有较大程度的重叠(图 3), 没有按照不同水系分离开, 不同水系种群之间的形态特征既相似又存在一定差异。通过横轴第一主成分正值方向, CJ可与其他水系种群区分开, SP、YZJ与LS、CJ在纵轴第二主成分上有一定区别。
|
| 图 3 不同水系松潘裸鲤26个形态学特征的主成分分析散点图 Fig. 3 Scatter plots of principal component analysis based on 26 morphometric characters of Gymnocypris potanini from different river drainages |
| |
利用26个形态参数对8个松潘裸鲤种群进行判别分析, 用逐步判别法对所有个体进行预测分类, 除个别个体被误判外, 所有个体的综合判别准确率为74.1%(表 4), 其中SP(100%)、LS(88.5%)和YZJ(86.7%)的判别率很高, 而NY(60 %)、DJ(46.7%)的判别率较低。为提升判别率, 筛选出8个对区分各群体有较大贡献率的变量, 并建立各种群的判别函数。V1~V8所对应形态测量参数分别为AB/体长、头长/体长、眼径/头长、尾柄高/体长、CH/体长、体高/体长、CD/体长、HI/体长。判别分析时将测量数据的校正值分别代入8个判别方程, 所得函数值最大即判别为该群体。
| 种群 Population |
SP | LS | YL | PX | NY | YZJ | CJ | DJ | 判别率 Percent of identification/% |
综合判别率 Total percent of discriminant/% |
| 松潘(SP) | 22 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 100.0 | 74.1 |
| 来苏(LS) | 0 | 23 | 0 | 2 | 0 | 0 | 0 | 1 | 88.5 | |
| 冶勒(YL) | 0 | 0 | 22 | 5 | 0 | 1 | 0 | 2 | 72.4 | |
| 普雄(PX) | 0 | 2 | 1 | 12 | 1 | 1 | 1 | 0 | 66.7 | |
| 宁源(NY) | 0 | 0 | 0 | 2 | 12 | 0 | 3 | 3 | 60.0 | |
| 依兹觉(YZJ) | 0 | 0 | 0 | 4 | 0 | 26 | 0 | 0 | 86.7 | |
| 冲江(CJ) | 0 | 0 | 0 | 2 | 5 | 0 | 22 | 1 | 73.3 | |
| 大具(DJ) | 0 | 4 | 3 | 3 | 2 | 2 | 2 | 14 | 46.7 |
SP=432.214V1+1 298.707V2+1 462.701V3+ 1 488.795V4+2 612.051V5-954.733V6+597.533V7+ 1 331.080V8
LS=420.308V1+1 403.842V2+1 323.706V3+ 876.714V4+1 091.768V5-381.430V6+1 118.628V7+ 1 025.525V8
YL=149.599V1+1 344.082V2+1 456.791V3+ 1 103.537V4+1 234.564V5-155.83V6+1 050.306V7+ 1 048.756V8
PX=277.705V1+1 402.169V2+1 527.081V3+ 1 438.153V4+1 287.587V5-412.822V6+1 074.42V7+ 956.313V8
NY=303.619V1+1 655.814V2+1 527.396V3+ 1 021.865V4+1 279.728V5-202.698V6+999.72V7+ 992.619V8
YZJ=327.842V1+1 403.117V2+1 329.223V3+ 1 649.662V4+1 256.298V5-218.532V6+1 128.92V7+872.084V8
CJ=438.449V1+1 726.003V2+1 605.759V3+ 805.288V4+1 107.291V5-272.276V6+1 014.894V7+ 1 027.766V8
DJ=341.537V1+1 413.041V2+1 437.896V3+ 1 107.974V4+1 217.341V5-206.043V6+1 008.302V7+ 1 142.578V8
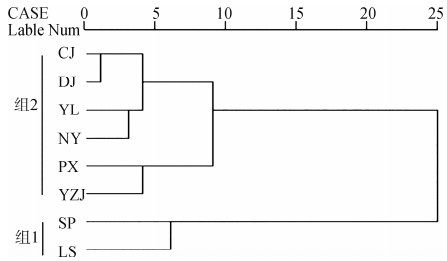
2.2.3 形态聚类分析基于不同松潘裸鲤种群形态性状的欧式距离绘制的聚类图显示, 岷江水系的2个种群SP和LS聚为一支, 其他水系的6个种群聚为另一支。采自金沙江的CJ、DJ 2个种群聚在一起, 而大渡河和雅砻江种群未按水系聚在一起, 地理距离较近的大渡河YL种群和安宁河NY种群、大渡河PX种群和安宁河YZJ种群分别聚为一支(图 4)。
|
| 图 4 基于松潘裸鲤种群间欧式距离构建的聚类图 Fig. 4 Cluster dendrogram of Gymnocypris potanini samples based on Euclidean distances |
| |
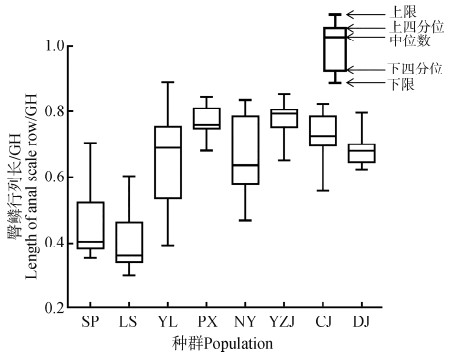
不同水系松潘裸鲤种群间平均 CD 为0.332, 仅在CG/体长和臀鳞行列长/GH 2个形态性状上超过了1.28。岷江SP种群在CG/体长这一体高特征上与除大渡河YL种群外的6个种群间有明显差异(CD =1.326~2.398)。在臀鳞行列长/GH的差异上, CD 超过1.28的有:岷江SP种群与安宁河YZJ种群(CD =1.543), 岷江LS种群分别与大渡河PX种群(CD =2.396)、安宁河YZJ种群(CD =2.046)、金沙江DJ种群(CD =1.715);岷江水系样本的臀鳞行列长/GH明显小于其他水系样本(图 5)。
|
| 图 5 不同水系松潘裸鲤臀鳞行列长 Fig. 5 The length of anal scale row of Gymnocypris potanini from different river drainages GH.腹鳍起点到臀鳍起点的距离 GH. the distance from the origin of pelvic fin to the origin of anal fin |
| |
鱼类的形态性状作为分类的重要依据, 是基因和环境共同作用的结果, 在中性选择的长期作用下, 不同水系地理种群产生了相应的适应性变异(Campana et al., 1995;杨琴等, 2019)。本研究表明, 岷江、大渡河、雅砻江、金沙江水系的松潘裸鲤在形态上存在一定的差异, 但鳃耙数和背鳍、胸鳍、腹鳍及臀鳍鳍条数等可数性状的差异无统计学意义, 不足以用于不同水系松潘裸鲤的形态鉴定。除岷江水系的SP(100%)、LS(88.5%)种群, 安宁河YZJ种群(86.7%)外, 其余种群的判别率均较低, 判别分析能较准确地识别岷江水系个体, 但对其余水系个体的识别有限。可见, 不同水系松潘裸鲤的外部形态特征差异不明显, 这可能与其生活的环境条件类似, 以及长期的适应性进化等有关。不过, 岷江水系松潘裸鲤的臀鳞行列长/GH明显小于其余水系个体, 形态差异系数分析结果显示, SP种群与YZJ种群、LS种群与PX种群、LS种群与YZJ种群、LS种群与DJ种群间的臀鳞行列长/GH差异系数超过了1.28。因此, 岷江水系个体臀鳞行列长度比例与其余水系个体存在明显差异, 结合形态性状的判别分析, 可以和其余水系个体进行有效的识别。
聚类分析结果表明, 岷江水系种群聚为一支, 金沙江水系种群聚在一起, 这2个水系内的松潘裸鲤具有较近的亲缘关系。大渡河、雅砻江水系种群和金沙江水系种群聚在一起, 显示其与金沙江水系比与岷江水系有更近的亲缘关系。大渡河YL种群和安宁河NY种群聚在一起, 大渡河PX种群和安宁河YZJ种群聚在一起, 这2个水系种群的亲缘关系与种群间的地理距离相关, YL种群和NY种群、PX种群、YZJ种群分别相距约20 km、67 km、69 km, PX种群与YZJ种群、YL种群、NY种群分别相距约19 km、67 km和68 km。依据形态特征的大渡河和安宁河松潘裸鲤种群间的亲缘关系与种群遗传分析结果一致, NY种群与YL种群具有较近的遗传关系, 而与同水系的YZJ种群有较大的遗传分化, 因而推测NY种群和YL种群是共同起源的(Zhou et al., 2018)。YZJ种群和PX种群也分布在地理距离靠近的河流源头区域, 基于形态特征的亲缘关系最近, 因而可以推测其也是共同起源的。
根据Mayr等(1953)提出的差异系数和75%规则, 若差异系数大于1.28, 则差异达到亚种水平, 小于1.28则属于种群间形态性状差异。松潘裸鲤在CG/体长、臀鳞行列长/GH这2个形态性状上的 CD 超过了1.28, 且岷江种群与其余水系种群间存在显著差异, 因此, 硬刺松潘裸鲤亚种是有效的, 并可根据臀鳞行列长鉴别不同的亚种。大渡河、雅砻江、金沙江水系松潘裸鲤间的形态差异不明显, 具有较近的亲缘关系, 且均具有较长的臀鳞行列, 因而大渡河和雅砻江水系的松潘裸鲤为硬刺松潘裸鲤亚种。
裸鲤属鱼类的下颌内侧或具角质, 但不形成锐利角质前缘(乐佩琦, 2000)。但本次形态检测中发现大渡河PX种群和安宁河YZJ种群中部分个体的下颌具有窄而薄的角质。该现象在纳木湖裸鲤 G. namensis 中也存在, 极少数个体形成细窄的角质前缘(乐佩琦, 2000)。这可能是为了取食着生藻类的适应性变化。在其他一些下颌有发达角质前缘的裂腹鱼类中却发现, 为了适应湖泊等静水环境, 角质前缘发生退化的适应性改变。如:九寨沟海子中的嘉陵裸裂尻鱼 Schizopygopsis kialingensis 下颌前缘角质退化(个人观察), 高原裸裂尻鱼 S. stoliczkai 班公湖亚种下颌锐利角质几乎完全退化(王贺崐元等, 2017), 齐口裂腹鱼 Schizothorax prenanti 伍须海样本的下颌角质前缘明显退化(Liang et al., 2011)。
致谢: 吴波、雷毅、文秦超参与了鱼类样本的采集, 在此表示感谢。
丁瑞华. 1994. 四川鱼类志[M]. 成都: 四川科学技术出版社.
|
胡佳祥. 2016.硬刺松潘裸鲤亚种与种的线粒体基因组、遗传多样性及其繁殖生物学的初步研究[D].四川: 四川农业大学.
|
乐佩琦. 2000. 中国动物志硬骨鱼纲鲤形目(下卷)[M]. 北京: 科学出版社.
|
雷毅. 2017.松潘裸鲤(Gymnocypris potanini )微卫星标记筛选及遗传多样性研究[D].成都: 四川大学.
|
茹辉军, 张燕, 李云峰, 等. 2016. 雅砻江支流安宁河鱼类群落组成及资源现状[J]. 水生态学杂志, 37(5): 68-74. |
王贺崐元, 汤永涛, 李国刚, 等. 2017. 高原裸裂尻鱼头部轮廓形状及其变异的几何形态测量分析[J]. 水生生物学报, 41(1): 182-193. |
武云飞, 吴翠珍. 1992. 青藏高原鱼类[M]. 成都: 四川科学技术出版社.
|
杨琴, 赵峰, 宋超, 等. 2019. 长江口及邻近海域凤鲚4个不同地理群体的形态差异[J]. 海洋渔业, 41(3): 294-303. |
Cai L, Zhang P, Johnson D, et al. 2019. Effects of prolonged and burst swimming on subsequent burst swimming performance of Gymnocypris potanini firmispinatus (Actinopterygii, Cyprinidae)[J]. Hydrobiologia, 843(1): 201-209. DOI:10.1007/s10750-019-04049-4 |
Campana SE, Gagné JA, McLaren JW. 1995. Elemental fingerprinting of fish otoliths using ID-ICPMS[J]. Marine Ecology Progress Series, 122: 115-120. DOI:10.3354/meps122115 |
Hu J, Cai Y, Xiong S, et al. 2016. The complete mitochondrial DNA of Gymnocypris potanini firmispinatus and comparative mitogenomic analyses of the Gymnocypris species[J]. Mitochondrial DNA Part B, 1(1): 436-437. DOI:10.1080/23802359.2016.1180556 |
Liang J, Liu Y, Zhang X, et al. 2011. An observation of the loss of genetic variability in prenant's schizothoracin, Schizothorax prenanti , inhabiting a plateau lake[J]. Biochemical Systematics and Ecology, 39(4-6): 361-370. DOI:10.1016/j.bse.2011.05.005 |
Ma B, Nie Y, Wei K, et al. 2019. Estimates on age, growth, and mortality of Gymnocypris firmispinatus (Cyprinidae:Schizothoracinae) in the Anning River, China[J]. Journal of Oceanology and Limnology, 37(2): 736-744. DOI:10.1007/s00343-019-7372-1 |
Mayr E, Linsley EG, Usinger RL. 1953. Methods and principles of systematic zoology[M]. New York: McGraw-Hill.
|
Zhou Y, Lei Y, Lu Y, et al. 2018. Population genetics of a Chinese endemic, Gymnocypris potanini Herzenstein, threatened by population isolation:conflicting patterns between microsatellites and mitochondrial DNA[J]. Hydrobiologia, 819(1): 145-159. DOI:10.1007/s10750-018-3633-9 |
 2020, Vol. 39
2020, Vol. 39