扩展功能
文章信息
- 杜浩, 罗江, 周亮, 熊伟, 吴金平, 乔新美, 冷小茜, 肖新平, 仝爽, 刘志刚, 危起伟
- DU Hao, LUO Jiang, ZHOU Liang, XIONG Wei, WU Jinping, QIAO Xinmei, LENG Xiaoqian, XIAO Xinping, TONG Shuang, LIU Zhigang, WEI Qiwei
- 长江鲟子三代繁育技术研究
- Technologies for Reproduction of the Third Generation of Acipenser dabryanus in Captive
- 四川动物, 2020, 39(2): 197-203
- Sichuan Journal of Zoology, 2020, 39(2): 197-203
- 10.11984/j.issn.1000-7083.20190401
-
文章历史
- 收稿日期: 2019-11-24
- 接受日期: 2020-01-07
2. 宜宾珍稀水生动物研究所, 四川宜宾 644000
2. Rare Aquatic Animal Research Institute, Yibin, Sichuan Province 644000, China
长江鲟Acipenser dabryanus又名达氏鲟,是我国长江上游特有鱼类,属于淡水定居型鲟鱼,主要分布于金沙江下游和长江中上游干流及其各大支流中(Boyd et al., 2003)。长江鲟作为软骨硬鳞鱼类,在研究地球气候变化和鱼类演化等方面具有重要意义(Zhang et al., 2018)。同时,长江鲟耐高温、抗病力强,具有巨大的潜在经济价值,其肉质鲜嫩、营养丰富,且无肌间刺,皮可应用于制胶和皮革方面,骨有利于防止老年骨质疏松和增强机体免疫力,特别是鲟鱼子酱具有“黑色黄金”之称,具有高蛋白、低糖的特点,氨基酸种类齐全,二十碳五烯酸(EPA)和二十二碳六烯酸(DHA)含量高,矿物质含量丰富,尤其是铁和锌。作为我国特有珍稀鱼类,长江鲟具备重大的产业利用潜能。
20世纪80年代后,由于过度捕捞、水工建设、航道整治等人类活动的影响,长江鲟自然种群规模急剧缩小,20世纪末,其自然繁殖活动停止,野外种群几乎灭绝。长江鲟1988年被列为国家Ⅰ级重点保护野生动物,1997年被列入濒危野生动植物种国际贸易公约(CITES)附录Ⅱ保护物种,2010年被世界自然保护联盟(IUCN)升级为极危(CR)物种。长江鲟物种保护自20世纪90年代开始,20多年来围绕长江鲟的资源修复(Du et al., 2014;Ye et al., 2016, 2018)、人工繁育(龚全等, 2015, 2016;颉璇等,2018)和保护养殖(褚志鹏等,2018;罗江等,2018;张磊等,2018)进行了系统研究。在人工繁育方面,四川省宜宾珍稀水生动物研究所(以下简称“宜宾所”)1998年率先突破了内塘驯养野生长江鲟的人工繁殖,获得第一批子一代长江鲟,并在2004年实现了规模化;2007年宜宾所与中国水产科学研究院长江水产研究所(以下简称“长江所”)联合攻关,实现了子一代长江鲟的规模化全人工繁殖,获得第一批子二代长江鲟;2016年长江所首次突破人工调控长江鲟的自然交配产卵(杜浩等,2016),并在2017年和2018年连续2年获得重复成功。
在2016—2017年的跟踪观测中,已发现部分雄鱼成熟,部分雌鱼性腺发育良好,有望2018年实现雌雄鱼的人工催产繁殖。2018年4月,通过对不同养殖条件下子二代长江鲟后备亲鱼的连续性腺发育监测,实现雌雄鱼的同步成熟与人工催产繁殖,成功繁育出子三代长江鲟苗种。本文对长江鲟子三代繁育技术进行了系统总结,以期为今后规模化长江鲟人工繁育和利用提供参考。
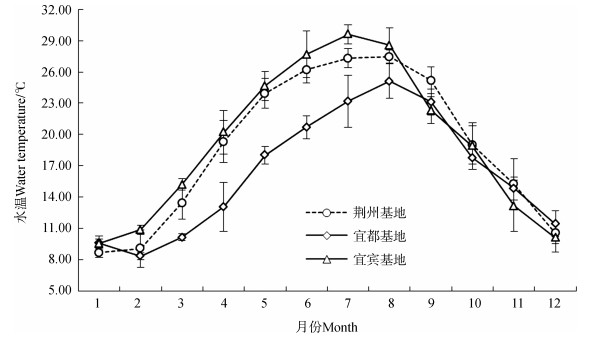
1 材料与方法 1.1 亲鱼来源此次繁育试验所用亲鱼来源于长江所荆州、宜都基地和宜宾所官兴基地经人工养殖的子二代长江鲟,年龄为6~8龄,各基地养殖条件见图 1和表 1,参照Du等(2017)对性腺发育期判定方法,采用Terason2000型B超仪对子二代长江鲟亲鱼性腺发育期进行判断。
|
| 图 1 各养殖基地水温周年变化 Fig. 1 Annual variation of water temperature at different farms |
| |
| 参数 Parameter |
地点Location | |||
| 荆州Jinzhou | 宜都Yidu | 宜宾Yibin | ||
| 水池规格/m | 直径16×深1.8 | 直径25×深2.5 | 长60×宽50×深1.5 | |
| 水源 | 湖水+地下水 | 水库 | 水库 | |
| 水温/℃ | 7~29 | 8~26 | 9~31 | |
| 密度/(kg·m-3) | 8~10 | 6~8 | 3~5 | |
| 年龄 | 6 | 6 | 7~8 | |
| 数量/尾 | 1 000 | 200 | ||
| 成熟比例/% | 5 | 20 | ||
子二代长江鲟亲鱼采用配合饲料、冰鲜饵料和鲜活饵料进行强化培育,配合饲料为键马牌鲟鱼专用10#饲料,冰鲜饵料为多春鱼Osmerus mordax,鲜活饵料为水蚯蚓Limnodrilus hoffmeisteri,日投喂量为体质量的0.5%,3种饵料投喂比例为1: 1: 1,投喂先后次序为配合饲料、冰鲜饵料和鲜活饵料。同时,每隔1星期,在多春鱼中添加养殖用多维(康益达生物有限公司),添加比例为6 g·kg-1,将多维装入空的胶囊内,塞入多春鱼体内,再进行投喂。
1.3 人工催产、授精及孵化2018年3月26—30日,同步对各基地子二代的长江鲟亲鱼实施催产,催产水温为19.0~20.0 ℃,催产剂为宁波市第二激素厂生产的促黄体素释放激素类似物(LRH-A2),雄鱼采用一针注射,剂量为5 μg·kg-1,雌鱼采用两针注射,第一针剂量为1 μg·kg-1,第二针剂量为9 μg·kg-1,中间间隔12 h。精卵均采用腹部按压法采集,精子采集后,于2~4 ℃充氧保存,每隔8 h更换氧气1次,卵子分批采集,采用干法授精,在显微镜下检查精子活力,挑选活力好的精子用于人工授精。采用滑石粉及充气脱粘装置进行受精卵脱粘,脱粘时间约45 min,采用瓶式孵化器进行孵化,孵化水温19.0~20.0 ℃。
1.4 苗种培育子三代长江鲟仔鱼孵化出膜后,用玻璃钢盆进行培育,规格为直径1 m×深0.4 m,待仔鱼卵黄囊完全吸收,沉入池底时(约5~6日龄),开始用剁碎的鲜活水蚯蚓进行开口,当全长至3 cm左右(约20日龄)时,开始转食,转食过程中逐渐往水蚯蚓中增加配合饲料,直至全部转为配合饲料:水蚯蚓→水蚯蚓+配合饲料→配合饲料。
1.5 数据统计长江鲟亲鱼的体长、体质量等利用担架固定鱼体后常规离水称量。定期抽样仔鱼,在培养皿中测量。
利用游标卡尺测量卵径,采用体积法估算产卵量,以平均卵质量估算绝对怀卵量;胚胎发育至原肠中后期开始统计受精率,用Excel 2010进行数据处理,按以下公式计算:
催产率=成功产卵(精)亲鱼数量/测试组雌(雄)亲鱼总数量×100%
受精率=受精卵数量/产卵总数量×100%
孵化率=出苗数量/受精卵数量×100%
利用游标卡尺测量卵径,采用体积法估算产卵量,以平均卵质量估算绝对怀卵量;胚胎发育至原肠中后期开始统计受精率,用Excel 2010进行数据处理,按以下公式计算:
2 结果与分析 2.1 子二代长江鲟亲鱼的生物学特性通过B超判定性腺发育期,本次繁殖实验共挑选出可用于催产的子二代长江鲟亲鱼12尾,其中雄鱼6尾,体质量9.9~22.2 kg,平均(17.02±4.97) kg,雌鱼6尾,体质量16.6~25.6 kg,平均(20.57±3.23) kg(表 2)。
| 性别 Sex |
编号 ID |
来源Source | 年龄 Age |
体长 Body length /cm |
体质量 Body mass /kg |
性腺发育期 Stage of gonad development |
基地 Farm |
|
| F1亲本 F1parent |
F0原种 F0original species |
|||||||
| 雄鱼 | 3507 | F1-2012 | F0-1993~F0-1996 | 6 | 110 | 14.7 | ♂Ⅳ- | 荆州 |
| 4051 | 6 | 105 | 9.9 | ♂Ⅳ | 宜都 | |||
| 3866 | F1-2010 | 8 | 108 | 13.7 | ♂Ⅳ+ | 官兴 | ||
| 3836 | 8 | 126 | 22.2 | ♂Ⅳ | 官兴 | |||
| 3830 | 8 | 116 | 20.1 | ♂Ⅳ+ | 官兴 | |||
| 3656 | 8 | 125 | 21.5 | ♂Ⅳ+ | 官兴 | |||
| 雌鱼 | 3554 | F1-2012 | F0-1993~F0-1996 | 6 | 113 | 18.6 | ♀Ⅳ- | 宜都 |
| 4010 | 6 | 112 | 16.6 | ♀Ⅳ | 官兴 | |||
| 4066 | F1-2010 | 8 | 117 | 19.9 | ♀Ⅳ+ | 官兴 | ||
| 3841 | 8 | 120 | 19.7 | ♀Ⅳ+ | 官兴 | |||
| 3531 | 8 | 128 | 25.6 | ♀Ⅳ | 官兴 | |||
| 4060 | 8 | 126 | 23.0 | ♀Ⅳ | 宜都 | |||
| 注:F0-1993~F0-1996表示在1993—1996年从野外采集的原种;F1-2010和F1-2012分别表示在2010年和2012年通过原种繁殖的子一代Note:F0-1993-F0-1996 indicate the original species collected in the field from 1993 to 1996;F1-2010 and F1-2012 indicate the first generation bred from the original species in 2010 and 2012,respectively | ||||||||
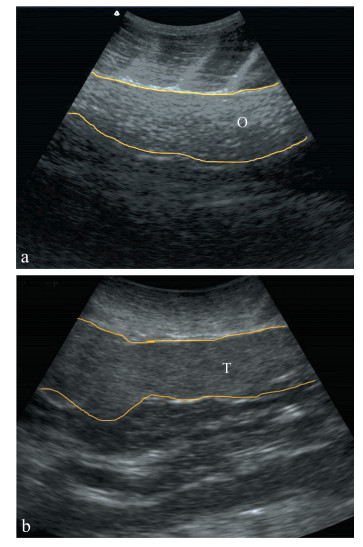
子二代长江鲟雌雄亲鱼Ⅳ期性腺在腹腔中均比较饱满,雌鱼Ⅳ期卵巢中卵粒清晰可见,整齐饱满,质地均匀(图 2:a),雄鱼Ⅳ期精巢呈高密度均质云状(图 2:b)。
|
| 图 2 子二代长江鲟成熟亲鱼腹部B超影像 Fig. 2 The B-ultrasonic images of the parent Acipenser dabryanus of the second generation in the abdomen a.雌鱼,b.雄鱼;O. Ⅳ期卵巢,T. Ⅳ期精巢 a. gonad of mature female fish, b. gonad of mature male fish; O. ovary (stage Ⅳ), T. testis (stage Ⅳ) |
| |
本次子二代长江鲟催产实验,成功催产雄鱼5尾和雌鱼2尾,催产率分别为83.33%和33.33%,效应时间分别为(12.40±1.67) h和(23.00±1.41) h,雌鱼产卵量为(4.50±2.12)万粒,卵径为(2.65±0.19) mm,雄鱼产精量为(510.2±129.1) mL,精子剧烈运动时间和精子寿命分别为(47.47±7.61) s和(236.00±57.71) s。共计获卵9万粒,获精液3 000 mL,平均受精率(87.53±5.36)%,平均孵化率(76.14±4.13)%,共孵出子三代长江鲟仔鱼约6万尾,获开口期仔鱼约3万尾(表 3)。
| 项目Item | 平均值Mean | 范围Range | |
| 效应时间/h | 雄 | 12.40±1.67 | 10~14 |
| 雌 | 23.00±1.41 | 22~24 | |
| 催产率/% | 雄 | 83.33 | / |
| 雌 | 33.33 | / | |
| 产卵量/(×104 ind.) | 4.50±2.12 | 3~6 | |
| 卵径/mm | 2.65±0.19 | 2.41~2.93 | |
| 采精量/mL | 510.2±129.1 | 450~800 | |
| 精子剧烈运动时间/s | 47.47±7.61 | 40~62 | |
| 精子寿命/s | 236.00±57.71 | 170~320 | |
| 受精率/% | 87.53±5.36 | / | |
| 孵化率/% | 76.14±4.13 | / | |
| 累计出苗量/(×104 ind.) | 6 | ||
| 开口期仔鱼量/(×104 ind.) | 3 | ||
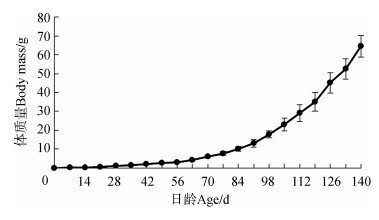
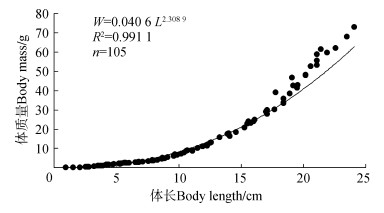
子三代长江鲟初孵仔鱼体长0.83~ 0.94 cm,平均(0.91±0.06) cm,体质量0.016~0.023 g,平均(0.021±0.003)g。仔鱼体质量呈指数增长(图 3),增长方程式为W=0.108 1e0.333 2t(R2=0.931 8,n=105,P < 0.01),体长呈直线增长(图 4),增长方程式为L=1.087 8t-1.7462(R2=0.986 1,n=105,P < 0.05),以方程W=aLb拟合体质量与体长之间相关关系为W=0.040 6L2.308 9(R2=0.991 1,n=105,P < 0.01)(图 5)。
|
| 图 3 子三代长江鲟仔鱼体质量增长曲线 Fig. 3 Body mass growth curve of the larva Acipenser dabryanus of the third generation |
| |

|
| 图 4 子三代长江鲟仔鱼体长增长曲线 Fig. 4 Body length growth curve of the larva Acipenser dabryanus of the third generation |
| |
|
| 图 5 子三代长江鲟仔鱼体质量与体长的关系曲线 Fig. 5 Correlation curve between body mass and body length of the larva Acipenser dabryanus of the third generation |
| |
鱼类繁殖力具有种间差异和种内差异,种间差异主要由遗传决定,也是物种进化过程中对自然环境长期适应的结果,种内差异主要受生长环境的影响(金丽,2004)。在本研究中,子二代长江鲟雌鱼初次性成熟年龄最小为6龄,但6龄成熟比例较小,仅有5%,野生雌鱼初次性成熟年龄为7~8龄,因此可认为人工养殖条件下的长江鲟与野生长江鲟初次性成熟年龄差异不大(表 4)。在年龄差异不大的情况下,不同世代长江鲟初次性成熟群体出现体质量逐渐增加的现象,这可能是因为在人工养殖条件下,长江鲟获得了充足的饵料供应,生长速度较野生个体快。人工养殖的长江鲟子一代和子二代绝对怀卵量差异不大,但都明显低于野生个体,卵径小于野生个体,这可能是因为在人工养殖条件下,长江鲟获得的饵料较野外充足,而空间较野外小,性腺中积累了大量脂肪,而野生个体性腺中脂肪含量很低,这与中华鲟A. sinensis(危起伟等,2013)和施氏鲟A. schrenckii(曲秋芝等,2002;张颖等,2016)的研究结果一致,因此,笔者认为人工养殖条件下,适当增大养殖空间和制造流速有利于提高长江鲟产卵量。
| 世代 Generation |
初次性成熟年龄 Age of first sexual maturity/年 |
体质量 Body mass/kg |
体长 Body length/cm |
绝对怀卵量 Absolute egg quantity/(×104ind.) |
卵径 Egg diameter/mm |
| 野生鱼 | 7~8 | 6~16 | 90~110 | 6~13 | 2.8~3.5 |
| 子一代F1 | 6~8 | 9~34(平均16.5) | / | 3~7 | 2.6~3.1 |
| 子二代F2 | 6~8 | 16~25(平均20.6) | 112~128 | 3~6 | 2.65 |
鱼类人工繁育过程中,成熟亲鱼的挑选尤为重要,鲟鱼具有独特的生理结构,在繁殖季节无明显副性征,外观上很难分辨雌雄和性腺发育成熟度。在生产上,一般采用腹腔穿刺的方法来进行鉴别,但这种方法工作量大、效率低,同时在检查时亲鱼容易产生较大的应激反应,对亲鱼的生长和性腺发育均不利,可能会影响催产效果。本文应用B超鉴定性腺发育成熟度的方法,准确度高、对亲鱼的伤害也较小,为长江鲟全人工繁殖提供了技术保障。
国内鲟鱼繁育技术已经比较成熟,催产药物主要有LRHA2、鲤鱼脑垂体和人绒毛膜促性腺激素释放激素等,催产方法也没有统一的标准,雄鱼一般采用1针注射,雌鱼一般采用2~3针注射,本文中雄鱼催产成功率较高(83%),但雌鱼催产成功率较低(33.3%),可能与本次繁殖所用亲鱼均是初次成熟产卵有关,催产方法还有待进一步研究。长江鲟子三代苗种培育方法与中华鲟(危起伟等,2013)、西伯利亚鲟A. baeri(曲秋芝,高艳丽,2005)、施氏鲟(曲秋芝等,2002)等类似,在本次培育过程中,出现了3次死亡高峰期,分别在出膜后、开口阶段和转食阶段,因此在今后的苗种培育中,应加强这3个阶段的养殖管理。
4 小结长江鲟子三代繁育成功,是长江鲟迁地保护的重大突破,预示着长江鲟可持续人工群体建设和人工保种的成功,将为今后长江鲟自然种群复壮及未来的养护利用奠定基础。
褚志鹏, 危起伟, 杜浩, 等. 2017. 不同糖源对达氏鲟幼鱼生长、体成分及生理生化指标的影响[J]. 中国水产科学, 24(2): 284-294. |
杜浩, 危起伟, 罗江, 等. 2016.人工调控达氏鲟实现自然交配产卵的方法[P]. 中国发明专利: CN106069899A.
|
龚全, 刘亚, 杜军, 等. 2016. 达氏鲟全人工繁殖技术研究[J]. 西南农业学报, 26(4): 1710-1714. |
龚全, 刘亚, 赖见生, 等. 2015. 不同开口饵料对达氏鲟鱼苗生长的影响[J]. 西南农业学报, 28(5): 2297-2300. |
颉璇, 厉萍, 席萌丹, 等. 2018. 达氏鲟精巢细胞消化分离和超低温冷冻保存[J]. 淡水渔业, 46(5): 19-24. |
金丽. 2004. 鱼类的繁殖习性和繁殖力[J]. 生物学教学, 29(7): 5-6. DOI:10.3969/j.issn.1004-7549.2004.07.005 |
罗江, 杜浩, 冷小茜, 等. 2018. 不同养殖密度对长江鲟稚鱼生长的影响[J]. 淡水渔业, 48(3): 107-111. DOI:10.3969/j.issn.1000-6907.2018.03.018 |
曲秋芝, 高艳丽. 2005. 西伯利亚鲟的人工繁殖[J]. 中国水产科学, 12(4): 492-495. DOI:10.3321/j.issn:1005-8737.2005.04.021 |
曲秋芝, 孙大江, 马国军, 等. 2002. 施氏鲟全人工繁殖研究初报[J]. 中国水产科学, 9(3): 277-279. DOI:10.3321/j.issn:1005-8737.2002.03.020 |
危起伟, 李罗新, 杜浩, 等. 2013. 中华鲟全人工繁殖技术研究[J]. 中国水产科学, 20(1): 1-11. |
张磊, 危起伟, 张书环, 等. 2018. 饲料蛋白水平对达氏鲟幼鱼生长性能、体组成、消化酶活性以及血液生化指标的影响[J]. 淡水渔业, 46(6): 79-85. |
张颖, 曲秋芝, 王斌, 等. 2016. 人工养殖下施氏鲟Acipenser schrenckii、达氏鳇Huso dauricus及其杂交后代的繁殖特性[J]. 水产学杂志, 29(3): 25-34. DOI:10.3969/j.issn.1005-3832.2016.03.005 |
Boyd K, Zhuang P, Zhang T, et al. 2003. Ontogenetic behavior and migration of Dabry's sturgeon, Acipenser dabryanus, from the Yangtze River, with notes on body color and development rate[J]. Environmental Biology of Fishes, 66(1): 27-36. |
Du H, Wei QW, Xie X, et al. 2014. Improving swimming capacity of juvenile Dabry's sturgeon, (Acipenser dabryanus Dumeril, 1869) in current enriched culture tanks[J]. Journal of Applied Ichthyology, 30(6): 1445-1450. DOI:10.1111/jai.12591 |
Du H, Zhang XY, Leng XQ, et al. 2017. Gender and gonadal maturity stage identification of captive Chinese sturgeon, Acipenser sinensis, using ultrasound imagery and sex steroids[J]. General and Comparative Endocrinology, 245(1): 36-43. |
Ye H, Yue HM, Yang XG, et al. 2016. Identification and sexually dimorphic expression of vasa isoforms in Dabry's sturgeon (Acipenser dabryanus), and functional analysis of vasa 3'-untranslated region[J]. Cell Tissue Research, 366(1): 203-218. DOI:10.1007/s00441-016-2418-6 |
Ye H, Yue HM, Yang XG, et al. 2018. Molecular characterization, tissue distribution, localization and mRNA expression of the bucky ball gene in the Dabry's sturgeon (Acipenser dabryanus) during oogenesis[J]. Gene Expression Patterns, 28(1): 62-71. |
Zhang SH, Xu QQ, Elisa B, et al. 2018. Characterization and expression analysis of g- and c-type lysozymes in Dabry's sturgeon (Acipenser dabryanus)[J]. Fish and Shellfish Immunology, 76(1): 260-265. |
 2020, Vol. 39
2020, Vol. 39




