扩展功能
文章信息
- 姚冲学, 王方, 王智红, 吕婷, 刘宇, 肖剑, 陈明勇
- YAO Chongxue, WANG Fang, WANG Zhihong, LYV Ting, LIU Yu, XIAO Jian, CHEN Mingyong
- 密度对大蹼铃蟾蝌蚪生长发育和存活率的影响初探
- A Preliminary Study of Density Effects on the Growth and Survival Rate of Bombina maxima Tadpoles
- 四川动物, 2019, 38(5): 544-548
- Sichuan Journal of Zoology, 2019, 38(5): 544-548
- 10.11984/j.issn.1000-7083.20190117
-
文章历史
- 收稿日期: 2019-04-02
- 接受日期: 2019-07-05
两栖类蝌蚪的生长发育受多种环境因素的综合影响,如温度、食物、种群密度、水位变化和天敌等。有关两栖类蝌蚪生长发育的研究得到广泛关注,无尾目Anura如东北林蛙Rana dybowskii(卫功庆等,2003)、中国林蛙Rana chensinensis(王汉屏,2007)、棘腹蛙Quasipaa boulengeri(陈高鹏等,2010;徐敬明等,2018)、泽陆蛙Fejervarya multistriata(施林强等,2011)、大树蛙Rhacophorus dennysi(谢文华等,2014)、棘胸蛙Quasipaa spinosa(章海鑫等,2014;毛剑婷等,2017)、中华蟾蜍Bufo gargarizans(李军德等,2016)等;有尾目Caudata如红螺疣螈Tylototriton shanjing(王本君等,2017)等。密度是影响蝌蚪生长发育的重要因素(谢文华等,2014),相关研究发现,高密度会导致中国林蛙、泽陆蛙和大树蛙的蝌蚪生长率下降、发育时间延长;Semlitsh和Caldwell(1982)也发现,高密度会导致霍氏掘足蟾Scaphiopus holbrooki蝌蚪发育时间缩短。在诸多研究中,密度常与其他因子一起作为综合因子来研究,而把密度作为单因子或主要因子来研究其影响两栖类蝌蚪生长发育的报道很少。
大蹼铃蟾Bombina maxima隶属于无尾目铃蟾科Bombinatoridae铃蟾属Bombina,生活在海拔2 000~3 300 m的静水塘、山溪缓流处石块下、井泉、路旁小沟内,主要分布于四川(昭觉、宜宾等西南部高山区)(费梁,1999)、贵州(费梁,1999)及云南(丽江、巧家、大姚、宁蒗、大理、宾川、洱源邓川、东川、威信、武定等)(杨大同,饶定齐,2008)。对该种的研究主要见于皮肤分泌液中抗菌活性肽的分离纯化及其性质(赖仞等,1998;张云,2006)、转录组深度分析及其免疫系统的功能研究(张英霞等,2008)、皮肤白蛋白的胰蛋白酶抑制剂活性研究(赵锋等,2013)以及两性异形(姚冲学等,2019)等方面。张云(2006)发现,从大蹼铃蟾皮肤分泌物中提取的maximin 3抗菌肽对人类免疫缺陷病毒(艾滋病病毒)有明显的抑制作用,因此,大蹼铃蟾对艾滋病病毒防治药物及其他科学研究具有重要价值。目前,有关大蹼铃蟾蝌蚪生长发育的研究尚未见报道。本文主要研究密度对大蹼铃蟾蝌蚪生长发育和存活率的影响,探索种群密度在该物种从幼体到成体的生长发育中的作用机制,为进一步了解该物种提供基础资料。
1 材料与方法 1.1 实验材料2018年6月1日,将正在抱对的5对大蹼铃蟾成体从云南昆明金殿水库后山(102.776 185°E,25.093 346°N,海拔1 989 m)带回实验室,分别放到水温20~25 ℃、pH6.6~7.0、水深3 cm的容器盒(长25 cm×宽16 cm×高17 cm)中产卵,每一对所产的卵置于相同条件下自然孵化(每天09: 00用经过氧气泵加氧后的自来水换水一次)。为了消除亲代遗传、母体效应等因素的影响(谢文华等,2014),400只蝌蚪均来自同一亲代,同时从400只刚孵化的蝌蚪中随机抽取50只,用电子数显游标卡尺(精度0.01 mm,上海恒量)测量:(1)全长(total length):自吻端至尾末端的长度;(2)尾长(tail length):自肛孔基部至尾末端的长度;(3)体宽(body width):体两侧的最大宽度(费梁,1999)。刚孵化的蝌蚪全长8.99 mm±0.10 mm(n=50)、尾长3.67 mm±0.09 mm(n=50)、体宽3.12 mm±0.06 mm(n=50),并以此为各组刚孵化的测定值。
1.2 仪器与设备实验器材与设备主要有:便携式pH计、上海恒量电子数显游标卡尺(精度0.01 mm)、GPS、捞网、直尺、解剖盘、圆规、容器盒等。
1.3 实验设计将刚孵化的400只大蹼铃蟾蝌蚪随机分成A组(30只/L)、B组(60只/L)和C组(90只/L)3个组(由于带回实验室的5对中产卵量最多一对为473粒,但只有405粒卵成功孵化,蝌蚪总数量有限,因此没有设置重复组)。实验组各设置1个平行组,平行组的个体数量、投食量和水量与实验组一致。当实验组中有蝌蚪死亡时,分别从相应的平行组中抽取与死亡个体全长相同或相近的个体进行补充(谢文华等,2014)。蝌蚪饲养在水温20~25 ℃、pH6.6~7.0、水深3 cm的容器盒中,5 d为一个测量周期,分别从每组中随机抽取20只测量全长、尾长、体宽,并记录每个测量周期内各组死亡数量,共测量8次。每天换水后将颗粒状鱼饲料研磨成粉末投食1次,A、B、C组投食量分别为0.1 g、0.2 g、0.3 g。
1.4 数据分析方法采用Excel和SPSS 23.0处理数据。首先用Kolmogorov-Smirnov和Levene分别检测所有数据的正态性和方差同质性,当测量数据符合正态性和方差同质性时,相关分析采用Pearson检验,否则用Spearman检验。当测量数据符合正态性和方差同质性时,可以直接进行方差分析,否则将数据进行转换以达到正态性和方差同质性后进行方差分析。以各组密度为自变量,蝌蚪的其他形态指标(全长、尾长和体宽)分别为因变量做一元线性回归分析,通过各组中一元回归方程斜率判断密度对大蹼铃蟾蝌蚪生长发育的影响程度。描述统计值用平均值±标准误(Mean±SE)表示,显著性水平设置为α=0.05。全长、尾长和体宽的生长率=(每组第40天测定值-刚孵化的测定值)/40 d(徐敬明等,2018)。
2 结果 2.1 密度对大蹼铃蟾蝌蚪生长发育的影响3组蝌蚪均呈早期快速生长、后期生长率逐渐减小的特点,饲养到40 d时,全长、尾长和体宽表现为:A组>B组>C组。C组蝌蚪第30天已经进入变态期,而A组和B组第35天才开始进入变态期。变态期时3组蝌蚪的全长、尾长和体宽达到最大值(表 1)。
| 形态特征 Morphological characteristics |
时间 Time/d |
组别Group | ||
| A | B | C | ||
| 全长/mm | 5 | 18.42±0.37 | 14.76±0.29 | 15.65±0.54 |
| 10 | 21.56±0.37 | 20.61±0.27 | 20.02±0.76 | |
| 15 | 23.62±0.44 | 23.21±0.27 | 22.28±0.56 | |
| 20 | 25.60±0.56 | 24.67±0.44 | 22.96±0.52 | |
| 25 | 26.84±0.56 | 26.21±0.58 | 25.28±0.57 | |
| 30 | 27.81±0.55 | 26.81±0.57 | 25.92±0.53 | |
| 35 | 28.47±0.66 | 27.19±0.63 | 23.11±0.65 | |
| 40 | 28.40±0.57 | 26.72±0.65 | 22.66±0.47 | |
| 尾长/mm | 5 | 10.13±0.30 | 7.40±0.22 | 8.27±0.34 |
| 10 | 11.70±0.34 | 11.04±0.20 | 11.13±0.47 | |
| 15 | 13.51±0.29 | 12.8±0.19 | 12.12±0.37 | |
| 20 | 14.57±0.34 | 13.96±0.29 | 12.87±0.32 | |
| 25 | 15.20±0.35 | 14.76±0.36 | 14.42±0.36 | |
| 30 | 15.87±0.39 | 15.09±0.32 | 14.70±0.36 | |
| 35 | 16.21±0.49 | 15.55±0.38 | 13.12±0.42 | |
| 40 | 16.19±0.35 | 15.27±0.44 | 12.31±0.32 | |
| 体宽/mm | 5 | 5.28±0.12 | 4.48±0.11 | 4.20±0.15 |
| 10 | 6.25±0.09 | 6.16±0.15 | 4.65±0.12 | |
| 15 | 6.44±0.12 | 6.36±0.14 | 6.27±0.15 | |
| 20 | 7.15±0.11 | 6.86±0.12 | 6.45±0.12 | |
| 25 | 7.28±0.14 | 7.09±0.20 | 6.91±0.14 | |
| 30 | 7.40±0.12 | 7.32±0.17 | 7.08±0.15 | |
| 35 | 7.49±0.17 | 7.19±0.17 | 6.38±0.21 | |
| 40 | 7.42±0.17 | 7.08±0.15 | 6.36±0.14 | |
密度与全长、尾长和体宽均具有显著负相关性(P<0.05),全长、尾长和体宽的r值为:A组<B组<C组(表 2)。
| 组别 Group |
自变量 Independent variable (x) |
因变量 Dependent variable (y) |
Pearson检验 Pearson test |
F | P | R2 | 直线回归方程 Linear regression equation |
| A | 密度 | 全长 | r=-0.780,P=0.007 | 10.900 | 0.013 | 0.553 | y=-1.185x+53.11 |
| 密度 | 尾长 | r=-0.766,P=0.008 | 9.914 | 0.016 | 0.527 | y=-0.747x+31.94 | |
| 密度 | 体宽 | r=-0.735,P=0.012 | 8.243 | 0.024 | 0.475 | y=-0.253x+12.84 | |
| B | 密度 | 全长 | r=-0.763,P=0.004 | 13.655 | 0.008 | 0.613 | y=-0.538x+48.19 |
| 密度 | 尾长 | r=-0.740,P=0.003 | 14.358 | 0.007 | 0.652 | y=-0.353x+29.27 | |
| 密度 | 体宽 | r=-0.721,P=0.007 | 10.284 | 0.015 | 0.537 | y=-0.116x+11.81 | |
| C | 密度 | 全长 | r=-0.718,P=0.015 | 7.456 | 0.029 | 0.447 | y=-0.248x+38.16 |
| 密度 | 尾长 | r=-0.702,P=0.018 | 6.791 | 0.035 | 0.420 | y=-0.157x+22.42 | |
| 密度 | 体宽 | r=-0.717,P=0.007 | 10.642 | 0.014 | 0.547 | y=-0.069x+10.56 |
密度与形态特征均具有显著相关性(P<0.05),全长、尾长和体宽的一元线性回归斜率为:A组<B组<C组(表 2)。
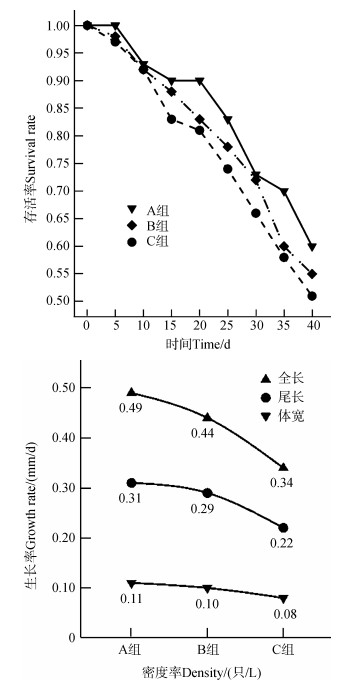
2.2 密度对存活率及全长、尾长和体宽生长率的影响密度与存活率间有显著相关性(r=0.877,P<0.01)。饲养第1~10天内,A、B和C 3组的存活率分别为0.93、0.92和0.92;第25天后各组存活率均急剧下降,分别为0.83、0.78和0.74(图 1)。
|
| 图 1 密度对大蹼铃蟾蝌蚪的存活率(上)及其生长率(下)的影响 Fig. 1 Effects of density on the survival rate (upper) and growth rate (bottom) of Bombina maxima tadpoles |
| |
饲养到第40天时,A、B和C 3组的全长生长率分别为0.49、0.44和0.34,尾长生长率分别为0.31、0.29和0.22,体宽生长率分别为0.11、0.10和0.08(图 1)。
3 讨论生存空间一定时,种群密度的增加会减小蝌蚪的生存空间,导致种内竞争加剧,从而影响蝌蚪的生长发育和存活率(Relyea,2002;Relyea & Hoverman,2003)。本研究结果表明,3组蝌蚪均呈早期快速生长、后期生长缓慢的特点,并且在每个生长测定点内,高密度饲养下的形态特征均小于低密度。密度对大蹼铃蟾蝌蚪的生长发育和存活率有显著的影响,随着密度增加,大蹼铃蟾蝌蚪生长率逐渐减小,存活率逐渐降低,这与中国林蛙(王汉屏,2007)、大树蛙(谢文华等,2014)等相关研究的结论一致。随发育时间增加,3组的生长率存在明显的差异,B组和C组蝌蚪的生长率较A组慢,这可能是B组和C组蝌蚪随着饲养时间增加,自身不断生长,在有限的空间内物理性接触的机会较A组多,种内竞争加剧,从而影响生长速率。Petranka(1989)发现豹蛙Rana pipiens蝌蚪在种内竞争加剧的情况下,生长速度快、较大个体的蝌蚪会分泌抑制素来降低较小个体的生长率,大蹼铃蟾蝌蚪是否具有类似的行为有待进一步研究。
本研究结果表明,密度对大蹼铃蟾蝌蚪的存活率具有显著的影响,即密度越大,存活率越低。饲养早期3组存活率差异不大,中后期3组的存活率急剧下降,而且在每个生长测定点内低密度饲养下的存活率始终大于高密度。这可能是蝌蚪生长引起生存空间缩小和溶氧量过度消耗,以及种内竞争加剧导致了死亡率升高(谢文华等,2014),前期蝌蚪较小,生存空间相对宽裕,种间竞争较小,存活率较高。在饲养过程中也发现蝌蚪相互撕咬尾巴和取食死亡蝌蚪尸体的现象,高密度组下饲养的蝌蚪个体间接触机会较多、相互撕咬的机率较大,这也是高密度组死亡率增加的一个主要原因。由此表明,在大蹼铃蟾蝌蚪的发育期,密度性制约因素对蝌蚪的存活率影响较为显著。
本研究还发现,C组第30天时进入变态期,而A组和B组第35天进入变态期。说明高密度组较低密度组更早进入变态期。进入变态期前,3组蝌蚪的形态指标达到了最大值,表现为A组>B组>C组,进入变态期后,形态特征逐渐减小。说明密度越大,蝌蚪进入变态期时的全长、尾长和体宽越小。由此可推测,高密度饲养下的蝌蚪较早进入变态期,这可能是蝌蚪生长发育过程中对高密度环境的一种适应性调节机制。
综上所述,有关密度对两栖类蝌蚪生长发育的影响已经有很多研究报道,但大多数都只是将密度作为综合因子之一来进行分析,并且结论不一,也不能完全反映出密度这一因子的影响成效。本文以密度为主要因子研究其对大蹼铃蟾蝌蚪生长发育和存活率的影响,结果表明,密度越大,大蹼铃蟾蝌蚪的生长率和存活率越低,同时,实验结果可推测在高密度饲养下的蝌蚪较低密度组更早进入变态期。影响大蹼铃蟾蝌蚪生长发育的其他环境因素很多,如温度、食物、水位变化和天敌等,其作用机理和程度仍有待进一步研究。
| 陈高鹏, 王德良, 李文健, 等. 2010. 不同开口饵料对棘腹蛙幼蛙生长和存活的影响[J]. 四川动物, 29(4): 587–589. |
| 费梁. 1999. 中国两栖动物图鉴[M]. 郑州: 河南科学技术出版社. |
| 赖仞, 叶文娟, 冉永禄, 等. 1998. 大蹼铃蟾皮肤分泌液中抗菌活性肽的分离纯化及其性质[J]. 动物学研究, 19(4): 257–262. |
| 李军德, 赵群, 康彦, 等. 2016. 密度与饲料对中华蟾蜍蝌蚪生长发育的影响[J]. 中国中药杂志, 41(6): 1001–1007. |
| 毛剑婷, 刘泽鹏, 张盼, 等. 2017. 不同饲料对棘胸蛙蝌蚪生长发育及变态率的影响[J]. 浙江农业科学, 58(9): 1610–1615. |
| 施林强, 毛飞, 马小梅. 2011. 密度对泽陆蛙蝌蚪生长发育和变态的影响[J]. 杭州师范大学学报(自然科学版), 10(5): 429–434. DOI:10.3969/j.issn.1674-232X.2011.05.009 |
| 王本君, 刘娜, 何一帆, 等. 2017. 捕食风险对红瘰疣螈幼体生长发育的影响[J]. 四川动物, 36(5): 513–518. |
| 王汉屏. 2007. 密度对中国林蛙蝌蚪生长发育的影响[J]. 四川动物, 26(2): 406–408. DOI:10.3969/j.issn.1000-7083.2007.02.050 |
| 卫功庆, 苏凤燕, 刘忠军. 2003. 不同饲料营养水平对东北林蛙蝌蚪生长发育的影响[J]. 经济动物学报, 7(2): 41–46. DOI:10.3969/j.issn.1007-7448.2003.02.014 |
| 谢文华, 陶双伦, 杨冬梅, 等. 2014. 密度对大树蛙蝌蚪生长发育和存活率的影响[J]. 生态学报, 34(22): 6583–6588. |
| 徐敬明, 姜玉松, 樊汶樵. 2018. 不同温度对棘腹蛙宜宾种群蝌蚪生长发育的影响[J]. 黑龙江畜牧兽医, 10(1): 207–210. |
| 杨大同, 饶定齐. 2008. 云南两栖爬行动物[M]. 昆明: 云南科技出版社. |
| 姚冲学, 吕婷, 王方, 等. 2019. 大蹼铃蟾的两性异形[J]. 四川动物, 38(2): 194–199. |
| 张英霞, 满初日嘎, 张云. 2008. 大蹼铃蟾皮肤白蛋白的胰蛋白酶抑制活性研究[J]. 科技通报, 24(2): 167–170. DOI:10.3969/j.issn.1001-7119.2008.02.005 |
| 张云. 2006. 两栖类动物皮肤分泌物及其生物学适应意义——大蹼铃蟾皮肤分泌物蛋白质多肽组的启示[J]. 动物学研究, 27(1): 103–114. |
| 章海鑫, 余智杰, 马保新, 等. 2014. 不同饲养环境因子水平对棘胸蛙蝌蚪变态的影响[J]. 贵州农业科学, 42(12): 180–182. DOI:10.3969/j.issn.1001-3601.2014.12.043 |
| 赵锋, 严超, 王宣, 等. 2013.应用高通量测序对大蹼铃蟾转录组深度分析及其免疫系统的功能研究[C].青岛: 中国生物毒素研究及医药应用年会. http://cpfd.cnki.com.cn/Article/CPFDTOTAL-ZGDV201310001012.htm |
| Petranka JW. 1989. Chemical interference competition in tadpoles:does it occur outside laboratory aquaria?[J]. Copeia, 1989(4): 921–930. DOI:10.2307/1445978 |
| Relyea RA. 2002. Competitor-induced plasticity in tadpoles:consequences, cues, and connections to predator-induced plasticity[J]. Ecological Monographs, 72(4): 523–540. DOI:10.1890/0012-9615(2002)072[0523:CIPITC]2.0.CO;2 |
| Relyea RA, Hoverman JT. 2003. The impact of larval predators and competitors on the morphology and fitness of juvenile treefrogs[J]. Oecologia, 134(4): 596–604. DOI:10.1007/s00442-002-1161-8 |
| Semlitsch RD, Caldwell JP. 1982. Effects of density of growth, metamorphosis, and survivorship in tadpoles of Scaphiopus holbrooki[J]. Ecology, 63(4): 905–911. DOI:10.2307/1937230 |
 2019, Vol. 38
2019, Vol. 38




