扩展功能
文章信息
- 何叶艳, 吕凯伦, 董加俊, 俞一钒, 何珂
- HE Yeyan, LYU Kailun, DONG Jiajun, YU Yifan, HE Ke
- 梅花鹿华南亚种和东北亚种警戒声比较
- Comparison of Vigilance-Related Calls Between Cervus nippon kopschi and Cervus nippon hortulorum
- 四川动物, 2019, 38(3): 241-248
- Sichuan Journal of Zoology, 2019, 38(3): 241-248
- 10.11984/j.issn.1000-7083.20180315
-
文章历史
- 收稿日期: 2018-10-23
- 接受日期: 2019-02-15
梅花鹿Cervus nippon曾广泛分布于我国的东北、华北、华中、华南、西南和青藏高原的东部,有山西亚种C. n. grassianus、华北亚种C. n. mandarinns、台湾亚种C. n. taiouanns、东北亚种C. n. hortulorum、华南亚种C. n. kopschi和四川亚种C. n. sichuanicus。前三者在20世纪40年代先后在野外灭绝,后三者分别呈隔离状分布于黑龙江、吉林、江西、浙江、安徽、四川和甘肃等省狭窄的区域内,种群数量不足1 500只(郭延蜀,郑惠珍,2000)。其中,梅花鹿华南亚种已经被世界自然保护联盟(IUCN)列为濒危(EN)物种,也是国家Ⅰ级重点保护野生动物,清凉峰国家级自然保护区的梅花鹿种群是浙江省内华南亚种的唯一野生种群。
我国现存的梅花鹿种群主要分布在4个狭窄的区域内,每个种群内部连成一个整体。梅花鹿是社群性哺乳动物,鸣声是主要的通讯方式之一,对其行为有非常重要的作用。不同物种为了适应各自的环境,以及生活史中各阶段的生命活动需要,产生不同的鸣声。如吼叫是雄性海南坡鹿C. eldii繁殖活动的一个表现指标,雄性个体的成功交配次数与吼叫次数呈显著正相关(曾治高等,2001);在雄性麋鹿Elaphurus davidianus中也存在类似现象(李春旺等,2001)。但目前仅有梅花鹿的少数研究资料,如产仔换茸期间的叫声和警戒、求偶的叫声等(杨承忠等,2012)。梅花鹿华南亚种有警戒叫声、求偶叫声、呼唤叫声和团体合唱声4种特点分明的叫声类型(付义强等,2008),但没有对梅花鹿不同亚种之间的鸣声进行分析,也没有在不同生存状态下进行比较。本研究利用数字录音机录制梅花鹿华南亚种和东北亚种的鸣声,分析了不同亚种在野生和圈养条件下的鸣声特征,为梅花鹿的保护提供数据支持。
1 材料和方法 1.1 动物状况梅花鹿华南亚种来自浙江省清凉峰国家级自然保护区多年收留被救助和繁殖的野生种群,目前已有50余头。83头梅花鹿东北亚种来自浙江省温州康寿鹿业科技有限公司的圈养种群。
1.2 声音采集梅花鹿华南亚种:2018年7月15—31日,将录音笔(频响范围:20 Hz~20 kHz;Newsmy)放在个体经常出现的区域,同时用望远镜观察个体行为,将声音和行为联系起来。梅花鹿东北亚种:2018年8月1—15日,将录音笔放置于舍门边的一个隐蔽处,观察者全天安静守候在梅花鹿圈舍旁。记录梅花鹿发出鸣声的同时采用全部事件记录法,记录与鸣声相应的行为特征,联系行为作后期分析。
1.3 声音分析方法声音特征分析划分采用的标准:以间隔在0.02~0.10 s的声音为一个音节,间隔0.10 s以上的视为不同音节,间隔超过1 s的为一个唱句;利用计算机筛选已转化好的声音,选择杂音较少的声音片段,再利用Adobe Audition对唱句进行剪辑、去噪、消除静音和音量调节后,对划分好的唱句利用Praat(荷兰)分析出语图,对语图进行目测判定。通过比较每个唱句中每个音节的形状及其频率范围和在时间间隔上的分布来区分不同音节类型。切分音节类型的具体方法:首先确定语图中的音节是否有明显转弯,有转弯的确定为A类,没有明显转弯的确定为B类;东北亚种发出的声音标记为D,华南亚种标记为H。利用Praat提取各音节的持续时间、基频、主频等特征。
1.4 数据处理在SPSS中利用KS检验检测样本参数是否偏离正态分布,独立样本t检验比较不同类型鸣声参数的差异,若不满足正态分布和方差同质性,采用Mann-Whitney U检验或Kruskal-Wallis非参数分析。显著水平设置为α=0.05。
2 结果2018年7—8月,共录制了124个有效鸣声片段(东北亚种90个,华南亚种34个)。其中,37个警戒声(东北亚种18个,华南亚种19个);51个团体合唱声(东北亚种36个,华南亚种15个);此外还录制到东北亚种的另外2类声音,一类多发生在饲喂时,推测为“求食”声音,为25个;另一类多发生在母鹿与仔鹿之间,推测为“母子交流”,为11个。通过提取声音的声学特征,证实了这种鸣声都不是简单的“噪音”。
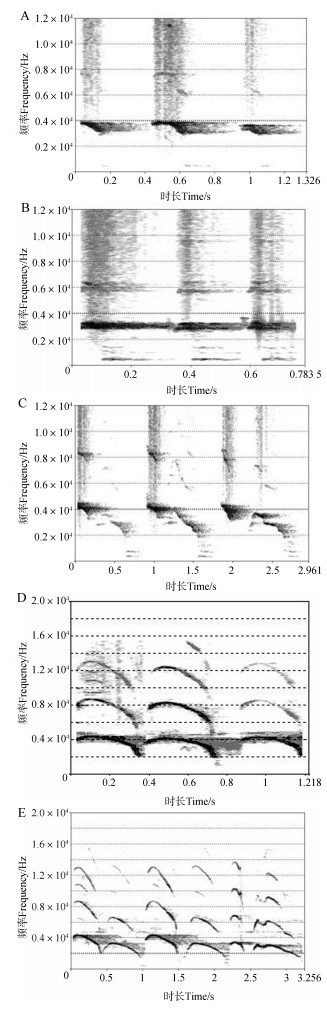
2.1 梅花鹿华南亚种和东北亚种的频谱特征、波形图、语图和强度分析图的比较东北亚种同时具有单音节、双音节警戒声,前者可分为2种不同类型的音节(记为DAⅠ和DB),能量集中频率在3 000~4 000 Hz(图 1:A、B),后者(一次警戒声含2个音节,分别记为DAⅡ-前和DAⅡ-后)能量集中频率在2 000~4000 Hz(图 1:C);华南亚种具有单音节警戒声(记为HAⅠ)和双音节警戒声(一次警戒声含2个音节,分别记为HAⅡ-前和HAⅡ-后)(图 1:D、E)能量集中频率为1 726~15 403 Hz,范围明显大于东北亚种(图 1)。
|
| 图 1 警戒声样本窄带语图 Fig. 1 Spectrogram of vigilance-related calls 梅花鹿东北亚种Cervus nippon hortulorum:A.单音节monosyllable (DAⅠ),B.单音节monosyllable (DB),C.双音节disyllable (DAⅡ);梅花鹿华南亚种C. n. kopschi:D.单音节monosyllable (HAⅠ),E.双音节disyllable (HAⅡ) |
| |
从声音样本窄带语图可以发现,东北亚种部分警戒声与华南亚种警戒声的音节都存在明显的转弯。相较于东北亚种,华南亚种单音节警戒声的转弯更明显,且同一音节含有3~4个转弯,转弯在高中低频率段均有分布(图 1)。从双音节警戒声总声音样本窄带语图可看出,华南亚种也可以在一次警戒声中发出2个音节,前一个音节的能量大于后一个音节,同样1个音节含有3~4个转弯,转弯分布在高中低频率段(图 1:E)。在东北亚种的单音节警戒声中,DB类型处于发出连续多次警戒声之后,能量(黑色区域)和能量集中的频率范围明显减少,因此在窄带语图中体现出音节的转弯不明显。
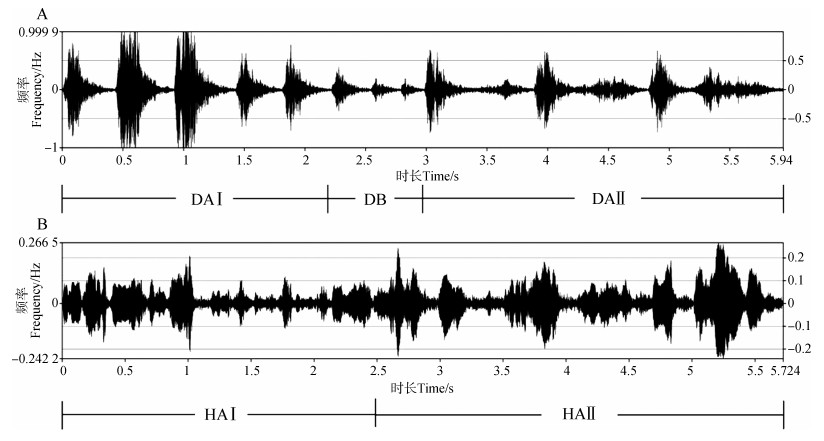
声音的音调与频率有关,频率越高,音调越高;声音的响度与振幅有关,振幅越大,响度越大。根据波形图识别音调,频率越低,音调越低。从波形图中发现:(1)东北亚种的警戒声在后期振幅变小,响度变小(图 2:A);(2)华南亚种警戒声的振幅范围明显低于东北亚种(图 2:B)。
|
| 图 2 梅花鹿东北亚种(A)和华南亚种(B)警戒声样本波形图 Fig. 2 Oscillograph of vigilance-related calls of Cervus nippon hortulorum (A) and C. n. kopschi (B) |
| |
对梅花鹿东北亚种和华南亚种警戒声进行单音节(DAⅠ vs. HAⅠ)、双音节(DAⅡ vs. HAⅡ)和相同亚种间不同类型叫声(DAⅠ vs. DAⅡ-前、DAⅠ vs. DAⅡ-后、HAⅠ vs. HAⅡ-前和HAⅠ vs.HAⅡ-后)比较分析,KS检验检测数据均符合正态分布。
梅花鹿东北亚种A类型单音节持续时间为0.439 s±0.050 s,B类型单音节持续时间为0.261 s± 0.059 s,2种音节持续时间之间存在有统计学意义的差异(P<0.05),推测为多次警戒后鸣声能量的下降导致B类型持续时间显著减少;东北亚种双音节DAⅡ-前和DAⅡ-后持续时间分别为0.350 s±0.034 s和0.637 s±0.098 s。华南亚种单音节警戒声持续时间为0.353 s±0.070 s,与东北亚种的差异有统计学意义(P<0.05),推测是亚种和环境差异造成的。2个亚种的双音节警戒声持续时间均极显著高于单音节(P<0.01),表明双音节的持续时间更长,能够更持久地发出信息。而2个亚种的双音节警戒声在持续时间上的差异无统计学意义(P>0.05)。
基频和主频是鸣声的特征参数,前者为鸣声中振幅最大、频率最低的分音的振动频率,后者是振幅最大所对应的频率。分析发现梅花鹿东北亚种DAⅠ的基频和主频均明显高于DB(P<0.05);华南亚种单音节警戒声HAⅠ的基频(3 663.89 Hz± 140.37 Hz)显著高于东北亚种DAⅠ(3 455.19 Hz± 171.96 Hz)(P<0.05),主频差异无统计学意义;双音节比较发现,前半段的基频和主频的差异均无统计学意义,而后半段DAⅡ-后的基频和主频均明显低于HAⅡ-后(P<0.05),特别是东北亚种双音节后半段的主频大幅度下降。
梅花鹿华南亚种HAⅠ与东北亚种DAⅠ样本能量集中频率相近,分别集中在3 574.23 Hz±155.00 Hz和3 524.60 Hz±222.54 Hz(P>0.05);而双音节均为前半段能量集中频率较高,后半段能量集中频率相对较低,但差异均无统计学意义(P>0.05);不同类型的警戒声能量集中频率的差异均有高度统计学意义(P<0.01)(表 1)。
| 亚种 | 鸣声类型 | 持续时间/s | 基频/Hz | 主频/Hz | 频域平均值/Hz | 共振峰/Hz | ||
| F1 | F2 | F3 | ||||||
| 东北亚种 | 单音节(DAⅠ) | 0.439±0.050 | 3 455.19±171.96 | 3 688.91±191.06 | 3 524.60±222.54 | 2 965.33±165.02 | 3 720.91±156.30 | 7 258.53±141.46 |
| 单音节(DB) | 0.261±0.059 | 3 038.16±5.65 | 2 927.16±82.21 | 2 575.72±295.35 | 2 423.02±129.20 | 4 365.01±407.21 | 7 434.28±462.53 | |
| 双音节-前(DAⅡ-前) | 0.350±0.034 | 3 981.67±112.73 | 4 056.33±125.16 | 4 049.07±121.35 | 3 636.78±221.61 | 4 106.09±69.19 | 7 884.53±211.16 | |
| 双音节-后(DAⅡ-后) | 0.637±0.098 | 1 903.05±128.84 | 376.66±13.73 | 1 956.37±1 000.76 | 2 131.58±147.35 | 3 475.15±57.91 | 793.48±140.05 | |
| 华南亚种 | 单音节(HAⅠ) | 0.353±0.070 | 3 663.89±140.37 | 3 919.65±282.92 | 3 574.23±155.00 | 3 588.94±188.62 | 4 909.90±897.86 | 7 881.03±476.77 |
| 双音节-前(HAⅡ-前) | 0.413±0.134 | 3 630.72±287.01 | 3 943.84±485.82 | 3 622.45±237.80 | 3 552.66±258.12 | 5 027.23±718.46 | 8 098.69±595.29 | |
| 双音节-后(HAⅡ-后) | 0.673±0.096 | 2 556.51±263.74 | 3 208.59±135.30 | 2 960.21±98.62 | 2 725.68±89.29 | 4 887.31±213.54 | 7 486.75±655.24 | |
| P(DAⅠ vs. HAⅠ) | * | * | NS | NS | *** | * | * | |
| P(DAⅡ-前vs. HAⅡ-前) | NS | NS | NS | NS | NS | NS | NS | |
| P(DAⅡ-后vs. HAⅡ-后) | NS | * | *** | NS | ** | *** | NS | |
| P(DAⅠ vs. DB) | ** | ** | *** | ** | ** | * | NS | |
| P(DAⅠ vs. DAⅡ-前) | * | ** | * | * | ** | ** | ** | |
| P(DAⅠ vs. DAⅡ-后) | ** | *** | *** | * | *** | * | NS | |
| P(HAⅠ vs. HAⅡ-前) | * | ** | * | * | ** | ** | ** | |
| P(HAⅠ vs. HAⅡ-后) | ** | *** | *** | * | *** | * | NS | |
| 注 Notes:* P<0.05,** P<0.01,*** P<0.001,NS. P>0.05 | ||||||||
在梅花鹿东北亚种DAⅠ、DB和DAⅡ-前中,前2个共振峰较为明显,且频率范围相近,在语图上形成1个3 000~4 000 Hz的频带。在华南亚种中,前3个共振峰较为明显,F1、F2、F3频率范围相差较大,在语图上反映为前2个频带的频率范围跨度大,分别为2 000~ 4 000 Hz、6 000~9 000 Hz,多频带的现象在HAⅠ、HAⅡ中均存在,甚至在HAⅡ中出现了4个频带。将不同类型的警戒声进行比较,发现东北亚种的共振峰频率低于华南亚种,且差异有高度统计学意义(P<0.01)(表 1),意味着东北亚种声波能量处在相对低频的波段,使其警戒声与华南亚种在听觉上的音色不同。
东北亚种的双音节警戒声中,前音节的基频均值为3 973.7 Hz;后音节的前半段基频均值为3 058.28 Hz,而后半段出现基频跳跃,基频降低至均值为364.48 Hz(图 3:A);华南亚种的双音节警戒声中也存在同样的现象,后音节末端的基频值由2 510.61 Hz降至410.97 Hz(图 3:B)。由于基频决定整个声音的音高,因此当梅花鹿发出双音节警戒声时,后半段警戒声的音高会陡然下降。

|
| 图 3 梅花鹿东北亚种(A)和华南亚种(B)双音节的基频跳跃(蓝色表示基频) Fig. 3 Fundamental frequency hopping of disyllable in Cervus nippon hortulorum (A) and C. n. kopschi (B)(the fundamental frequency is represented in blue) |
| |
动物的鸣声特征可以反映动物的生物学特征。昆虫不同种类鸣声的时域和频域不同,并作为昆虫分类的一个重要指标(Hemp & Kehl,2010)。两栖类动物中也发现不同种群鸣声的频域特征存在巨大的差异(徐俊晓等,2005)。群居的鹿科动物能够通过急促而高频的警戒声吓退争抢资源的其他个体,本研究主要针对这部分鸣声进行分析。
根据鸣声的脉冲数、音调、调频和频率等特征可将鸣声分为不同的类型,不同类型的鸣声产生于不同的行为。本研究发现5种不同类型的梅花鹿警戒声,分别为东北亚种的单音节警戒声(DAⅠ和DB)、双音节警戒声(DAⅡ),华南亚种的单音节警戒声(HAⅠ)和双音节警戒声(HAⅡ)。结果表明,华南亚种和东北亚种警戒声之间的差异有统计学意义,(1)华南亚种警戒声的振幅范围明显低于东北亚种;(2)华南亚种的鸣声分布在1 726~15 403 Hz,语图明显可见3~4个频带,而东北亚种鸣声能量集中频率仅分布在2 000~4 000 Hz,仅1个明显清晰的频带;(3)华南亚种单音节警戒声的转弯相较于东北亚种的警戒声明显,2种单音节警戒声之间的叫声持续时间和基频之间的差异有统计学意义,主频和集中能量的频率之间的差异无统计学意义,华南亚种的共振峰频率明显高于东北亚种;双音节警戒声中,2个亚种的双音节-前在各参数方面之间的差异均无统计学意义,而在双音节-后的基频、主频和共振峰频率之间的差异均有统计学意义。
综合梅花鹿警戒声的研究(表 2),已报道四川亚种的雄性个体报警鸣声中存在双音节和三音节,雌性个体和亚成体的警戒声中仅为单音节,有2个频带,为多谐波(杨承忠等,2012);江西桃红岭自然保护区梅花鹿华南亚种雄性个体的警戒声仅为单音节,未记录到雌鹿的警戒声,雌鹿呼唤同伴时为含有1~2个单音节和1个双音节的混合鸣声,均仅有1个频率区间(付义强等,2008)。本研究梅花鹿东北亚种的警戒声有单音节和双音节2种,均存在1个明显清晰的频带;而华南亚种警戒声也有单音节和双音节2种,均存在3~4个明显清晰的频带,各个频带之间间隔相等,为多谐波。华南亚种的警戒声频率范围更广、频带更多、音节较为丰富,这可能是环境或遗传因素造成的。
| 亚种(状态) | 性别 | 声音类型 | 频率范围/Hz | 持续时间/s | 频带 | 来源 |
| 四川亚种(野生) | 雄 | 双音节 | 2 133~7 103、625~6 067 | 0.522 | 2 | |
| 0.879 | ||||||
| 三音节 | 1 243~7 026、1 045~5 684、 757~6 686 | 0.599 | ||||
| 0.700 | 2 | 杨承忠等,2012 | ||||
| 1.356 | ||||||
| 雌 | 单音节 | 2 336~7 710 | 2.192 | 2 | ||
| 亚成体 | 单音节 | 580~6 765 | 0.444 | 2 | ||
| 华南亚种(江西桃红岭)(野生) | 雄 | 警戒 | 326.5~3 673.5 | 0.148 | 1 | 付义强等,2008 |
| 华南亚种(浙江清凉峰)(野生) | 雌 | 单音节 | 1 726~15 403 | 0.353±0.070 | 3~4 | 本研究 |
| 双音节 | 1 731~15 400 | 0.413±0.134 | 3~4 | |||
| 0.673±0.096 | ||||||
| 东北亚种(圈养) | 雌 | 单音节A | 2 883~3 986 | 0.439±0.050 | 1 | 本研究 |
| 单音节B | 2 672~3 277 | 0.286±0.057 | 1 | |||
| 双音节 | 307~4 523 | 0.350±0.034 | 1 | |||
| 0.637±0.098 |
环境条件(背景噪音和生境等)等影响种群的鸣声差异,动物的鸣声要不被环境噪音和其他种类的鸣声所淹没,其鸣声特征也要随环境而改变(Slabbekoorn & Ripmeester,2010)。鸟类鸣声研究发现,开阔生境中的种群的鸣声频率较高,使用较多频率幅度变化大的音节,而密林中的种群则采用频率较低的音节,这主要是由于在密林地区声音的高频部分更容易发生反射和衍射,造成能量的衰减和声源位置的模糊,减少接受者得到的信息量(夏灿玮,张雁云,2009)。和梅花鹿其他亚种比较,清凉峰华南亚种的频率范围最广,这可能和其选择的主要栖息地的植被类型一般是灌草丛和山地沼泽有关(付义强等,2006;章叔岩等,2016)。东北亚种的大多数栖息地为次生林灌及林间,四川亚种生境主要为森林、灌丛草甸等(郭延蜀,郑惠珍,2000)。3个亚种所在的环境差异可能对其鸣声造成自然选择,导致亚种鸣声的差异。
遗传因素同样影响种群的鸣声特征,孙儒泳(1992)认为广布种在不同地区的种群(或亚种)会表现出不同形态、生理、行为和生态特征。如分布广泛的马鹿C. elaphus有多个亚种,生活在中亚的大夏马鹿C. e. bactrianus具有低频和高频的混合鸣声,而欧洲马鹿C. e. corsicanus吼叫声的基频较低(F0均值为40 Hz),西伯利亚马鹿C. e. sibiricus基频超过1 000 Hz(Volodin et al., 2013)。研究者推测欧洲马鹿在扩散过程中丧失了高频率基频的鸣声,而西伯利亚亚种则丢失了低频率基频的鸣声(Volodin et al., 2013)。本研究关注的梅花鹿华南亚种浙江种群和其他隔离种群之间的遗传距离最远(吴华等,2008),线粒体分析和分子变异分析认为隔离种群形成了浙江和东北-四川-江西2个单系(Wu et al., 2004)。在研究过程中,还收集到一些梅花鹿华南亚种雌性个体的团体合唱鸣声,分析后同样也发现3~4个频带,说明多频带的特点并非警戒声所特有,而是在华南亚种各种类型的鸣声中均存在。这种高频率范围和多频带的鸣声特征可能与华南亚种的进化存在一定的关系。
本研究发现的梅花鹿东北亚种警戒声较为简单,虽有单音节和双音节,但只有1个明显清晰的频带。该亚种目前在其分布区内已很难发现活动痕迹(李彤等,2001),均为圈养种群。推测可能是长期的人为干预,使得该亚种的鸣声简单化。Golosova等(2017)研究不同状态种群(自由的、半约束和约束)的西伯利亚马鹿求偶鸣声,发现在持续时间和频率等方面存在显著差异。推测圈养种群的生存较野生种群遇险率低,使其在生理上的刺激处于较低状态,不用随时保持高度警惕状态,因此体现出较为单一和频率范围较窄的鸣声。
此外,研究还发现梅花鹿华南亚种警戒声的振幅范围明显低于东北亚种,这可能和录音的距离存在一定的关系,华南亚种为野生状态,警惕性高,不容易靠近获取资料,而东北亚种在饲养员的帮助下能够近距离收集信息。由于录音笔随机录制到不同个体的声音,录制距离随梅花鹿离录音笔的距离而改变(5~10 m)。
综上所述,通过分析梅花鹿2个亚种的警戒声,认为华南亚种具有较广的频率范围、较多的频带、较丰富的音节,推测可能是由于环境或遗传因素所造成的;东北亚种仅有1个明显清晰的频带且频率范围较窄,推测可能与长期的人工养殖存在一定的关系。但在长期进化过程中,2个亚种在遇到危险时仍具有相似的行为特性,即遇见危险发出短促高频的警戒声,且伴随着“抬起一只前蹄有力地踏地面”的行为,这种行为可能会持续数10 min;在双音节警戒声中均存在基频跳跃的现象,推测可能与梅花鹿紧张戒备情绪有关,生理和心理上的变化导致语音的变化(高慧等,2004)。
| 付义强, 胡锦矗, 郭延蜀, 等. 2006. 桃红岭自然保护区梅花鹿对春季栖息地的利用[J]. 动物学杂志, 41(4): 60–63. DOI:10.3969/j.issn.0250-3263.2006.04.011 |
| 付义强, 胡锦矗, 朱欢兵, 等. 2008. 华南梅花鹿声音通讯行为的初步研究[J]. 四川动物, 27(2): 266–268. |
| 高慧, 苏广川, 陈善广. 2004. 情绪化语音特征分析与识别的研究进展[J]. 航天医学与医学工程, 17(5): 386–390. DOI:10.3969/j.issn.1002-0837.2004.05.018 |
| 郭延蜀, 郑惠珍. 2000. 中国梅花鹿地史分布、种和亚种的划分及演化历史[J]. 兽类学报, 20(3): 168–179. DOI:10.3969/j.issn.1000-1050.2000.03.002 |
| 李春旺, 蒋志刚, 曾岩. 2001. 雄性麋鹿的吼叫行为、序位等级与成功繁殖[J]. 动物学研究, 22(6): 449–453. DOI:10.3321/j.issn:0254-5853.2001.06.004 |
| 李彤, 蒋劲松, 吴志刚, 等. 2001. 吉林省东北虎的调查[J]. 兽类学报, 21(1): 1–6. DOI:10.3969/j.issn.1000-1050.2001.01.001 |
| 孙儒泳. 1992. 动物生态学原理[M]. 北京: 北京师范大学出版社. |
| 吴华, 胡杰, 万秋红, 等. 2008. 梅花鹿的微卫星多态性及种群的遗传结构[J]. 兽类学报, 28(2): 109–116. DOI:10.3969/j.issn.1000-1050.2008.02.001 |
| 夏灿玮, 张雁云. 2009. 鸟类鸣声地理变异的形成机制[J]. 四川动物, 28(5): 777–780. |
| 徐俊晓, 谢锋, 江建平, 等. 2005. 我国12种无尾类的鸣叫特征参数[J]. 动物学杂志, 40(3): 12–19. DOI:10.3969/j.issn.0250-3263.2005.03.003 |
| 杨承忠, 张修月, 岳碧松, 等. 2012. 四川梅花鹿产仔换茸期声行为的研究[J]. 四川动物, 31(1): 10–16. DOI:10.3969/j.issn.1000-7083.2012.01.003 |
| 曾治高, 宋延龄, 李善元, 等. 2001. 海南坡鹿雄鹿发情期的吼叫行为及其在繁殖中的意义[J]. 动物学报, 47(5): 481–487. |
| 章叔岩, 郭瑞, 刘伟, 等. 2016. 华南梅花鹿研究现状及展望[J]. 浙江林业科技, 36(2): 90–94. DOI:10.3969/j.issn.1001-3776.2016.02.018 |
| Golosova OS, Volodin IA, Isaeva IL, et al. 2017. Effects of free-ranging, semi-captive and captive management on the acoustics of male rutting calls in Siberian wapiti Cervus elaphus sibiricus[J]. Mammal Research, 62(4): 387–396. DOI:10.1007/s13364-017-0322-4 |
| Hemp C, Kehl S. 2010. Taxonomic changes and new species of the flightless genus Parepistaurus Karsch, 1896 (Orthoptera:Acrididae, Coptacridinae) from mountainous east Africa[J]. Journal of Orthoptera Research, 19: 31–39. DOI:10.1665/034.019.0106 |
| Slabbekoorn H, Ripmeester EA. 2010. Birdsong and anthropogenic noise:implications and applications for conservation[J]. Molecular Ecology, 17(1): 72–83. |
| Volodin I, Frey R, Carranza J, et al. 2013. Spectrographic analysis points to source-filter coupling in rutting roars of Iberian red deer[J]. Acta Ethologica, 16(1): 57–63. DOI:10.1007/s10211-012-0133-1 |
| Wu H, Wan QH, Fang SG. 2004. Two genetically distinct units of the Chinese sika deer (Cervus nippon):analyses of mitochondrial DNA variation[J]. Biological Conservation, 119(2): 183–190. DOI:10.1016/j.biocon.2003.10.027 |
 2019, Vol. 38
2019, Vol. 38




