扩展功能
文章信息
- 郑佩华, 汪蕾, 张秀霞, 王冬梅, 李军涛, 鲁耀鹏, 冼健安, 王安利
- ZHENG Peihua, WANG Lei, ZHANG Xiuxia, WANG Dongmei, LI Juntao, LU Yaopeng, XIAN Jian'an, WANG Anli
- 凡纳滨对虾细胞色素P450(CYP370C2)基因的克隆与表达分析
- Molecular Cloning and Expression Analysis of Cytochrome P450 (CYP370C2) Gene in Litopenaeus vannamei
- 四川动物, 2018, 37(6): 628-636
- Sichuan Journal of Zoology, 2018, 37(6): 628-636
- 10.11984/j.issn.1000-7083.20180131
-
文章历史
- 收稿日期: 2018-04-25
- 接受日期: 2018-07-30
2. 华南师范大学脑科学与康复医学研究院, 广州 510631;
3. 华南师范大学生命科学学院, 广州 510631
2. Institute for Brain Research and Rehabilitation, South China Normal University, Guangzhou 510631, China;
3. College of Life Sciences, South China Normal University, Guangzhou 510631, China
凡纳滨对虾Litopenaeus vannamei俗称南美白对虾,由于具有生长速度快、抗逆性强、肉质鲜美、经济价值高等特点,成为目前世界上养殖范围最广、产量最高的三大对虾养殖品种之一。近年来,随着虾类养殖集约化程度的不断提高,养殖环境的日趋恶化,虾类疾病的危害日趋严重,养成率低下、经济损失严重。虾类抗胁迫和抗病的免疫防御机制是解决上述问题的理论基础,也是一直以来的研究重点。
细胞色素P450(cytochrome P450,CYP)酶系是一类结构上含有血红素和硫羟基,功能上参与生物体代谢途径、调节外源物质和内源物质相互转化的末端氧化酶,广泛存在于不同生物体的各种细胞和组织中(李术等,2013;梁艳等,2014)。CYP在细胞内的毒素、环境污染物、致癌物质及药物等代谢方面均发挥重要作用(冷欣夫,邱星辉,2001;Parmentier et al., 2005)。目前,关于昆虫CYP的研究已较深入,尤其是CYP对昆虫杀虫剂抗药性的影响(邱星辉,冷欣夫,1999),以及CYP参与保幼激素、蜕皮激素等内源性化合物的合成与代谢(艾均文,2008)。关于甲壳动物CYP的研究较少,在龙虾Homarus americanus(Snyder et al., 1998)、沟虾Orconects limosus(Dauphin et al., 1999)、岸蟹Carcinus maenas(Rewitz et al., 2003)和凡纳滨对虾(夏西超等,2012)中有CYP4家族的研究报道,该家族可能主要与蜕皮激素的代谢有关;淡水枝角水蚤Daphnia pulex的CYP被划分为4个家族:线粒体型、CYP2、CYP3和CYP4,其中,CYP2家族中的CYP370家系基因数量较多,占CYP基因总量的20%,CYP370家系的具体功能仍不清楚,推测淡水枝角水蚤拥有较大量的CYP370家系基因,可能与CYP370家系参与环境胁迫响应有关,这些胁迫因子包括水体中各类毒性污染物以及类似植物生物碱毒素的生长和行为的刺激物等(Baldwin et al., 2009)。
本研究在凡纳滨对虾氨氮胁迫转录组的差异表达基因中发现了1个CYP基因,通过cDNA末端快速克隆(RACE)技术克隆得到全长cDNA序列,经国际细胞色素P450命名委员会进行序列比对,该基因属于CYP370家系,命名为CYP370C2。本研究对CYP370C2基因进行了序列分析和组织特异性表达量分析,并测定了其在氨氮胁迫作用下以及脂多糖(LPS)刺激下的表达响应,探讨其在抗胁迫和抗病原体免疫防御中的作用,为进一步研究提高对虾的抗胁迫和抗病能力提供研究基础,同时也拓展了凡纳滨对虾的基因资源库,为对虾基因资源的利用提供了基础信息。
1 材料与方法 1.1 实验对虾凡纳滨对虾于2017年6月购自海南省海口市某养殖场,选取500尾生长状态良好的个体,雌雄随机分配,平均体质量11.8 g±1.7 g。在实验室循环养殖系统中暂养,水温24 ℃±2 ℃,盐度18‰,pH7.9~8.0,不间断曝气,并循环过滤。
1.2 总RNA的提取和cDNA第一链的合成取1尾凡纳滨对虾肝胰腺放入液氮中研磨,按照Trizol法提取总RNA,用微量分光光度计NanoDrop 2000(NanoDrop Technologies,USA)检验所提取的总RNA纯度并用1%琼脂糖凝胶电泳检验其完整性,用PrimeScript RT reagent Kit With gDNA Eraser(TaKaRa,大连)试剂盒将总RNA反转录成cDNA。
1.3 中间片段序列克隆从凡纳滨对虾转录组数据库中得到CYP370C2基因的初步cDNA序列,根据此序列设计中间片段引物CYP370-F1和CYP370-R1(表 1)。以凡纳滨对虾的肝胰腺cDNA为模板进行第一轮PCR扩增,程序如下:94 ℃预变性3 min;94 ℃ 30 s,58 ℃ 30 s,72 ℃ 1 min,35个循环;72 ℃延伸10 min。1%琼脂糖凝胶电泳检验。PCR产物使用SanPrep柱式DNA胶回收试剂盒[生工生物工程(上海)股份有限公司]进行纯化,再连接至pMD18-T载体(TaKaRa,大连),重组质粒转化到大肠杆菌Escherichia coli DH5α感受态细胞(TaKaRa,大连),培养并挑选阳性克隆送至华大基因公司测序。
| 引物 Primers |
序列(5'-3') Sequences (5'-3') |
| CYP370-F1 | GGGCTTCGGGAAACGC |
| CYP370-R1 | CCTCCTGGGATACGATGACC |
| CYP370-3'F1 | CAGCAACTGTAGCCTTTTCCGTCA |
| CYP370-5'R1 | CGCTTTAGCAAAGACTCTGAACTCCG |
| 3' RACE Outer primer | TACCGTCGTTCCACTAGTGATTT |
| UPM Long primer | CTAATACGACTCACTATAGGGCAAGCAGTGGTATCAACGCAGAGT |
| Short primer | CTAATACGACTCACTATAGGGC |
| CYP370-RT-F1 | GTGATGTTCGTGGAGGGTG |
| CYP370-RT-R1 | CCTGTAGTTTGACGCTGCC |
| β-actin F | GCCCATCTACGAGGGATA |
| β-actin R | GGTGGTCGTGAAGGTGTAG |
cDNA 3'末端克隆按照3'-Full RACE Core Set with PrimeScript RTase试剂盒(TaKaRa,大连)进行操作,设计基因特异性引物CYP370-3'F1和3'RACE Outer Primer进行PCR扩增,程序如下:94 ℃变性3 min;94 ℃ 30 s,58 ℃ 30 s,72 ℃1 min,30个循环;72 ℃延伸10 min。
cDNA 5'末端克隆按照SMART RACE cDNA Amplification Kit试剂盒(Clontech,USA)进行操作,使用特异性引物CYP370-5'R1和universal primer mix(UPM)进行PCR扩增,程序如下:94 ℃ 30 s,68 ℃ 30 s,72 ℃ 3 min,30个循环。获得5'-和3'-RACE PCR产物后进行凝胶纯化、连接载体、转入感受态细胞并测序。将获得的中间片段序列、3'末端序列和5'末端序列进行拼接,获得序列全长。
1.5 生物信息学分析使用DNAStar中的EdiSeq程序推导开放阅读框序列;利用NCBI网站上的BLAST(http://www.ncbi.nlm.nih.gov/blast)对基因的核酸序列和氨基酸序列进行同源性分析;用SignalP 3.0(http://www.cbs.dtu.dk/services/SignalP-3.0/)预测信号肽。蛋白理化性质预测使用的是Expasy(http://au.expasy.org/tools/)。运用Clustal X对氨基酸序列进行多序列比对,再使用MEGA 6.0中的邻接法构建系统进化树,并用Bootstrap重复1 000次计算各分支的置信度。
1.6 氨氮胁迫和LPS注射实验 1.6.1 氨氮胁迫实验选取健康的凡纳滨对虾随机分为对照组和氨氮胁迫组,每组3个平行,每个平行25尾。胁迫组中的水体氨氮浓度设置为20 mg·L-1(实测值为19.9 mg·L-1±0.8 mg·L-1) (Liu & Chen,2004),对照组不添加氨氮(氨氮未检出),其他实验条件与暂养期间一致。胁迫实验共进行48 h,实验期间每24 h换水1次,每次换水量为总水量的1/3,以保证相应的水体氨氮浓度。在氨氮胁迫后的0 h、3 h、6 h、12 h、24 h和48 h取样,每个时间点对照组和氨氮胁迫组各随机采集9尾,取肝胰腺和鳃立即在液氮中速冻,然后置于-80 ℃保存备用。
1.6.2 LPS注射实验将LPS(2 mg·mL-1,E. coli L2880,Sigma)溶解于生理盐水(0.8%NaCl)中,配制成终浓度为2 μg·μL-1的LPS工作液。将健康对虾随机分成对照组和LPS注射组,每组3个平行,每个平行25尾。LPS注射组每尾注射LPS工作液5 μL(Xian et al., 2016, 2017),对照组注射等量的无菌生理盐水。在LPS注射后的0 h、3 h、6 h、12 h、24 h和48 h取样,每个时间点对照组和LPS注射组各随机采集9尾,取肝胰腺和鳃立即在液氮中速冻,然后置于-80 ℃保存备用。
1.7 相对表达量分析根据测得的凡纳滨对虾CYP370C2基因的cDNA序列设计荧光定量引物CYP370-RT-F1和CYP370-RT-R1,以β-actin作为内参基因,引物序列为β-actin F和β-actin R(表 1)。实时荧光定量PCR的反应程序为:94 ℃ 3 min,95 ℃ 15 s,58 ℃ 15 s,72 ℃ 20 s,40个循环。实验仪器为美国Agilent公司的Stratagene Mx 3005P,实验结果采用2-△△Ct法计算相对表达量。
1.8 统计分析实验数据表示为平均值±标准差(Mean±SD)。组织表达量数据通过SPSS 19.0进行单因素方差分析(One-Way ANOVA);氨氮胁迫和LPS注射实验的数据通过SPSS 19.0进行t检验分析。
2 结果 2.1 CYP370C2基因cDNA序列分析凡纳滨对虾CYP370C2基因的cDNA序列如图 1所示,全长1 745 bp,包含1个1 464 bp的开放阅读框,编码由487个氨基酸构成的多肽,预测理论等电点为7.24,分子量为55.06 kDa。5'和3'非编码区分别为139 bp和142 bp,3'末端有1个终止密码子(TAA)、1个多聚腺苷酸加尾信号(AATAAA)和1个poly A尾。氨基酸序列中包括CYP蛋白特有的血红素结合区FxxGxRxCxG(FGKGRRLCLG)、Ⅰ螺旋保守区AGxxT(AGAET)、C螺旋保守区WxxxR(WKEQR)和K螺旋保守区ExxR、PxRF(EIFR、PERF)。氨基酸序列信号肽分析显示,N端氨基酸2~21为信号肽,是一种分泌蛋白。

|
| 图 1 凡纳滨对虾CYP370C2基因的核苷酸序列及其推导的氨基酸序列 Fig. 1 Nucleotide and deduced amino acid sequences of CYP370C2 gene of Litopenaeus vannamei 起始密码子(ATG)和终止密码子(TAA)用方框表示,多聚腺苷酸加尾信号(AATAAA)用下划线表示,P450蛋白特有的血红素结合区(FGKGRRLCLG)、Ⅰ螺旋保守区(AGAET)、C螺旋保守区(WKEQR)和K螺旋保守区(EIFR、PERF)用灰色阴影显示 The letters in box indicate the start codon (ATG) and the stop codon (TAA), the region underlined indicates the polyadenylation signal sequence (AATAAA), the areas shaded in gray indicate heme-binding domain (FGKGRRLCLG), Ⅰ-helix (AGAET), C-helix(WKEQR) and K-helix(EIFR, PERF) |
| |
运用BLAST分析得到,凡纳滨对虾CYP370C2基因序列与三疣梭子蟹Portunus trituberculatus CYP基因(GenBank登录号:AJF94637.1)序列相似度最高,为64%;与甲壳纲Crustacea的淡水枝角水蚤(GenBank登录号:EFX83696.1)、昆虫纲Insecta的湿木白蚁Zootermopsis nevadensis(GenBank登录号:KDR19530.1)、内口纲Entognatha的跳虫Orchesella cincta(GenBank登录号:ODM99561.1)的相似度次之,为43%;与昆虫纲的台湾乳白蚁Coptotermes formosanus(GenBank登录号:AGQ48062.1)、甲壳纲的大型蚤Daphnia magna(GenBank登录号:KZS13729.1)和太平洋折翅蠊Diploptera punctata(GenBank登录号:AAS13464.1)的分别为41%、40%和39%。
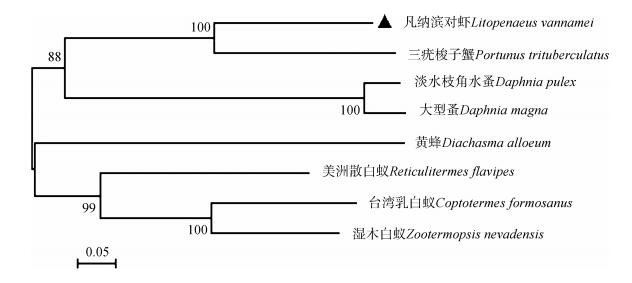
与凡纳滨对虾CYP370C2基因和序列相似性最高的均属于节肢动物门Arthropoda的7个物种的CYP基因序列构建系统进化树。结果显示,这些CYP基因在系统进化树上分为2个分支。凡纳滨对虾首先与软甲纲Malacostraca的三疣梭子蟹聚为一支,该分支与甲壳纲的淡水枝角水蚤和大型蚤聚为小分支,昆虫纲等翅目Isoptera的物种聚为一支,然后与膜翅目Hymenoptera聚为小分支(图 2)。
|
| 图 2 使用邻接法对凡纳滨对虾CYP370C2基因的系统进化分析 Fig. 2 Phylogenetic analysis of Litopenaeus vannamei CYP370C2 gene by using neighbor-joining method |
| |
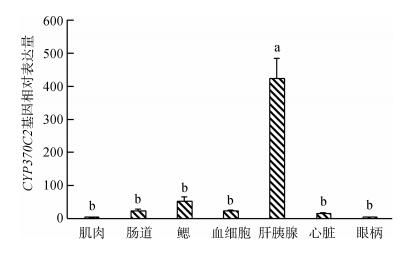
CYP370C2基因在凡纳滨对虾的肌肉、肠道、鳃、血细胞、肝胰腺、心脏和眼柄等7个组织中均有表达,在肝胰腺中的相对表达量最高,显著高于其他组织(P<0.05),其次是鳃、肠道、血细胞、心脏和眼柄,在肌肉中的相对表达量最低(图 3)。
|
| 图 3 CYP370C2基因在凡纳滨对虾不同组织中的相对表达量 Fig. 3 Relative expression levels of CYP370C2 gene in different tissues of Litopenaeus vannamei 不同小写字母表示不同组织之间的差异有统计学意义(P<0.05) Different lowercase letters show there is a significant difference between different tissues (P < 0.05) |
| |
在48 h的氨氮胁迫试验中,凡纳滨对虾肝胰腺中CYP370C2基因相对表达量在胁迫的24 h和48 h显著上调(P<0.05,P<0.01),在48 h时达到峰值,约为对照组的3.26倍;鳃中CYP370C2基因相对表达量在胁迫的12~48 h显著上升(12 h:P<0.05,24 h:P<0.01,48 h:P<0.001),在24 h时达到最高值,为对照组的16.67倍(图 4)。

|
| 图 4 氨氮胁迫对凡纳滨对虾肝胰腺(A)和鳃(B)中CYP370C2基因相对表达量的影响 Fig. 4 Effects of ammonia-N stress on the relative expression levels of CYP370C2 gene in hepatopancrea (A) and gill (B) of Litopenaeus vannamei * P<0.05,** P<0.01,*** P<0.001;下同the same below |
| |
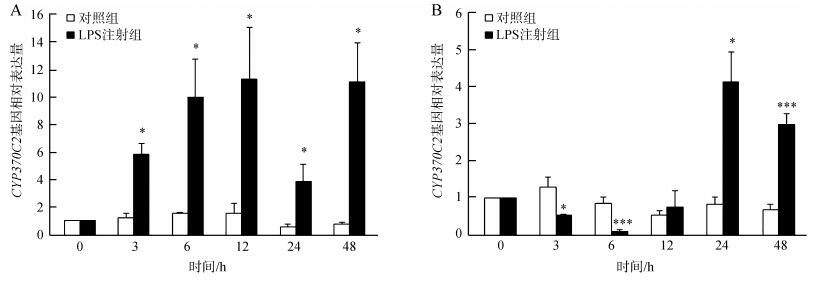
凡纳滨对虾肝胰腺中的CYP370C2基因相对表达量在LPS注射后的3~48 h均显著上调(P<0.05),最大值出现在注射后的12 h,约为对照组的11.29倍;鳃中CYP370C2基因相对表达量在注射后的3 h和6 h呈现显著的下降(P<0.05,P<0.01),在12 h恢复至对照组水平,在24 h和48 h急剧上调,24 h达到最大值,约为对照组的4.16倍(图 5)。
|
| 图 5 脂多糖(LPS)注射对凡纳滨对虾肝胰腺(A)和鳃(B)中CYP370C2基因相对表达量的影响 Fig. 5 Effects of lipopolysaccharide (LPS) injection on the relative expression levels of CYP370C2 gene in hepatopancrea (A) and gill (B) of Litopenaeus vannamei |
| |
本研究克隆的凡纳滨对虾CYP基因属于CYP2家族中的CYP370家系,命名为CYP370C2,经比对,其序列与节肢动物门其他物种相似。凡纳滨对虾CYP370C2基因与夏西超等(2012)克隆得到的CYP4V18基因的一致性只有18.36%,2个基因序列的较大差异表明它们的蛋白可能拥有不同的生理功能。几种节肢动物的CYP370C2基因系统发育树表明,CYP370C2基因的聚类关系符合物种系统发育关系。
CYP在各种组织和器官中广泛存在,但其分布具有组织特异性。在鱼类研究中发现,CYP在肝胰脏中分布最多,在鳃、肾脏、心脏等组织中少量存在(Brittebo et al., 1994;王芳等,2006;胡晓等,2011),这与本研究的结果较一致。肝胰腺是外源有毒物质代谢的主要场所,通过CYP的氧化反应以及谷胱甘肽氧化还原系统,使外源物质活性降低、水溶性增加,从而经肾脏等排出体外(Benet et al., 1996)。鳃是水生动物的呼吸器官,由于鳃与外界水环境直接接触,与其他组织器官相比,鳃更容易受到病原体的侵染以及水体污染物的毒害。CYP370C2基因在肝胰腺和鳃中的高表达量表明,它在这3个重要器官的防御机制中发挥重要作用。
3.2 凡纳滨对虾CYP370C2基因对氨氮胁迫的表达响应养殖水体中的氨氮主要来源于水生动物含氮废物的排泄和食物分解,是水产养殖中常见的水污染物之一(孙国铭等,2002;姜令绪等,2004;冼健安等,2014)。以往的研究表明,氨氮对水生动物包括甲壳纲十足目Decapoda动物具有较强的毒性。氨氮会抑制对虾的生长和变态,损坏其组织和器官,影响其免疫与代谢功能,降低其对环境的适应力、耐受力及对疾病的抵抗能力,造成对虾发病死亡(冼健安等,2014)。本实验中,在氨氮胁迫后期,对虾肝胰腺和鳃中CYP370C2基因的表达量均呈现显著上调,表明CYP370C2基因可能在抗氨氮胁迫的防御机制中发挥重要作用。目前关于甲壳动物CYP370家系的研究仅见于淡水枝角水蚤,该研究发现,相对于昆虫的CYP基因,淡水枝角水蚤CYP370家系基因数量得到了扩充,约占其CYP基因总量的20%。目前关于CYP370家系的研究仍甚少,推测CYP370家系基因数量的扩充可能与其在对抗环境胁迫的响应过程中发挥重要作用(Baldwin et al., 2009)。据本研究结果,推测凡纳滨对虾CYP370C2基因可能参与了氨氮胁迫下毒性代谢物的代谢过程,将氨氮胁迫所引起的有毒有害代谢物进行分解,以解除毒性并利于代谢废物排出体外,从而降低氨氮胁迫带来的损害。
比较肝胰腺和鳃,CYP370C2基因在敏感度和表达水平上均有一定的差异。鳃中CYP370C2基因相对表达量在胁迫的12 h开始显著上调,肝胰腺中CYP370C2基因相对表达量在24 h开始出现显著上升,表明鳃中CYP370C2基因对氨氮胁迫响应的敏感度高于肝胰腺。另一方面,氨氮胁迫下,鳃中CYP370C2基因相对表达量比肝胰腺高,最高值达到了对照组的16.67倍,而在肝胰腺中,最高值仅为对照组的3.26倍。鳃是对虾直接与外部环境接触的器官,水环境中的氨会通过鳃上皮细胞进入血淋巴,再被运输至其他部位,鳃是首先受到氨氮持续性毒害作用的组织器官,这可能是鳃中CYP370C2基因对氨氮胁迫具有更高敏感度和更强烈表达响应的原因,机体通过上调鳃中CYP370C2基因的表达量,起到对鳃的抗胁迫保护作用。肝胰腺是发挥解毒作用的器官,研究显示在氨氮胁迫作用下,氨氮主要积累在对虾的肝胰腺中(Chen & Chen,2000),可能是虾体将氨氮运输至肝胰腺进行解毒代谢。本研究结果显示,肝胰腺中CYP370C2基因的基础表达量远高于其他组织,在氨氮胁迫作用下,其表达量也被进一步诱导上调,表明CYP370C2基因可能参与了氨氮胁迫下肝胰腺的解毒代谢过程。
3.3 凡纳滨对虾CYP370C2基因对LPS刺激的表达响应LPS是革兰氏阴性细菌细胞壁组分之一,具有高度抗原性和细胞毒性,也被称为内毒素。研究显示LPS可诱导活性氧(ROS)引起的Ca2+介导的血细胞凋亡,导致血细胞数量下降,同时也会引起血细胞脱颗粒释放酚氧化酶原系统等一系列的免疫响应(Xian et al., 2016, 2017)。经LPS刺激后,对虾许多与免疫相关的基因在鳃或肝胰腺中都有不同程度的上调,例如,与Toll样受体(TLR)-NF-kB途径相关的Sptzle基因、NOS、溶菌酶等(Yao et al., 2010;Peregrino-Uriarte et al., 2012;Yuan et al., 2017),表明这些免疫相关基因参与了抗菌防御过程。在本研究中,LPS对凡纳滨对虾肝胰腺和鳃中的CYP370C2基因表达量也产生了显著影响。CYP370C2基因对LPS刺激的表达响应在肝胰腺和鳃中存在一定差异。经LPS刺激后,在肝胰腺中,CYP370C2基因的相对表达量在48 h内一直呈现上调的状态;而在鳃中,CYP370C2基因的转录先被抑制,然后恢复,在后期再升高。该基因在不同器官间可能存在不同的调控机制,肝胰腺作为虾类重要的免疫和解毒器官,其中,CYP370C2基因的表达迅速被LPS刺激所诱导上调并持续保持高表达,表明CYP370C2基因可能作为重要的解毒酶参与了肝胰腺抗LPS毒性的防御过程。另一方面,CYP370C2基因在2个组织中的表达强度也存在差异。经LPS刺激后,CYP370C2基因在肝胰腺中的最高表达量可达对照组的11.29倍,而在鳃中的相对表达量约为对照组的4.16倍,肝胰腺表现出更为强烈的表达响应,这一结果与氨氮胁迫的结果相反,这可能与环境胁迫和病原体侵染过程的差异有关。
| 艾均文. 2008.家蚕(Bombyx mori)全基因组细胞色素P450基因结构与进化分析及CYP18A1克隆与功能分析[D].重庆: 西南大学. http://cdmd.cnki.com.cn/Article/CDMD-10635-2008094081.htm |
| 胡晓, 房文红, 汪开毓, 等. 2011. 氟甲喹对异育银鲫细胞色素CYP450主要药酶的影响[J]. 中国水产科学, 18(2): 392–399. |
| 姜令绪, 潘鲁青, 肖国强. 2004. 氨氮对凡纳对虾免疫指标的影响[J]. 中国水产科学, 11(6): 537–541. DOI:10.3321/j.issn:1005-8737.2004.06.009 |
| 冷欣夫, 邱星辉. 2001. 细胞色素P450酶系的结构、功能与应用前景[M]. 北京: 科学出版社. |
| 李术, 付瑶, 李铭, 等. 2013. 阿特拉津和毒死蜱对鲤鱼鳃组织细胞色素P450酶系影响[J]. 东北农业大学学报, 44(6): 107–111. |
| 梁艳, 李彦, 白清清, 等. 2014. CYP450基因多态性研究进展[J]. 武警医学, 25(5): 529–532. |
| 邱星辉, 冷欣夫. 1999. 昆虫细胞色素P450基因的表达与调控及P450介导抗性的分子机制[J]. 农药学学报, 1(1): 7–14. |
| 孙国铭, 汤建华, 仲霞铭. 2002. 氨氮和亚硝酸氮对南美白对虾的毒性研究[J]. 水产养殖(1): 22–24. DOI:10.3969/j.issn.1004-2091.2002.01.010 |
| 王芳, 李凯彬, 聂湘平, 等. 2006. 唐鱼细胞色素P450 1A基因cDNA克隆及分析[J]. 生态科学, 25(6): 526–529. DOI:10.3969/j.issn.1008-8873.2006.06.011 |
| 夏西超, 王文锋, 杨洪, 等. 2012. 凡纳滨对虾细胞色素P450家族新基因CYP4V18的克隆及KK-42对其转录的抑制[J]. 中国水产科学, 19(5): 767–774. |
| 冼健安, 钱坤, 郭慧, 等. 2014. 氨氮对虾类毒性影响的研究进展[J]. 饲料工业, 35(22): 52–58. |
| Baldwin WS, Marko PB, Nelson DR. 2009. The cytochrome P450 (CYP) gene superfamily in Daphnia pulex[J]. BMC Genomics, 10: 169. DOI:10.1186/1471-2164-10-169 |
| Benet LZ, Kroetz DL, Sheiner LB. 1996. Pharmacokinetics: the dynamics of drug absorption, distribution and elimination[M]//Brunton LL, Laza JS, Parker KL. Goodman & Gilman's the pharmacological basis of therapeutic. New York: McGraw-Hill Companies: 3-27. |
| Brittebo EB. 1994. Metabolism-dependent binding of the heterocyclic amine Trp-P-1 in endothelial cells of choroid plexus and in large cerebral veins of cytochrome P450-induced mice[J]. Brain Research, 659(1-2): 91–98. DOI:10.1016/0006-8993(94)90867-2 |
| Chen JM, Chen JC. 2000. Study on the free amino acid levels in the hemolymph, gill, hepatopancreas and muscle of Penaeus monodon exposed to elevated ambient ammonia[J]. Aquatic Toxicology, 50: 27–37. DOI:10.1016/S0166-445X(99)00095-8 |
| Dauphin VC, Bocking D, Tom M, et al. 1999. Cloning of a novel cytochrome P450 (CYP4C15) differentially expressed in the steroidogenic glands of an arthropod[J]. Biochemical Biophysical Research Communications, 264: 413–418. DOI:10.1006/bbrc.1999.1363 |
| Liu CH, Chen JC. 2004. Effect of ammonia on the immune response of white shrimp Litopenaeus vannamei and its susceptibility to Vibrio alginolyticus[J]. Fish & Shellfish Immunology, 16: 321–334. |
| Nelson DR, Kamataki T, Waxman DJ, et al. 1993. The P450 superfamily: update on new sequences, gene mapping, accession numbers, early trivial names of enzymes, and nomenclature[J]. DNA & Cell Biology, 12(1): 1–51. |
| Parmentier JH, Lavrentyev EN, Falck JR, et al. 2005. Evaluation of cytochrome P450 4 family as mediator of phospholipase D activation in aortic vascular smooth muscle cells[J]. Life Sciences, 77(9): 1015–1029. DOI:10.1016/j.lfs.2005.03.002 |
| Peregrino-Uriarte AB, Muhlia-Almazan AT, Arvizu-Flores AA, et al. 2012. Shrimp invertebrate lysozyme i-lyz: gene structure, molecular model and response of c and i lysozymes to lipopolysaccharide (LPS)[J]. Fish & Shellfish Immunology, 32(1): 230–236. |
| Rewitz Z, Styrishave B, Andersen O, et al. 2003. CYP330A1 and CYP4C39 enzymes in the shore crab Carcinus maenas: sequence and expression regulation by ecdysteroids and xenobiotics[J]. Biochemical Biophysical Research Communications, 310: 252–260. DOI:10.1016/j.bbrc.2003.09.063 |
| Snyder MJ. 1998. Identification of a new cytochrome P450 family, CYP45, from the lobster, Homarus americanus, and expression following hormone and xenobiotic exposures[J]. Archives of Biochemistry and Biophysics, 358: 271–276. DOI:10.1006/abbi.1998.0878 |
| Xian JA, Zhang XX, Guo H, et al. 2016. Cellular responses of the tiger shrimp Penaeus monodon haemocytes after lipopolysaccharide injection[J]. Fish & Shellfish Immunology, 54: 385–390. |
| Xian JA, Zhang XX, Wang DM, et al. 2017. Various cellular responses of different shrimp haemocyte subpopulations to lipopolysaccharide stimulation[J]. Fish & Shellfish Immunology, 69: 195–199. |
| Yao CL, Ji PF, Wang ZY, et al. 2010. Molecular cloning and expression of NOS in shrimp, Litopenaeus vannamei[J]. Fish & Shellfish Immunology, 28(3): 453–460. |
| Yuan K, Yuan FH, Weng SP, et al. 2017. Identification and functional characterization of a novel Spätzle gene in Litopenaeus vannamei[J]. Developmental & Comparative Immunology, 68: 46–57. |
 2018, Vol. 37
2018, Vol. 37




