扩展功能
文章信息
- 何雨桐, 孙哲, 王刚
- HE Yutong, SUN Zhe, WANG Gang
- 聚乙烯亚胺增强Pluronic介导的BALB/c小鼠骨骼肌原位基因传递和表达效率
- Polyethyleneimine Enhances in situ Gene Delivery and Expression in Skeletal Muscles of BALB/c Mice in the Pluronic-Mediated System
- 四川动物, 2018, 37(6): 620-627
- Sichuan Journal of Zoology, 2018, 37(6): 620-627
- 10.11984/j.issn.1000-7083.20180156
-
文章历史
- 收稿日期: 2018-03-14
- 接受日期: 2018-05-25
人体骨骼肌分布广、体积大且血管丰富,通过肌肉注射的方式将编码功能蛋白的基因传递到骨骼肌细胞中,以之为“工厂”在患者体内“生产”治疗性蛋白,实现个体化、精准化治疗,是一种意义重大且前景广阔的治疗策略(Lu et al., 2003a)。如何安全高效地将外源基因传递到肌肉细胞内表达是该策略成功的关键。尽管质粒DNA(pDNA)可以被传递到肌肉细胞中表达,但由于直接注射pDNA易被降解、入胞效率低等,转染效率并不理想。因此,人们一直致力于开发各种基因传递策略来提高肌肉内基因传递和表达效率,如电转移法、超声法和载体介导法等(Mir et al., 1998;Guérin,2000;Lauritzen et al., 2002;Lu et al., 2003b;Wells,2004;Lee et al., 2012)。本文探究了阳离子聚合物——聚乙烯亚胺(polyethyleneimine,PEI)作为基因载体,在骨骼肌原位基因传递体系中应用的可能性,利用PEI/pDNA复合物和Pluronic L64联用构建了安全高效的基因传递体系(L/P/D),其中,L代表Pluronic L64,P代表PEI,D代表pDNA。通过对不同氮磷比(N/P)的L/P/D体系介导的基因表达效率及体内生物安全性评估,揭示了N/P与肌肉内基因转染效率的关系,并确立了PEI在骨骼肌内应用的有效方案。该方案为筛选和开发高效的、适用于临床治疗的骨骼肌原位基因传递系统提供了适当的原理和策略。
1 材料和方法 1.1 实验动物5~7周龄体质量为20~25 g的BALB/c雄性小鼠若干,购于成都达硕生物科技有限公司[实验动物生产许可证号:SYXK(川)2015-030]。动物实验均在四川大学伦理委员会认可下进行,符合相关法规及制度[实验动物使用许可证号:SYXK(川)2013-017]。将小鼠在21 ℃、湿度45%~65%的环境中随机分笼饲养。每组6只,所有小鼠均注射双侧小腿胫骨前肌。
1.2 试剂及仪器支化聚乙烯亚胺25 kDa、Pluronic L64(Sigma-Aldrich,美国);β-半乳糖苷酶(pCMV-LacZ)原位染色试剂盒(碧云天,中国);E.Z.N.A.TM质粒小量提取试剂盒、PureLinkTM高纯质粒大量提取试剂盒(Invitrogen,美国);Luciferase Assay Kit(Promega,美国);BCA蛋白分析试剂盒(Thermo,美国)。编码β-半乳糖苷酶、荧光素酶(pCMV-Luc)和远红外荧光蛋白(pCMV-E2)的3种质粒由本实验室刘益丽博士提供。ChemiDocTM XRS+凝胶成像系统(Bio-Rad,美国);Varioskan Flash多功能酶标仪(Thermo,美国);NanoS ZEN 1600型纳米粒度及电位分析仪(Malven,英国);NanoDrop 2000(Thermo,美国);MFP-3D-BIOTM原子力显微镜(Bruker,美国);In-Vivo Imaging System(CRI,美国)。
1.3 实验方法 1.3.1 质粒的制备与鉴定所有质粒在大肠杆菌Escherichia coli DH5α中转化扩增,并用上述提及的质粒提取试剂盒提取获得。制备好的质粒用NanoDrop 2000测定浓度和纯度,1%琼脂糖凝胶电泳鉴定,于-20 ℃短期保存,-80 ℃长期保存。
1.3.2 肌肉原位注射操作配制各实验组样品,浓度为2 mg·mL-1的pDNA溶液与等浓度的PEI工作液按相应N/P混合,其中,DNA总质量为10 μg,室温孵育20 min后形成N/P分别为0.5、3和10的PEI/pDNA复合物。随后,取不同比例的复合物与10 μL 0.4%(W/V)Pluronic L64混合,用生理盐水稀释到40 μL,Pluronic L64终浓度为0.1%(W/V),混合物室温静置5 min,形成L/P/D体系(L/P/D-0.5、L/P/D-3、L/P/D-10),其中,L/P/D-0.5组代表PEI与pDNA的N/P=0.5,L/P/D-3组为N/P=3,L/P/D-10组为N/P=10。以生理盐水组为阴性对照组,pDNA组为阳性对照组1,Pluronic L64/pDNA混合液(L/D)组为阳性对照组2。
小鼠7 d适应期后,其两侧胫骨前肌均被脱毛、消毒。用注射器分别吸取40 μL对照组溶液和实验组溶液。肌肉注射时沿平行肌纤维方向进针约2 mm,2~5 s完成注射。
1.3.3 报告基因检测采用3种报告基因检测体系分别从定性、定量以及基因表达持续性评估L/P/D体系:
(1) β-半乳糖苷酶定性检测:对组织以原位染色的方式进行检测,通过观察着色范围和颜色深浅判断基因表达情况。按照β-半乳糖苷酶原位染色试剂盒说明书进行实验,包括在冰上于染色固定液中固定20 min,用磷酸盐缓冲液(PBS)洗涤3次后,固定的样本进行染色处理2 h以上,最后用数码照相机采集图像。
(2) 荧光素酶定量检测:采用Luciferase Reporter Assay Kit试剂盒进行检测。具体步骤包括:样品经冰上匀浆、-80 ℃过夜裂解及4 ℃ 12 000 r·min-1离心3 min后,取20 μL上清液于不透光白色96孔酶标板中,用多功能酶标仪自动加样并读取吸光值。同时,采用BCA Protein Assay Kit进行样品含量测定和均一化处理。标准品和样品用酶标仪测定OD562下的吸光值,根据标准曲线方程计算出样品中蛋白质含量,使用相对荧光素酶活性(RLU/mg Protein)表示结果。
(3) 远红外荧光蛋白检测基因持续表达情况:采用活体成像系统对肌肉原位注射后第7、14天后的红色荧光蛋白E2-Crimson表达情况进行检测。检测前小鼠胫骨前肌脱毛处理,用黄光激发,在600~700 nm处扫描荧光信号,最后用仪器自带软件进行荧光成像分析。
1.3.4 组织病理学检测对注射后的肌肉组织和主要脏器(心、肝、脾、肺、肾)切片进行染色及观察,评估阳离子与Pluronic联用的基因传递体系的生物安全性,为临床使用提供依据。肌肉注射7 d后分离小腿胫骨前肌或尾静脉注射4 d后解剖取出小鼠主要脏器,用PBS洗涤后放入4%(W/V)多聚甲醛固定液中固定48 h后,在乙醇和二甲苯溶液中进行梯度脱水。脱水后的样品经过石蜡包埋、切片、苏木精-伊红(HE)染色处理后,用光学显微镜拍照。
1.3.5 L/P/D-0.5体系中PEI/pDNA复合物的粒径、电位及形貌表征3 μg或20 μg pDNA与浓度为100 ng·μL-1 PEI工作液按相应N/P混合,室温孵育20 min后用MilliQ水稀释到1 mL。将装有1 mL样本溶液的1 cm石英比色皿放入马尔文纳米粒度及电位分析仪(Zeta-sizer,Malvern)中,通过动态光散射法(dynamic light scattering,DLS)对N/P为0.5时PEI/pDNA复合物的粒径、分散性以及表面电位进行检测,样品DNA终浓度为3 μg·mL-1,每个样品重复3次。将复合物吸附于云母片上并干燥后,使用原子力显微镜(AFM)表征其粒径和形态学特征,样品DNA终浓度为20 μg·mL-1。
1.4 统计学分析采用Origin、Prism5.0对数据进行统计学分析,采用组间单因素方差(One-Way ANOVA)或t检验进行分析,P<0.05为差异有统计学意义。
2 结果 2.1 β-半乳糖苷酶定性和荧光素酶定量分析考察不同比例L/P/D体系对基因表达效率的影响,是应用阳离子材料构建高效的骨骼肌原位基因传递体系的关键。肌肉注射7 d后,在β-半乳糖苷酶(图 1:A)和荧光素酶(图 1:B)的表达水平上,L/P/D-0.5组的基因表达水平明显高于阳性对照组1和阳性对照组2。然而,随着N/P增加(L/P/D-3和L/P/D-10),基因表达量开始明显下降。从数值上看,L/P/D-0.5组介导的荧光素酶表达量是阳性对照组1的28.6倍、阳性对照组2的2.5倍。然而,当N/P增加到3和10时,几乎检测不到外源基因的表达,相比于其他组其数值减少了至少4个数量级。这些结果说明,只有在特定低的N/P时,PEI才能对该体系中的基因传递和表达产生积极的影响。因此,L/P/D-0.5为最优化的L/P/D体系。

|
| 图 1 L/P/D体系中肌肉内报告基因表达水平 Fig. 1 Intramuscular expression of reporter genes in L/P/D system 肌肉注射7 d后,A. β-半乳糖苷酶表达,B.荧光素酶活性;a.阳性对照组1,b.阳性对照组2,c. L/P/D-0.5组,d. L/P/D-3组,e. L/P/D-10组;与阳性对照组1比较,*P<0.05 7 days after intramuscular injection, A. the image of β-galactosidase expression, B. the luciferase activity; a. positive control group 1, b. positive control group 2, c. L/P/D-0.5 group, d. L/P/D-3 group, e. L/P/D-10 group; compared with positive control group 1, * P < 0.05 |
| |
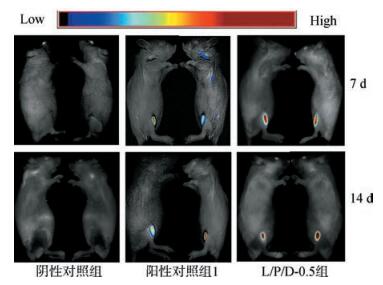
在动物活体内持续考察外源基因表达,对于评估基因表达强度和持续性更有说服力(Pu et al., 2014)。活体成像的结果显示,阳性对照组1和L/P/D-0.5组的荧光信号能持续表达至少2周且未出现明显衰减。L/P/D-0.5组的荧光信号明显高于阳性对照组1 (图 2)。
|
| 图 2 活体内原位荧光蛋白表达 Fig. 2 In vivo expression of the in-situ fluorescent protein |
| |
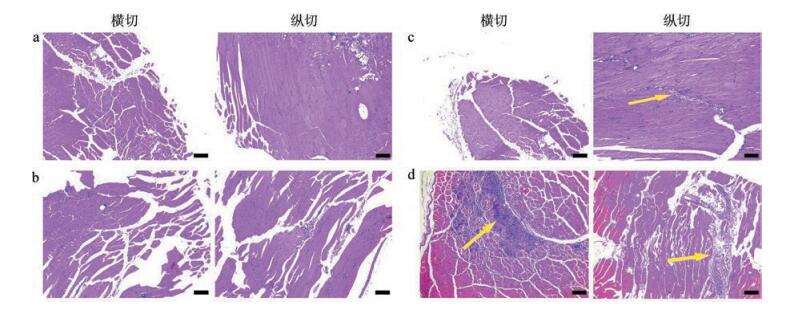
肌肉注射7 d后,L/P/D-0.5组与阴性对照组的HE染色切片均未发现组织病变(图 3:a、b),说明少量的PEI用于骨骼肌原位基因传递体系中是安全的。随着N/P增加,L/P/D-3组显示出肌纤维变性及炎细胞浸润等病理变化(图 3:c)。当N/P达到10时,HE染色切片中出现大面积的炎症细胞浸润、淋巴细胞浸润和肌纤维坏死等病理变化(图 3:d)。
|
| 图 3 不同比例的L/P/D体系中局部肌肉的组织学分析(苏木精-伊红染色,标尺=100 μm) Fig. 3 Histological analysis of local muscles in L/P/D systems with different N/P ratios (hematoxylin-eosin staining, scale bars=100 μm) a.阴性对照组,b. L/P/D-0.5组,c. L/P/D-3组,d. L/P/D-10组;黄色箭头为炎症浸润 a. negative control group, b. L/P/D-0.5 group, C. L/P/D-3 group, D. L/P/d-10 group; the yellow arrow shows inflammatory infiltration |
| |
尾静脉注射4 d后,通过观察主要脏器的组织切片,评估该体系的体内急性毒性。L/P/D-0.5组与阴性对照组的结果一致,未出现明显的器官损伤(图 4),说明与局部注射的结果一致,尾静脉注射L/P/D-0.5不会造成脏器病变,进一步说明该体系具有良好的生物相容性。

|
| 图 4 主要脏器的组织学分析(苏木精-伊红染色,标尺=100 μm) Fig. 4 Histological analysis of major organs (hematoxylin-eosin staining, scale bar=100 μm) |
| |
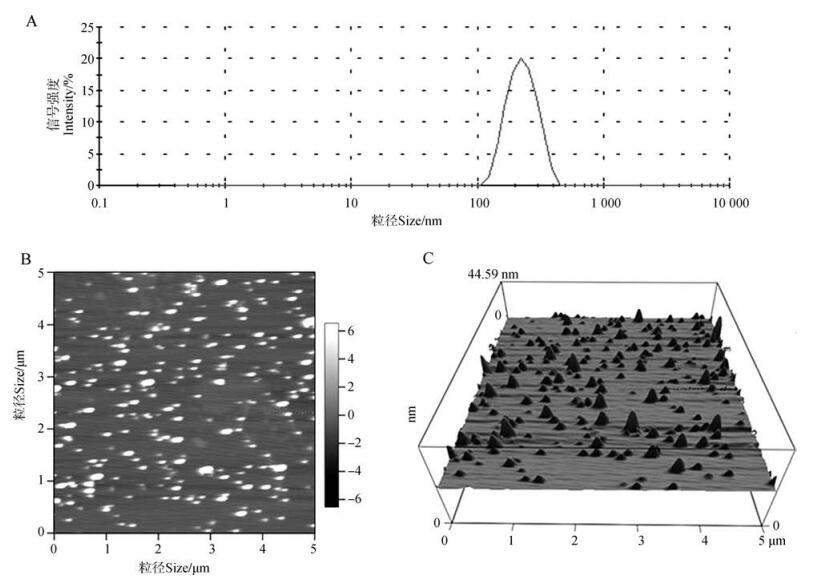
N/P为0.5的PEI/pDNA复合物(PEI/pDNA-0.5)的粒径见图 5:A,该比例复合物具有纳米尺寸[304 nm±7.6 nm,多分散系数(polydispersity index,PDI)=0.43],且zeta电位为负(-15.9 eV±1.4 eV),表明当N/P为0.5时,PEI与pDNA形成了纳米尺寸的复合物粒子。通过AFM表征复合物的形貌特征,结果显示,PEI/pDNA-0.5复合物具有近似球体的三维结构(图 5:B、C)。而AFM测定的粒径结果显示该复合物的粒径在100~200 nm,这和动态光散射法的结果存在一定差异。
|
| 图 5 PEI/pDNA-0.5复合物的粒径(A)和形貌特征(B、C) Fig. 5 Size (A) and morphologies (B, C) analysis of PEI/pDNA at N/P=0.5 A.利用动态光散射仪测试的纳米粒子粒径及多分散性;B.原子力显微镜(AFM)对纳米粒子的形貌测试结果,右侧灰度靶表示粒子的高度;C.利用AFM测试的纳米粒子立体形貌图 A. the particle size and polydispersity index of nanoparticles tested by dynamic light scattering instrument, B. the test results of atomic force microscope (AFM) on the morphology of nanoparticles, C. the three-dimensional morphology of nanoparticles tested by AFM |
| |
骨骼肌原位基因传递和表达体系为基因治疗提供了理想的策略,该体系的开放性允许将多种方法联合应用,以获得更好的治疗效果。非离子型材料Pluronic可以提高基因传递效率,主要用于:(1)和病毒载体联用以提高其安全性并增强基因转染效率(Feldman et al., 1997;Dishart et al., 2003);(2)作为载体修饰基团(Jeon et al., 2003)或辅剂(Astafieva et al., 1996)改善阳离子非病毒载体在血清/生理环境中的稳定性并提高基因转染效率;(3)单独或与物理方法联用,能显著增强外源基因在肌肉原位基因传递体系中的传递/表达水平(Guérin,2000;Song et al., 2013;Liu et al., 2014)。Pluronic可能通过多种分子机制促进外源基因传递和表达,譬如,通过增强细胞膜通透性以增强pDNA、病毒载体或阳离子材料/DNA复合物的摄取(Gebhart et al., 2002);促进pDNA在骨骼肌中的渗透、分布或入核作用等(Guérin,2000;Pitard et al., 2002)。在一种Pluronic L64介导的高效的骨骼肌内基因传递方案中,Pluronic L64利用相似的磷脂分子层结构与细胞膜相互作用,干扰其完整性,提高膜渗透性(Liu et al., 2014)。然而在该体系中,由于其Pluronic L64不与pDNA相互作用,未受保护的DNA在复杂的体内环境中容易被核酸酶降解,难以顺利、安全传递到目标位点(Schmidtwolf & Schmidtwolf,2003)。与此同时,相比于被压缩成纳米级的核酸分子,未被压缩的pDNA由于疏松的分子链状态,其跨膜运动的效率会降低(Godbey et al., 1999)。
一种常见的核酸保护策略是利用阳离子载体通过电荷作用对带负电荷的核酸分子进行压缩保护。支化聚乙烯亚胺作为一种公认的核酸载体被广泛应用于体外基因转染,展示出优异的转染效果(Xu et al., 2009;He et al., 2013)。然而,大多数体内实验却揭示了阳离子材料对肌内基因传递和表达的无效性甚至强烈的抑制作用(Tros et al., 2010;Song et al., 2013;Pu et al., 2014)。这可能是由于体外细胞培养环境和复杂体内肌肉环境的不同所造成的(Ruponen et al., 1999)。细胞外基质(extracellular matrix,ECM)中大量带负电荷的分子能结合带正电荷的PEI/pDNA复合体,从而干扰复合物向肌肉细胞内的传递,极大地降低了肌内基因传递效率并引发严重的组织炎症(Pitard et al., 2004;Burke & Pum,2008)。因此推测,带负电荷或电中性的材料/pDNA复合物能避免与ECM中电负性分子的非特异性结合,可能适合于肌内基因传递体系。在PEI与pDNA的复合体系中,通过调节阳离子PEI与pDNA的比例,制备出带有不同表面电荷的复合物。因此,本研究希望找到一个合适的PEI与pDNAs的比例,使之形成整体带负电荷的复合物,从而避免与ECM中带负电荷分子的相互作用,同时,降低PEI用量也可以减轻甚至避免局部炎症反应等,这些都可能有利于目的基因向肌肉细胞中的传递和表达。本实验结果证实,只有L/P/D-0.5组可以明显提升外源基因表达水平,并能在监测时间范围内维持高水平表达,当N/P增加,L/P/D介导的基因表达急剧下降,甚至低于阳性对照组1。同时,无论是肌肉原位注射还是尾静脉注射,L/P/D-0.5均表现出很好的生物相容性,能够安全适用于骨骼肌基因传递以增强外源基因的表达水平,而提高N/P肌肉组织会有不同程度的病理变化,特别是高N/P时(N/P=10)。上述基因表达水平和生物安全性的数据与预期结果一致,证明在特定的低比例条件下,PEI/pDNA复合物的电负性特征的确有助于构建高效安全的骨骼肌原位基因传递/表达体系。值得一提的是,这个比例在体外基因转染实验中完全无效,体外转染细胞时,N/P在10~15为最佳转染条件。这也表明了体内外基因传递所需条件截然不同,这可能与体内外细胞所处环境不同有关。
由于PEI完全压缩DNA时的N/P为3(Dai et al., 2011;Dai & Wu,2012),因此,N/P为0.5时,复合物中的DNA并不能被完全压缩,但少量PEI的加入已使DNA的结构变得相对紧密,形成了具有一定三维形态且带负电荷的纳米复合物。虽然由2种检测手段检测出的复合物粒径有所差异,其误差可能是不同的制样条件导致的。AFM图像反映的是干燥后的纳米粒子的三维结构,而DLS则需要纳米粒子在溶液状态时测定(Li et al., 2001)。我们推测,在L/P/D-0.5体系中,PEI/pDNA复合物的电负性特征使其免于被滞留于ECM中,有利于其向细胞内的传递;两亲性Pluronic L64分子利用其与细胞膜的相似性而扰动并提高细胞膜的通透性(Chen et al., 2015),为复合物分子进入细胞创造了有利条件;PEI压缩pDNA形成了结构较为紧密的复合物分子,更有利于其穿过通透性增高的细胞膜,并抵御了核酸酶的降解。这些条件使L/P/D-0.5体系的传递和表达效率超过了质粒和单纯Pluronic L64介导的体系,达到了一个新的高度。
本研究以BALB/c小鼠为模型,验证了一个重要概念:将pDNA压缩成带负电荷的纳米复合物粒子,能够应用于并提高Pluronic L64介导的骨骼肌原位基因传递和表达水平。这一概念的验证,为如何促进DNA/材料复合物分子进入骨骼肌细胞提供了一个解决之道,对构建更加高效的原位基因传递/表达体系将产生推动作用,由此可以设计更合适的材料分子压缩DNA,进一步提高外源基因表达水平,甚至可能将该体系推进到应用水平。事实上,在本项研究中,一次性肌注后,红色荧光蛋白在小鼠骨骼肌细胞中持续稳定的高表达,已经展示了该体系对一些长期、慢性病变的应用前景。
| Astafieva I, Maksimova I, Lukanidin E, et al. 1996. Enhancement of the polycation-mediated DNA uptake and cell transfection with Pluronic P85 block copolymer[J]. Febs Letters, 389(3): 278–280. DOI:10.1016/0014-5793(96)00607-2 |
| Burke RS, Pun SH. 2008. Extracellular barriers to in vivo PEI and PEGylated PEI polyplex-mediated gene delivery to the liver[J]. Bioconjugate Chemistry, 19(3): 693–704. DOI:10.1021/bc700388u |
| Chen J, Luo J, Zhao Y, et al. 2015. Increase in transgene expression by pluronic L64-mediated endosomal/lysosomal escape through its membrane-disturbing action[J]. ACS Applied Materials & Interfaces, 7(13): 7282–7293. |
| Dai Z, Gjetting T, Mattebjerg MA, et al. 2011. Elucidating the interplay between DNA-condensing and free polycations in gene transfection through a mechanistic study of linear and branched PEI[J]. Biomaterials, 32(33): 8626–8634. DOI:10.1016/j.biomaterials.2011.07.044 |
| Dai Z, Wu C. 2012. How does DNA complex with polyethylenimine with different chain lengths and topologies in their aqueous solution mixtures?[J]. Macromolecules, 45(10): 4346–4353. DOI:10.1021/ma2027963 |
| Dishart KL, Denby L, George SJ, et al. 2003. Third-generation lentivirus vectors efficiently transduce and phenotypically modify vascular cells: implications for gene therapy[J]. Journal of Molecular & Cellular Cardiology, 35(7): 739–748. |
| Feldman LJ, Pastore CJ, Aubailly N, et al. 1997. Improved efficiency of arterial gene transfer by use of poloxamer 407 as a vehicle for adenoviral vectors[J]. Gene Therapy, 4(3): 189–198. DOI:10.1038/sj.gt.3300382 |
| Gebhart CL, Sriadibhatla S, Vinogradov S, et al. 2002. Design and formulation of polyplexes based on pluronic-polyethyleneimine conjugates for gene transfer[J]. Bioconjugate Chemistry, 13(5): 937–944. DOI:10.1021/bc025504w |
| Godbey WT, Wu KK, Mikos AG. 1999. Size matters: molecular weight affects the efficiency of poly(ethylenimine) as a gene delivery vehicle[J]. Journal of Biomedical Materials Research, 45(3): 268–275. DOI:10.1002/(ISSN)1097-4636 |
| Guérin N. 2000. A combination of poloxamers increases gene expression of plasmid DNA in skeletal muscle[J]. Gene Therapy, 7(11): 986–991. DOI:10.1038/sj.gt.3301189 |
| He Y, Cheng G, Xie L, et al. 2013. Polyethyleneimine/DNA polyplexes with reduction-sensitive hyaluronic acid derivatives shielding for targeted gene delivery[J]. Biomaterials, 34(4): 1235–1245. |
| Jeon E, Kim HD, Kim JS. 2003. Pluronic-grafted poly-(L)-lysine as a new synthetic gene carrier[J]. Journal of Biomedical Materials Research Part A, 66A(4): 854–859. DOI:10.1002/(ISSN)1097-4636 |
| Lauritzen HP, Reynet C, Schjerling P, et al. 2002. Gene gun bombardment-mediated expression and translocation of EGFP-tagged GLUT4 in skeletal muscle fibres in vivo[J]. Pflugers Arch, 444(6): 710–721. DOI:10.1007/s00424-002-0862-5 |
| Lee JL, Lo CW, Ka SM, et al. 2012. Prolonging the expression duration of ultrasound-mediated gene transfection using PEI nanoparticles[J]. Journal of Controlled Release, 160(1): 64–71. DOI:10.1016/j.jconrel.2012.03.007 |
| Li J, Qin D, James RB Jr., et al. 2001. The characterization of high generation poly (amidoamine) G9 dendrimers by atomic force microscopy (AFM)[J]. Macromolecular Symposia, 167(1): 257–269. DOI:10.1002/1521-3900(200103)167:1<257::AID-MASY257>3.0.CO;2-I |
| Liu S, Ma L, Tan R, et al. 2014. Safe and efficient local gene delivery into skeletal muscle via a combination of Pluronic L64 and modified electrotransfer[J]. Gene Therapy, 21(6): 558–565. DOI:10.1038/gt.2014.27 |
| Lu QL, Bougharios G, Partridge TA. 2003a. Non-viral gene delivery in skeletal muscle: a protein factory[J]. Gene Therapy, 10(2): 131–142. DOI:10.1038/sj.gt.3301874 |
| Lu QL, Liang HD, Partridge T, et al. 2003b. Microbubble ultrasound improves the efficiency of gene transduction in skeletal muscle in vivo with reduced tissue damage[J]. Gene Therapy, 10(5): 396–405. DOI:10.1038/sj.gt.3301913 |
| Mir LM, Bureau MF, Rangara R, et al. 1998. Long-term, high level in vivo gene expression after electric pulse-mediated gene transfer into skeletal muscle[J]. Comptes Rendus De Lacadémie Des Sciences Série Ⅲ Sciences De La Vie, 321(11): 893–899. |
| Pitard B, Belloroufaï M, Lambert O, et al. 2004. Negatively charged self-assembling DNA/poloxamine nanospheres for in vivo gene transfer[J]. Nucleic Acids Research, 32(20): e159. DOI:10.1093/nar/gnh153 |
| Pitard B, Pollard H, Agbulut O, et al. 2002. A nonionic amphiphile agent promotes gene delivery in vivo to skeletaland cardiac muscles[J]. Human Gene Therapy, 13(14): 1767–1775. DOI:10.1089/104303402760293592 |
| Pu L, Geng Y, Liu S, et al. 2014. Electroneutralized amphiphilic triblock copolymer with a peptide dendron for efficient muscular gene delivery[J]. ACS Applied Materials & Interfaces, 6(17): 15344–15351. |
| Ruponen M, Yläherttuala S, Urtti A. 1999. Interactions of polymeric and liposomal gene delivery systems with extracellular glycosaminoglycans: physicochemical and transfection studies[J]. Biochimica et Biophysica Acta, 1415(2): 331–341. DOI:10.1016/S0005-2736(98)00199-0 |
| Schmidtwolf GD, Schmidtwolf IG. 2003. Non-viral and hybrid vectors in human gene therapy: an update[J]. Trends in Molecular Medicine, 9(2): 67–72. DOI:10.1016/S1471-4914(03)00005-4 |
| Song H, Liu S, Li C, et al. 2013. Pluronic® L64-mediated stable HIF-1α expression in muscle for therapeutic angiogenesis in mouse hindlimb ischemia[J]. International Journal of Nanomedicine, 9(1): 3439–3452. |
| Tros dIC, Sun Y, Düzgünesş N. 2010. Gene delivery by lipoplexes and polyplexes[J]. European Journal of Pharmaceutical Sciences, 40(3): 159–170. DOI:10.1016/j.ejps.2010.03.019 |
| Wells DJ. 2004. Gene therapy progress and prospects: electroporation and other physical methods[J]. Gene Therapy, 11(18): 1363–1369. DOI:10.1038/sj.gt.3302337 |
| Xu P, Quick G, Yeo Y. 2009. Gene delivery through the use of a hyaluronate-associated intracellularly degradable cross-linked polyethyleneimine[J]. Biomaterials, 30(29): 5834–5843. DOI:10.1016/j.biomaterials.2009.07.012 |
 2018, Vol. 37
2018, Vol. 37




