扩展功能
文章信息
- 蒋平, 吴丽华, 廖信军, 龙婉婉, 王安萍, 郭聪
- JIANG Ping, WU Lihua, LIAO Xinjun, LONG Wanwan, WANG Anping, GUO Cong
- 横纹金蛛卵袋丝的力学行为与生物学功能之间的关系
- Relationship Between Tensile Behaviors and Biological Function of Egg-Case Silks of Argiope bruennichi
- 四川动物, 2018, 37(5): 556-562
- Sichuan Journal of Zoology, 2018, 37(5): 556-562
- 10.11984/j.issn.1000-7083.20170136
-
文章历史
- 收稿日期: 2017-04-25
- 接受日期: 2018-05-25
2. 井冈山大学商学院, 江西吉安 343009;
3. 四川大学生命科学学院, 生物资源与生态环境教育部重点实验室, 成都 610065
2. Business College, Jinggangshan University, Ji'an, Jiangxi Province 343009, China;
3. Key Laboratory of Bio-Resources and Eco-Environment of Ministry of Education, College of Life Sciences, Sichuan University, Chengdu 610065, China
蜘蛛丝是蜘蛛4亿年进化的结果(Garwood et al., 2016),其适应进化和生物学功能塑造了特有的物理化学结构和性能(Swanson et al., 2006;Blackledge et al., 2012a, 2012b;Madurga et al., 2016)。蜘蛛丝具有优良的机械性能与特性(Gosline et al., 1986;Vollrath,2000;Kubik,2002),被广泛应用于医药、组织工程材料、新型特种纤维、国防、航天航空、日常生活等领域(Viney,2004;Lefèvre & Auger,2016)。现已发现并命名的蜘蛛有47 297种(World Spider Catalog,2018),它们分布极广,生活史多样,可在几小时内耐受超过30 ℃和70%相对湿度的变化幅度,为适应复杂多变的生态环境,蜘蛛丝纤维在组成、结构、性能与生物学功能等方面均呈现出种间和种内多样性(Blamires et al., 2017)。因此,蜘蛛丝已成为一种研究纤维材料结构、性能与功能之间关系的良好模式纤维(Fang et al., 2016)。为此,在了解横纹金蛛Argiope bruennichi卵袋结构和组成的基础上(蒋平等,2011),采用电子单纤强力仪对其卵袋框丝、卵袋内层丝与卵袋外覆盖层丝被3种不同功能蜘蛛丝的力学行为进行测试,采用电子天平对卵袋丝的生物学功能进行量化,拟探明蜘蛛卵袋丝的力学行为与生物学功能之间的关系。本研究将加深人们对蜘蛛丝的结构、力学行为和性能与生物学功能之间关系的认识和理解。
1 材料与方法 1.1 材料来源及测量56只雌性横纹金蛛均于2016年8月20—26日采自江西井冈山国家级自然保护区。饲养方法与卵袋收集参考蒋平等(2011a, 2011b, 2011c)。选取其中4只,用干净的镊子、刀片和剪刀从完整的卵袋上将黄色的框架丝取下,然后对卵袋进行解剖,并收集不同颜色的卵袋层,用于力学行为测式。采用电子天平(A1204型Mettler Toledo,精确度为0.1 mg)称量卵袋、卵块和蜘蛛的质量。
1.2 力学行为的测试采用LLY-06B型电子单纤强力仪(莱州市电子仪器有限公司),在夹持距20 mm,下降速度10 mm·min-1,温度20 ℃,湿度65%的条件下,对蜘蛛丝进行拉伸测试。其中,卵袋外覆盖层丝被直接剪成宽3 mm、长25~30 mm的样品。通过扫描电镜观察测量与丝样品相邻近的丝可获得丝纤维的最初直径,然后使用等式π(D0/2)2L0=π(D/2)2L,把相对应的负荷-位移曲线转换成应力-应变曲线,获得蛛丝的力学性能参数(Pérez-Rigueiro et al., 2001, 2002;Guinea et al., 2005, 2006;蒋平等, 2010a, 2010b, 2010c, 2011;Jiang et al., 2011, 2014)。在进行拉伸实验前应小心,以免将丝纤维拉伸。
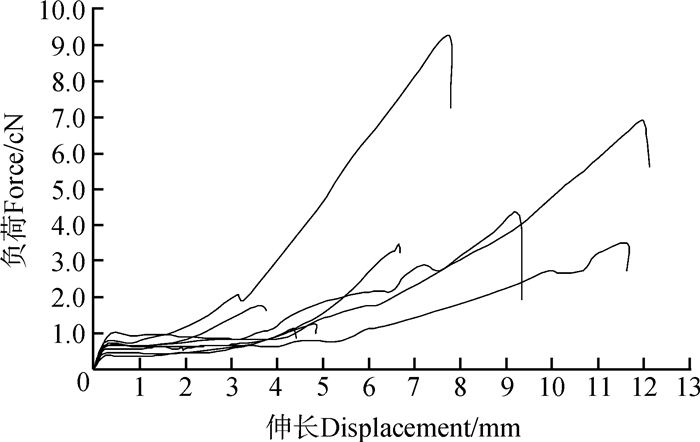
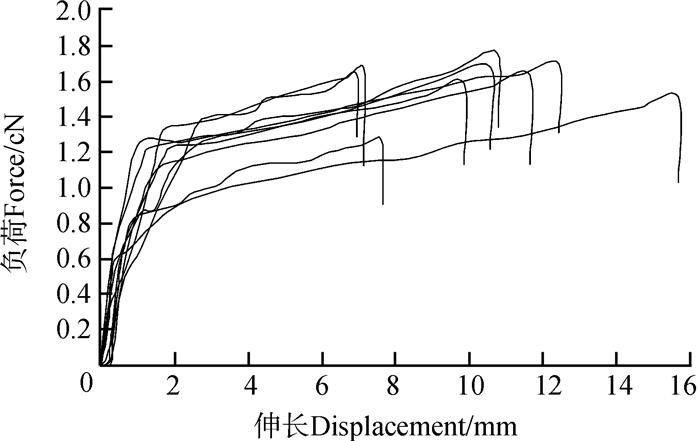
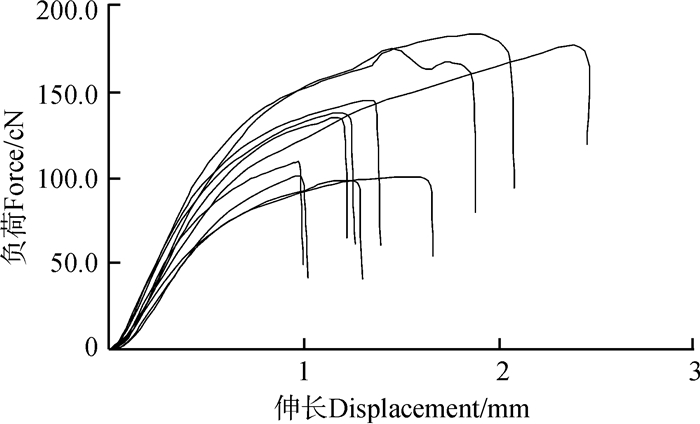
2 结果与分析 2.1 3种卵袋丝的力学行为力学行为测试结果表明,卵袋框丝(图 1)具有与典型蜘蛛拖牵丝相似的力学行为,表现为较复杂的负荷-位移曲线,由初始的弹性区、屈服点、屈服区和上扬的加强区及断裂点组成;卵袋内层丝(图 2)的力学行为与卵袋框丝不同,由初始的弹性区、屈服点或很小的屈服区、较平缓的加强区及断裂点组成,对屈服区投入很小;而卵袋外覆盖层丝被(图 3)的力学行为与卵袋内层丝相似,但曲线表现较为平缓,无明显的屈服点。
|
| 图 1 横纹金蛛卵袋框丝拉伸力学行为 Fig. 1 Tensile behavior of the scaffolding silk from egg-case of Argiope bruennichi |
| |
|
| 图 2 横纹金蛛卵袋内层丝拉伸力学行为 Fig. 2 Tensile behavior of the inner cover silk fiber from egg-case of Argiope bruennichi |
| |
|
| 图 3 横纹金蛛卵袋外覆盖层丝被拉伸力学行为 Fig. 3 Tensile behavior of the outer silk cover from egg-case of Argiope bruennichi |
| |
横纹金蛛卵袋丝负荷-位移曲线的屈服点和断裂点力学性能参数结果表明(表 1),卵袋内层丝的屈服点负荷与伸长及断裂点伸长均比卵袋框丝高,但断裂点负荷比卵袋框丝低。卵袋外覆盖层丝被断裂点伸长为1.60 mm±0.12 mm,断裂点负荷却高达131.00 cN±8.68 cN,并且3种丝样品间的差异均有统计学意义(P<0.05)。这表明横纹金蛛卵袋框丝有较大的断裂点负荷,但是延展性较差,屈服点较低;卵袋内层丝的断裂点负荷较低,但延展性较好,屈服点较高;而卵袋外覆盖层丝被的屈服点和断裂点负荷远远大于卵袋内层丝和卵袋框丝,延展性较差。
| 丝纤维 | 力学性能参数 | |||||||
| 初始模量 /GPa |
屈服点 伸长/mm |
屈服点 伸长率/% |
屈服点 负荷/cN |
断裂点 伸长/mm |
断裂点 伸长率/% |
断裂点 负荷/cN |
断裂强度 /MPa |
|
| 卵袋框丝 | 4.04 | 0.30±0.04 | 1.60±0.15 | 0.50±0.07 | 3.00±0.56 | 37.60±5.73 | 2.60±0.30 | 380.70 |
| 卵袋内层丝 | 3.53 | 1.00±0.12 | 5.20±0.60 | 0.90±0.06 | 9.90±0.52 | 49.60±2.60 | 1.60±0.04 | 464.20 |
| 卵袋外覆盖层丝被 | — | 0.50±0.04 | 2.60±0.22 | 79.80±7.13 | 1.60±0.12 | 8.00±0.61 | 131.00±8.68 | — |
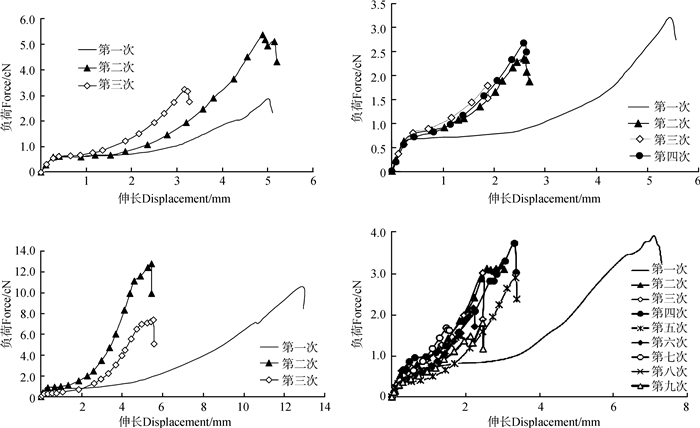
力学行为测试结果表明,卵袋框丝可反复拉伸3~4次,有的可以反复拉伸9次(图 4,表 2)。卵袋框丝在反复拉伸的过程中,经过丝的屈服点后,其加强区发生改变,均比第一次更加上扬,即后面拉伸的加强区力学性能均比第一次好;屈服点先升高后降低,丝纤维第一次拉伸的屈服区均比后面反复拉伸的更明显,投入更多,即在后面拉伸过程中丝纤维发生的分子结构改变比第一次小;断裂点伸长表现为逐渐下降的趋势,但断裂点负荷却在反复拉伸过程中有的增加,有的减小。从反复拉伸9次的个体4可以看到,丝纤维从第二次到第四次拉伸,其屈服点升高,弹性区的投入增加,随后几次的拉伸过程中,屈服点下降,弹性区的投入减小。
|
| 图 4 横纹金蛛卵袋框丝反复拉伸力学行为 Fig. 4 Repeated tensile behavior of the scaffolding silk from egg-case of Argiope bruennichi |
| |
| 蜘蛛个体与拉伸次数 | 力学性能参数 | ||||
| 屈服点伸长/mm | 屈服点负荷/cN | 断裂点伸长/mm | 断裂点负荷/cN | ||
| 个体1 | 第一次 | 0.31 | 0.59 | 5.01 | 2.87 |
| 第二次 | 0.28 | 0.59 | 4.89 | 5.36 | |
| 第三次 | 0.27 | 0.56 | 3.17 | 3.30 | |
| 个体2 | 第一次 | 0.25 | 0.63 | 5.45 | 3.21 |
| 第二次 | 0.43 | 0.79 | 2.62 | 2.33 | |
| 第三次 | 0.41 | 0.79 | 1.86 | 1.78 | |
| 第四次 | 0.44 | 0.72 | 2.59 | 2.67 | |
| 个体3 | 第一次 | 0.28 | 0.95 | 12.90 | 10.57 |
| 第二次 | 0.32 | 0.87 | 5.44 | 12.75 | |
| 第三次 | 0.17 | 0.27 | 5.54 | 7.39 | |
| 个体4 | 第一次 | 0.26 | 0.63 | 7.11 | 3.92 |
| 第二次 | 0.22 | 0.52 | 2.58 | 3.12 | |
| 第三次 | 0.26 | 0.64 | 2.46 | 3.01 | |
| 第四次 | 0.61 | 0.96 | 3.32 | 3.74 | |
| 第五次 | 0.27 | 0.35 | 3.35 | 2.90 | |
| 第六次 | 0.29 | 0.43 | 2.22 | 2.15 | |
| 第七次 | 0.35 | 0.53 | 1.48 | 1.68 | |
| 第八次 | 0.28 | 0.43 | 1.79 | 1.49 | |
| 第九次 | 0.19 | 0.29 | 2.46 | 1.80 | |
横纹金蛛的卵块质量为200~400 mg,即重量为0.2~0.4 cN;雌蛛个体质量为400~1 200 mg,即重量为0.4~1.2 cN。因此,结合表3数据可知,若卵块质量为400 mg(0.4 cN),则将卵袋框丝拉至屈服点(屈服点负荷)所需要的力(0.50 cN±0.07 cN)是卵块重量的1.25倍,将其拉断(断裂点负荷)所需的力(2.60 cN±0.30 cN)是卵块重量的6.5倍;将卵袋内层丝拉至屈服点所需要的力(0.90 cN±0.06 cN)是卵块重量的2.25倍,将其拉断所需要的力(1.60 cN±0.04 cN)是卵块重量的4倍;将卵袋外覆盖层丝被拉至屈服点所需要的力(79.80 cN±7.13 cN)是卵块重量的199倍,将其拉断所需要的力(131.00 cN±8.68 cN)是卵块重量的327.5倍。若蜘蛛体质量为1 200 mg(1.2 cN),则将卵袋框丝拉断所需的力是蜘蛛重量的2.2倍;将卵袋内层丝拉断所需要的力是蜘蛛重量的1.3倍;将卵袋外覆盖层丝被拉至屈服点所需要的力(79.80 cN±7.13 cN)是蜘蛛重量的66.5倍,将其拉断所需要的力(131.00 cN±8.68 cN)是蜘蛛重量的109倍。综上,横纹金蛛卵袋框丝、卵袋内层丝和卵袋外覆盖层丝被的屈服点和断裂点负荷远大于卵块和蜘蛛的重量。
3 讨论 3.1 3种卵袋丝的力学行为蜘蛛丝是一种半结晶的高分子聚合物(Dong et al., 1991)。结晶相主要由An或(GA)n氨基酸基序的β-折叠构成,分子间作用力较大,赋予蜘蛛丝高强度和高模量;非结晶相由富含甘氨酸的(GGX)n或(GPGXX)n或(GPGQQ)n基序的无定型结构和微孔构成(Frische et al., 1998),赋予蜘蛛丝良好的延展性和弹性。
卵袋框丝伸长,其负荷呈线性上升趋势,当拉伸应变至1.6%左右时,出现第二类屈服(杨湧等,2001),曲线呈现出明显的转折,拉伸至屈服点后,负荷趋于平缓或有较小的下降,模量骤降,随后负荷和模量再次升高,出现成颈现象,成颈行为有利于对所受外力(如天敌捕食卵块时)的缓冲,更好地耗散其动能;卵袋内层丝表现为:当拉伸应变至5.2%左右时,出现第二类屈服(杨湧等,2001),拉伸至屈服点后,负荷缓慢增大,然后趋于平缓,模量骤降,无成颈现象,但增加了弹性区的投入,表现出良好的延展性,屈服点高。这一策略与卵袋内层丝较少受到很大外力作用相符,其为卵块和若蛛的发育提供支持和保护的功能(蒋平等, 2010b, 2010c, 2011;Jiang et al., 2011)。卵袋外覆盖层丝被主要由大直径的柱状腺丝与少量的小直径葡萄状腺细丝组成,其力学行为与仅由柱状腺丝构成的卵袋内层丝相似,也与蚕丝和蚕茧丝被力学行为相似(Pérez-Rigueiro et al., 2002;Zhao et al., 2005;Jiang et al., 2006),对屈服区的投入介于前二者之间。但柱状腺丝与蚕丝的氨基酸组成截然不同,其相似的力学行为的分子机制还不清楚,有待进一步深入研究。虽然蚕茧与蜘蛛卵袋都是丝蛋白纤维构成,但二者的生物学功能完全不同。蚕茧是蚕休眠期即蛹期织制的袋形保护层(Danks,2004),而蜘蛛卵袋是蜘蛛生活史早期用于支持和保护卵块和若蛛的类丝茧状物。因此,蜘蛛卵袋丝与蚕茧丝的力学性能投入策略有所不同(蒋平等,2011)。
3.2 卵袋框丝反复拉伸的力学行为根据已有蜘蛛拖牵丝在拉伸过程中蛋白质分子构象变化的研究(Sirichaisi et al., 2000),由于横纹金蛛卵袋框丝第一次拉伸的屈服区比再次拉伸的屈服区长,即有更多的投入,因此,在第一次拉伸过程中发生了更多的α螺旋或者无规则卷曲等向β折叠的构象转变,以便更好适应卵袋框丝高断裂强力的生物学功能要求,为卵袋提供了很好的固定与支持。本研究中,卵袋框丝的反复拉伸次数最高可达9次,第一次拉伸时丝的力学性能并未处于最佳状态,而从第二次开始在一定的拉伸次数内,丝的力学性能趋于稳定,即在一定的拉伸次数内,卵袋框丝随着拉伸次数的增加,其力学性能达到一种最佳状态。这种力学性能被拉伸的频次效应与文献中蛛丝被纺出后随着放置时间的延长,其力学性能有所提高,然后趋于平稳的时间效应一致(Elices et al., 2005),均涉及蛛丝寿命。但大壶状腺丝在蜘蛛的自然生活史中功能发挥的主要表现形式就是被反复拉伸,如在捕食猎物时,由大壶状腺丝组成的网的铆钉丝、框丝和半径丝会随着网面来回被反复拉伸。因此,本研究蜘蛛卵袋框丝的反复拉伸特性是蛛丝为适应其生物学功能长期进化而来,也是其微观生态学进化的反映。这种反复拉伸特性也是蜘蛛丝机械性能策略(蒋平等,2011)的另外一种表现,但还有待进一步深入研究。
3.3 卵袋丝力学行为与蜘蛛生物学功能的关系横纹金蛛卵袋丝的屈服点和断裂点负荷均为卵块重量的数倍,由此可见,雌蛛在后代的保护方面投入巨大。不同丝腺体丝的屈服点和断裂点负荷不同,单根卵袋内层丝就能够承受整个卵块的重量,说明蜘蛛丝的结构与性能是以最佳优化组合来保证卵袋能支持、保护卵块和若蛛,并为若蛛的生长发育提供一个安全的环境。卵袋框丝细丝纤维组成变化大(蒋平等,2011),拉伸力学行为变化也较大,其单丝的拉伸行为重复性很差,这表明蜘蛛能通过改变丝纤维的直径与分子结构来调节丝纤维的力学性能,以适应卵袋所处的异质环境;而卵袋内层丝均为单丝纤维,且直接变化较小,其拉伸行为也表现出良好的重复性,这表明蜘蛛能通过某种机制来精确控制丝纤维的分子结构,使其力学性能具有良好的重复性,适应卵块所处同质稳定的微环境。
研究表明,蜘蛛丝可以通过截然不同的力学性能来实现相同或不同的生物学功能:如,均纺自大壶状腺的蛛网框丝与三维陷阱外面部分的拦截丝,分别以高强度和具有反复拉伸特性与低强度和不具有反复拉伸特性一同来耗散吸收猎物的动能,从而实现捕获猎物的生物学功能(Moore & Tran,1999;Vollrath,2000)。而本研究表明,纺自大壶状腺的卵袋框丝与仅纺自柱状腺的卵袋内层丝和主要纺自柱状腺的卵袋外覆盖层丝被,以较大的屈服区投入、具有反复拉伸特性和较大的力学行为变异性与较大的弹性区投入和力学行为良好的重复性分别完成铆钉卵袋与保护卵块和若蛛的功能。这可为人们进行新型丝纤维材料的仿生设计提供相关理论依据。
| 蒋平, 刘姝, 卓春晖. 2010a. 干燥与拉伸对蜘蛛拖牵丝超收缩性能的影响[J]. 材料科学与工程学报, 28(3): 352–356. |
| 蒋平, 吕太勇, 肖永红, 等. 2010b. 悦目金蛛和棒络新妇卵袋丝物理化学结构表征及其力学性能研究[J]. 生物物理学报, 26(2): 149–163. |
| 蒋平, 吕太勇, 肖永红, 等. 2011a. 横纹金蛛卵袋结构与纤维组成[J]. 动物学杂志, 46(4): 92–101. |
| 蒋平, 吕太勇, 肖永红, 等. 2011b. 三种不同功能蛛丝的超微结构与拉伸力学行为[J]. 材料科学与工程学报, 29(5): 734–741. |
| 蒋平, 乔圆圆, 柯坫华, 等. 2011c. 横纹金蛛多次产卵生物量分配初步研究[J]. 动物学杂志, 46(2): 90–96. |
| 蒋平, 吴梦玲, 肖永红, 等. 2010c. 棒络新妇卵袋丝氨基酸组成及其力学性能[J]. 纺织学报, 31(5): 1–5. |
| 杨湧, 陈新, 周平, 等. 2001. 不同温度下桑蚕丝的力学性能[J]. 高等学校化学学报, 22(9): 1592–1596. DOI:10.3321/j.issn:0251-0790.2001.09.024 |
| Blackledge TA, Kuntner M, Marhabaie M, et al. 2012a. Biomaterial evolution parallels behavioral innovation in the origin of orb-like spider webs[J]. Scientific Reports, 2: 833. DOI:10.1038/srep00833 |
| Blackledge TA, Pérez-Rigueiro J, Plaza GR, et al. 2012b. Sequential origin in the high performance properties of orb spider dragline silk[J]. Scientific Reports, 2: 782. DOI:10.1038/srep00782 |
| Blamires SJ, Blackledge TA, Tso I-Min. 2017. Physicochemical property variation in spider silk:ecology, evolution, and synthetic production[J]. Annual Review of Entomology, 62: 443–460. DOI:10.1146/annurev-ento-031616-035615 |
| Danks HV. 2004. The role of insect cocoons in cold conditions[J]. European Journal of Enotomology, 101: 433–437. DOI:10.14411/eje.2004.062 |
| Dong Z, Lewis RV, Middaugh CR. 1991. Molecular mechanisms of spider silk elasticity[J]. Archives of Biochemistry and Biophysics, 284(2): 53–57. |
| Elices M, Pérez-Rigueiro J, Plaza GR, et al. 2005. Finding inspiration in Argiope trifasciata spider silk fibers[J]. The Journal of The Minerals, Metals & Materials Society, 57(2): 60–66. |
| Fang GQ, Huang YF, Tang YZ, et al. 2016. Insights into silk formation process:correlation of mechanical properties and structural evolution during artificial spinning of silk fibers[J]. ACS Biomaterials Science & Engineering, 2(11): 1992–2000. |
| Frische S, Maunsbach AB, Vollrath F. 1998. Elongate cavities and skin-core structure in Nephila spider silk observed by electron microscopy[J]. Journal of Microscopy, 189(1): 64–70. DOI:10.1046/j.1365-2818.1998.00285.x |
| Garwood RJ, Dunlop JA, Selden PA, et al. 2016. Almost a spider:a 305-million-year-old fossil arachnid and spider origins[J]. Proceedings of the Royal Society B:Biological Science, 283(1827): 1–8. |
| Gosline JM, Demont ME, Denny MW. 1986. The strucure and properties of spider silk[J]. Endeavor, 10(1): 37–43. DOI:10.1016/0160-9327(86)90049-9 |
| Guinea GV, Elices M, Real JI, et al. 2005. Reproducibility of the tensile properties of spider (Argiope trifasciata) silk obtained by forced[J]. Journal of Experimental Zoology, 303(1): 37–44. |
| Guinea GV, Pérez-Rigueiro J, Plaza GR, et al. 2006. Volume constancy during stretching of spider silk[J]. Biomacromolecules, 7(7): 2173–2177. |
| Jiang P, Guo C, Lv TY, et al. 2011. Structure, composition and mechanical properties of the silk fibres of the egg case of the Joro spider, Nephila clavata (Araneae, Nephilidae)[J]. Journal of Biosciences, 36(5): 897–910. |
| Jiang P, Liu HF, Wang CH, et al. 2006. Tensile behavior and morphology of differently degummed silkworm cocoon silk fibres[J]. Materials Letters(60): 919–925. |
| Jiang P, Lv TY, Xiao YH, et al. 2011. Morphology, fibrous composition and tensile properties of drag-silk produced by two species of orb spider[J]. International Journal of Materials Research, 102(10): 1261–1269. |
| Jiang P, Maríbuyé N, Madurga R, et al. 2014. Spider silk gut:development and characterization of a rovel strong spider silk[J]. Scientific Reports, 4: 7326. DOI:10.1038/srep07326 |
| Kubik S. 2002. High-performance fibers from spider silk[J]. Angewandte Chemie International Edition, 41(15): 2721–2723. DOI:10.1002/1521-3773(20020802)41:15<2721::AID-ANIE2721>3.0.CO;2-3 |
| Lefèvre T, Auger M. 2016. Spider silk as a blueprint for greener materials:a review[J]. International Materials Reviews, 6(2): 127–153. |
| Madurga R, Plaza GR, Blackledge TA, et al. 2016. Material properties of evolutionary diverse spider silks described by variation in a single structural parameter[J]. Scientific Reports, 6: 18991. DOI:10.1038/srep18991 |
| Moore AM, Tran K. 1999. Material properties of cobweb silk from the black widow spider Latrodectus hesperus[J]. International Journal of Biological Macromolecules, 24(2-3): 277–282. DOI:10.1016/S0141-8130(98)00090-7 |
| Pérez-Rigueiro J, Elices M, Llorca J, et al. 2001. Tensile properties of Argiope trifasciata drag line silk obtained from the spider's web[J]. Journal of Applied Polymer Science, 82(9): 2245–2251. DOI:10.1002/app.v82:9 |
| Pérez-Rigueiro J, Elices M, Llorca J, et al. 2002. Effect of degumming on the tensile properties of silkworm (Bombyx mori) silk fiber[J]. Journal of Applied Polymer Science, 84(7): 1431–1437. |
| Sirichaisit J, Young RJ, Vollrath F. 2000. Molecular deformation in spider dragline silk subjected to stress[J]. Polymer, 41(3): 1223–1227. DOI:10.1016/S0032-3861(99)00293-1 |
| Swanson BO, Blackledge TA, Hayashi CY, et al. 2006. Spider dragline silk:correlated and mosaic evolution in high-performance biological materials[J]. Evolution, 60(12): 2539–2551. DOI:10.1111/evo.2006.60.issue-12 |
| Viney C. 2004. Self-assembly as a route to fibrous materials:concepts, opportunities and challenges[J]. Current Opinion in Solid State & Materials Science, 8(2): 95–101. |
| Vollrath F. 2000. Strength and structure of spider' silks[J]. Biological Macromolecules, 74(2): 67–83. |
| World Spider Catalog. 2018. World spider catalog, version 19[EB/OL].[2018-01-20]. http://www.wsc.nmbe.ch. |
| Zhao HP, Feng XQ, Yu SW, et al. 2005. Mechanical properties of silkworm cocoons[J]. Polymer, 46(21): 9192–9201. DOI:10.1016/j.polymer.2005.07.004 |
 2018, Vol. 37
2018, Vol. 37




