扩展功能
文章信息
- 王循刚, 王守红, 李玉龙, 张美华, 张梦洁, 刘露莎, 江建平
- WANG Xungang, WANG Shouhong, LI Yulong, ZHANG Meihua, ZHANG Mengjie, LIU Lusha, JIANG Jianping
- 饰纹姬蛙的人工驯养与繁殖
- Reproduction and Artificial Domestication of Microhyla fissipes
- 四川动物, 2018, 37(2): 197-201
- Sichuan Journal of Zoology, 2018, 37(2): 197-201
- 10.11984/j.issn.1000-7083.20170310
-
文章历史
- 收稿日期: 2017-10-12
- 接受日期: 2017-12-26
2. 中国科学院大学, 北京 100049;
3. 南京师范大学生命科学学院, 南京 210046
2. University of Chinese Academy of Sciences, Beijing 100049, China;
3. School of Life Sciences, Nanjing Normal University, Nanjing 210046, China
饰纹姬蛙 Microhyla fissipes 隶属于两栖纲 Amphibia 无尾目 Anura 姬蛙科 Microhylidae 姬蛙属 Microhyla ,分布于东亚及东南亚地区,国内主要分布于华东、华南、华北和西南部分地区,具有种群数量大、个体发育迅速、产卵量多、蝌蚪透明、一年多次产卵且繁殖期长、变态时间短、性成熟较快等特点(费梁等,2009),在胚胎发育、适应性机制、人类疾病及环境健康等方面有重要价值(Liu et al ., 2016)。
目前,有关饰纹姬蛙的研究涉及多方面,耿宝荣等(1996)、刘绍龙等(1996)、徐梦阳和徐剑(2012)以及Wang等(2017)对饰纹姬蛙的胚胎发育过程进行了相关研究;薛清清等(2005)、郭赛男等(2014)采用静态换水法研究了杀虫剂、除草剂及杀菌剂对饰纹姬蛙蝌蚪的急性毒性及联合毒性,并对其进行了安全性评价;韦力等(2013)、魏洁(2016)对饰纹姬蛙求偶鸣声特征和繁殖特征进行了研究;另外,还涉及生物地理学和群体遗传学(Zhang et al ., 2013;Yuan et al ., 2016)、基于转录组学的变态发育和肺发育过程中重要基因调控的研究(Zhao et al ., 2016;Liu et al ., 2017)。这些研究不仅促进了饰纹姬蛙的模式化,也对饰纹姬蛙的人工饲养及人工繁育提出了要求。
本研究对饰纹姬蛙进行实验室饲养驯化,并对其进行人工繁育,分析实验室条件下饰纹姬蛙的繁殖行为和产卵情况等,旨在完善人工繁殖和饲养技术,为研究工作提供适宜的研究材料,也可为无尾两栖动物的人工驯化提供参考。
1 材料与方法 1.1 材料来源188只饰纹姬蛙繁殖亲本于2015年7月—2017年5月分别采自四川省双流区(103.842 8°E,30.582 5°N)、四川省绵阳市(104.192 2°E,31.354 4°N)、四川省乐山市(103.782 7°E,29.453 5°N)和海南省万宁市(110.478 3°E,18.946 7°N) (表 1)。在实验室将雌雄分开以每盒5只饲养在透明饲养盒A(长32 cm×宽22 cm×高15 cm;模拟自然环境:盒中布置苔藓、砂石,加少量水,并标注产地、采集时间等信息;图 1:A)。每天定时投喂残翅果蝇 Drosophila melanogaster ,后期挑选具有优良繁殖性状的雌雄个体进行人工催产。
| 采集时间Date | 采集地点Site | 东经East longitude/° | 北纬North latitude/° | 雌性数量Female number/只 | 雄性数量Male number/只 |
| 2015/7 | 四川双流 | 103.842 8 | 30.582 5 | 8 | 8 |
| 2016/7 | 四川绵阳 | 104.192 2 | 31.354 4 | 4 | 4 |
| 四川双流 | 103.842 8 | 30.582 5 | 24 | 24 | |
| 2016/8 | 四川双流 | 103.842 8 | 30.582 5 | 3 | 3 |
| 海南万宁 | 110.478 3 | 18.946 7 | 30 | 30 | |
| 2017/5 | 四川乐山 | 103.782 7 | 29.453 5 | 25 | 25 |

|
| 图 1 饲养盒 Fig. 1 Breeding containers |
| |
电子秤(0.001 g)、游标卡尺(0.01 mm)、一次性注射器(1 mL)、培养皿(直径12 cm)、塑料吸管(3 mL)、注射用促黄体素释放激素类似物A3(luteinizing hormone releasing hormone,LHRH-A3;宁波市三生药业有限公司)、螺旋藻粉(中盐制盐工程技术研究院)。
1.3 实验方法 1.3.1 雌雄亲本的挑选挑选繁殖体征较好的雌雄亲本,雌性选择腹部较大且软,从腹部能明显看到成熟卵子的个体,其卵粒较大,动植物极明显(动物极黑褐色,植物极乳白色);雄性选择能鸣叫,声囊大且颜色较黑,腹部靠近泄殖腔位置发红且有2条“V”形白线的个体。测量体质量和体长。
1.3.2 人工催产将LHRH-A3用灭菌的0.65%生理盐水配成注射液(3 μg·mL-1),对饰纹姬蛙进行腹腔注射(0.3 μg/g)。将注射后的饰纹姬蛙亲本按雌雄1: 1置于繁殖饲养盒B(长27 cm×宽17 cm×高15 cm;模拟自然环境:盒内用青苔、水草、砂石进行布置,水陆面积比为3: 2;图 1:B),每盒雌雄各1只,并标注编号。繁殖环境气温控制在28 ℃。注射LHRH-A3当晚人工观测繁殖行为,并记录求偶过程和交配时间。为了将人为干扰程度降到最低,使用仿月光夜间灯照明,且避免光照对动物饲养盒的直射。繁殖亲本完成抱对产卵后,结束观察。12 h左右后查看产卵情况,及时将受精卵从繁殖饲养盒B中取出并转入大的白色饲养盒C(长45 cm×宽32 cm×高11 cm;图 1:C)中进行自然孵化。统计产卵总数、受精数、孵化数等,并再次称量产卵后雌雄亲本的体质量以计算繁殖投入。数据均以平均数±标准差表示。
2 实验结果 2.1 繁殖行为对挑选好的饰纹姬蛙雌雄亲本人工注射LHRH-A3催产,3 h后观察记录其繁殖行为,雄蛙会持续不间断鸣叫一段时间,同时面朝雌蛙展示声囊大小,求偶成功后抱对。产卵前,雌蛙会躁动不安,然后跃入水中;产卵时,雌蛙漂浮于水面,将头埋入水中,尾部上翘与雄蛙尾部贴近,抖动,从泄殖腔排出卵粒,反复多次;产卵完毕后,雄蛙和雌蛙分开。通过观察,发现抱对持续时间为7~12 h。
2.2 产卵情况 2.2.1 产卵量与繁殖周期2015年7月—2017年5月,饰纹姬蛙共有98次成功人工催产产卵的记录,包括四川省双流区、四川省乐山市、四川省绵阳市、海南省万宁市4个不同地点的亲本。其中,2015年繁殖成功8次,2016年繁殖成功53次,2017年繁殖成功37次。窝卵数15~1 100枚,平均每只雌蛙单次产卵310枚±203枚(n =98)。其中,海南省万宁市一组亲本(编号:HN001P)于2016年8月13日采回,至2017年5月共成功繁殖产卵5次,产卵日期分别为2016年8月14日、2016年9月29日、2017年3月21日、2017年4月6日和2017年5月5日。在2017年的繁殖实验中发现,饰纹姬蛙同一亲本2次繁殖时间间隔最小可缩短到16 d。
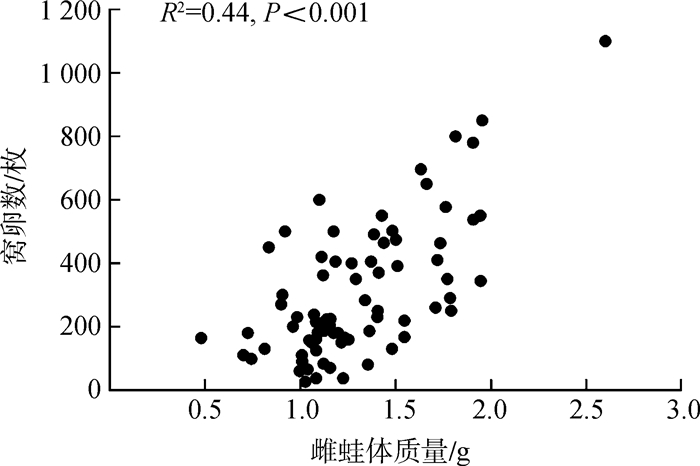
2.2.2 雌雄亲本大小对产卵量的影响共获得76对成功产卵饰纹姬蛙亲本的产卵前体质量、体长测量值。雌蛙体质量1.30 g±0.36 g,体长22.6 mm±1.9 mm;雄蛙体质量1.05 g±0.24 g,体长21.8 mm± 2.1 mm。分析结果发现,76对饰纹姬蛙平均成功产卵309枚±214枚,与雌蛙体质量显著正相关(R2=0.44,P <0.001,n =76;图 2),与雄蛙体质量、雌蛙体长及雄蛙体长均无相关关系。
|
| 图 2 饰纹姬蛙窝卵数与雌蛙体质量的关系 Fig. 2 Relationship between female body mass andthe clutch size of Microhyla fisspes |
| |
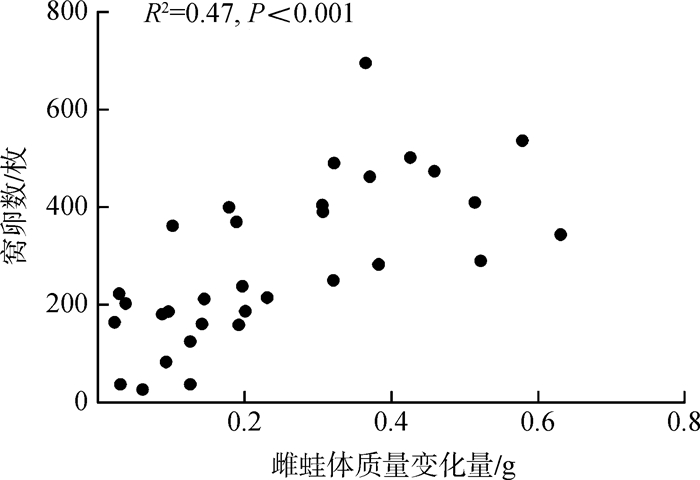
共获得32对繁殖亲本产卵前后体质量的测量值,雌蛙体质量减少量为0.24 g±0.17 g,与产卵量显著正相关(R2=0.47,P <0.001,n =32;图 3)。表明雌蛙繁殖投入与体质量变化显著相关,但产卵量与雄蛙体质量变化无相关关系。
|
| 图 3 饰纹姬蛙窝卵数与雌蛙繁殖投入的关系 Fig. 3 Relationship between female reproductive input andthe clutch size of Microhyla fisspes |
| |
刚孵化的饰纹姬蛙蝌蚪靠体内的卵黄提供营养,待卵黄消失(蝌蚪发育至26期)(Wang et al ., 2017)时以熟鸡蛋黄开口(少量多次投喂)。开口1、2 d后饲喂螺旋藻粉,每天早晚各投喂1次。为保证水体中溶解氧含量高于6 mg·L-1,用充气泵24 h不间断充空气,并且每3 d换1次水。水温控制在26 ℃,光照周期12L: 12D。
2.3.2 幼蛙的饲喂完成变态的幼蛙(发育至45期)一般1~2 d后即可喂食,饵料为棘跳虫 Ony chiuyus fimeitayius linnaeus 和白符跳 Folsomia candida 。按1只幼蛙10~15只的投喂量投喂。每天投喂1次,根据进食情况适当增加或者减少投喂量。随着幼蛙的生长发育,一个月后逐渐过渡到饲喂残翅果蝇。环境温度保持26 ℃,相对湿度保持70%,光照周期12L: 12D。
2.3.3 成蛙的饲喂成蛙主要投喂残翅果蝇,每天投喂1次。按1只成蛙5~10只的投喂量投喂,并观察采食情况。根据成蛙体型进行合理密度的饲养调整。对于成功繁殖后代的雌雄亲本,在饲养盒A中继续饲养,并每隔15 d查看雌雄亲本的身体状况,以便后续人工繁殖。其他饲养环境条件与幼蛙一致。
3 讨论结合野外采集饰纹姬蛙的情况和实验室饲养情况,推测其繁殖期为3—10月,其中5—8月为高峰期。人工繁殖实验发现,同一对饰纹姬蛙亲本在9个月内成功繁殖并产卵5次(平均产卵量为133枚± 64枚),且繁殖间隔可以缩短到16 d。蔡明章等(1991)曾发现一只雌性饰纹姬蛙一年可以产卵6次。因此,饰纹姬蛙具有繁殖期长、繁殖间隔短、多次产卵等优点,为其模式化提供了基础条件。同时也说明,本实验室的饲养条件可以满足饰纹姬蛙的生长和繁殖需求。
早期蛙类的人工繁殖(蔡明章,1980;陈世濂,张艳璇,1994)是将雄蛙处死以取其睾丸进行人工受精,无法观察其繁殖行为,因此后来选用LHRH-A3、绒毛膜促性腺激素(HCG)等激素类针剂对两栖动物进行人工催产(潘炯华,梁淡茹,1990;刘韬等,2009;唐秀锋等,2016)。在实验过程中发现,对饰纹姬蛙注射LHRH-A3的效果好于HCG。这对今后实验室无尾两栖动物的人工繁殖提供了一定的参考。
此外,雌蛙产卵量与亲本体质量、体长相关性比较结果表明,在整个繁殖过程中,雌蛙的身体指标至关重要,这与其他多数研究结果一致(Kozlowska,1971;Gibbons & Mccarthy,1986;李斌,卢欣,2004)。同时,雌蛙的繁殖投入与产卵量也呈显著正相关关系,即雌蛙经历一次繁殖,产卵量越多,体质量减少越多。因此,在进行蛙类人工繁殖时,应该选择体型较大、繁殖性状较好的雌性个体进行催产,以便获取更多更好的实验材料;为了后续多次优质产卵,促进体况尽早恢复至关重要。
本研究中,在蝌蚪早期饵料选择时,首先用鱼饵料和蛋黄一天2次交替饲喂,但无论是蛋黄还是饲料都很容易破坏水质,需要勤换水,不仅给蝌蚪造成不良应激反应,同时加大工作量。后期又尝试饲喂丰年虾,效果有了一定改善。通过不断地实验探索,发现以螺旋藻粉饲喂饰纹姬蛙蝌蚪效果最好,更符合其自然取食的种类和环境。螺旋藻粉既不容易坏水,蝌蚪也比较喜食,生长状况较好。变态后幼蛙和成蛙的饲养相对蝌蚪容易,模拟野外取食习性,幼蛙投喂跳虫,亚成体及成蛙投喂残翅果蝇。经过近2年的饲养驯化,不论是蝌蚪、幼蛙还是成蛙,都已经对固定的饵料投喂有了很好的适应性,并且建立了饵料饲养体系,即“熟蛋黄-螺旋藻粉(饲喂蝌蚪)-跳虫(饲喂刚变态的幼蛙)-残翅果蝇(饲喂亚成体和成体蛙)”,为成功进行实验室人工驯养繁殖饰纹姬蛙提供了基础保障。
致谢: 杨登为、曾一唯、常利明同学在饰纹姬蛙野外采集过程中给予了帮助,王燕老师在动物饲养方面提供了指导和帮助,谨此一并衷心感谢。| 蔡明章, 郭刚, 杨明筑, 等. 1991. 饰纹姬蛙Microhyla ornata (Dumeril et Bibron)生殖频次初探[J]. 福建师范大学学报(自然科学版), 7(3): 87–89. |
| 蔡明章. 1980. 蛙类催产和人工授精方法[J]. 动物学杂志, 15(2): 51–52. |
| 陈世濂, 张艳璇. 1994. 几种激素对棘胸蛙人工催产作用研究[J]. 福建省农科院学报, 9(1): 47–50. |
| 费梁, 胡淑琴, 叶昌媛, 等. 2009. 中国动物志两栖纲(中卷)[M]. 北京: 科学出版社: 904-910. |
| 耿宝荣, 温青, 张秋金. 1996. 饰纹姬蛙的早期胚胎发育[J]. 动物学杂志, 31(5): 17–21. |
| 郭赛男, 童美玲, 陈文君, 等. 2014. 烯唑醇·苯醚甲环唑和咪鲜胺锰盐对饰纹姬蛙蝌蚪的急性和联合毒性[J]. 安徽农业科学, 42(27): 9350–9353. DOI:10.3969/j.issn.0517-6611.2014.27.037 |
| 李斌, 卢欣. 2004. 中国林蛙繁殖产量与雌体大小及年龄的关系[J]. 武汉大学学报(理学版), 50(4): 493–496. |
| 刘绍龙, 宋志明, 张家藻, 等. 1996. 饰纹姬蛙早期胚胎发育的研究[J]. 四川大学学报(自然科学版), 33(3): 323–329. |
| 刘韬, 庄志鸿, 杨声强. 2009. 基于生物技术调控棘胸蛙繁殖与养殖的研究[J]. 中国农学通报, 25(7): 26–29. |
| 潘炯华, 梁淡茹. 1990. 虎纹蛙的人工繁殖初报[J]. 四川动物, 9(2): 34–35. |
| 唐秀锋, 刘本祥, 杨家贵, 等. 2016. 大鲵室内培育及人工繁殖技术研究[J]. 南方农业, 10(16): 67–69. |
| 韦力, 邵伟伟, 林植华. 2013. 饰纹姬蛙求偶鸣声特征分析[J]. 动物学研究, 34(1): 14–20. |
| 魏洁. 2016. 同域分布饰纹姬蛙和泽陆蛙的繁殖特征及其蝌蚪反捕食行为[D]. 杭州: 杭州师范大学. |
| 徐梦阳, 徐剑. 2012. 粤北山区饰纹姬蛙胚后发育的初步观察[J]. 四川动物, 31(4): 83–86, 183. |
| 薛清清, 姚丹, 黄泽宇, 等. 2005. 杀虫剂敌敌畏和除草剂丁草胺对饰纹姬蛙蝌蚪的急性毒性实验[J]. 四川动物, 24(2): 209–212. |
| Gibbons MM, Mccarthy TK. 1986. The reproductive output of frogs Rana temporaria (L.) with particular reference to body size and age[J]. Journal of Zoology, 209(4): 579–593. DOI:10.1111/jzo.1986.209.issue-4 |
| Kozlowska M. 1971. Differences in the reproductive biology of mountain and lowland common frogs, Rana temporaria L.[J]. Acta Biologica Cracovie, Seriensia Zoologique, 14: 17–32. |
| Liu LS, Wang SH, Zhao LY, et al. 2017. De novo transcriptome assembly for the lung of the ornamented pygmy frog (Microhyla fissipes)[J]. Genomics Data, 13: 44–45. DOI:10.1016/j.gdata.2017.07.002 |
| Liu LS, Zhao LY, Wang SH, et al. 2016. Research proceedings on amphibian model organisms[J]. Zoological Research, 37(4): 237–245. |
| Wang SH, Zhao LY, Liu LS, et al. 2017. A complete embryonic developmental table of Microhyla fissipes (Amphibia, Anura, Microhylidae)[J]. Asian Herpetological Research, 8(2): 108–117. |
| Yuan ZY, Suwannapooma C, Yan F, et al. 2016. Red River barrier and Pleistocene climatic fluctuations shaped the genetic structure of Microhyla fissipes complex (Anura:Microhylidae) in southern China and Indochina[J]. Current Zoology, 62(6): 531–543. DOI:10.1093/cz/zow042 |
| Zhang J, Wang J, Jiang JP. 2013. Development and characterization of 15 polymorphic microsatellite markers for a highly adaptive and wide-range frog (Microhyla fissipes)[J]. Asian Herpetological Research, 4(3): 202–206. DOI:10.3724/SP.J.1245.2013.00202 |
| Zhao LY, Liu LS, Wang SH, et al. 2016. Transcriptome profiles of metamorphosis in the ornamented pygmy frog Microhyla fissipes clarify the functions of thyroid hormone receptors in metamorphosis[J]. Scientific Reports, 6: 27310. DOI:10.1038/srep27310 |
 2018, Vol. 37
2018, Vol. 37




