扩展功能
文章信息
- 焦盛武, 蒋科毅, 左奥杰, 吴明, 雷光春, 周延
- JIAO Shengwu, JIANG Keyi, ZUO Aojie, WU Ming, LEI Guangchun, ZHOU Yan
- 我国越冬白头鹤觅食行为和食物资源研究
- Foraging Behavior and Food Resources of Wintering Grus monacha in China
- 四川动物, 2017, 36(4): 392-397
- Sichuan Journal of Zoology, 2017, 36(4): 392-397
- 10.11984/j.issn.1000-7083.20160296
-
文章历史
- 收稿日期: 2016-10-28
- 接受日期: 2017-05-10
2. 北京林业大学自然保护区学院, 北京 100083;
3. 南京林业大学生物与环境学院, 南京 210037
2. School of Nature Conservation, Beijing Forestry University, Beijing 100083, China;
3. College of Biology and the Environment, Nanjing Forestry University, Nanjing 210037, China
在适者生存的自然选择法则下,野生动物采取最有效的方式获取食物,这种高效的觅食策略可以增加物种存活几率以及繁殖成功率(Davies,1977)。MacArthur和Pianka(1966)对动物觅食行为策略进行研究,并提出了最优觅食理论。鸟类对食物的选择不仅取决于从食物中获得的能量,还包括食物的处理时间、遇见率以及取食这种食物被捕食的几率,所以最优食物在食谱中应具有高能量值、易于获取以及安全性等特征(Krebs et al., 1972;Stephens & Charnov,1982)。但是这个理论在学术界也存在争议,许多理论研究和野外观察并没有与其很好的匹配(Pyke et al., 1977;Ollason,1980)。
栖息地质量是栖息地维持物种正常生存的环境能力。在繁殖季节,鸟类在选择栖息地时不仅考虑食物因素,还要为自身和卵/雏鸟的安全寻找庇护所(Martin,1973)。在非繁殖季节,食物是鸟类最重要的限制因素,决定着其时空分布及行为节律(Hutto,1985)。越冬栖息地质量决定了候鸟春迁以及到达繁殖地的身体状态,间接影响候鸟繁殖成功率(Gill et al., 2001)。候鸟在越冬期获得的能量主要用于维系自身生理功能运转以及脂肪存储(Nelson et al., 1996)。理论上,候鸟的分布与食物资源呈正相关;但当栖息地食物无限制或物种没有达到最大环境容纳量时,这种关系也就不存在(Rotenberry & Wiens,1980)。
白头鹤Grus monacha为国家Ⅰ级重点保护野生动物,IUCN将其列为易危物种(VU)。白头鹤的全球种群估计为11 600只,绝大部分种群越冬于日本出水市,其余越冬于我国长江中下游地区和朝鲜半岛(BirdLife International,2012)。在我国越冬的白头鹤主要取食田间农作物、植物根茎或冬芽等(Zhou,1991;Collar,2001;赵雨云等,2002)。随着湿地萎缩和人为干扰的加剧,白头鹤的栖息生境和食物资源受到限制(敬凯等,2002;Yang et al., 2015)。滩涂围垦和围湖造田使越冬白头鹤自然生境减少,另外水位波动影响白头鹤的食物资源变化和日活动节律,白头鹤更多选择人工生境栖息(张姚等,2014;Zhang et al., 2015)。
湿地是鹤类赖以生存的环境,而湿地景观和生态系统变化影响鹤类的生存和分布。尤其是长江三峡对其下游湖泊水文节律的改变,同时围湖造田、水产养殖也威胁着鹤类栖息生境。本研究通过对白头鹤觅食行为和食物资源的研究和分析,探讨其在我国越冬时期的觅食生境利用方式,为物种及其栖息地保护和管理提供基础资料。
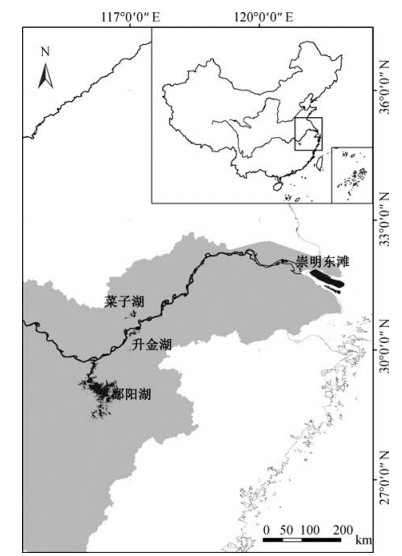
1 研究地概况我国越冬白头鹤主要分布在长江中下游地区的湖泊和沿海滩涂。人为活动加剧导致适宜栖息地锐减,白头鹤的分布也趋于集中。目前主要集中在江西的鄱阳湖保护区,安徽的升金湖保护区、菜子湖湿地公园和上海的崇明东滩保护区(图 1)。本研究选取升金湖、鄱阳湖和崇明东滩国家级自然保护区作为研究地。升金湖国家级自然保护区位于116°55′~ 117°15′E,30°15′~30°30′N,地处安徽南部池州市境内,濒临长江,主要保护对象为湿地生态环境及越冬水禽。鄱阳湖位于115°47′~116°45′E,28°22′~29°45′N,地处江西省北部、长江中下游南岸。鄱阳湖迄今仍然保持着通江、浅水和草型湖泊的自然特征和生态功能。鄱阳湖湿地显著的水位自然涨落给水生植物提供了稳定合理的生存空间,同时也为动物提供了丰富的食物资源,最终成就了鄱阳湖极其丰富的生物多样性。崇明东滩鸟类国家级自然保护区位于长江入海口,崇明岛的最东端,是由长江径流夹带的巨量泥沙在江海的相互作用下沉积而成,地理坐标121°50′~122°05′E,31°25′~31°38′N,是长江口规模最大、发育最完善的河口型潮汐滩涂湿地,其南北狭,东西宽,区内潮沟密布,高、中、低潮滩分带十分明显,是亚太地区迁徙水鸟的重要通道。
|
| 图 1 越冬白头鹤在我国长江中下游地区觅食生境和觅食策略的研究地 Fig. 1 The study area of foraging habitat and strategy for wintering Grus monacha at the middle and lower reaches of the Yangtze River, China |
| |
目前,白头鹤在我国越冬的种群数量估计为1 000~1 500只(Wetlands International,2012)。通过近年的野外调查和整理1981年以来的观测及文献数据,发现白头鹤在一些地区的种群数量存在显著下降的趋势,例如湖北龙感湖和湖南东洞庭湖保护区(胡鸿兴等,2005)。白头鹤在长江中下游地区是常见的越冬候鸟,本文选择的研究地包含了我国越冬白头鹤的大部分种群。
2 研究方法 2.1 行为观察白头鹤每年10月底至11月初迁徙到我国长江中下游的越冬地,并于次年3月底或4月初离开。行为观察时间为2013年11月至2014年3月。升金湖的稻田和草洲、鄱阳湖的草洲以及崇明东滩的蚕豆地被选作行为观察的生境。考虑到种群数量可能对行为造成的影响,观察的白头鹤种群在30~50只,每种生境在2周内完成观察。
根据鹤类觅食高峰期,所有的观察样本集中在07: 00—09: 00和16: 00—18: 00采集。观察方法为目标物种取样法,以10 min为单位,随机选取种群中的个体进行观察。如果观察样本的时间低于10 min,则视为无效。为了消除影响,本文不采集幼鹤样本。首先利用双筒望远镜(OLYMPUS 8×25 WP I)寻找到白头鹤种群,然后用数码摄像机(SONY HDR-PJ820E)记录白头鹤的行为;对于距离较远的种群,采用单筒望远镜(SWAROVSKI STS 80) 目视观察并将其行为记录在表格上,最后进行数字化整理。
鉴于本文的研究目的,将白头鹤行为分为觅食、警戒和其他(包括休息、理羽、移动、飞行等)。觅食行为主要描述为白头鹤低头探寻、挖掘以及搜寻食物;警戒行为被定义为白头鹤突然伸长脖子并以此姿势保持至少5 s;除此之外的行为归类其他。同时记录白头鹤在1 min内警戒的次数以了解白头鹤在面临不同干扰情况下警戒频次的差异。
2.2 食物资源及营养测试根据文献资料、实地食物资源调查和行为观察,白头鹤在越冬期以植食性食物为主,但在不同越冬地的食物不尽相同。本研究选择白头鹤的主要食物包括升金湖草洲生境中蓼子草Polygonum criopolitanum的根和水稻田遗落的稻谷、鄱阳湖草洲中下江委陵菜Potentilla limprichtii的根以及崇明东滩蚕豆地的蚕豆。在白头鹤的觅食生境中随机选择长50 cm×宽50 cm×深10 cm的样方(捡拾稻田生境50 cm×50 cm里遗落的稻谷),挖取样方内的食源植物。将采集的食物样品清洗干净、称量(记录数量)。
为了解白头鹤食物的主要营养成分,将采集的稻谷、蚕豆、蓼子草根和下江委陵菜根送公司测试。测试指标有:能量、粗蛋白、粗脂肪、粗纤维、水分,测试方法详见表 1。
| 能量 | 粗蛋白 | 粗脂肪 | 粗纤维 | 水分 | |
| 方法 | 氧氮热值测定法 | 凯氏定氮法 | 索氏抽提法 (国标GBT6433-2006) |
Weende法 | 物理水分蒸发 |
| 仪器 | 氧氮仪测试仪 (PARR6300) |
凯氏定氮仪 (FOSS8400) |
索氏抽提器 | 纤维素测定仪 (FIWE3/6) |
恒温烘干箱 (上海精宏) |
本研究采用单因素方差分析(One-Way ANOVA)处理越冬白头鹤在不同觅食生境之间的觅食和警戒行为的差异性,若存在差异,则进行2个独立样本t检验,根据Bonferroni校正,显著性水准将调整为0.008(0.05/6),若不存在差异,显著性水平依然为0.05,并采用非参数检验(two independent samples test)分析白头鹤在不同觅食生境之间的警戒次数。
3 结果 3.1 觅食行为时间分配根据对白头鹤行为观察数据的整理结果,共统计到行为样本1 245只次,其中草洲-升金湖284只次、草洲-鄱阳湖224只次、稻田-升金湖469只次和蚕豆地-崇明268只次。
根据越冬白头鹤觅食行为的Bonferroni校正结果(P<0.01,表 3),其差异显著性水平调整为0.008(0.05/6)。t检验结果表明,白头鹤在稻田和蚕豆地的觅食行为时间比例非常高(0.904±0.013,0.805±0.016,表 2),其余的行为时间比例较少,越冬白头鹤在升金湖稻田生境与升金湖草洲、鄱阳湖草洲生境差异有统计学意义,崇明蚕豆地生境与鄱阳湖草洲生境差异有统计学意义(P<0.008,表 4)。选择升金湖草洲生境的白头鹤花费少数时间觅食(0.372±0.083),而鄱阳湖白头鹤在草洲的觅食行为占据超过一半的行为时间(0.554± 0.056)。
| 生境 | 觅食行为 | 警戒行为 | 其他 |
| 草洲-升金湖 | 0.372±0.083 | 0.161±0.017 | 0.467±0.059 |
| 草洲-鄱阳湖 | 0.554±0.056 | 0.113±0.031 | 0.333±0.085 |
| 稻田-升金湖 | 0.904±0.013 | 0.058±0.012 | 0.038±0.014 |
| 蚕豆地-崇明 | 0.805±0.016 | 0.095±0.017 | 0.100±0.010 |
| 离差平方和 | 自由度 | 均方 | F | P值 | |
| 组间 | 5.729 | 3 | 1.910 | 20.156 | <0.01 |
| 组内 | 10.516 | 111 | 0.95 | ||
| 总和 | 16.245 | 114 |
| 生境 | 草洲-升金湖 | 草洲-鄱阳湖 | 稻田-升金湖 | 蚕豆地-崇明 |
| 草洲-升金湖 | — | 0.124 | <0.008 | 0.01 |
| 草洲-鄱阳湖 | — | <0.008 | <0.008 | |
| 稻田-升金湖 | — | 0.718 | ||
| 蚕豆地-崇明 | — |
对越冬白头鹤警戒行为的检验结果显示(P<0.01,表 5),其差异显著性水平调整为0.008(0.05/6)。随后4种生境两两比较的t检验结果表明,白头鹤的警戒行为在整个越冬期的行为谱中占据比率很小,但彼此之间差异无统计学意义(表 6)。白头鹤在升金湖稻田的警戒行为时间低于草洲生境(0.058±0.012,0.161±0.017),但是单位时间内白头鹤在稻田生境的警戒次数比在升金湖草洲生境的多,且差异有高度统计学意义(7.34± 0.48,3.61±0.24,Z=-4.772,P<0.01;表 7)。同样是草洲生境,白头鹤在鄱阳湖的警戒行为时间低于升金湖的警戒行为(0.113±0.031,0.161±0.017),但差异无统计学意义。
| 离差平方和 | 自由度 | 均方 | F | P值 | |
| 组间 | 0.198 | 3 | 0.66 | 5.362 | 0.02 |
| 组内 | 1.364 | 111 | 0.12 | ||
| 总和 | 1.562 | 114 |
| 生境 | 草洲-升金湖 | 草洲-鄱阳湖 | 稻田-升金湖 | 蚕豆地-崇明 |
| 草洲-升金湖 | — | 0.547 | 0.01 | 0.251 |
| 草洲-鄱阳湖 | — | 0.440 | 0.991 | |
| 稻田-升金湖 | — | 0.893 | ||
| 蚕豆地-崇明 | — |
| 生境 | 警戒次数Mean±SE | Z | P |
| 稻田 | 7.34±0.48 | -4.772 | <0.01 |
| 草洲 | 3.61±0.24 |
食物资源采集的样方数分别为:升金湖稻田生境286个、升金湖草洲206个、鄱阳湖草洲214个和崇明蚕豆地183个。通过对稻谷、蚕豆、下江委陵菜根和蓼子草根的营养成分和能量值测试的结果得知(表 8),相较于下江委陵菜和蓼子草的根,单位质量和样方的蚕豆和稻谷能提供更高的能量。作为高能储存物质,脂肪是候鸟冬季保温和能量储备的一个重要指标,其在蚕豆和稻谷中含量最高(7.46%和7.03%)。
| 样品 | 质量/g | 能量/(kJ·g-1) | 粗蛋白/% | 粗脂肪/% | 粗纤维/% | 单位样方能量/kJ |
| 蚕豆 | 4.04±0.33 | 14.41 | 27.95 | 7.46 | 11.82 | 58.216 4 |
| 稻谷 | 2.91±0.27 | 15.06 | 8.42 | 7.03 | 2.52 | 43.824 6 |
| 下江委陵菜根 | 6.05±0.41 | 6.54 | 6.00 | 4.10 | 4.51 | 39.023 0 |
| 蓼子草根 | 7.39±1.07 | 3.84 | 6.08 | 3.29 | 5.67 | 28.377 6 |
鸟类对食物的选择通常由食物特性、种间和种内竞争以及干扰等方面决定。鸟类行为时间预算是其行为模式很好的诠释,也是评价食物资源的重要途径(Marchi et al., 2014)。水鸟越冬时期的行为预算能够推算出栖息地和食物资源的差异,动物花费在觅食上的时间被认为是维持能量平衡的一个重要指标(Uttley et al., 1994)。营养、能量和行为模式之间的关系可以清楚地评价动物的觅食生态学。
4.1 越冬白头鹤觅食行为捕食者总会面临不同食物的选择及其时空变化(Schoener,1971)。越冬期食物是鸟类选择觅食生境和日常行为节律的主要限制因子。为最大程度优化它们的食物选择(最大的净能量输入),鸟类会根据不同的觅食生境改变其行为节律(Wolda,1990)。潮汐波动、食物的埋藏深度与食物的可获得性决定了白头鹤在崇明东滩栖息地的利用和取食行为(敬凯等,2002;Ma et al., 2003)。本研究结果表明,白头鹤在人工生境(蚕豆和稻田)的觅食行为比例不仅高于自然生境,也高于同域自然生境分布的灰鹤G. grus(蒋剑虹等,2015)。在长期的观察中,白头鹤选择人为活动较少的清晨和傍晚在人工生境觅食。虽然主要农田耕作已经结束,但是家鸭养殖、田间小道等偶尔影响白头鹤的觅食,因此白头鹤在人工生境的警戒频次要高于自然生境。对许多草食或者杂食性动物而言,平衡营养摄取也是重要的,因而动物也取食一些频度低的植物种类(张大勇,2000)。虽然人为干扰较少,但它们并没有表现出在人工生境那样高强度的觅食,侧面反映白头鹤在人工生境已经获取足够的能量。鄱阳湖的白头鹤绝大部分时间栖息在草洲生境,它们的觅食行为在一天之内无明显的差异,白头鹤半数的时间花费在觅食上。鸟类如何搜寻和获取食物是评价食物可获得性的一个可替代的测量方法,分析鸟类的觅食行为可以反映食物可获得性(Johnson & Sherry,2001)。从觅食行为角度分析,蚕豆和稻谷是白头鹤易于获取的食物资源。
4.2 越冬白头鹤食物的能量以及可获得性有研究证明净热量摄入是食物选择的重要影响因子,也有人提到鸟类在觅食地停留时间的重要性(Davies,1977)。如果有利的食物丰富且易于获取,则花费在搜寻上的时间就少,所以捕食者会特化这种食物;相反,捕食者会转向取食其他食物;当食物资源匮乏时,捕食者会选择随机性捕食,但会满足适宜度最大化(Pyke et al., 1977)。孙森等(1995)测定了圈养白头鹤在越冬期的营养需要和消化率,发现白头鹤对营养物质成分(干物质、粗蛋白、粗脂肪、粗纤维NEF和能量)都呈现了较高的消化率(除粗纤维77%,其余成分均超过80%)。从食物的营养成分和能量测试结果看,蚕豆和稻谷可以提供高的食物热量以及用于能量储备的脂肪,而且取食难度较小。现代机械收割造成大量的稻谷散落在地上,利于白头鹤捡拾;蚕豆已长出嫩芽且土壤较为湿润,易于白头鹤发现和取食;升金湖蓼子草群落稀疏散落在草洲上,虽然根系埋藏较浅,但是主根被须根缠绕,不宜取食。鄱阳湖的下江委陵菜广布于草洲干燥的土壤,也不易于获取(Jia et al., 2013)。所以就取食难易程度而言,蓼子草和下江委陵菜都不应该是白头鹤首选食物,但是可利用生境以及人为干扰等因素决定它们的食物和生境选择。动物在不同栖息地斑块之间转换和行为差异的理论是基于它们企图调整觅食行为来最大化自身的适宜度,同时也是食物可获得性差异的反映。
4.3 白头鹤的觅食理论与最优觅食理论随着人类对自然生境的开发加剧,野生动物直接暴露在人类干扰之下,这也对它们的生活和生存带来新的挑战(Fernandez-Juricic & Telleria,2000)。对于集群鸟类而言,群体警戒能够降低自身对干扰的能量消耗,并最大限度地获取能量。白头鹤等鸟类越来越多地出现在农田、养殖塘等人类活动较为频繁的生境觅食,鸟类在长期进化中需要通过调整行为来适应这种变化(Harris & Mirande,2013)。白头鹤作为大型涉禽,自然界中基本没有天敌,所以人类活动是它们的主要威胁因子。白头鹤在稻田生境以觅食为主,但警惕性非常高,即使没有人为活动,白头鹤也会时常警觉地观察四周。草洲生境作为白头鹤次要的觅食地,警戒次数并未因为干扰少而减少。理想的觅食生境是不存在的,物种总会受到不同的干扰。为躲避捕食和干扰,觅食者可能在资源较差的地方或捕食效率较低的时间觅食,因而觅食效率显然比理论预测的低(张大勇,2000)。在本研究中,白头鹤倾向于取食能量较高且易于获取的食物,但受制于人为活动的干扰,最优觅食理论受到了限制。
| 胡鸿兴, 康洪莉, 贡国鸿, 等. 2005. 湖北省湿地冬季水鸟多样性研究[J]. 长江流域资源与环境, 14(4): 422–428. |
| 蒋剑虹, 戴年华, 邵明勤, 等. 2015. 鄱阳湖区稻田生境中灰鹤越冬行为的时间分配与觅食行为[J]. 生态学报, 35(2): 270–279. |
| 敬凯, 唐仕敏, 陈家宽, 等. 2002. 崇明东滩白头鹤的越冬生态[J]. 动物学杂志, 37(6): 29–34. |
| 孙森, 叶仁福, 刘国世, 等. 1995. 白头鹤营养需要及消化率的初测[J]. 黑龙江畜牧兽医, 10: 1–5. |
| 张大勇. 2000. 理论生态学研究[M]. 北京: 高等教育出版社. |
| 张姚, 谢汉宾, 曾伟斌, 等. 2014. 崇明东滩人工湿地春季水鸟群落结构及其生境分析[J]. 动物学杂志, 49(4): 490–504. |
| 赵雨云, 马志军, 陈家宽. 2002. 崇明东滩越冬白头鹤食性的研究[J]. 复旦学报(自然科学版), 41(6): 609–613. |
| BirdLife International. 2012. Grus monacha. The IUCN red list of threatened species[EB/OL]. http://www.iucnredlist.org/details/22692151/0. |
| Collar NJ. 2001. Threatened birds of Asia:the birdlife international red data book[M]. Cambridge, UK:Bird Life International. |
| Davies NB. 1977. Prey selection and searching strategies of the spotted flycatcher (Muscicapa striata), a field study on optimal foraging[J]. Animal Behavior, 25: 1016–1033. DOI:10.1016/0003-3472(77)90053-7 |
| Fernandez-Juricic E, Telleria JL. 2000. Effects of human disturbance on spatial and temporal feeding patterns of blackbird Turdus merula in urban parks in Madrid, Spain[J]. Bird Study, 47(Part 1): 13–21. |
| Gill JA, Norris K, Potts PM, et al. 2001. The buffer effect and large-scale population regulation in migratory birds[J]. Nature, 412: 436–438. DOI:10.1038/35086568 |
| Harris J, Mirande C. 2013. A global overview of cranes:status, threats and conservation priorities[J]. Chinese Birds, 4(3): 189–209. DOI:10.5122/cbirds.2013.0025 |
| Hutto RL. 1985. Habitat selection by nonbreeding, migration land birds[M]//Cody ML. Habitat selection in birds. Orlando, Florida:Academic Press Inc:455-476. |
| Jia Y, Jiao S, Zhang Y, et al. 2013. Diet shift and its impact on foraging behavior of siberian cranes (Leucogeranus leucogeranus) in Poyang Lake[J]. PLoS ONE, 8(6): e65843. DOI:10.1371/journal.pone.0065843 |
| Johnson MD, Sherry TW. 2001. Effects of food availability on the distribution of migratory warblers among habitats in Jamaica[J]. Journal of Animal Ecology, 70: 546–560. DOI:10.1046/j.1365-2656.2001.00522.x |
| Krebs JR, Macroberts MH, Cullen JM. 1972. Flocking and feeding in the great tit Parus major an experimental study[J]. Ibis, 114: 507–530. |
| Ma ZJ, Li B, Jing K, et al. 2003. Effects of tidewater on the feeding ecology of hooded crane (Grus monacha) and conservation of their wintering habitats at Chongming Dongtan, China[J]. Ecological Research, 18(3): 321–329. DOI:10.1046/j.1440-1703.2003.00557.x |
| MacArthur RH, Pianka ER. 1966. On the optimal use of a patchy environment[J]. American Nature, 100: 603–609. DOI:10.1086/282454 |
| Marchi GD, Chiozzi G, Dell'Omo G, et al. 2014. Low incubation investment in the burrow-nesting crab plover Dromas ardeola, permits extended foraging on a tidal food resource[J]. Ibis, 157(1): 31–43. |
| Martin TE. 1973. Nest predation and nest sites[J]. Bioscience, 43: 523–532. |
| Nelson JT, Slack DR, Gee GF. 1996. Nutritional value of winter foods for whooping cranes[J]. Wilson Bull, 108(4): 728–739. |
| Ollason JG. 1980. Learning to forage optimally?[J]. Theoretical Population Biology, 18: 44–56. DOI:10.1016/0040-5809(80)90039-8 |
| Pyke GH, Pulliam HR, Charnov EL. 1977. Optimal foraging:a selective review of theory and tests[J]. The Quarterly Review of Biology, 52: 137–154. DOI:10.1086/409852 |
| Rotenberry JT, Wiens JA. 1980. Habitat structure, patchiness, and avian communities in north American steppe vegetation:a multivariate analysis[J]. Ecology, 61: 1228–1250. DOI:10.2307/1936840 |
| Schoener TW. 1971. Theory of feeding strategies[J]. Annual Review of Ecology and Systematics, 11: 369–404. |
| Stephens DW, Charnov EL. 1982. Optimal foraging:some simple stochastic models[J]. Behavioral Ecology and Sociobiology, 10: 251–263. DOI:10.1007/BF00302814 |
| Uttley JD, Walton P, Monaghan P, et al. 1994. The effects of food abundance on breeding performance and adult time budgets of guillemots Uria aalge[J]. Ibis, 136: 205–213. |
| Wetlands International. 2012. Waterbird population estimates, 5th ed[M]. Wageningen, The Netherlands:Wetlands International. |
| Wolda H. 1990. Food availability for an insectivore and how to measure it[J]. Studies in Avian Biology, 13: 38–43. |
| Yang L, Zhou L, Song Y. 2015. The effects of food abundance and disturbance on foraging flock patterns of the wintering hooded crane (Grus monacha)[J]. Avian Research, 6(3): 1–8. |
| Zhang D, Zhou L, Song Y. 2015. Effect of water level fuctuations on temporal-spatial patterns of foraging activities by the wintering hooded crane (Grus monacha)[J]. Avian Research, 6(1): 1–9. DOI:10.1186/s40657-015-0010-5 |
| Zhou HZ. 1991. Winter ecology of the hooded cranes[M]//Hams J. Proc1987 international crane workshop. Baraboo, Wisconsin:International Crane Foundation:101-104. |
 2017, Vol. 36
2017, Vol. 36




