扩展功能
文章信息
- 段宇杰, 赵清, 张仙红, 张虎芳
- DUAN Yujie, ZHAO Qing, ZHANG Xianhong, ZHANG Hufang
- 2种辉蝽的精巢和染色体研究(半翅目:蝽科)
- Study on Testes and Chromosomes of Two Species of Genus Carbula (Hemiptera:Pentatomidae)
- 四川动物, 2016, 35(6): 897-904
- Sichuan Journal of Zoology, 2016, 35(6): 897-904
- 10.11984/j.issn.1000-7083.20160141
-
文章历史
- 收稿日期: 2016-05-26
- 接受日期: 2016-08-29
2. 忻州师范学院, 山西忻州 034000
2. Xinzhou Teachers University, Xinzhou, Shanxi Province 034000, China
蝽科Pentatomidae是异翅亚目Heteroptera最大的类群之一,包括大量的农作物、果树和蔬菜害虫,对农业造成了不可忽视的危害。该科世界性分布,已知8亚科896属4 722种(Kuar & Sharma,2015),我国分布有4个亚科,分别是短喙蝽亚科Phyllocephalinae、益蝽亚科Asopinae、蝽亚科Pentatominae和舌蝽亚科Podopinae。辉蝽属Carbula隶属于蝽亚科,目前全世界有99种,我国记录有10种。
关于蝽类昆虫染色体的研究主要有核型、性别决定机制以及染色体在减数分裂中的行为等,所有种类在细胞遗传学方面具有一些相同的特征,主要表现为:(1)染色体均为全着丝粒染色体,即没有主缢痕,在减数分裂中表现为染色体分离的动力限制在染色体的末端(Lanzone & Souza,2006;Papeschi & Bressa,2006;Souza et al.,2011,2014);(2)常染色体和性染色体减数分裂行为颠倒,在第一次减数分裂时,常染色体进行减数分裂,性染色体进行等价分离,第二次减数分裂时,常染色体进行等价分离,而性染色体进行减数分裂(张虎芳,郑乐怡,1998;Rebagliati et al.,2005;Papeschi & Bressa,2006);(3)减数分裂前期存在一个特殊的时期——弥散期,在这个时期细胞变大,常染色体去固缩呈弥散状态分布在整个细胞核内,而性染色体正异固缩和核仁凝聚在一起,经过这个时期后常染色体再次固缩出现在双线期(Rebagliati et al.,2005;Lanzone & Souza,2006;Souza & Itoyama,2011)。
蝽科昆虫在细胞遗传学方面也具有其自身的特点:无m-染色体(micro-chromosomes)(Rebagliati et al.,2005;Kuar & Sharma,2015);性别决定机制为XY机制,除了Macropygium reticulare (Fabricius)、Thynata calceata (Say)和二星蝽Eysarcoris guttiger (Thunberg)的性别决定机制为X1X2Y及Rhytidolomia senilis (Say)的性别决定机制为Neo-XY(张虎芳,郑乐怡,2001a;Rebagliati et al.,2005;Kuar & Sharma,2015);蝽科昆虫的染色体数目多样化,最小的为2n=6,最大的为2n=27=24A+X1X2Y,但是典型的染色体数目为2n=14,占蝽科昆虫总数的85%(Rebagliati et al.,2001,2005;Souza et al.,2008)。蝽科物种多样性丰富,然而截至目前,有关蝽科昆虫细胞遗传学研究报道的种类不超过400种(Rebagliati et al.,2005;Papeschi & Bressa,2006;Rebagliati & Mola,2010;Kuar & Sharma,2015),不到蝽科昆虫总数的10%。在中国,蝽类昆虫的细胞遗传学自张虎芳于1999年首次研究发表以来,迄今为止报道了4科45种,其中蝽科31种。
精巢作为生殖系统的一部分可以为形态分类和系统发育提供一定的依据,尤其是精巢形态在不同的分类阶元中具有明显的差异。张晓红和张虎芳(2012,2013)、张晓红等(2013)对蝽科14种昆虫和缘蝽总科Coreoidea 9种昆虫的精巢进行了研究,表明精巢在属内种间具有相对稳定性和相似性,在属间和亚科间差异性较大,可以提供较稳定的种属间鉴别特征,具有一定的形态分类价值;而Souza等(2011)通过对蝽科和缘蝽科Coreidae昆虫精巢的研究,发现精巢的外被颜色在科级和亚科级间没有明显差异,其不能作为科级阶元有效的鉴定特征。由于目前蝽类昆虫精巢的研究很少,所以需要更多的资料进一步证实精巢在蝽类昆虫分类中的作用。
辉蝽属全世界共有99种,目前有14种进行过染色体分析,但大部分仅对核型和性别决定机制进行了描述,没有涉及染色体在减数分裂中的行为;同时有关辉蝽属精巢的研究尚未见报道,本文对蝽科辉蝽属的红角辉蝽Carbula crassiventris和北方辉蝽C. putoni精巢形态和染色体进行了研究,以期为蝽类分类学工作提供更多依据。
1 材料与方法 1.1 实验材料本研究所用的材料为雄性个体的精巢(标本详细信息见表 1),残体保存于山西农业大学农学院昆虫实验室。
| 物种 | 采集时间 | 采集地点 | 个体数 |
| 蝽亚科Pentatominae | |||
| 辉蝽属Carbula | |||
| 红角辉蝽C. crassiventris | 2015年8月 | 云南省保山市百花岭 | 3 |
| 北方辉蝽C. putoni | 2015年7月 | 吉林省桦南县七星峰 | 5 |
在野外将采集到的雄性昆虫腹部侧接缘剪开,放入矿泉水中低渗处理20~30 min,如果雄虫个体太小,将整体放入水中低渗处理并且适当延长处理时间,而后将其移入固定液(甲醇: 冰醋酸=3: 1)中10~14 h,期间更换固定液2次,最后放入70%酒精中,4 ℃冰箱保存备用。
1.2.2 精巢的解剖与观察将昆虫放入盛有70%酒精培养皿中,剪掉腹部两侧的侧接缘,掀开背板,露出腹部内组织器官,在LEICA体视显微镜下用镊子轻轻将其他组织器官移去,暴露出完整的精巢,然后观察、拍照。
1.2.3 玻片标本制备采用涂片法,在70%酒精中解剖出精巢,置于新配置的固定液(甲醇: 冰醋酸=3: 1)中1~2 h;取出放在充分冰冻的干净载玻片上,迅速用尖头镊子敲打并夹碎材料,清除结缔组织等,再加1滴固定液,吹散细胞,过火焰干燥,经过2~3 d老化后,用吉姆萨染液染色20~30 min,然后冲洗、晾干,在OlympusBX-51显微镜下观察,记录染色体的数目及行为特点,选取典型的分裂相进行拍摄。
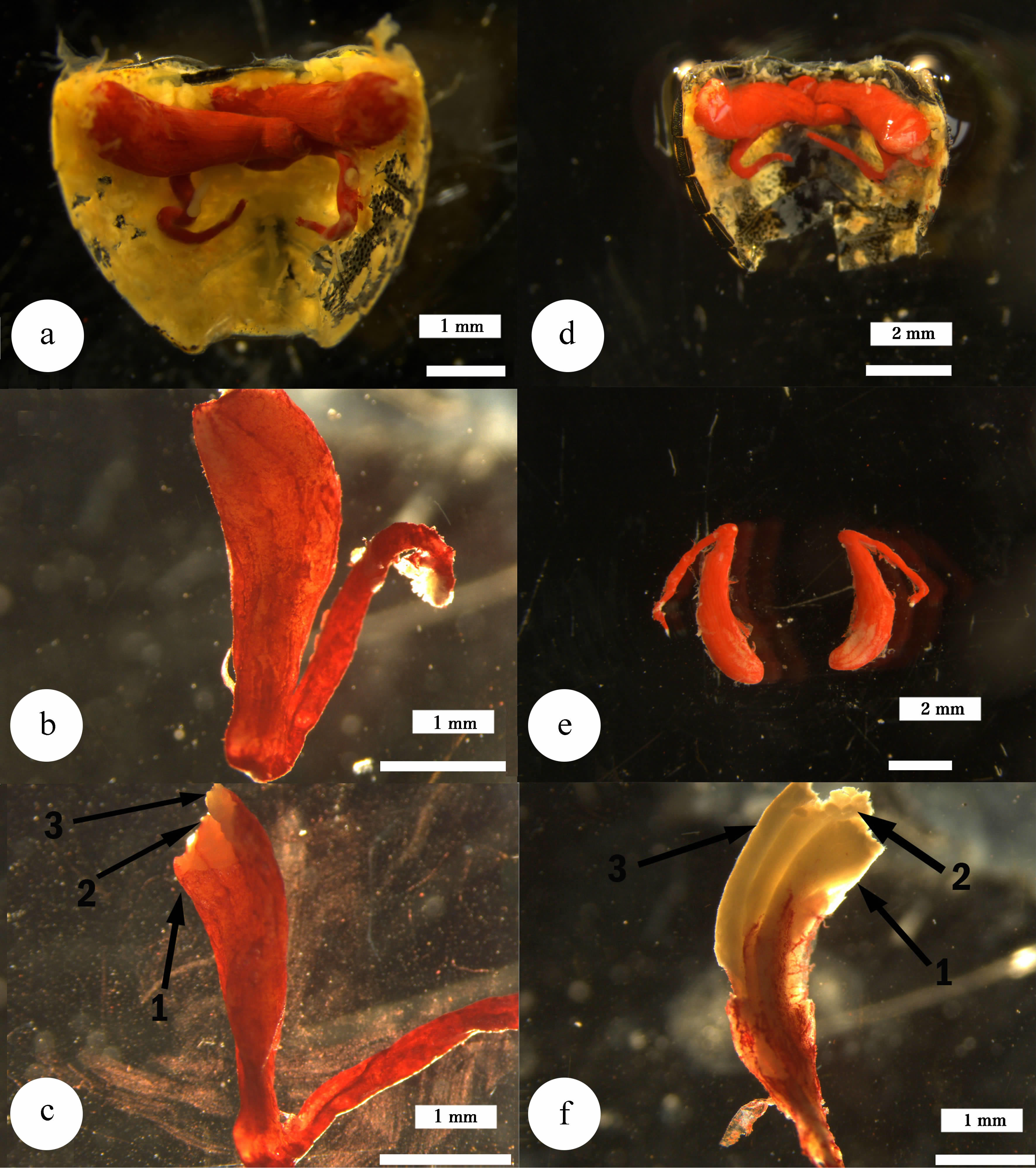
2 结果 2.1 精巢形态 2.1.1 红角辉蝽精巢位于腹部第2~5节的中央两侧,左右精巢近侧区相互接触,整体呈“一”字状对称排列(图版Ⅰ:a)。精巢的外被为鲜红色被膜,中等大小,呈圆棒状(图版Ⅰ:b)。构成精巢的精巢 叶有3个,且精巢叶大小相等、直径相同(图版Ⅰ:c)。 输精管细长,外被同样鲜红色,在腹部中央呈“U”形弯曲(图版Ⅰ:a)。
|
| 图版 Ⅰ 红角辉蝽(a,b,c)和北方辉蝽(d,e,f)的精巢 Plate Ⅰ Testes of Carbula crassiventris (a,b,c)and C. putoni (d,e,f) a,d. 精巢的位置,b,e. 精巢的颜色和形状,c,f. 精巢叶(叶数为3)。 a,d. location of testicles,b,e. color & shape of testicles,c,f. testicular lobes(arrows show three testicular lobes). |
| |
精巢位于腹部第2~5节的中央两侧,左右精巢近侧区相互接触,整体呈接近水平的“八”字状对称排列(图版Ⅰ:d)。精巢的外被为鲜红色被膜,中等大小,呈圆棒状(图版Ⅰ:e)。构成精巢的精巢叶有3个,并且精巢叶大小相等、直径相同(图版Ⅰ:f)。输精管细长,外被同样鲜红色,在腹部中央呈“U”形弯曲(图版Ⅰ:d)。
2.2 染色体减数分裂的行为 2.2.1 红角辉蝽红角辉蝽在第一次减数分裂中期具有8条染色体(图版Ⅱ:7),6条常染色体中1条最大,3条中等大小,1条次之,1条较小;X染色体比最小的常染色体小且略负异固缩,可以区分,Y染色体最小且负异固缩,单倍体染色体组成为n=8(6A+XY),由此可得知该种的双倍体染色体组成为2n(♂)=14(12A+XY)。

|
| 图版 Ⅱ 红角辉蝽染色体的减数分裂 Plate Ⅱ Meiotic characteristics of Carbula crassiventris 1.粗线期,2. 弥散期,3. 双线期,4~7. 终变期,8~10. 中期-Ⅰ,11. 后期-Ⅰ,12. 后期-Ⅱ; 比例尺=10 μm。 1. pachytene,2. diffuse stage,3. diplotene,4~7. diakinesis,8~10. metaphase-Ⅰ,11. anaphase-Ⅰ,12. anaphase-Ⅱ; scale bar=10 μm. |
| |
在前期-Ⅰ的粗线期,X和Y染色体形成正异固 缩的染色质块凝聚在一起,并与核仁融合位于核的一侧,常染色体呈花束状分布在细胞核中(图版Ⅱ:1)。接着出现弥散期,在此期间常染色体去固缩,呈弥散状态分布在细胞核内,而性染色体仍然表现为正异固缩(图版Ⅱ:2)。在双线期,性染色体仍和核仁聚集在一起,二价体联会消失形成四分体,常染色体缩短变粗(图版Ⅱ:3)。在终变早期,常染色体交叉末端化,其中大多数细胞(162/275)有1条常染色体双交叉表现为“0”型,其余常染色体皆为单交叉;
有些细胞(32/275)有2条常染色体双交叉表现为“0”型,其余为单交叉;有些细胞(65/275)有3条常染色体双交叉表现为“0”型,其余常染色体都为单交叉;有个别细胞(16/275)所有的常染色体均表现为单交叉(图版Ⅱ:4~6);在终变后期,核仁完全消失,X和Y染色体分离,而且都转变为负异固缩(图版Ⅱ:7)。在中期-Ⅰ,有些细胞(10/31)X和Y染色体位于常染色体组成的环上而一个常染色体位于环外(图版Ⅱ:8),也有些细胞(12/31)的5条常染色体纵轴平行排列成一个规则的环状,X染色体位于环上而Y染色体和1条常染色位于环外(图版Ⅱ:9),还有些细胞(9/31)X和Y染色体在常染色体组 成的环上(图版Ⅱ:10)。在后期-Ⅰ,常染色体进行减数分裂,同源染色体分离,而性染色体进行等价分裂,姊妹染色单体分离(图版Ⅱ:11)。细胞不经过间期,直接进入第二次减数分裂,常染色体进行等价分离,而性染色体进行减数分裂,最终形成6A+X和6A+Y的2个子细胞(图版Ⅱ:12)。
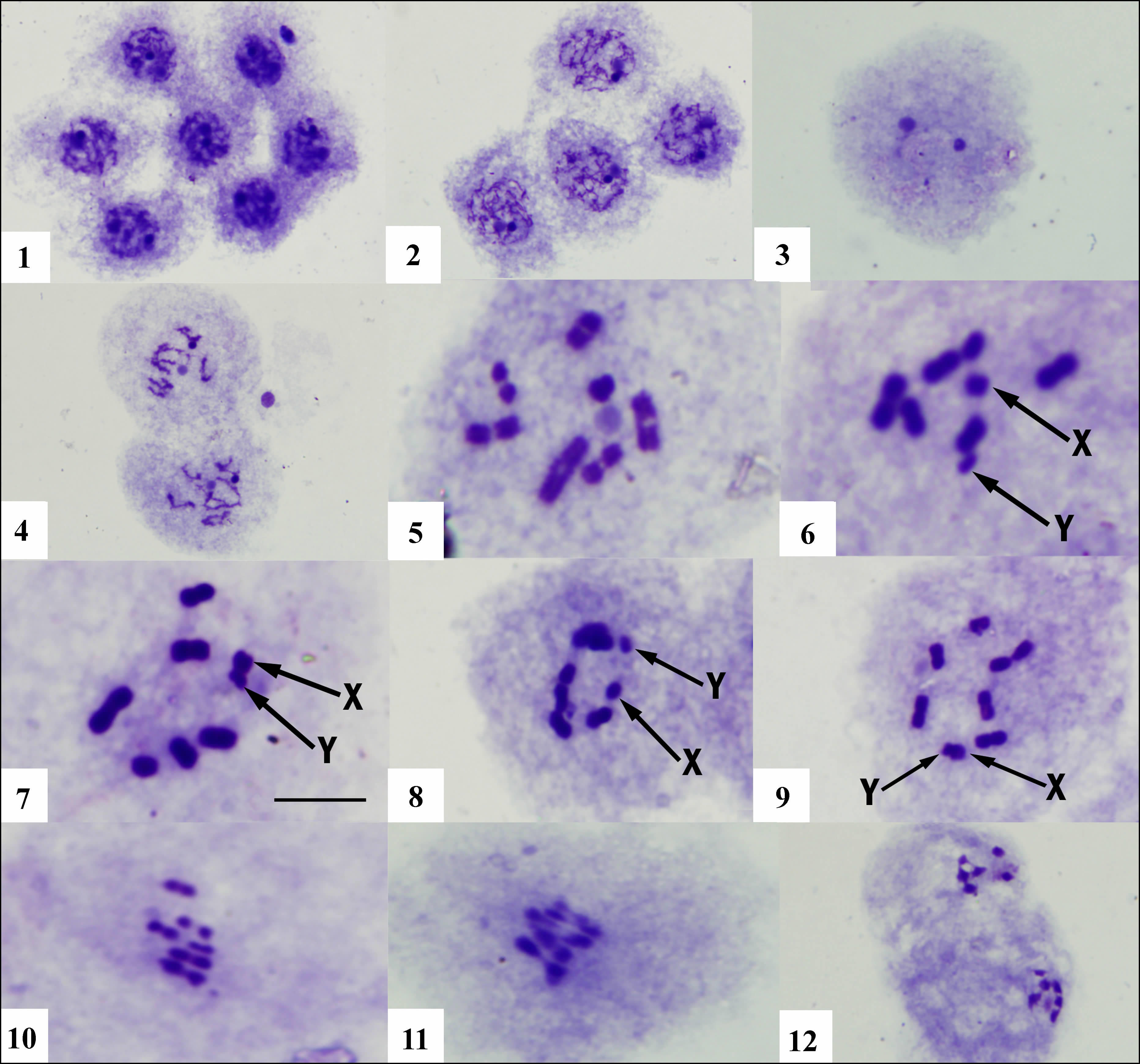
2.2.2 北方辉蝽北方辉蝽在第一次减数分裂中期,共有8条染色体(图版Ⅲ:7),其中常染色体有6条,1条最大,4条中等大小,1条较小;X染色体比最小的常染色体略小且表现等固缩,Y染色体最小,表现负异固缩,极易辨别,由此可知北方辉蝽的单倍染色体组n=8(6A+XY),双倍体染色体组成为2n=14(♂)(12A+XY)。
|
| 图版 Ⅲ 北方辉蝽染色体的减数分裂 Plate Ⅲ Meiotic characteristics of Carbula putoni 1.细线期,2. 粗线期,3. 弥散期,4. 双线期,5,6. 终变期,7~9. 中期-Ⅰ,10. 中期-Ⅱ; 11. 后期-Ⅱ,12. 末期-Ⅱ;比例尺=10 μm。 1. leptotene,2. pachytene,3. diffuse stage,4. diplotene,5,6. diakinesis,7~9. metaphase-Ⅰ,10. metaphase-Ⅱ,11. anaphase-Ⅱ,12. telophase-Ⅱ; scale bar=10 μm. |
| |
在减数分裂前期的细线期,常染色体呈细丝状分布在细胞核内,X和Y性染色体正异固缩和核仁凝聚在一起成圆形小球靠近核膜一侧(图版Ⅲ:1)。在粗线期,常染色体联会配对,明显变粗,核仁和性染色体分离,且核仁染色较浅(图版Ⅲ:2)。在弥散期,常染色体完全去固缩,而性染色体仍然正异固缩分布在细胞核内(图版Ⅲ:3)。在双线期,核仁和性染色体依旧分离,同源染色体联会消失变成四分体(图版Ⅲ:4)。在终变早期,XY性染色体正异固缩并且开始分离,核仁仍染色较浅,常染色体交叉端移,均为单交叉;在晚终变期,XY性染色体完全分离,分离后X染色体呈现为等固缩而Y染色体呈现为负异固缩,核仁消失,每条常染色体清晰可辨(图版Ⅲ:5,6)。在中期-Ⅰ,有些细胞(10/27)的5条常染色体和XY染色体排列成一个不规则的环,1条常染色体位于环外(图版Ⅲ:7);有些细胞(17/27)的常染色体排列成一个不规则的环状,X和Y染色体末端相连位于环上(图版Ⅲ:8,9)。细胞不经过间期,直接进入第二次减数分裂,在第二次减数分裂中期和后期,常染色体进行等价分离而性染色体进行减数分裂(图版Ⅲ:10,11)。在末期-Ⅱ,染色体汇聚在两极,各自排列成一个紧密的环,性染色体位于环中央(图版Ⅲ:12)。
3 讨论目前关于蝽类昆虫精巢的研究主要集中在精巢的位置、外被颜色、形态和精巢叶等。张晓红和张虎芳(2012)通过对蝽科的蝽亚科和舌蝽亚科9属13种昆虫精巢和输精管的研究,认为蝽科昆虫精巢和输精管在属及亚科阶元具有稳定的特征,属内种间具有相似性,而在属间、亚科间变异较大,呈现多样性。对于精巢的位置,本文研究的红角辉蝽和北方辉蝽精巢都位于腹部第2~5节中央两侧;张晓红和张虎芳(2012)描述的二星蝽属Eysarcoris 4个种和珠蝽属Rubiconia 1个种精巢都位于腹部第1~4节两侧,菜蝽属Eurydema 2个种、斑须蝽属Dolycoris 1个种、果蝽属Carpocoris 1个种精巢都位于腹部第2~4节两侧,茶翅蝽属Halyomorpha 1个种精巢位于腹部第2~3节两侧。有关精巢的形态,本研究的辉蝽属2个种精巢形态均为圆棒状;而张晓红和张虎芳(2012)研究的绿蝽属Nezara精巢呈规则的卵圆形,斑须蝽属、二星蝽属精巢为不规则卵圆形,茶翅蝽属为近似卵圆形的三角形,麦蝽属Aelia精巢与菜蝽属相似,都为大型棒状结构。通过比较可以看出,蝽科精巢的位置和形态在属间差异明显,属内比较稳定,证实了精巢在属级有稳定的鉴定特征。但是由于目前关于蝽科昆虫精巢的研究数据较少,所以进一步证明精巢形态和位置的分类价值还需要做大量的实验。
关于精巢外被颜色,本研究所选取的辉蝽属2个种,其精巢外被颜色均为鲜红色,Souza等(2007b,2011)通过对蝽科昆虫精巢的大量观察,发现在蝽科昆虫中,精巢的外被颜色仅有红色和黄色2种颜色,通过与张晓红和张虎芳(2012)描述的蝽科13种昆虫精巢外被颜色进行比较,与Souza等(2011)的观点一致,在蝽科昆虫中精巢外被颜色没有固定的模式,在属间和亚科间并没有明显的差异。Souza等(2007a,2009)也对缘蝽科昆虫的精巢外被颜色进行了分析,发现在缘蝽科中精巢外被颜色也只存在红色、黄色和透明色3种类型。综上所述,精巢的外被颜色在蝽科和缘蝽科中没有明显差异,颜色变化基本一致,但是在所有的蝽类昆虫中是否也表现为单一性还需要大量观察后定论。
蝽类昆虫的精巢都是由紧挨着的精巢叶构成的,而且每个精巢叶的大小几乎一致。Souza等(2007a,2009,2011)通过对精巢叶的观察,发现在缘蝽科和蝽科中,精巢叶的数目为3~7;Grozeva和Kuznetsova(1992)发现在长蝽科Lygaeidae中,精巢叶的数目有2、4、6、7。但是他们的研究都集中在科内精巢叶数目的变化,并没有在属间和亚科间进行比较分析。通过对Souza等(2007b,2011)发表的蝽科各个属精巢叶数目的比较,发现Loxa属3个种的精巢叶数目都是7个,Rhytidolomia属2个种和Euschistus属6个种的精巢叶数目都是6个,Murgantia属2个种的精巢叶数目都是5个,Oebalus属3个种的精巢叶数目都是4个,Edessa属3个种的精巢叶数目都是4个以及Banasa属2个种及本文辉蝽属2个种的精巢叶数目都是3个。因此可以推断出蝽科的精巢叶数目在属内可能比较稳定,在属间有所差别,但是目前关于精巢叶数目的研究报道还很少,所以需要大量的实验去进一步论证。
目前辉蝽属昆虫染色体仅有14个种进行过分析,分别是Carbula socia和Carbulasp.(Manna,1951);辉蝽C. humerigera和C. biguttata (Yosida,1950,1956);C. aspavia (Parshad,1957);棘角辉蝽C. scutellata (Mittal & Leelamma,1981);C. capito、C. carbula、C. limpoponis、C. melacantha和Carbula sp. aff.sjostedti (Nuamah,1982);印度辉蝽C. indica (Dey & Wang,1988);C. putoni 和C. sinica (Zhang & Zheng,2003),其中Nuamah等在1982年之前仅对染色体数目进行报道,但关于染色体在减数分裂中的行为并没有描述;而后Satapathy和Patnaik(1989)对C. bigutatta 和C. socia以及Zhang和Zheng(2002)对北方辉蝽、凹肩辉蝽C. sinica和辉蝽的核型和染色体在减数分裂中的行为都进行了详细的叙述。通过与本文研究的辉蝽属2个种的观察比较,发现在辉蝽属中已报道种类的双倍体染色体组成均为2n(♂)=14(12A+XY),均符合蝽科典型的染色体数目,再次证实了蝽科昆虫在进化过程中核型保守的特点。
已有研究表明,蝽科昆虫不同属间、种间的减数分裂行为不同,而且染色体在减数分裂中的行为具有一定的属、种特异性,常染色体和性染色体在减数分裂中期-Ⅰ的排列方式更是如此,可为昆虫分类提供一定的依据(张虎芳,郑乐怡,2001b)。本研究通过对红角辉蝽和北方辉蝽的比较,进一步验证了这一结论。两者在减数分裂中的行为特异性主要表现在以下几个方面:(1)在异翅亚目昆虫中经常有一个弥散期,存在于粗线期之后、双线期之前,弥散期存在的时间长短以及常染色体在此期间的去固缩程度在不同的种类之间都有一定的差异(Rebagliati & Mola,2010)。在北方辉蝽中观察到典型的弥散期,细胞和核仁变大,常染色体完全去固缩呈点状分布在整个细胞核中,并且弥散期存在的时间比较长;但是在红角辉蝽中观察到的弥散期,常染色体不完全去固缩,可以看到明显的染色丝,同时弥散期存在的时间较短。虽然弥散期的机制还没有了解清楚,但是却被认为是区别减数分裂和有丝分裂的重要特征(Lanzone & Souza,2006;Kuar & Semahagn,2010)。(2)Bressa等(2002)提出在减数分裂前期的细线期-偶线期,X染色体表现为正异固缩,到终变末期时X染色体转变为等固缩,并且在减数分裂前期,性染色体和核仁经常融合在一起。但是在红角辉蝽和北方辉蝽中,性染色体的固缩程度却有其特殊性。红角辉蝽在终变末期,X和Y染色体从正异固缩转变为负异固缩;北方辉蝽在终变末期,X染色体从正异固缩转变为等异固缩,但是Y染色体却转变为负异固缩,并且在粗线期核仁就和性染色体分离直到终变期消失。(3)在异翅亚目昆虫中,每对同源染色体在终变期都存在一个交叉(Satapathy & Patnaik,1988;Lanzone & Souza,2006),本文研究的北方辉蝽中,所有常染色体在终变期均表现为单交叉;但是在红角辉蝽终变期的细胞(约占94.5%)中,至少有1对同源染色体存在双交叉表现为“0”型,而且Rebagilati和Mola(2010)提出常染色体双交叉在蝽科昆虫中是普遍的。(4)在中期-Ⅰ,大多数蝽科昆虫的常染色体排列成一个中空的环而性染色体位于环中央(Rebagliati et al.,2001;Lanzone & Souza,2006),Souza等(2011,2014)也指出在蝽科昆虫中,无论性别决定机制是XY还是XnY,在中期-Ⅰ,性染色体始终排列在常染色体的环中央。但是在本文研究的红角辉蝽和北方辉蝽中,常染色体和性染色体在中期-Ⅰ却表现出不同的排列方式。其中有2种排列方式都存在于红角辉蝽和北方辉蝽中:一种情况是XY性染色体和5条常染色体排列成一个中空的环,1条常染色体位于环外;另一种情况是6条常染色体和XY性染色体共同组成一个规则的环。还有一种情况是红角辉蝽特有的,5条常染色体纵轴平行排列成一个规则的环,X染色体位于环上而Y染色体和1条常染色体位于环外。说明蝽科有些种类的染色体在减数分裂过程中比较活跃,性染色体和常染色体在中期-Ⅰ有多种排列方式,并且具有一定的种间特异性。
| 张虎芳, 郑乐怡. 1998. 半翅目昆虫染色体研究进展[J]. 昆虫知识 , 35(4) : 243–246. |
| 张虎芳, 郑乐怡. 2001a. 五种蝽科昆虫的细胞分类学研究(半翅目:异翅亚目)[J]. 昆虫分类学报 , 23(4) : 265–276. |
| 张虎芳, 郑乐怡. 2001b. 六种蝽象的染色体研究(半翅目:蝽科)[J]. 昆虫学报 , 44(2) : 129–134. |
| 张晓红, 李敏, 张虎芳. 2013. 缘蝽总科4种雄性昆虫减数分裂期染色体形态分析(半翅目:缘蝽总科)[J]. 西北农林科技大学学报(自然科学版) , 41(4) : 169–177. |
| 张晓红, 张虎芳. 2012. 蝽科昆虫精巢形态及其反映的属种间亲缘关系[J]. 动物分类学报 , 37(4) : 712–717. |
| 张晓红, 张虎芳. 2013. 缘蝽总科昆虫精巢形态[J]. 四川动物 , 32(2) : 219–223. |
| Bressa MJ, Fumagalli E, Ituarte S, et al. 2002. Meiotic studies in Dysdercus Guérin Méneville 1831 (Heteroptera:Pyrrhocoridae). Ⅱ. Evidence onvariations of the diffuse stage between wild and laboratory-inbred populations of Dysdercus chaquency Freiberg[J]. Hereditas , 137 : 125–131. DOI:10.1034/j.1601-5223.2002.01650.x |
| Dey SK, Wangdi T. 1988. Chromosome number and sex chromosome system in forty-four species of Heteroptera[J]. Chromosome Information Service , 45 : 5–8. |
| Grozeva S, Kuznetsova VG. 1992. The reproductive system of some bug families (Heteroptera, Pentatomomorpha)[M]. Advances in Regulation of Insect Reproduction:97-102. |
| Kaur H, Semahagn BK. 2010. Meiotic behavior of chromosomes in three predator species of the subfamily Asopinae (Heteroptera:Pentatomidae)[J]. Comparative Cytogenetics , 4(2) : 133–139. DOI:10.3897/compcytogen.v4i2.47 |
| Kaur H, Sharma K. 2015. First report on meiotic behavior of chromosomes in three species of subfamily Pentatominae (Pentatomidae:Heteroptera)[J]. Zootaxa , 3920(2) : 393–400. DOI:10.11646/zootaxa.3920.2 |
| Lanzone C, Souza M. 2006. Chromosome complement and meiosis in three species of the Neotropical bug genus Antiteuchus (Heteroptera:Pentatomidae:Discocephalinae)[J]. Genetics and Molecular Biology , 103 : 239–243. |
| Manna GK. 1951. A study of chromosomes during meiosis in forty-three species of Indian Heteroptera[J]. Proceedings of the Zoological Society of London, Bengal , 4 : 1–116. |
| Mittal OP, Joseph L. 1981. Chromosome number and sex mechanism in twenty eight species of Indian pentatomid bugs[J]. Chromosome Information Service , 30 : 6–7. |
| Nuamah KA. 1982. Karyotypes of some Ghanian shield bugs and the higher systematics of the Pentatomidae (Hemiptera, Heteroptera)[J]. Insect Science Application , 3 : 9–28. |
| Papeschi AG, Bressa MJ. 2006. Evolutionary cytogenetics in Heteroptera[J]. Brazilian Journal of Medical and Biological Research , 5 : 3–21. |
| Parshad R. 1957. Cytological studies in Heteroptera Ⅲ[J]. A comparative study of the chromosomes in the male germ-cell of eleven species of the subfamily Pentatominae[J]. Research Bulletin of Panjab University , 122 : 401–420. |
| Rebagliati PJ, Mola LM, Papeschi AG, et al. 2005. Cytogenetic studies in Pentatomidae (Heteroptera):a review[J]. Journal of Zoological Systematics and Evolutionary Research , 43 : 199–213. DOI:10.1111/jzs.2005.43.issue-3 |
| Rebagliati PJ, Mola LM, Papeschi AG. 2001. Karyotype and meiotic behaviour of the holokinetic chromosomes of six Argentine species of Pentatomidae (Heteroptera)[J]. Caryologia , 54 : 339–347. DOI:10.1080/00087114.2001.10589245 |
| Rebagliati PJ, Mola LM. 2010. Meiotic behavior and karyotype variation in Aclerda (Pentatomidae, Heteroptera)[J]. Genetics and Molecular Research , 9(2) : 739–749. DOI:10.4238/vol9-2gmr763 |
| Satapathy SN, Patnaik SC. 1988. Chromosomal studies in seven species of family Pentatomidae (Heteroptera)[J]. Caryologia , 41(1) : 49–60. DOI:10.1080/00087114.1988.10797847 |
| Souza HV, Arakaki RLM, Dias LN, et al. 2007a. Cytogenetical aspects of testicular cells in economically important species of Coreidae family (Heteroptera)[J]. Cytologia , 72 : 49–56. DOI:10.1508/cytologia.72.49 |
| Souza HV, Bicudo HEMC, Costa LAA, et al. 2007b. A study of meiosis and spermatogenesis in different testicular lobes of Antiteuchus tripterus (Heteroptera:Pentatomidae)[J]. European Journal of Entomology , 104 : 353–362. DOI:10.14411/eje.2007.053 |
| Souza HV, Castanhole MMU, Castanhole HEM, et al. 2008. Morphological patterns of the heteropycnotic chromatin and nucleolar material in meiosis and spermiogenesis of some Pentatomidae (Heteroptera)[J]. Genetics and Molecular Biology , 31 : 686–691. DOI:10.1590/S1415-47572008000400014 |
| Souza HV, Castanhole MMU, Gomes MO, et al. 2014. Meiotic behavior of 18 species from eight families of terrestrial Heteroptera[J]. Journal of Insect Science , 14(149) : 1–8. |
| Souza HV, Itoyama MM. 2011. Comparative analysis of heteropyknotic chromatin and silver-stained material in Platycarenus umbractulatus (Pentatomidae:Discocephalinae)[J]. Journal of Reproduction and Development , 55 : 65–72. |
| Souza HV, Murakami AS, Moura J, et al. 2011. Comparative analysis of the testes and spermatogenesis in species of the family Pentatomidae (Heteroptera)[J]. European Journal of Entomology , 108 : 333–345. DOI:10.14411/eje.2011.041 |
| Souza HV, Souza FB, Maruyama SRC, et al. 2009. Meiosis, spermatogenesis and nucleolar behavior in the seminiferous tubules of Alydidae, Coreidae and Rhopalidae (Heteroptera) species[J]. Genetics and Molecular Research , 8 : 1383–1396. DOI:10.4238/vol8-4gmr672 |
| Yosida TH. 1950. A chromosomal survey in twelve species of the Hemiptera[J]. Coordinate Communication and Research Genetics , 1 : 85–91. |
| Yosida TH. 1956. Studies on the chromosomes of Coleoptera and Hemipteran insects with special regard to quantitative relationship between autosomes and sex chromosomes[M]. Proceedings of 10th International Congress on Entomology, Montreal, 2:979-989. |
| Zhang HF, Zheng LY. 2002. Study on the karyotype of three species of genus Carbula (Heteroptera:Pentatomidae)[J]. Entomologia Sinica , 9(2) : 59–67. |
 2016, Vol. 35
2016, Vol. 35



