扩展功能
文章信息
- 蒋文燕, 何永亮, 杨锋, 钟振东, 万峰, 吴大蓉, 王红星
- JIANG Wenyan, HE Yongliang, YANG Feng, ZHONG Zhendong, WAN Feng, WU Darong, WANG Hongxing
- 益母草注射液小鼠急性毒性和Beagle犬重复给药毒性试验研究
- Acute Toxicity of Leonurus japonicus Injection in Mice and Repeated Toxicity in Beagle Dogs
- 四川动物, 2016, 35(6): 871-878
- Sichuan Journal of Zoology, 2016, 35(6): 871-878
- 10.11984/j.issn.1000-7083.20160206
-
文章历史
- 收稿日期: 2016-08-01
- 接受日期: 2016-09-26
2. 成都第一制药有限公司, 成都 610018
2. Chengdu First Pharmaceutical Co. Ltd., Chengdu 610018, China
益母草Leonurus japonicus Houtt在中医药文献中记载其功效为活血、祛瘀、调经、消水,素有“血脉圣药”“经产良方”之称。益母草注射液(YMC)为唇形科植物益母草的干燥地上部分经水提醇沉等加工制成的纯中药注射剂,曾列为国家基本药物。临床常规用于防治剖宫产、阴道分娩产后出血,人工流产药物流产出血,功能性子宫出血,妇科手术术中、术后出血,经量过多等妇产科疾病的防治。本品的执行标准曾纳入1977版中国药典,后归入《中华人民共和国卫生部药品标准 中药成方制剂 第二十册》。2004年后,以《中药、天然药物注射剂基本技术要求》为依据,对YMC的药材、生产工艺等质量标准进行了全面提升,并对YMC药理、毒理试验进行了再评价研究,为临床安全用药提供参考。
1 材料与方法 1.1 受试药物YMC,浅黄色透明液体,批号:060201,每支5.0 mL,含益母草总生物碱80.33 mg·mL-1(本研究以总生物碱计),室温保存。为子宫收缩药,用于止血调经,通过促进子宫收缩和凝血两方面发挥止血作用,益母水苏碱、葫芦巴碱是其药效物质基础(赵小梅等,2014;李燕等,2015)。临床拟静脉注射或滴注,用0.9%氯化钠注射液配制,最大日用量拟为150 mg,现临床用法为肌内注射,YMC由成都第一制药有限公司提供。
1.2 实验动物SPF级ICR小鼠60只,雌雄各半,体质量18~22 g,实验动物生产许可证号:SCXK(川)2004-16,室温20~26 ℃,湿度60%~70%,实验动物使用许可证号SYXK(川)2004-059,适应性饲养3 d后用于试验。Beagle犬32只,6~7月龄,雌、雄各半,7.5~9.5 kg,实验动物生产许可证号:SCXK(川)2004-15,不锈钢金属笼单笼饲养,每天定量饲喂犬全价颗粒饲料(广东顺德泰峰膨化饲料有限公司产品),温度18~26 ℃,实验动物使用许可证号:SYXK(川)2004-58,检疫驯养5周,合格后用于试验。
1.3 试剂血球稀释液,批号:051105;溶血素,批号:051105,均由四川美生医疗设备有限责任公司提供。PT检测试剂盒,批号:050506A1,法国STAGO公司产品。APPT检测试剂盒,批号:20050603,陕西方舟医学科技有限公司产品。AST检测试剂盒,批号:020091、060171;ALT检测试剂盒,批号:050181、060351;T-Bil试剂盒,批号:300051、060131,均为中生北控生物科技股份有限公司产品。TP检测试剂盒,批号:0705051、040611;CREA检测试剂盒,批号:1005071、0806131;Urea检测试剂盒,批号:1005081、0906161;Glu检测试剂盒,批号:1005051、0606101,均为四川迈克科技有限公司产品。血清电解质检测试剂A标准液,批号:20060307;B标准液,批号:20050131,均为深圳市航创医疗设备有限公司产品。
1.4 仪器LABOR Coa DATA-4001型半自动血凝测定仪(德国),海狮-18全自动血球计数仪(意大利),SECOMAM半自动生化分析仪(法国),ECG-6511心电图仪(上海光电医用电子仪器股份有限公司产品),HC-9883电解质分析仪(深圳航创医疗设备有限公司产品),徕卡-2015切片机(德国),TSJ-Q型全自动封闭式组织脱水机、BMJ-Ⅲ型包埋机、PHY-Ⅲ型病理组织漂烘仪(常州市中威医疗仪器有限公司产品),显微镜(日本尼康)。
1.5 方法 1.5.1 急性毒性试验预试验结果显示,尾静脉注射YMC,浓度1 413.60 mg·kg-1下的小鼠死亡率为10/10,706.80 mg·kg-1的死亡率为2/10,1 060.20 mg·kg-1的死亡率为10/10,883.50 mg·kg-1 的死亡率为7/10,954.18 mg·kg-1的死亡率为10/10。故根据预试验结果,将小鼠按体质量均衡随机分为YMC 626.00 mg·kg-1、695.60 mg·kg-1、 772.89 mg·kg-1、858.76 mg·kg-1、954.18 mg·kg-1 剂量组和0.9%氯化钠注射液对照组,每组10只。以1∶ 0.90的组间比用低比稀释法(徐叔云等,1991)将YMC配制成31.300 mg·mL-1、34.780 mg·mL-1、38.644 mg ·mL-1、42.938 mg ·mL-1、47.709 mg ·mL-1,按0.2 mL/10 g尾静脉注射给予受试药液(30~40 s内匀速)。给药后,观察记录4 h内小鼠出现的毒性反应症状和持续时间以及死亡情况。之后,每天上、下午各观察1次,观察2周,给药后第3天、第7天、第10天和第14天称量体质量。死亡后及时进行大体解剖观察,存活小鼠于第15天颈椎脱臼处死并进行大体解剖观察。
1.5.2 重复给药毒性试验根据预试验结果,Beagle犬按体质量随机分为YMC高、中、低剂量组(240.99 mg·kg-1、120.50 mg·kg-1、60.25 mg·kg-1)和0.9%氯化钠注射液对照组,每组8只。药物用 0.9%氯化钠注射液配制成所需浓度,按10 mg·kg-1 体质量静脉滴注给药,滴速为每分钟20~25滴,每周给药6 d,连续180 d,停药恢复30 d。给药后每天 观察Beagle犬的临床症状,包括外观体征、行为活动 情况和精神状况等,每天定量给食并观察Beagle犬的摄食情况。每周测量体质量,根据体质量调整给药量。给药前,给药第45天、第90天、第135天、第180天及停药第30天,对《中药、天然药物长期毒性研究技术指导原则》中规定的血液学、血液生化学、血清电解质、尿液、肢体Ⅱ导联心电图、体温、眼科学等指标进行检测。给药结束时(第181天)各组取4只,恢复期结束时(停药第31天)各组取4只进行系统解剖、脏器称量、大体病理学及组织病理学检查。解剖前,Beagle犬麻醉后髂骨上脊穿刺抽取骨髓进行骨髓涂片镜检。
1.5.3 统计分析用SPSS 13.0进行统计分析。对数据进行方差齐性检验,方差齐 性用Dunnett法(双侧)进行组间比较,方差不齐则用Tamhane's T2法进行组间比较。定性频数计数数据用秩和检验进行分析。用Bills法计算半致死剂量(LD50)(中华人民共和国卫生部药政局,1993;袁伯俊等,2006)。
2 结果 2.1 急性毒性试验YMC小鼠单次尾静脉注射给药,LD50为845.64 mg·kg-1(95%可信限689.41~956.48 mg·kg-1)。毒性症状表现为跳跃、烦躁、嗜睡、活动减少、阵挛性抽搐、眼球突出、尿失禁等,急性死亡及存活小鼠的心、肝、脾、肺、肾等器官均无肉眼可见异常。存活小鼠体质量增长与对照组的差异无统计学意义(表 1)。
| 组别 | 体质量/g | 死亡数/只 | ||||
| 0 d | 3 d | 7 d | 10 d | 14 d | ||
| YMC 954.18 mg·kg-1 剂量组 | 20.41±0.64 (n=10) | 24.05±0.35 (n=2) | 26.05±0.50 (n=2) | 28.85±1.34 (n=2) | 32.65±1.63 (n=2) | 8 |
| YMC 858.76 mg·kg-1 剂量组 | 20.60±0.95 (n=10) | 23.44±1.00 (n=5) | 25.74±1.56 (n=5) | 28.50±1.33 (n=5) | 30.70±1.90 (n=5) | 5 |
| YMC 772.89 mg·kg-1 剂量组 | 20.27±1.06 (n=10) | 23.06±1.76 (n=7) | 26.47±1.33 (n=7) | 28.16±2.22 (n=7) | 30.77±3.02 (n=7) | 3 |
| YMC 695.60 mg·kg-1 剂量组 | 20.13±0.88 (n=10) | 24.26±1.14 (n=10) | 27.70±2.51 (n=10) | 29.92±2.74 (n=10) | 32.29±3.05 (n=10) | 0 |
| 对照组 | 20.60±1.13 (n=10) | 25.17±1.46 (n=10) | 27.80±1.19 (n=10) | 30.65±1.76 (n=10) | 32.79±2.00 (n=10) | 0 |
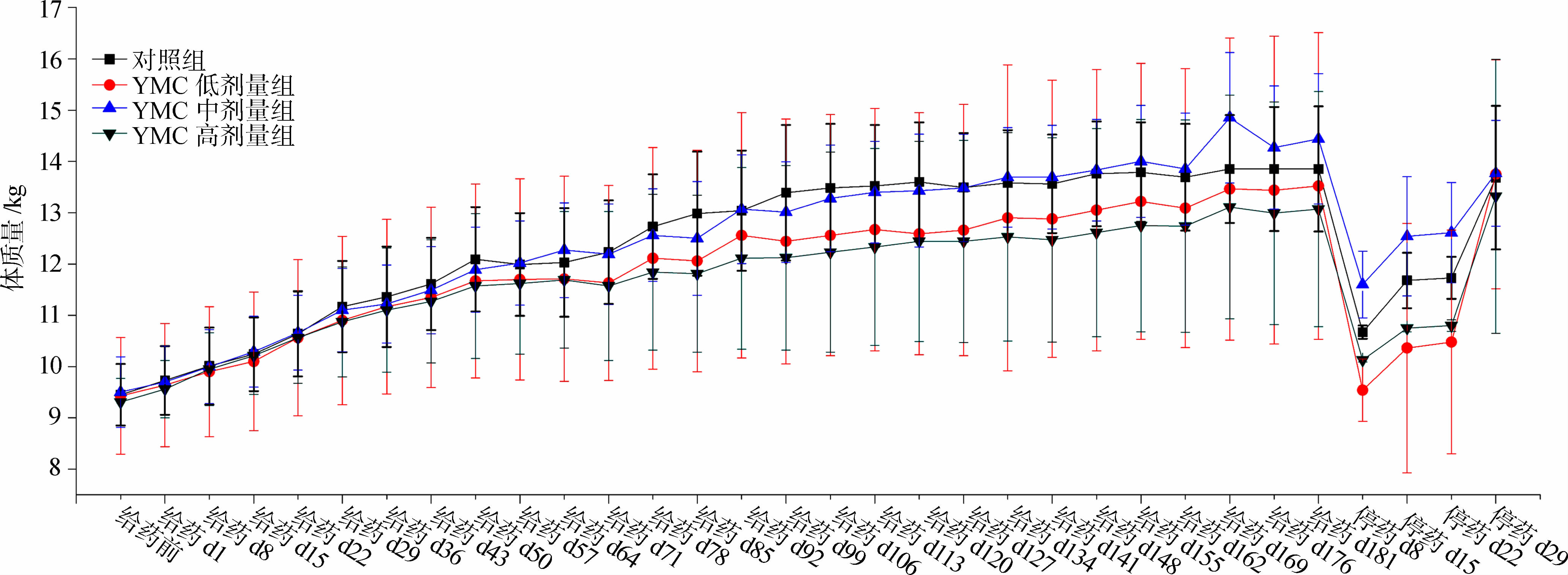
首次给药,YMC高剂量组在给药15~20 min出现流涎,YMC中剂量组Beagle犬在给药30~50 min出现流涎,YMC低剂量组一半个体出现流涎,流涎持续至给药结束后逐渐消失。1周后YMC中、低剂量组流涎症状逐渐消失,YMC高剂量组仍有个别个体(1~2只)在给药过程中偶见流涎和/或轻度呕吐(有少量黏液吐出,偶见少量食物),症状持续至给药期结束。给药期和恢复期各组Beagle犬均正常摄食,体质量增长无明显差异(图 1)。
|
| 图 1 益母草注射液对Beagle犬体质量的影响 Fig. 1 Effect of L. japonicus injection on body mass of Beagle dogs |
| |
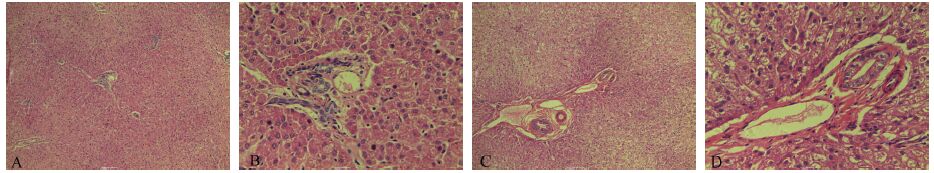
YMC各剂量组Beagle犬的体温(表 2)、心电图指标(表 3)、眼科检查、骨髓涂片、大体解剖观察、各脏器系数(表 4)均未见明显异常。血液学指标(表 5)及血清电解质指标(表 6)也均未见与药物相关的异常。YMC高剂量组给药第135天肌酐(CREA)降低,给药第180天丙氨酸氨基转移酶(ALT)升高;YMC中剂量组给药前CREA升高,但这些指标的降低或升高幅度均较小,均在正常生理范围和背景值范围内,无明显的剂量相关性,故这种变化不具有生物学意义,其余血液生化学指标均未见与药物相关的异常(表 7)。组织病理学检查结果显示,YMC高剂量组给药期结束时有1例Beagle犬的肝细胞可见轻度水肿变性(图 2),但肝小叶结构清晰。其余Beagle犬的肝、肾等各脏器组织均未见与药物相关的组织病理学改变。
|
| 图 2 Beagle犬肝脏组织观察 Fig. 2 Liver tissue of Beagle dogs A.正常肝脏组织,100×,B. 正常肝脏细胞,400×,C. 益母草注射液高剂量组水肿变形的肝脏组织,100×,D. 益母草注射液高剂量组水肿变形的肝脏组织,400×。 A. normal liver tissue,100×,B. normal liver cell,400×,C. abnormal liver tissue (hydropic degeneration) under high-dose Leonurus japonicus injection,100×,D. abnormal liver cell (hydropic degeneration) under high-dose Leonurus japonicus injection,400×. |
| |
| 组别 | 体温/℃ | |||
| 高剂量组 | 中剂量组 | 低剂量组 | 对照组 | |
| 给药前(n=8) | 39.26±0.19 | 39.25±0.30 | 39.18±0.23 | 39.21±0.24 |
| 给药d45(n=8) | 39.26±0.35 | 39.46±0.26 | 39.38±0.28 | 39.25±0.29 |
| 给药d90(n=8) | 39.44±0.28 | 39.51±0.15 | 39.50±0.27 | 39.25±0.29 |
| 给药d135(n=8) | 39.46±0.27 | 39.46±0.30 | 39.48±0.23 | 39.48±0.20 |
| 给药d180(n=8) | 39.51±0.16 | 39.45±0.18 | 39.45±0.19 | 39.55±0.14 |
| 停药d30(n=4) | 39.48±0.13 | 39.55±0.13 | 39.35±0.24 | 39.50±0.24 |
| 组别 | 检测时间 | 心率/(次/分) | P波/mv | P波/ms | R波/mv | Q-T间期/ms | S-T间期/ms |
| 高剂 量组 | 给药前 | 135.00±21.66 | 0.196±0.033 | 52.50±7.07 | 0.761±0.189 | 182.50±13.89 | 115.63±11.78 |
| 给药d45 | 118.13±26.90 | 0.245±0.039 | 53.75±5.18 | 1.003±0.216 | 196.25±14.08 | 120.63±10.16 | |
| 给药d90 | 112.75±16.74 | 0.256±0.048 | 65.00±7.56 | 1.194±0.385 | 207.50±17.53 | 146.25±20.66 | |
| 给药d135 | 119.00±18.53 | 0.231±0.037 | 57.50±8.86 | 1.106±0.276 | 205.00±15.12 | 120.00±22.04 | |
| 给药d180 | 128.88±21.40 | 0.225±0.030 | 60.00±0.00 | 1.073±0.237 | 230.75±15.98 | 137.50±8.86 | |
| 停药d30 | 117.75±19.48 | 0.225±0.046 | 55.00±5.77 | 1.288±0.193 | 200.00±27.08 | 125.00±17.32 | |
| 中剂 量组 | 给药前 | 138.13±27.41 | 0.203±0.029 | 56.25±5.18 | 1.156±0.295 | 196.25±9.166 | 121.25±8.35 |
| 给药d45 | 115.00±16.60 | 0.240±0.037 | 56.25±7.44 | 1.393±0.265 | 200.00±10.69 | 121.25±8.35 | |
| 给药d90 | 117.38±18.58 | 0.269±0.044 | 62.50±4.63 | 1.469±0.310 | 203.75±9.16 | 146.25±7.44 | |
| 给药d135 | 137.00±14.48 | 0.238±0.035 | 61.25±3.54 | 1.313±0.327 | 208.75±8.35 | 118.75±17.27 | |
| 给药d180 | 132.25±23.61 | 0.234±0.030 | 61.25±3.54 | 1.384±0.295 | 186.25±17.68 | 117.50±21.21 | |
| 停药d30 | 113.25±11.00 | 0.213±0.048 | 57.50±5.00 | 1.450±0.286 | 210.00±8.16 | 130.00±14.14 | |
| 低剂 量组 | 给药前 | 134.88±19.57 | 0.220±0.043 | 53.75±7.44 | 1.048±0.385 | 181.88±11.32 | 116.25±8.76 |
| 给药d45 | 134.25±21.88 | 0.250±0.038 | 55.00±5.35 | 1.333±0.397 | 200.00±10.69 | 125.63±15.22 | |
| 给药d90 | 131.63±21.95 | 0.291±0.044 | 63.75±5.18 | 1.281±0.467 | 205.00±13.09 | 141.25±16.42 | |
| 给药d135 | 142.00±15.04 | 0.256±0.068 | 58.75±6.41 | 1.331±0.435 | 197.50±8.86 | 113.75±11.88 | |
| 给药d180 | 134.38±17.49 | 0.241±0.038 | 60.00±7.56 | 1.195±0.377 | 203.75±7.44 | 135.00±7.56 | |
| 停药d30 | 133.25±6.50 | 0.250±0.074 | 57.50±5.00 | 1.238±0.301 | 210.00±25.82 | 125.00±19.15 | |
| 对照组 | 给药前 | 151.75±26.67 | 0.198±0.035 | 53.75±7.44 | 1.115±0.189 | 190.00±11.95 | 122.25±13.27 |
| 给药d45 | 141.63±17.23 | 0.246±0.037 | 58.75±3.54 | 1.550±0.207 | 195.00±9.26 | 118.75±13.56 | |
| 给药d90 | 130.25±15.45 | 0.275±0.033 | 66.25±5.18 | 1.700±0.242 | 200.00±22.04 | 140.00±14.14 | |
| 给药d135 | 143.75±21.56 | 0.263±0.058 | 60.00±7.56 | 1.506±0.209 | 205.00±18.52 | 113.75±23.87 | |
| 给药d180 | 141.75±14.69 | 0.218±0.066 | 63.75±9.16 | 1.481±0.179 | 200.00±5.35 | 127.50±13.89 | |
| 停药d30 | 148.75±6.40 | 0.250±0.035 | 55.00±5.77 | 1.600±0.041 | 212.50±12.58 | 120.00±8.16 |
| 脏器 | 检测时间 | 高剂量组 | 中剂量组 | 低剂量组 | 对照组 |
| 心脏 | 给药d180 | 7.476±0.810 | 7.754±0.425 | 7.888±1.047 | 7.369±0.286 |
| 停药d30 | 8.124±1.048 | 7.434±0.838 | 7.798±1.193 | 7.971±0.400 | |
| 肝脏 | 给药d180 | 25.522±3.328 | 24.142±2.443 | 24.302±1.512 | 25.232±2.747 |
| 停药d30 | 25.953±4.869 | 26.086±2.148 | 28.097±4.924 | 26.625±3.623 | |
| 脾脏 | 给药d180 | 2.061±0.227 | 2.421±0.361 | 2.203±0.447 | 2.111±0.445 |
| 停药d30 | 3.151±0.414 | 2.894±0.489 | 2.692±0.243 | 3.435±0.905 | |
| 肺脏 | 给药d180 | 6.164±0.328 | 6.680±0.919 | 5.745±1.600 | 6.140±0.242 |
| 停药d30 | 6.764±0.694 | 6.227±0.961 | 6.471±0.793 | 6.916±0.193 | |
| 肾脏 | 给药d180 | 4.451±0.690 | 4.146±0.104 | 4.289±0.809 | 4.437±0.587 |
| 停药d30 | 4.174±0.236 | 4.133±0.382 | 4.141±0.576 | 3.871±0.273 | |
| 脑(小脑) | 给药d180 | 6.300±0.825 | 5.876±0.937 | 6.338±1.399 | 6.192±0.477 |
| 停药d30 | 5.793±0.933 | 5.778±0.545 | 5.902±0.953 | 5.976±0.965 | |
| 胸腺 | 给药d180 | 0.424±0.109 | 0.716±0.281 | 0.587±0.247 | 0.777±0.458 |
| 停药d30 | 0.598±0.202 | 0.535±0.249 | 0.630±0.337 | 0.685±0.281 | |
| 肾上腺 | 给药d180 | 0.111±0.022 | 0.097±0.026 | 0.097±0.028 | 0.094±0.014 |
| 停药d30 | 0.113±0.022 | 0.103±0.012 | 0.108±0.024 | 0.100±0.015 | |
| 甲状腺 | 给药d180 | 0.053±0.003 | 0.045±0.001 | 0.062±0.012 | 0.051±0.007 |
| 停药d30 | 0.062±0.016 | 0.052±0.015 | 0.065±0.032 | 0.057±0.007 | |
| 垂体 | 给药d180 | 0.005 2±0.001 8 | 0.004 3±0.000 7 | 0.005 1±0.001 7 | 0.005 2±0.000 7 |
| 停药d30 | 0.004 2±0.000 7 | 0.004 7±0.000 3 | 0.004 4±0.000 6 | 0.004 6±0.000 7 | |
| 睾丸 | 给药d180 | 1.255±0.205 | 1.255±0.013 | 1.090±0.146 | 1.368±0.195 |
| 停药d30 | 1.328±0.067 | 1.422±0.157 | 1.329±0.072 | 1.508±0.483 | |
| 附睾 | 给药d180 | 0.310±0.021 | 0.310±0.034 | 0.278±0.014 | 0.299±0.049 |
| 停药d30 | 0.280±0.062 | 0.314±0.013 | 0.386±0.064 | 0.311±0.010 | |
| 前列腺 | 给药d180 | 0.496±0.001 | 0.656±0.039 | 0.406±0.063 | 0.392±0.049 |
| 停药d30 | 0.540±0.036 | 0.532±0.060 | 0.491±0.044 | 0.581±0.304 | |
| 子宫 | 给药d180 | 0.999±0.091 | 0.230±0.104 | 0.251±0.105 | 0.746±0.483 |
| 停药d30 | 1.105±0.079 | 0.575±0.415 | 0.757±0.755 | 0.507±0.451 | |
| 卵巢 | 给药d180 | 0.134±0.084 | 0.068±0.018 | 0.074±0.009 | 0.133±0.037 |
| 停药d30 | 0.141±0.040 | 0.112±0.028 | 0.089±0.029 | 0.107±0.024 |
| 组别 | 检测 时间 | 白细胞计数 WBC/(×109/L) | 红细胞计数 RBC/(×1012/L) | 血红蛋白 HGB/(g·L-1) | 血小板计数 PLT/(×109/L) | 凝血酶原 时间PT/s | 活化部分凝血 活酶时间APTT/s |
| 高剂 量组 | 给药前 | 8.17±1.93 | 5.97±0.46 | 111.1±9.3 | 293.0±43.8 | 5.64±0.65 | 18.26±1.30 |
| 给药d45 | 8.83±1.47 | 6.06±0.44 | 113.6±8.9 | 261.4±41.5 | 6.19±1.35 | 16.38±1.26 | |
| 给药d90 | 7.98±1.36 | 7.03±0.50 | 121.4±17.6 | 255.1±38.2 | 6.13±0.74 | 16.84±0.64 | |
| 给药d135 | 7.14±0.93 | 6.75±0.50 | 128.2±10.7 | 314.5±90.0 | 6.14±1.29 | 16.45±0.85 | |
| 给药d180 | 8.40±1.97 | 7.16±0.39 | 136.6±8.6 | 264.0±57.9 | 6.25±0.93 | 16.13±1.04 | |
| 停药d30 | 8.04±1.43 | 7.96±0.38 | 143.2±4.6 | 287.5±44.6 | 5.80±0.29 | 16.03±0.54 | |
| 中剂 量组 | 给药前 | 7.95±2.19 | 5.77±0.26 | 108.1±6.0 | 257.2±46.8 | 5.73±0.69 | 18.84±2.22 |
| 给药d45 | 7.54±1.56 | 5.92±0.27 | 111.6±5.9 | 210.1±41.2 | 6.13±0.96 | 15.69±0.56 | |
| 给药d90 | 9.81±1.86 | 6.92±0.60 | 125.0±11.0 | 201.9±39.6 | 5.76±0.35 | 18.23±0.86 | |
| 给药d135 | 7.37±1.85 | 6.78±0.42 | 124.8±16.8 | 226.5±33.7 | 6.16±1.35 | 17.15±1.51 | |
| 给药d180 | 8.64±2.37 | 6.67±0.40 | 130.8±6.1 | 209.1±44.2 | 6.06±1.29 | 16.03±0.79 | |
| 停药d30 | 8.49±0.45 | 7.42±0.73 | 139.2±9.3 | 192.5±89.3 | 5.78±0.13 | 18.08±0.51 | |
| 低剂 量组 | 给药前 | 7.10±1.70 | 6.02±0.56 | 114.0±12.0 | 285.8±48.8 | 5.90±0.69 | 16.90±1.24 |
| 给药d45 | 8.62±1.53 | 6.24±0.42 | 114.4±9.0 | 256.8±55.5 | 5.81±0.30 | 16.66±0.96 | |
| 给药d90 | 8.49±1.81 | 6.80±0.44 | 118.8±9.8 | 236.1±42.5 | 5.68±0.22 | 17.16±1.27 | |
| 给药d135 | 5.98±1.59 | 6.87±0.32 | 118.5±33.1 | 236.8±31.9 | 5.63±0.28 | 17.35±1.31 | |
| 给药d180 | 6.68±2.07 | 7.08±0.35 | 134.5±8.1 | 242.4±45.1 | 6.18±1.36 | 16.49±1.82 | |
| 停药d30 | 6.81±0.85 | 7.29±0.51 | 137.5±7.1 | 234.2±40.0 | 5.78±0.21 | 17.43±1.41 | |
| 对照组 | 给药前 | 7.82±2.12 | 5.68±0.41 | 108.2±8.3 | 262.1±84.2 | 5.78±0.55 | 17.63±1.40 |
| 给药d45 | 8.81±1.82 | 7.13±0.85 | 130.8±13.1 | 293.8±60.3 | 5.74±0.38 | 18.79±1.49 | |
| 给药d90 | 8.75±2.02 | 7.02±0.41 | 122.2±8.8 | 216.4±51.7 | 5.59±0.83 | 18.98±2.78 | |
| 给药d135 | 7.03±0.86 | 7.51±0.40 | 140.4±6.3 | 239.1±52.6 | 5.83±0.21 | 19.40±3.00 | |
| 给药d180 | 6.88±2.37 | 7.35±0.57 | 139.2±7.9 | 231.9±50.8 | 6.01±0.54 | 16.23±0.75 | |
| 停药d30 | 6.11±0.83 | 7.68±0.56 | 139.8±6.4 | 252.0±56.0 | 6.15±0.31 | 17.80±1.73 |
| 电解质指标 | 检测时间 | 高剂量组 | 中剂量组 | 低剂量组 | 对照组 |
| K+/(mmol·L-1) | 给药前 | 4.88±0.14 | 4.82±0.10 | 4.94±0.11 | 4.89±0.21 |
| 给药d45 | 4.90±0.25 | 4.69±0.15 | 4.76±0.18 | 4.79±0.13 | |
| 给药d90 | 4.73±0.19 | 4.70±0.10 | 4.72±0.20 | 4.73±0.17 | |
| 给药d135 | 4.77±0.25 | 4.56±0.15 | 4.56±0.08 | 4.70±0.15 | |
| 给药d180 | 4.47±0.22 | 4.40±0.09 | 4.39±0.10 | 4.50±0.13 | |
| 停药d30 | 4.59±0.18 | 4.53±0.07 | 4.60±0.09 | 4.63±0.14 | |
| Na+/(mmol·L-1) | 给药前 | 151.48±0.90 | 150.43±0.32 | 151.30±0.75 | 150.95±0.84 |
| 给药d45 | 153.78±1.52 | 153.14±1.55 | 153.26±1.29 | 151.61±0.93 | |
| 给药d90 | 150.53±1.39 | 150.26±0.52 | 150.53±0.82 | 150.35±1.35 | |
| 给药d135 | 146.59±1.26 | 144.64±1.37 | 144.50±1.18 | 144.53±2.59 | |
| 给药d180 | 147.25±2.20 | 146.56±1.09 | 146.29±1.31 | 145.61±1.56 | |
| 停药d30 | 147.05±1.42 | 145.70±0.98 | 146.60±1.80 | 145.40±2.27 | |
| Cl-/(mmol·L-1) | 给药前 | 111.23±0.60 | 110.74±1.06 | 111.70±1.73 | 111.01±1.53 |
| 给药d45 | 115.50±1.65 | 115.14±1.89 | 115.02±1.95 | 113.25±1.52 | |
| 给药d90 | 113.10±1.41 | 112.21±1.53 | 113.45±1.58 | 113.24±0.83 | |
| 给药d135 | 113.75±1.20 | 110.66±1.49 | 111.71±0.98 | 111.05±0.90 | |
| 给药d180 | 114.31±1.29 | 113.93±1.63 | 114.14±1.08 | 113.79±0.78 | |
| 停药d30 | 113.35±1.65 | 113.48±1.21 | 113.20±0.60 | 113.03±1.67 |
| 组别 | 检测 时间 | 天门冬氨酸 氨基转移酶 AST/(u·L-1) | 丙氨酸氨 基转移酶 ALT/(u·L-1) | 总蛋白 TP/(g·L-1) | 总胆红素T-Bil /(μmol·L-1) | 尿素Urea /(mmol·L-1) | 肌酐CREA /(μmol·L-1) | 血糖Glu /(mmol·L-1) |
| 高剂 量组 | 给药前 | 34.4±5.4 | 35.2±11.7 | 85.6±5.8 | 5.3±1.2 | 5.6±1.5 | 80.8±5.8 | 7.2±1.5 |
| 给药d45 | 29.4±2.0 | 45.6±27.2 | 67.4±4.3 | 4.4±0.4 | 6.1±0.5 | 81.3±4.5 | 5.9±0.2 | |
| 给药d90 | 31.0±5.8 | 39.8±10.4 | 70.3±5.4 | 4.7±0.3 | 5.4±1.2 | 74.3±4.0 | 4.3±0.5 | |
| 给药d135 | 25.5±4.6 | 35.2±5.8 | 68.5±5.4 | 5.2±1.1 | 4.4±0.5 | 70.9±8.0* | 5.0±0.5 | |
| 给药d180 | 28.4±5.3 | 44.1±9.6* | 71.4±7.2 | 5.4±1.2 | 3.7±0.7 | 86.5±6.9 | 5.4±0.5 | |
| 停药d30 | 29.5±4.4 | 36.5±13.3 | 69.4±2.5 | 7.2±1.3 | 4.9±1.0 | 90.4±4.2 | 5.5±0.6 | |
| 中剂 量组 | 给药前 | 32.6±5.7 | 29.2±6.6 | 86.1±5.0 | 5.4±0.8 | 5.6±0.7 | 82.7±5.9* | 7.2±0.6 |
| 给药d45 | 26.9±3.4 | 33.9±6.6 | 71.3±3.2 | 5.3±0.8 | 5.7±1.0 | 86.8±5.7 | 6.4±0.5 | |
| 给药d90 | 29.8±5.6 | 32.9±6.0 | 69.9±4.3 | 5.5±0.7 | 5.1±0.5 | 77.6±5.6 | 4.4±0.4 | |
| 给药d135 | 27.8±6.3 | 33.8±11.7 | 69.2±5.2 | 5.4±0.6 | 4.4±0.4 | 76.6±2.5 | 5.2±0.3 | |
| 给药d180 | 28.8±3.6 | 34.2±6.3 | 76.6±7.0 | 5.2±0.4 | 3.4±0.9 | 84.5±4.8 | 5.1±1.0 | |
| 停药d30 | 28.0±7.4 | 27.2±2.6 | 66.8±5.8 | 8.3±1.1 | 4.0±0.5 | 91.5±3.4 | 5.6±0.3 | |
| 低剂 量组 | 给药前 | 32.4±2.9 | 33.2±4.8 | 84.9±3.8 | 5.0±0.9 | 5.3±0.6 | 80.4±3.7 | 6.5±0.3 |
| 给药d45 | 29.2±3.4 | 34.1±6.2 | 66.8±4.5 | 4.9±0.6 | 5.7±1.0 | 82.5±5.1 | 6.2±0.6 | |
| 给药d90 | 30.0±4.1 | 33.0±5.2 | 71.6±4.6 | 4.8±0.8 | 4.5±0.8 | 72.9±5.0 | 4.6±0.6 | |
| 给药d135 | 24.0±3.6 | 33.4±6.6 | 70.4±5.0 | 5.3±0.8 | 4.3±0.5 | 78.1±4.7 | 5.2±0.3 | |
| 给药d180 | 28.9±10.3 | 41.4±6.6 | 73.0±8.0 | 5.0±1.0 | 3.4±0.4 | 85.0±3.7 | 5.3±0.7 | |
| 停药d30 | 25.5±3.1 | 33.2±9.5 | 70.3±7.1 | 6.9±0.6 | 4.4±0.8 | 84.8±2.2 | 5.3±0.9 | |
| 对照组 | 给药前 | 32.1±3.7 | 25.1±5.6 | 83.9±4.8 | 4.6±0.7 | 5.2±1.2 | 74.8±4.4 | 6.3±0.6 |
| 给药d45 | 30.4±2.7 | 29.2±6.7 | 70.7±5.6 | 4.3±0.5 | 5.1±0.9 | 83.8±9.3 | 6.2±0.8 | |
| 给药d90 | 31.0±6.6 | 32.5±6.7 | 70.4±4.4 | 4.8±0.6 | 4.9±0.8 | 71.5±6.0 | 4.2±0.4 | |
| 给药d135 | 27.9±4.4 | 28.8±7.7 | 67.7±3.6 | 5.6±1.0 | 4.3±0.8 | 79.2±7.2 | 4.8±0.4 | |
| 给药d180 | 26.8±6.2 | 32.5±10.8 | 73.2±6.4 | 5.2±0.7 | 3.3±0.6 | 80.7±6.4 | 4.9±0.4 | |
| 停药d30 | 24.8±3.3 | 22.8±8.3 | 69.8±3.7 | 8.0±1.8 | 4.1±0.9 | 88.0±6.9 | 4.8±0.3 | |
| 注: 与对照组比较, *P<0.05。 | ||||||||
| Note: compared with the control group,*P<0.05. | ||||||||
历代本草未言益母草有毒,说明其毒性较低,在正常范围内使用是较安全的,但近年临床应用研究表明长期或超剂量使用益母草口服制剂,可产生肝、肾毒性(冯群等,2014;赵红等,2015)。动物实验研究也证实了益母草长期经口给药对大鼠有肝、肾毒性(罗毅等,2009;孙蓉等,2014),致大鼠天门冬氨酸氨基转移酶(AST)、ALT水平显 著增高,对大鼠肾 损害部位主要在髓质,特别是间质中,以间质纤维化、毛细血管扩张或受压、肾小管萎缩为主;石油醚提取物灌胃给药还可使大鼠ALT、AST、CREA、尿素水平升高,肝、肾组织可见肿胀、少量炎细胞浸润等病理损伤。
本研究结果显示,YMC小鼠尾静脉给药,急性毒性症状表现为跳跃、烦躁、嗜睡、活动减少、阵挛性抽搐、眼球突出、尿失禁,LD50为845.64 mg·kg-1,相当于临床拟用剂量的394.6倍,提示YMC有较高的安全性,其急性毒性靶器官可能主要为中枢神经系统和自主神经。Beagle犬长期静脉滴注给予YMC 240.99 mg·kg-1、120.50 mg·kg-1、60.25 mg·kg-1(相当于临床拟用剂量的112.5倍、56.2倍、28.1倍),给药初期Beagle犬出现流涎,其出现时间、动物数及程度呈剂量反应趋势,以高剂量组较明显,降低给药滴速,Beagle犬的流涎症状可减轻或消失,随着给药天数的增加,Beagle犬流涎的症状减轻、出现频率降低或消失,到给药中、后期仅高剂量组个别犬偶见流涎或呕吐,表明Beagle犬对给药可能产生一定的适应性自我调节;同时提示YMC可能对Beagle犬的中枢神经系统有影响,或可致Beagle犬出现特异质反应(梁爱华等,2010),这有待进一步研究。组织病理学检查仅见高剂量组给药期结束时1例动物(1/4)出现肝细胞轻度水肿变性,但肝功指标未见异常,表明这种病变与药物的毒性无关,可能为动物自发性病变(朱奎成等,2011)。Beagle犬的重复给药毒性试验未明显发现在大鼠毒性研究中出现的肝、肾毒性,这除了实验动物种属因素影响外,还可能与制剂、成分含量、纯度、给药途径、药材品种及来源(俞捷等,2010;吕莉莉等,2015)等因素有关。益母草不同品种、药用部位获得的提取物的化学成分、含量不尽相同,大鼠毒性研究常用的益母草水煎剂、醇提制剂化学成分复杂、种类繁多(邓屾等,2014;Zhou et al,2015),主要化学成分包括生物碱类(盐酸水苏碱、益母草碱等)、黄酮类、二萜类、脂肪酸类、挥发油类等,有研究报道益母草生物碱含量与毒性有一定的相关性(李晓宇等,2014)。而YMC成分明确,主要为水溶性生物碱,不含非水溶性生物碱(何成军等,2014),生物碱主要成分为水苏碱和葫芦巴碱、未发现益母草碱,这也可能是YMC在Beagle犬试验中未见肝、肾毒性的因素。临床研究显示,42个中心参与的全国多中心非干预YMC不良反应集中监测与危险因素巢式病例对照研究结果表明,与药物相关的不良反应发生率为8/10 094(罕见),不良反应以皮疹、心慌、恶心、发热为主,未见肝、肾毒性等严重药物不良反应,表明YMC在临床合理使用是安全的,与本研究的动物试验结果具有较好的一致性。
综上所述,在本试验中YMC小鼠尾静脉给药LD50为845.64 mg·kg-1(相当于临床拟用剂量的394.6倍);YMC重复给药可致Beagle犬出现流涎、呕吐症状,未见造成肝、肾功能的损害,Beagle犬的安全剂量为120.50 mg·kg-1(相当于临床拟用剂量的56.2倍),提示YMC具有较高的安全性。但为慎重用药,临床用药应严格参考说明书,以减少不良反应的发生。如临床长期大量使用,仍建议对肝、肾功能进行监测。
| 邓屾, 刘丽丽, 陈玥. 2014. 益母草化学成分研究Ⅲ[J]. 中国当代新医药论丛 , 6 : 12–20. |
| 冯群, 赵红, 孙蓉. 2014. 益母草临床应用和不良反应研究进展[J]. 中国药物警戒 , 11(2) : 74–80. |
| 何成军, 彭成, 戴鸥, 等. 2014. 益母草注射液化学成分研究[J]. 中草药 , 45(21) : 3048–3052. |
| 李晓宇, 冯群, 吕丽莉, 等. 2014. 复方配伍对益母草急性毒性和总生物碱含量影响的实验研究[J]. 中国药物警戒 , 11(2) : 77–80. |
| 李燕, 谢晓芳, 余泉毅, 等. 2015. 基于大鼠离体子宫活动的益母草注射液缩宫活性部位筛选[J]. 时珍国医国药 , 26(2) : 288–291. |
| 梁爱华, 李春英, 赫然, 等. 2010. 用清醒Beagle犬进行中药注射液的类过敏试验方法研究[J]. 中国新药杂志 , 35(17) : 2328–2333. |
| 罗毅, 冯晓东, 刘红燕. 2009. 大剂量益母草对大鼠肝肾的亚急性毒性作用[J]. 中国药师 , 12(19) : 1180–1182. |
| 吕莉莉, 赵红, 李世民, 等. 2015. 不同提取方式对益母草小鼠急性毒性及毒靶器官的影响[J]. 中国药物警戒 , 12(12) : 705–710. |
| 孙蓉, 冯群, 赵庆华, 等. 2014. 益母草毒性研究进展[J]. 中国药物警戒 , 11(2) : 70–73. |
| 徐叔云, 卞如濂, 陈修. 1991. 药理实验方法学(第二版)[M]. 北京: 人民卫生出版社 . |
| 俞捷, 王瑾, 赵荣华, 等. 2010. 益母草肾脏不良反应研究进展[J]. 中国中药杂志 , 35(9) : 1213–1216. |
| 袁伯俊, 廖明阳, 李波. 2006. 药物毒理学实验方法与技术[M]. 北京: 化学工业出版社 . |
| 赵红, 李世民, 窦立雯, 等. 2015. 益母草生物碱药理毒理学研究进展[J]. 中国药物警戒 , 12(12) : 722–726. |
| 赵小梅, 谢晓芳, 熊亮. 2014. 益母草注射液主要提取成分对凝血系统影响的筛选[J]. 中国实验方剂学杂志 , 20(4) : 128–130. |
| 中华人民共和国卫生部药政局. 1993. 新药临床前研究指导原则汇编[M]. 北京:199. |
| 朱奎成, 刘娜, 王纯耀, 等. 2011. 比格犬自发疾病的病理组织学研究[J]. 实验动物科学 , 28(2) : 76–80. |
| Zhou QM, Peng C, Yang H, et al. 2015. Liang Xiong. Steroids from the aerial parts of Leonurus japonicus[J]. Phytochemistry Letters (12) : 287–290. |
 2016, Vol. 35
2016, Vol. 35



