扩展功能
文章信息
- 王亚美, 黄丽娜, 艾新宇, 魏原杰, 刘小宁, 高希武
- WANG Yamei, HUANG Lina, AI Xinyu, WEI Yuanjie, LIU Xiaoning, GAO Xiwu
- 棉蚜细胞色素P450 CYP6J1的克隆与表达
- Cloning and Expression of Cytochrome P450 CYP6J1 from Aphis gossypii
- 四川动物, 2016, 35(3): 378-383
- Sichuan Journal of Zoology, 2016, 35(3): 378-383
- 10.11984/j.issn.1000-7083.20150393
-
文章历史
- 收稿日期: 2015-12-08
- 接受日期: 2016-01-30
2. 中国农业大学农学与生物技术学院, 北京 100193
2. College of Agronomy and Biotechnology, China Agricultural University, Beijing 100193, China
细胞色素P450(cytochrome P450,cytochrome CYPs,简称P450)是一类以血红素为辅基的B族细胞色素超家族(Kubota et al.,2009)。P450基因是一个超家族,包括CYP4、CYP6、CYP9和CYP12共48个家族(Amenya et al.,2008),其中CYP4(Snyder & Van Antwerpen,1998)和CYP6(Feyereisen et al.,1995;Wang & Hobbs,1995)的表达过量与昆虫抗性品系的出现有关。昆虫P450参与外源性化合物和内源性物质的代谢解毒过程(Tan & Guo,1996)。早在20世纪就有研究表明其代谢解毒作用是多种昆虫获得杀虫药剂抗性的普遍机制(Eldefrawi et al.,1960)。P450参与杀虫剂抗药性是由于其解毒作用的增强,表现为相应的P450酶活性或其表达量的增加(Scott & Wen,2001)以及作用部位的敏感性降低(Denholm & Rowland,1992)。另外也有文献报道称昆虫存在行为抗性,通过改变自身的习性和行为以逃避杀虫剂的作用(Ahuja et al.,2010)。在所有表达系统中,大肠杆菌Escherichia coli表达系统在蛋白质表达方面有很多优点,本实验以P450 CYP6J1的异源表达为主要目标,通过融合表达(Deeni et al.,2001)的技术手段建立简单、有效的P450酶系原核表达系统。
棉蚜Aphis gossypii是一种多食性害虫,繁殖能力极高,容易猖獗发生。棉蚜在我国是棉花苗期的一种重要害虫,也是影响棉花产量和品质的一个主要因素。由于化学杀虫剂的不科学使用造成棉蚜抗药性的增强,对棉蚜的防治带来了巨大的困难,而化学药品的大规模应用会导致环境恶化和食品污染,严重影响人体健康(Crinnion,2009;Komarek et al.,2010),越来越不被大众接受,同时也让害虫承受很高的选择压力(张学涛等,2012)。棉蚜抗性的发展主要与其体内解毒酶的变化有关,这为我们调控棉蚜体内解毒酶的表达,延缓害虫抗药性的发展提供新思路。因此本研究对棉蚜P450 CYP6J1基因进行克隆和原核表达,并对表达的融合蛋白His-CYP6J1进行鉴定,为后期棉蚜的研究提供了基础。
1 材料与方法 1.1 供试昆虫、菌株和载体棉蚜采自新疆维吾尔自治区乌鲁木齐市乌鲁木齐县安宁渠镇,并于室内用棉苗长期饲养,饲养条件为:室温25 ℃,相对湿度75%,光周期(L∶D)16 h∶8 h。表达载体pET28a质粒由本实验室保藏,为原核表达载体,卡纳(Kana)抗性。克隆菌株E. coli DH5α和表达菌株E. coli BL21感受态细胞均购自北京全式金生物技术有限公司。
1.2 实验试剂与仪器DNA Marker、Oligo d(T)18 Primers、Reverse Transcriptase M-MLV(RNase Hˉ)、Recombinant Ribonuclease Inhibitor、pMD19-T(simple)、T4 DNA连接酶、限制性内切酶、Taq DNA聚合酶和dNTP(10 mM)购于宝生物工程(大连)有限公司;RNA-Solv Reagent提取液为Omega Bio-tek公司产品,蛋白Marker购于Thermo Scientific;SanPrep柱式DNA胶回收试剂盒、PCR回收试剂盒、SanPrep柱式质粒DNA小量提取试剂盒、实验引物合成、DNA序列测定均购自生工生物工程(上海)股份有限公司;一抗鼠抗His-Tag单克隆抗体、辣根过氧化物酶标记的山羊抗鼠IgG购自北京中杉金桥生物技术有限公司;醋酸纤维素膜购自Merck Millipore;实验引物由生工生物工程(上海)股份有限公司合成;其余所用的化学试剂均为国产分析纯。
1.3 实验方法 1.3.1 棉蚜总RNA提取及cDNA合成使用RNA-Solv Reagent提取液,约50只棉蚜用于提取总RNA。棉蚜总RNA经1%琼脂糖凝胶电泳检测RNA的完整性,紫外/可见分光光度计检测总RNA的浓度(ng·μL-1)和纯度(OD260/280)。当提取的RNA较纯时,取1 μg总RNA作为逆转录反应的模板,Oligo d(T)18为下游引物逆转录合成棉蚜cDNA。
1.3.2 棉蚜P450 CYP6J1基因的克隆根据前期得到的P450 CYP6J1基因全长序列(GenBank登录号:JN989967.1),设计合成了P450 CYP6J1 PCR扩增所需的2个引物,扩增的片段约为1 398 bp。下划线为引入的酶切位点(BamHI和XhoI)序列:上游引物:5'-CGCGGATCCATGAAAAC-3',下游引物:5'-CCTCGAGTTAGTTTTTTCTCTTGGTAAC-3'。以棉蚜cDNA为模板扩增P450 CYP6J1基因序列。扩增反应条件为:94 ℃变性4 min;94 ℃变性30 s,58 ℃退火45 s,72 ℃延伸1 min,35个循环;最后72 ℃延伸10 min。1%琼脂糖凝胶电泳检测PCR产物。PCR产物经PCR回收试剂盒回收后与pMD19-T(simple)载体16 ℃过夜连接并转化入DH5α感受态细胞,筛选阳性重组子,正确的重组质粒命名为pMD19-T-CYP6J1,由生工生物工程(上海)股份有限公司进行测序。
1.3.3 棉蚜P450 CYP6J1基因的生物信息学分析对获得的棉蚜P450 CYP6J1基因进行生物信息学分析,使用DNAMAN将开放阅读框翻译成氨基酸序列,进行理论蛋白分子量、等电点的预测;利用SignalP 4.1查找信号肽;利用ExPASy(ProtScale)进行蛋白的亲水性和疏水性分析;在NCBI网站上利用BLAST分析棉蚜P450 CYP6J1基因与不同物种氨基酸序列的相似性;利用MEGA 5对不同物种P450 CYP6J1氨基酸序列进行多重比对,通过邻接法(neighbor-joining,NJ)构建氨基酸的系统进化树。
1.3.4 原核表达质粒pET28a-CYP6J1的构建将pMD19-T-P450 CYP6J1和含His-Tag的pET28a载体分别用BamHI和XhoI进行双酶切,P450 CYP6J1与pET28a经回收试剂盒回收后,16 ℃过夜连接,连接产物转化入DH5α感受态细胞,筛选阳性重组子,提取质粒进行双酶切鉴定,正确的重组质粒命名为pET28a-CYP6J1,送至生工生物工程(上海)股份有限公司进行测序。
1.3.5 含His-Tag的融合蛋白His-CYP6J1的表达及Western-blot鉴定将测序结果正确的阳性克隆转化到BL21感受态,将菌液PCR鉴定正确的阳性克隆活化到对数期OD600=0.4~0.6后,加入终浓度为0.5 mmol·L-1的异丙基硫代半乳糖苷(IPTG),37 ℃振荡培养4 h后超声破碎至相对透亮,并将上清和沉淀分开处理,以同时转化BL21的空载体pET28a及未诱导的菌液作对照,用15% SDS聚丙烯酰胺凝胶电泳检测重组蛋白的表达。
通过Western-blot检验目的蛋白在BL21菌株中的正确表达。将未经IPTG诱导的菌液及空载体pET28a和诱导的融合蛋白His-CYP6J1及空载体pET28a经15%SDS聚丙烯酰胺凝胶电泳分离后,使用Mini-PROTEAN 3 Trans-Blot系统将融合蛋白转移至醋酸纤维素膜上。用5%脱脂奶粉37 ℃封闭2 h;磷酸盐吐温缓冲液(PBST)冲洗3次,加入1∶3 000稀释的抗His-Tag的抗体(一抗),室温孵育2 h;PBST冲洗3次后加入1∶5 000稀释的辣根过氧化物酶标记的山羊抗鼠IgG抗体(二抗),室温孵育1 h;PBST冲洗3次后采用DAB法显色后观察。
2 结果与分析 2.1 棉蚜P450 CYP6J1基因的克隆用设计的特异性引物,以棉蚜cDNA为模板PCR扩增棉蚜P450 CYP6J1基因后,用1%琼脂糖凝胶电泳进行检测。结果显示,在约1 400 bp处有1条明显的特异性扩增带(图 1:A)。经PCR产物回收试剂盒回收扩增的目的基因后与pMD19-T(simple)载体连接转化大肠杆菌DH5α感受态细胞,菌液PCR筛选阳性重组子(图 1:B),经生工生物工程(上海)股份有限公司测序后,用DNAMAN与棉蚜P450 CYP6J1基因序列比对,结果一致,说明获得的目的基因大小正确。

|
| 图 1 P450 CYP6J1基因的PCR扩增及重组质粒的PCR鉴定 Fig. 1 PCR amplification of P450 CYP6J1 gene and identification of recombinant plasmid A: M. DL2000,1. PCR扩增产物,2. 阴性对照; B: M. DL2000,1. 阴性对照,2. 重组质粒的PCR鉴定。 A: M. DL2000,1. PCR amplification,2. Negative control; B: M. DL2000,1. Negative control,2. PCR identification of recombinant plasmid(digested products of pET28a-CYP6J1 by BamHI and XhoI). |
| |
在NCBI网站上利用BLAST进行相似性比对,分析表明所得序列为P450超家族。利用DNAMAN 6分析P450 CYP6J1 cDNA序列,结果表明棉蚜P450 CYP6J1基因有完整的开放阅读框,全长1 398 bp。起始密码自ATG至终止密码子TAA,共编码465个氨基酸。P450的特有结构域,血红素结合区:FxxGxRxCxGx,螺旋K区:ExxR,螺旋I区:(A/G)Gx(D/E)T(T/S)。理论分子量53.67 kD,理论等电点8.80(图 2)。利用MEGA 5对蚜虫不同物种的P450氨基酸序列构建系统进化树,通过NJ法Bootstrap重复1 000次,其他参数设置均采用默认设置。结果表明,蚜虫不同物种间P450保守区较稳定,其中所得棉蚜cDNA序列推导的氨基酸与豌豆蚜Acyrthosiphon pisum的保守性最为接近,一致性可达92%(图 3)。

|
| 图 2 棉蚜P450 CYP6J1基因的cDNA核苷酸序列及其推导的氨基酸序列 Fig. 2 The cDNA sequence and deduced amino acid sequence of P450 CYP6J1 gene from Aphis gossypii 实线下划线的ATG和TAA分别表示起始密码子和终止密码子,实线框表示血红素结合区,虚线框表示螺旋Ⅰ区,虚线下划线表示螺旋K区。 Solid lines underlined ATG and TAA represent initiation codon and termination codon, respectively; solid box represents the heme-binding domain,dash box represents a screw Ⅰ area, dashed line underlined represents a screw K area. |
| |

|
| 图 3 昆虫细胞色素P450超家族系统进化树 Fig. 3 Phylogenetic tree of cytochrome P450 superfamily from insects 分支上数字代表从1 000次重复中得到的相应的P450分为同一分支的置信水平; 标尺显示了对应分支上单个位点发生氨基酸位点变异的估计值。 The branch number represents from 1 000 times of the corresponding P450s,which is divided into the confidence level of the same branch; Scale shows the estimates on a single site of amino acid sites mutation. |
| |
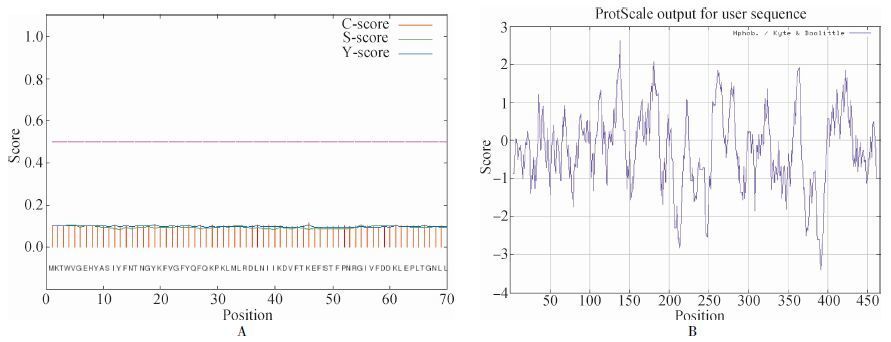
经SignalP 4.1预测,棉蚜His-CYP6J1蛋白无信号肽序列,因此该蛋白属包内分泌蛋白(图 4:A)。用ExPASy ProtParam预测其总平均疏水性指数(GRAVY)为-0.249,显示该蛋白属亲水性蛋白(图 4:B)。
|
| 图 4 棉蚜P450 CYP6J1蛋白的信号肽及亲疏水性分析 Fig. 4 Signal peptide and hydrophobic analyses of P450 CYP6J1 from Aphis gossypii A.棉蚜His-CYP6J1蛋白的信号肽分析,B. 棉蚜His-CYP6J1蛋白的亲疏水性分析。 A.Signal peptide analysis of His-CYP6J1 from A. gossypii,B. Hydrophobic analysis of His-CYP6J1 from A. gossypii. |
| |
P450 CYP6J1经BamHI和XhoI双酶切后与原核表达载体pET28a连接后转化DH5α感受态细胞,提取重组质粒后用BamHI和XhoI双酶切鉴定,酶切出约1 400 bp的目的条带(图 5:A)。双酶切鉴定正确的重组质粒经生工生物工程(上海)股份有限公司测序后用DNAMAN对氨基酸序列进行分析,测序结果与棉蚜P450 CYP6J1氨基酸序列一致,说明原核表达质粒pET28a-CYP6J1构建成功。

|
| 图 5 重组质粒的双酶切鉴定、蛋白His-CYP6J1的诱导表达及Western-blot鉴定 Fig. 5 Digested products of pET28a-CYP6J1 by BamHI and XhoI,the induction expression of His-CYP6J1 protein and its identification by Western-blot A.重组质粒pET28a-CYP6J1双酶切鉴定: M. Mark 15 000,1. 重组质粒pET28a-CYP6J1,2. 重组质粒pET28a-CYP6J1的双酶切产物; B. 蛋白His-CYP6J1的诱导表达: M. 180.0 kD,1. BL21-pET28a诱导前,2. BL21-pET28a诱导后,3. BL21-His-CYP6J1诱导前,4. BL21-His-CYP6J1诱导后总蛋白,5. BL21-His-CYP6J1诱导后上清,6. BL21-His-CYP6J1诱导后沉淀; C. 融合蛋白His-CYP6J1的Western-blot鉴定: M. 180.0 kD,1. pET28a诱导前,2. pET28a诱导后,3. His-CYP6J1诱导前,4. His-CYP6J1诱导后总蛋白。 A. Double enzyme digestion of recombinant plasmid pET28a-CYP6J1: M. Mark 15 000,1. pET28a-CYP6J1,2. Digested products of pET28a-CYP6J1 by BamHI and XhoI; B. The induction expression of His-CYP6J1 protein: M. 180.0 kD,1. BL21-pET28a without IPTG,2. BL21-pET28a with IPTG,3. BL21-His-CYP6J1 without IPTG,4. BL21-His-CYP6J1 with IPTG,5. BL21-His-CYP6J1 supernatant with IPTG,6. BL21-His-CYP6J1 precipitation with IPTG; C. Identification of fusion protein by Western-blot: M. 180.0 kD,1. pET28a without IPTG,2. pET28a with IPTG,3. His-CYP6J1 without IPTG,4. His-CYP6J1 with IPTG. |
| |
通过15%的SDS-PAGE检测融合蛋白His-CYP6J1的表达显示(图 5:B),与诱导表达前相比,重组质粒pET28a-CYP6J1转化到表达菌BL21经IPTG诱导表达后有1条蛋白质增强条带,表达载体分子量约为57 kD,与预期的His-CYP6J1蛋白相对分子量相似,初步说明融合蛋白His-CYP6J1诱导表达成功。菌体超声破碎后的上清和沉淀分别处理后经15%的SDS-PAGE检测显示,表达的融合蛋白-CYP6J1主要存在于沉淀中,说明该蛋白属于包涵体。
用鼠抗His-Tag单克隆抗体对IPTG诱导表达的融合蛋白做进一步验证(图 5:C),Western-blot检测结果显示经IPTG诱导表达后与诱导表达前相比,诱导表达后有1条57 kD明显的条带,说明融合蛋白His-CYP6J1表达正确,为棉蚜P450 CYP6J1多克隆抗体制备提供了素材。
3 讨论几乎所有的生物都存在P450酶系,包括动物、植物、昆虫等。一般认为昆虫P450的各家族中CYP6和CYP4家族与杀虫剂抗性有关(Scott & Lee,1993;Carino et al.,1994;邱星辉等,2003)。P450氧化酶在昆虫的生长、发育及对外源有毒物质的胁迫下发挥重要作用。要了解生物体是通过哪些方式降解这些外源物质的毒性,尤其是对于农业害虫来说,了解其解毒机制对于害虫的治理至关重要。
本实验为今后进一步研究P450 CYP6J1基因的结构、功能及其蛋白在分子生物学研究中的作用提供基础资料,同时也为棉蚜的防治做铺垫。实验中克隆得到了棉蚜P450 CYP6J1基因,并将其构建到表达载体pET28a上,0.5 mmol·L-1的IPTG诱导表达得到了棉蚜融合蛋白His-CYP6J1,为棉蚜P450 CYP6J1多克隆抗体的制备提供前提条件。棉蚜P450 CYP6J1基因经生物信息学分析结果显示,该基因的开放阅读框长1 398 bp,且没有信号肽,共编码465个氨基酸,理论蛋白分子量53.67 kD,理论等电点8.80。由棉蚜P450 CYP6J1基因推导的氨基酸序列经生物信息学分析,其具有P450超家族特有的结构域,包括血红素结合区、螺旋K区、螺旋I区,这与文献报道的一致(贺丽虹等,2008;Liu et al.,2013)。同源性比对分析表明,所得棉蚜cDNA序列推导的氨基酸与豌豆蚜的保守性最为接近,一致性可达92%。
为进一步了解融合蛋白His-CYP6J1的特性,将克隆得到的P450 CYP6J1基因与表达载体pET28a进行连接,构建了棉蚜pET28a-CYP6J1重组表达质粒,将重组质粒转化到感受态细胞BL21中,用IPTG诱导表达融合蛋白His-CYP6J1。由于pET28a上带有6个His-Tag,它是最常用的纯化蛋白的融合标签,具有分子量相对小、不影响目的蛋白功能、免疫原性相对较低、成本低等优点(Graslund et al.,2008;Uchinomiya et al.,2013),因此为我们后续实验利用亲和层析法纯化目的蛋白提供素材。
 2016, Vol. 35
2016, Vol. 35




