扩展功能
文章信息
- 周晨辉, 王正鲲, 林小涛, 许忠能, 李江涛, 杨亚运, 曾鹏
- ZHOU Chenhui, WANG Zhengkun, LIN Xiaotao, XU Zhongneng, LI Jiangtao, YANG Yayun, ZENG Peng
- 溪流唐鱼种群时空格局及其主要影响因子
- Temporal and Spatial Variations of Tanichthys albonubes Population in a Stream and the Main Affecting Factors
- 四川动物, 2016, 35(3): 344-350
- Sichuan Journal of Zoology, 2016, 35(3): 344-350
- 10.11984/j.issn.1000-7083.20150397
-
文章历史
- 收稿日期: 2015-12-10
- 接受日期: 2016-04-05
唐鱼Tanichthys albonubes隶属于鲤形目Cypriniformes鲤科Cyprinidae亚科Danioninae唐鱼属Tanichthys (潘炯华,1991),是国家Ⅱ级重点保护水生野生动物。唐鱼主要分布于华南地区森林溪流,其中广东省从化地区是唐鱼的主要分布地,已发现有唐鱼分布的溪流十几条(陈国柱等,待发表)。鱼类种群时空分布是种群生态学一项重要研究内容,掌握鱼类种群动态对渔业资源的评估以及种质资源保护等均具有重要意义。以往在溪流鱼类的调查研究中,大都采用电鱼工具进行采样(任长江等,2005;李红敬,林小清,2010),但唐鱼属濒危物种,不能采用此方法,而目前尚没有一套较为科学、成熟的采样及研究方法,故国内外学者对唐鱼的研究多集中在基础生物学和实验研究(Freyhoh & Herder,2001;Wang et al.,2010;姜鹏等,2012;Jing et al.,2013;王正鲲等,2015),而对于溪流自然环境中唐鱼种群的时空格局未见报道。
鱼类种群的时空分布格局和变动规律受到多种环境因素的影响,如温度影响鱼类的繁殖周期和洄游(李峣等,2007;Kielbassa et al.,2010;李倩等,2012),水流影响鱼类的生长和分布(张慧杰等,2007),而食物作为一种影响摄食和生长发育的重要因素(吴金明等,2015)与鱼类种群动态变化密切相关(陈大刚,1997)。唐鱼属亚热带鱼类,对温度变化尤其是低温更加敏感,其栖息的华南地区森林溪流生境由于受亚热带季风影响,面临周期性暴雨和山洪冲刷(王德良等,2012),流速波动大。水流不仅直接影响鱼类种群,同时也影响水体中浮游生物的种类组成和数量分布(Peters & Marrase,2000;朱宜平等,2010;Li et al.,2013),而浮游生物是唐鱼的重要食物之一(程炜轩等,2006)。因此唐鱼种群的时空变化理应受到水温、水流和浮游生物等环境因子的影响。基于此,作者经过长达1年的时间,尝试用分段围隔、全部唐鱼活体捕捞、全员统计、样本全部放回的方法,对从化地区森林溪流塘肚溪唐鱼种群的时空变化特征进行调查,并探讨其与水温、水流和浮游生物等因子之间的关系,拟为唐鱼种群生态学研究及其资源保护提供基础数据。
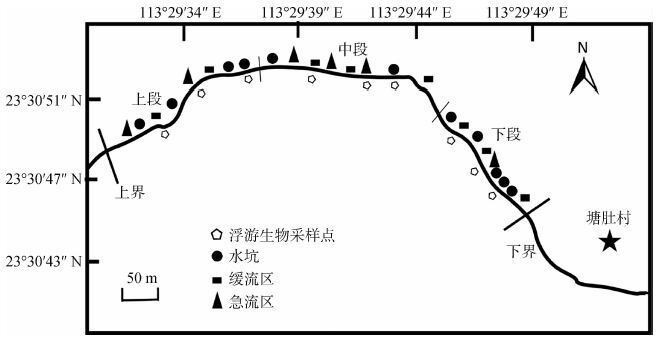
1 材料与方法 1.1 采样溪流环境特征2014年4月—2015年3月,每月1次对广东省从化神岗镇山区塘肚溪(23°30'51″N,113°29'39″E)进行调查。塘肚溪为Ⅰ级溪流,生境多样,水质清澈,底质为碎石,唐鱼资源较为丰富,为研究唐鱼时空分布格局的理想场地。采样点(区域)布设见图 1。塘肚溪全长758 m,其中,最上游82 m溪段和最下游201 m溪段由于坡度大、溪岸较高且陡峭、溪中杂草丛生不利于采样,所以本研究选取靠肉眼可轻易发现唐鱼并能进行采样的中间溪段,此溪段长度为457 m,最宽处2.3 m,最窄处0.8 m,水深18~85 cm,其中有唐鱼分布的溪段水深一般为18~65 cm。为方便采样和比较,根据不同溪段宽度、流速等特征,将可采样溪流再划分为上、中、下3段,其中,上段长约141 m,宽度较小但溪流中有较大石头等障碍物且有4个水坑,流速总体较缓;中段长约169 m,溪流中石头、水草等障碍物少且水坑数只有2个,流速较大;下段长约147 m,宽度总体较大,石头、水草等障碍物较多且有5个水坑,流速最缓。事先用精密水位流速仪(Unidata-6526G2,澳大利亚)
|
| 图 1 塘肚溪唐鱼及浮游生物采样区域(点)布设示意图 Fig. 1 Sampling areas(point)of Tanichthys albonubes and plankton in Tangdu Stream |
| |
测定各溪段不同区域的流速,并按照流速的大小将采样点(区域)分为3种类型,分别为水坑(流速<75 mm·s-1)、缓流区(75 mm·s-1≤流速≤115 mm·s-1)和急流区(流速>115 mm·s-1)。
1.2.1 唐鱼采样方法每月采样1次。唐鱼为群居鱼类,喜群游,有利于采样工作的进行。但由于唐鱼会在一定区域内活动,因此采样并非在固定的点而是相对固定的区域。每次采样自下游方向逐步往上,在每个溪段各流速区域(图 1)中仔细观察,一旦发现唐鱼即用2张拦网分别在前后方向将其包围在1个围隔中,用手抄网尽数捕捞围隔中的唐鱼,捕捞时做到轻抓轻放,避免造成鱼体损伤。由于野外条件下肉眼区分仔鱼和稚鱼较为困难,因此将两者合并计数。将捕捞到的唐鱼置于盛有溪水且容积为2.5 L的小桶中,然后按照不同生活史阶段(陈国柱,2005)将所有唐鱼分为成鱼(体长>23 mm)、幼鱼(12 mm≤体长≤23 mm)和仔、稚鱼(体长<12 mm),并用小手抄网捞出,分开暂养于3个小盆中进行计数,计数结束后将全部唐鱼样本原位放回围隔中。然后继续往上游方向采样,待到下一个围隔的捕捞、计数结束后才将上一个围隔拆除,以此类推,直到整条溪流的采样结束为止。
1.2.2 浮游生物和水温、水流调查方法浮游生物的采集时间与唐鱼的调查同步,在各溪段3种流速区域中各选择1个具有代表性的点,全溪共9个点作为固定的采样点(图 1)。浮游植物的采集方法:用自制的小型采水器(500 mL)取水样500 mL,5%福尔马林固定,经沉淀、浓缩后在显微镜下进行计数(胡鸿钧等,1980)。浮游动物的采集方法:用2 L的小桶取水样,经25#浮游生物网过滤共20 L水样后,5%福尔马林固定,将滤液置于量筒中沉淀,而后在显微镜下进行计数。计数用浮游生物计数框(CC-F,北京普力特仪器有限公司)对滤液重复计数3次,最后取其平均值(杜明勇等,2014)。采样时现场用水质分析仪(YSI-09L100503,美国)测定水温,用精密水位流速仪(Unidata-6526G2,澳大利亚)测定水流量。
1.3 数据处理和分析采用Excel和SPSS 13.0进行数据处理。溪流环境的特殊性和唐鱼的行为特性导致不同时间及采集点的唐鱼数量分布差异巨大,因此按常规统计方法求出平均值和标准差并进行差异显著性检验的意义不大,所以本文对唐鱼数量时空分布的数据均以其特定空间的总数量或不同时间的累计总数量表示,而浮游生物则以平均密度表示。对所有进行相关性分析的数据以lg进行转换后,分别对每月全溪唐鱼总数量与对应月份的水温及水流量值、每月全溪唐鱼总数量与对应月份的全溪各采样点浮游生物平均密度、各溪段各流速区域全年累计唐鱼总数量与对应流速区域全年浮游生物平均密度作回归分析,线性回归相关性检验均采用协方差分析(ANCOVA)。
2 结果与分析 2.1 塘肚溪唐鱼种群周年变化塘肚溪全溪唐鱼种群数量和各年龄段组成周年变化如图 2所示。唐鱼种群数量在冬后开始上升,7月达到最大值后下降,在10月又回升出现另一个数量高峰,随后逐步下降,至2月达到全年最低值。7月和10月高峰期种群数量分别为3 649尾和3 829尾,而2月采到唐鱼数量仅为166尾。从不同生活史阶段看,仔、稚鱼的数量变动规律最为明显,同样在7月和10月数量最大,分别为2 455尾和2 231尾,占唐鱼种群总数的67%和58%。而1月、2月均没有发现仔、稚鱼。

|
| 图 2 塘肚溪唐鱼种群数量和年龄组成周年变化 Fig. 2 Annual variation in population size and age composition of Tanichthys albonubes in Tangdu Stream |
| |
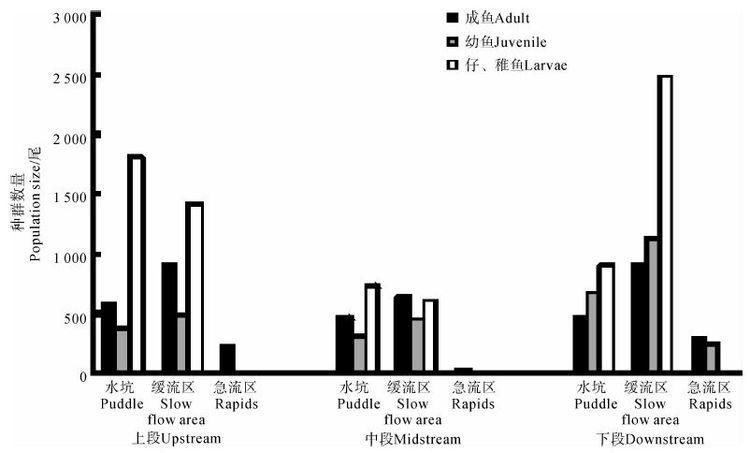
上段、中段、下段不同流速采样区域全年累计唐鱼种群数量及结构特征见图 3。唐鱼种群数量空间分布在各溪段均表现出相同的规律,主要分布在上段、中段、下段的缓流区和水坑处,分别占48%~63%和29%~47%,而在急流区的数量较少,占1%~8%。
|
| 图 3 塘肚溪上、中、下段不同流速区域唐鱼数量和年龄组成 Fig. 3 Population size and age composition of Tanichthys albonubes at different current velocities in Tangdu Stream |
| |
从不同生活史阶段来看,上段仔、稚鱼的数量较大,下段以幼鱼和仔、稚鱼居多,而中段则各个生活史阶段的唐鱼数量接近。从不同流速区域看,上段、中段、下段的急流区、水坑、缓流区均有成鱼分布,而幼鱼和仔、稚鱼则主要分布在水坑和缓流区。
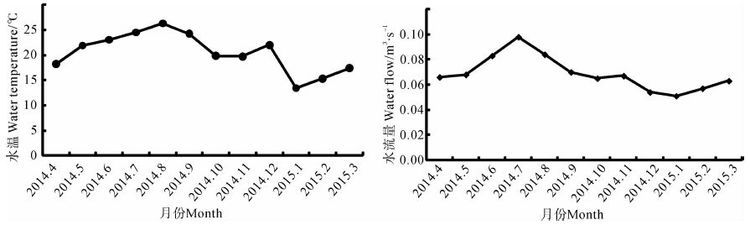
2.3 水温和水流量的周年变化塘肚溪水温、水流量周年变化见图 4。水温全年变化范围在13.4 ℃~26.4 ℃,最低水温出现在1月,最高水温出现在8月。水流量季节变化明显,最大水流量出现在7月,约为0.098 m3·s-1,最小水流量出现在1月,约为0.051 m3·s-1。
|
| 图 4 塘肚溪水温及水流量周年变化 Fig. 4 Annual variation of water temperature and water flow in Tangdu Stream |
| |
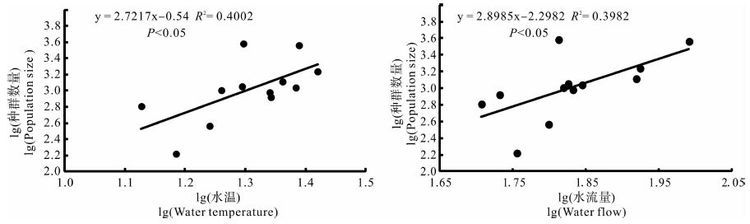
对每月全溪唐鱼种群总数量与对应月份的水温、水流量数据以lg转换后分别进行回归分析,发现水温或水流量年变化均与唐鱼种群数量变化呈显著线性正相关(P<0.05)(图 5)。
|
| 图 5 唐鱼种群数量与水温、水流量的关系 Fig. 5 Relationship between population size of Tanichthys albonubes and water temperature,water flow |
| |
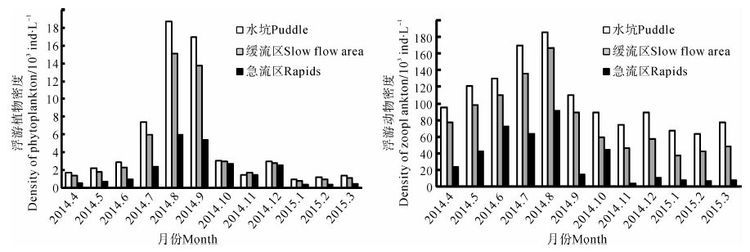
全溪不同流速采样点浮游生物密度周年变化见图 6。急流区、缓流区、水坑的浮游生物丰度周年变化均表现为先升高后降低,8月达到最高峰(浮游植物132.6×103 ind·L-1,浮游动物148 ind·L-1),1月或2月降到最低值(浮游植物6.81×103 ind·L-1,浮游动物37 ind·L-1)。无论哪个月份,浮游植物的数量分布均表现为水坑最多,缓流区次之,急流区最少,即随流速增大,浮游植物密度减少。水坑浮游植物密度分别为缓流区的1.2(0.9~1.2)倍和急流区的2.6(1.0~3.1)倍。浮游动物数量的空间分布趋势与浮游植物类似,即表现为流速越大,浮游动物密度越小。水坑浮游动物密度分别为缓流区和急流区的1.4(1.1~1.8)倍和7.3(1.8~24.7)倍。
|
| 图 6 塘肚溪不同流速区域采样点浮游生物密度周年变化 Fig. 6 Annual variation of plankton density at different current velocities in Tangdu Stream |
| |
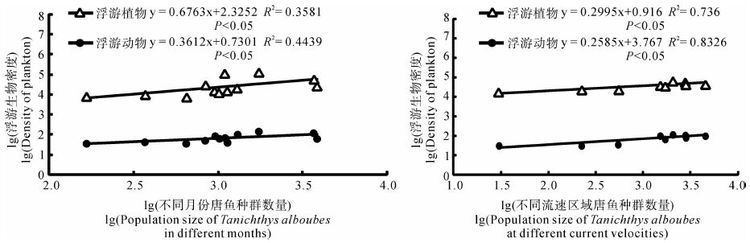
对各月份全溪唐鱼总数量与对应月份全溪不同区域浮游生物平均密度数据以lg转换后进行回归分析,发现无论浮游植物或浮游动物,其不同月份密度变化均与唐鱼种群数量变化呈显著线性正相关(P<0.05)(图 7:A)。对各流速区域唐鱼全年累加数量与对应流速区域浮游生物月平均密度数据进行同样处理和回归分析,发现无论浮游植物或浮游动物,其不同流速区域密度变化均与对应区域唐鱼种群数量变化呈显著线性正相关(P<0.05)(图 7:B)。
|
| 图 7 塘肚溪唐鱼种群数量与浮游生物密度的关系 Fig. 7 The relationship between population size of Tanichthys albonubes and plankton density in Tangdu Stream |
| |
本次调查结果显示,从化塘肚溪唐鱼种群数量在冬季后开始上升,7月达到最大值后下降,在10月又回升出现另一个数量高峰,随后逐步下降,至2月达到全年最低值;空间特征则表现为唐鱼主要分布在各溪段的缓流区和水坑处,而急流区数量较少。唐鱼种群数量的时空分布格局可能与水温、水流及饵料生物密度的变化有关。
鱼类种群变化与繁殖活动密切相关,因此温度可以通过影响鱼类繁殖活动而最终影响其种群数量与结构的变化。唐鱼作为亚热带鱼类,其繁殖活动需要相对较高的温度。陈国柱等(待发表)在实验室可控条件下研究发现,当水温高于14 ℃时,唐鱼开始产卵,而当水温下降到14 ℃以下时,大部分雌鱼不再产卵,即使产卵,数量也很少,且绝大多数卵不能正常完成胚胎发育,因此,14 ℃是唐鱼繁殖的温度阈值。本次调查显示塘肚溪水温全年变化范围在13.4 ℃~26.4 ℃,最低水温出现在1月,最高水温出现在8月。在1—2月,唐鱼种群数量最少,且未发现仔、稚鱼,这可能是由于1—2月塘肚溪流水温已低于14 ℃,唐鱼停止了繁殖活动的缘故。结合易祖盛等(2004)和史方等(2008)的研究报道,可以基本确认从化地区唐鱼的繁殖期为3—12月。另外,从年龄组成的周年变化规律看,7月和10月唐鱼仔、稚鱼数量及其所占比例最高,种群数量形成2个高峰,故此可推测塘肚溪唐鱼的繁殖盛期为7月和10月。另一方面,由于唐鱼繁殖盛期恰好处于溪流丰水期,而冬季为枯水期,唐鱼停止繁殖,因此水流量大小也与唐鱼种群数量呈正相关。
鱼类的摄食、生长、发育和繁殖也与水流速度密切相关(李秀明,2013;穆小平等,2015),因此水流也能影响鱼类种群的空间分布。唐鱼为溪流鱼类,具有一定的逆流游泳能力,但由于个体小,其绝对游泳能力并不强(刘明中等,2014)。本次调查中,塘肚溪上段、下段唐鱼数量明显多于中段,这种现象尤其在仔、稚鱼的分布上表现得更为明显。而在各溪段,唐鱼主要分布在缓流区和水坑处,而急流区唐鱼数量较少,且主要以成鱼和幼鱼为主。这可能与溪流不同区域流速大小不同有关。塘肚溪中段水坑数、障碍物和杂草少,导致其整体水流速度大于上段和下段,不利于唐鱼生长和繁殖,因此中段唐鱼种群数量最少。而与成鱼和幼鱼相比,仔、稚鱼的鱼鳍较稚嫩,甚至还未发育完全,故游泳能力弱,因此在高流速区域分布显著减少。而唐鱼成鱼的临界游泳速度约为0.3 m·s-1,能够逆流穿越流速为0.5 m·s-1、坡度为10%的溪段(徐采等,待发表),因而成鱼在急流区亦能生存。
浮游生物是鱼类的重要饵料之一。唐鱼为杂食性小型溪流鱼类,主要摄食藻类、浮游动物和水生昆虫(陈宜瑜,1998;易祖盛等,2004;程炜轩等,2006)。本研究显示,无论浮游植物或浮游动物的密度均与唐鱼种群数量呈显著正相关。然而从两者数量的时间变化看,尽管浮游生物密度的周年变化规律与唐鱼种群数量的变化趋势大致相同,但两者并不完全同步,具体表现在7月和10月由于仔、稚鱼数量的剧增导致唐鱼种群密度形成2个峰值,而浮游生物数量在7月和10月变化并不明显。由于两者峰值并不重叠,因此繁殖盛期唐鱼仔、稚鱼面临较大的觅食压力,相对较少的浮游生物量不能满足唐鱼种群特别是仔、稚鱼的摄食需求,最终致其死亡率增高,这可能是在接下来的8月和11月其种群中的幼鱼数量没有明显增加的主要原因。
本研究通过选取特定的溪段和特殊的采样方法初步掌握了濒危动物——唐鱼的种群数量和结构的时空变化规律及其影响因素。塘肚溪唐鱼种群时空变化明显,并受到水温、水流和浮游生物的影响。其中水温和水流量影响唐鱼种群的时间变化,流速则影响唐鱼的空间分布,而浮游生物密度与唐鱼数量的时空变化都有密切的关系。但由于采样区域和条件的限制,种群数量和年龄结构的数据可能存在一定的偏差。关于唐鱼种群时空格局更为详实的变化规律,还有待进一步的研究。
 2016, Vol. 35
2016, Vol. 35




