

2. 中山大学附属第一医院 中医科, 广东 广州 510080;
3. 广州中医药大学 中药学院, 广东 广州 510006
2. Dept of Traditional Chinese Medicine, the First Affiliated Hospital, Sun Yat-sen University, Guangzhou 510080, China;
3. College of Traditional Chinese Medicine, Guangzhou University of Chinese Medicine, Guangzhou 510006, China
目前,大剂量化疗是治疗恶性肿瘤的一种重要手段并已广泛应用于临床。5-FU利用抑制胸腺嘧啶核苷酸合成酶活性来抑制脱氧核糖核酸合成。它是目前使用非常广泛的嘧啶类抗癌药物,但随着化疗的推进,出现了严重的毒副作用。在细胞中转化为核苷酸后,它优先被肿瘤和分裂活性组织吸收,因此,5-FU在快速杀灭肿瘤细胞的同时,对人体中处于活跃分裂状态的细胞也具有极大的杀伤力。BMSCs是成体干细胞的一种,具有强大的自我增殖能力和多向分化潜能[1]。BMSCs的这种特性,使其处于一种活跃分裂状态,也正是由于这种特性使其在化疗过程中容易成为5-FU“误伤”的对象,从而引发严重的骨髓抑制毒副作用[2]。因此,研发可保护处于快速增殖状态的干细胞免受化疗药物攻击从而减轻肿瘤患者化疗毒副作用的药物或者方法是非常有必要的。
从已有的报道来看,在中医上具有“补肾”、“壮阳”、“补气”、“补血”等补益作用的多种中药或单味中药的有效成分、含有药物的血清和复方中药能够促进BMSCs在体外的增殖[3-4],抑制其凋亡或诱导其分化[5-6],部分药物甚至兼具多种作用。例如,黄芪和人参皂苷不但可以促进BMSCs的增殖生长,而且还可以抑制凋亡[7]。
ICA是一种异黄酮化合物,它是淫羊藿的主要有效成分。现代药理学实验表明,ICA具备了抗肿瘤、抗炎、抗氧化、促进成骨、增强免疫功能、改善心血管和脑血管功能、调节内分泌等多种药理作用,是近几年来国内外研究比较热门的中药单体。有研究证明,ICA能够促进BMSCs增殖与分化[8-10]、还能够在一定程度上抑制BMSCs凋亡,对抗有害因素给细胞造成的损伤,保护细胞及其部分特性[11]。本文通过研究ICA对5-FU诱导的大鼠BMSCs损伤的影响,探讨ICA对5-FU所致大鼠BMSCs损伤的保护作用及其机制,为中西医结合防治临床肿瘤化疗引起的骨髓抑制及相关疾病提供实验依据与理论指导。
1 材料与方法 1.1 动物4周龄SD ♂大鼠,SPF级,体质量为(80~90) g,购自广州中医药大学实验动物中心,使用许可证号:SYXK(粤)2018-0085,购入后直接用于取材,原代BMSCs培养。
1.2 药物试剂ICA(icariin,中国食品药品检定研究院);5-氟尿嘧啶(Solarbio公司,1126A023);SD大鼠BMSCs专用培养基(Cyagen公司,T161122G001)、胰蛋白酶(Gibco公司,19521H12);单克隆抗体CD90、CD45(Santa Cruz公司,sc-19615、sc-18914),caspase-3抗体(Abcam公司,ab2302);NOS测定试剂盒、Annexin V-FITC/PI双染试剂盒(南京建成生物工程研究所,20161019、20161025);Hoechst 33258试剂盒、caspase-3活性检测试剂盒(碧云天生物技术);其他试剂均为国产分析纯。
1.3 仪器超净工作台(苏州名牌之星净化台);二氧化碳培养箱(上海力申科学仪器有限公司);倒置显微镜(Olympus);荧光细胞成像显微镜(美国Bio-Rad公司);紫外可以分光光度计(日本岛津公司);分析天平(梅特勒公司);流式细胞分析仪(美国BD公司);Elx800型酶标仪(美国Biotek公司);Experion型蛋白印记电泳系统(美国Bio-Rad公司),多功能酶标仪(美国PerkinElmer公司)。
2 方法 2.1 BMSCs的取材、分离培养及纯化SD大鼠处死,双侧股骨和胫骨在无菌状态下分离,剪断骨膜末端,露出骨髓腔。用基础培养液冲洗骨髓腔,将收集的细胞液800 r·min-1,离心8 min,弃上清,沉淀加入完全培养液,反复吹打均匀后转移至培养瓶中,37 ℃、5% CO2培养箱培养24 h后换液,之后每2 d换液一次。当细胞生长融合达80 %~90 %时,胰酶消化,1 : 2传代。
2.2 BMSCs的流式鉴定胰酶消化收集细胞并制成单细胞悬液,调整细胞数目1×109个/L,每管加入300 μL细胞悬液,分别加入抗体CD45-FITC、CD90-PE及同型对照抗体各5 μL,孵育30 min后,PBS洗涤重悬,过筛,上流式细胞仪进行测定。
2.3 实验分组及给药实验根据随机对照的原则分为3组:①空白对照组(正常组):无特殊处理。②单用5-FU组(模型组):5-FU的质量浓度为2.5×10-2 g·L-1 (5-FU对大鼠BMSCs IC50值)。③5-FU +ICA共同作用组(实验组):MTT实验中ICA的浓度为5、10、20、40、80 μmol·L-1,Hoechst 33258染色、Annexin V-FITC/PI,Western blot实验中ICA的浓度为10和20 μmol·L-1。
2.4 MTT法检测细胞存活率对数期细胞接种于96孔培养板,培养过夜后,按分组给药。培养48 h后,每孔加入MTT(5 g·L-1)20 μL,继续培养4 h,除去培养液,每孔加入150 μL DMSO,摇床振荡10 min后,于酶标仪492 nm波长处读取吸光值。取5孔吸光度(A)值的均数,按公式计算细胞存活率。
细胞存活率/%=(实验孔A均值-空白孔的A均值)/(对照孔A均值-空白孔的A均值)×100 %
2.5 大鼠BMSCs凋亡过程细胞核形态检测接种对数期细胞于6孔板内并继续培养过夜,根据预先设置给药,48 h后,吸去上清液,加入0.5 mL固定溶液。4 ℃固定,PBS洗涤细胞后,加入0.5 mL Hoechst 33258染色溶液,染色5 min后,PBS洗涤2次。加入抗荧光猝灭封闭液并混匀,于荧光显微镜下观察检测细胞核。
2.6 大鼠BMSCs凋亡过程流式检测按实验分组及给药48 h后,将细胞上清培养液吸入离心管,贴壁细胞PBS洗涤、胰酶消化并收集至上述离心管中,1 000 r·min-1离心5 min,除去上清液,收集沉淀并用PBS洗涤1次。按照Annexin V-FITC/PI试剂盒步骤对细胞进行处理,然后上机检测,以分析不同凋亡阶段的细胞,并进行各组间的比较。
2.7 Western blot法检测Cleaved caspase-3蛋白水平以及caspase-3活性检测试剂盒检测caspase-3酶活性6孔板内,种入细胞培养过夜,按实验分组及给药,48 h后,消化收集并裂解细胞,收集蛋白质样品并予以定量。经电泳、转膜、封闭后;再经一抗(1 : 1 000)、二抗(1 : 5 000)孵育,ECL化学荧光发光反应,将膜放至暗盒,显影、定影。灰度扫描仪扫描条带,并使用Bandscan 4.30软件分析条带的光密度值。蛋白质的相对表达由目标蛋白质光密度值/内参蛋白光密度值表示。
按“2.2”的实验分组和给药,处理48 h后,离心收集细胞,PBS洗涤,冰浴裂解,取上清液进行caspase-3酶活性检测。按照试剂盒步骤在反应体系中依次加入检测缓冲液、样品,适当混匀,随后再加入10 μL Ac-DEVD-pNA(2 mmol·L-1),37 ℃孵育。当颜色变化比较明显时即可于酶标仪405 nm处测定各组样品的吸光度(A)值,将样品A值代入pNA标准曲线即可计算出各组样品caspase-3催化产生的pNA量。pNA的量/样品蛋白含量即为单位重量蛋白所含caspase-3的酶活力单位,实验重复3次。
2.8 NOS试剂盒检测NOS含量按“2.2”的实验分组和给药,处理48 h后,每组取细胞上清液200 μL,分别用于TNOS和iNOS含量检测。根据NOS测定试剂盒操作步骤:TNOS测定,空白管和测定管分别加入双蒸水、双蒸水和细胞上清液各100 μL;iNOS测定,空白管和测定管分别加入双蒸水和试剂六各100 μL、细胞上清液和试剂六各100 μL。所有试管置于试管架并摇匀,各管分别依次加入试剂一、二、三,混匀,37 ℃水浴15 min,各管依次加入试剂四、五,混匀,以蒸馏水调零于530 nm处测定各管吸光度值。
2.9 统计学处理应用GraphPad Prism 7.0对实验结果进行统计分析,实验结果均使用x±s, n表示,两组之间采用单向ANOVA检验分析。
3 结果 3.1 BMSCs的形态观察本实验采用全骨髓培养法,根据干细胞生长特性来分离、提纯BMSCs。刚取材培养的细胞呈球形悬浮于培养液,并混有少量血细胞等杂质细胞。接种后的24 h内,大量细胞被贴壁情况良好,但是有少量血细胞附着在培养瓶壁上,能够通过更换培养液逐渐去除。3 d后,贴壁细胞明显增加,并以纺锤体或多边形形态增殖,分布不均,形成多个增殖群。如Fig 1所示,在7~14 d后,细胞逐渐聚合,能够传代。
|
| Fig 1 Morphology of BMSCs on 8th day under primary culture (×200) |
第3代细胞的流式细胞仪检测结果表明,纯化培养的BMSCs均一表达CD90,阳性率为99.7%,而CD45阳性率仅为1.59%,呈阴性,表明本实验分离培养的细胞确为BMSCs,见Fig 2。

|
| Fig 2 Surface marker expression of BMSCs |
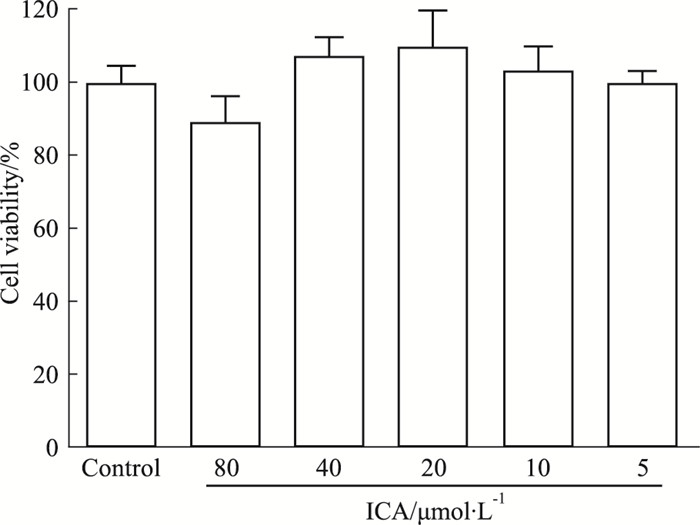
用5、10、20、40和80 μmol·L-1 ICA作用大鼠BMSC 48 h后,大鼠BMSCs的存活率分别为(99.7±2.80) %、(103.1±6.20) %、(107.6±9.98) %、(107.3±4.42) %和(89.0±6.49) %。与对照组(99.9±4.20) %比较,5 μmol·L-1 ICA对大鼠BMSCs的增殖无明显影响,10、20、40 μmol·L-1 ICA可一定促进大鼠BMSCs增殖,而80 μmol·L-1 ICA则对大鼠BMSCs具有一定的细胞毒性作用,可抑制大鼠BMSCs的增殖,见Fig 3。
|
| Fig 3 Effect of different concentrations of ICA on proliferation of BMSCs (x±s, n=5) |
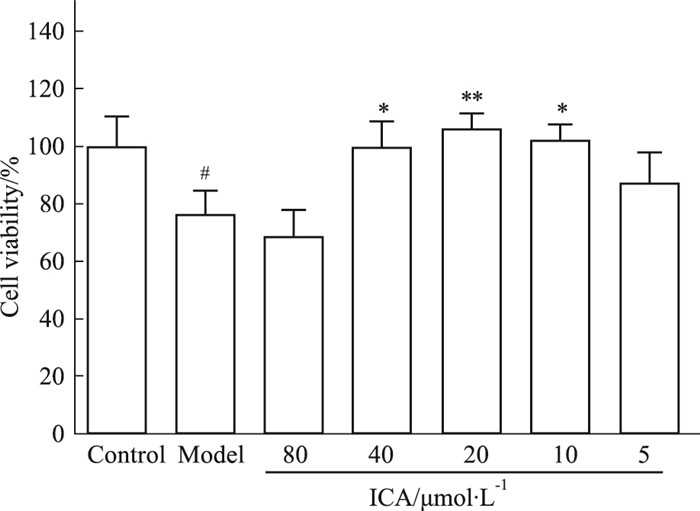
由Fig 4可知:与正常对照组相比,模型组细胞活性明显下降。与模型组相比,ICA给药组细胞活性显著增加,说明ICA对5-FU抑制BMSCs增殖有明显的拮抗作用。5 μmol·L-1 ICA组有一定拮抗作用,但是较弱,10、20、40 μmol·L-1 ICA组可明显拮抗,其增殖率接近甚至高于正常对照组,而80 μmol·L-1 ICA组增殖率低于模型组,可能是因为其对大鼠BMSCs细胞毒性作用与5-FU的损伤作用相叠加,显著抑制了大鼠BMSCs的增殖。
|
| Fig 4 Effect of different concentrations of ICA on proliferation of BMSCs injured by 5-FU (x±s, n=5) #P < 0.05 vs control; *P < 0.05, **P < 0.01 vs 5-FU model |
Hoechst 33258是一种核酸染料,可以穿透细胞膜并与细胞核DNA相互嵌合。正常细胞的膜膜完整性较好,染色质分布均匀,因此在荧光显微镜下可见正常细胞的细胞核呈现均一的淡蓝色;凋亡细胞膜通透性增强,染色体DNA固缩甚至断裂,因而细胞核呈致密浓染亮蓝色或颗粒状荧光。在荧光显微镜下,正常对照组中BMSCs的染色质以扩散均匀的低强度荧光均匀分布(Fig 5A)。5-FU模型组中的BMSCs具有大量细胞凋亡,细胞核致密或粒状荧光(Fig 5B),细胞数量明显低于正常组。而与模型组比较,10、20 μmol·L-1 ICA组内的大鼠BMSCs细胞核致密或颗粒荧光的细胞数量均有降低,大多数细胞呈弥散均匀的低强度荧光(Fig 5C、D),趋向正常组。初步表明,5-FU具有促进大鼠BMSCs凋亡的作用,ICA可抑制5-FU诱导的大鼠BMSCs的凋亡。

|
| Fig 5 Apoptosis morphology of BMSCs in different groups (Hoechst 33258, Bar=25μm) A:Control; B:5-FU; C:5-FU+ICA10 μmol·L-1; D:5-FU+ICA20 μmol·L-1 |
为了确定ICA对BMSCs的抗凋亡作用,根据“3.4”的实验结果,本实验进一步检测10、20 μmol·L-1ICA组对5-FU化疗损伤大鼠BMSCs细胞凋亡率的情况。Annexin V-FITC凋亡检测试剂盒测定结果发现:相对于对照组,模型组早晚期凋亡率均显著升高;10、20 μmol·L-1ICA干预后,与模型组相比,两组BMSCs早期和晚期凋亡率均显著减少,差异存在统计学意义(P < 0.01),见Fig 6。

|
| Fig 6 Effect of ICA on cell apoptosis induced by 5-FU in BMSCs detected by flow cytometry (x±s, n=3) ##P < 0.01 vs control; **P < 0.01 vs 5-FU model |
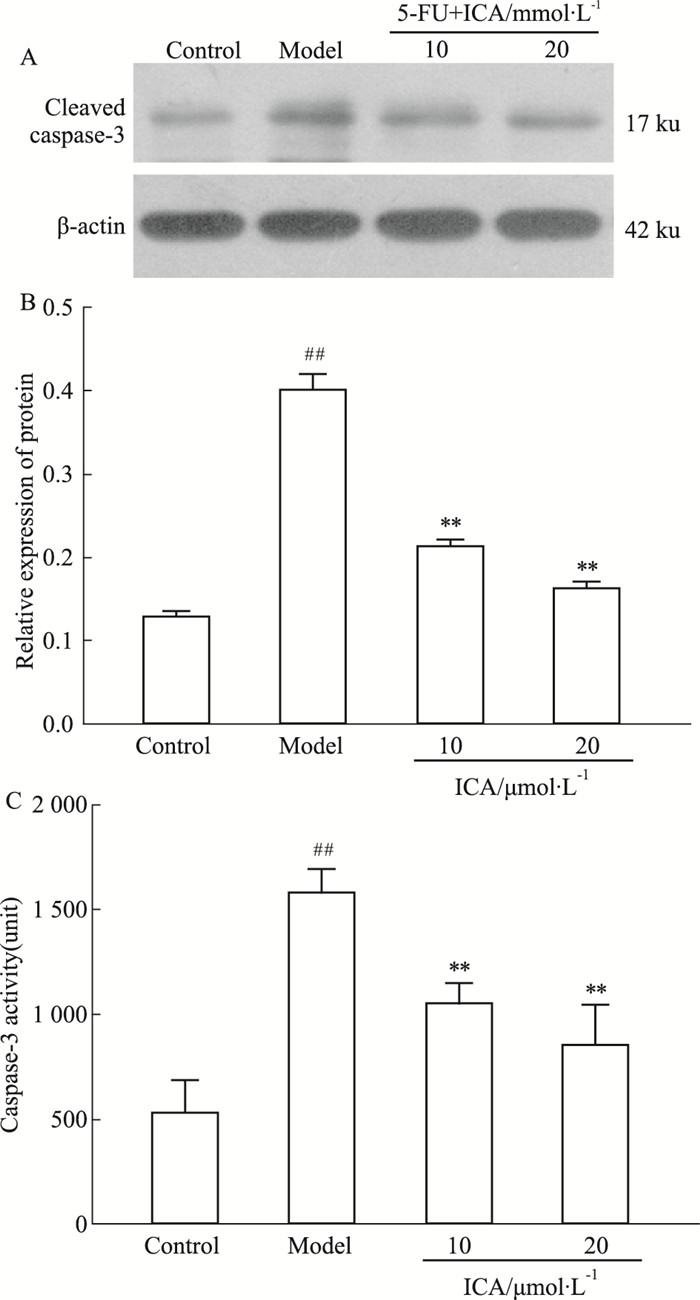
蛋白免疫印迹分析显示(Fig 7A、B):ICA处理组的Cleaved caspase-3蛋白表达水平比模型组要低,甚至基本接近正常组(P < 0.01)。分光光度法检测各组caspase-3活性,结果显示,与正常对照组比较,模型组细胞caspase-3活性明显升高,ICA实验组caspase-3活性与模型组比较明显降低(P < 0.05),如Fig 7C。提示ICA其对BMSCs的保护作用可能与抑制caspase-3的活化有关。
|
| Fig 7 Effects of ICA on cleaved caspase-3 expression and caspase-3 activity of BMSCs injury induced by 5-FU (x±s, n=3) ##P < 0.01 vs control; **P < 0.01 vs 5-FU model |
|
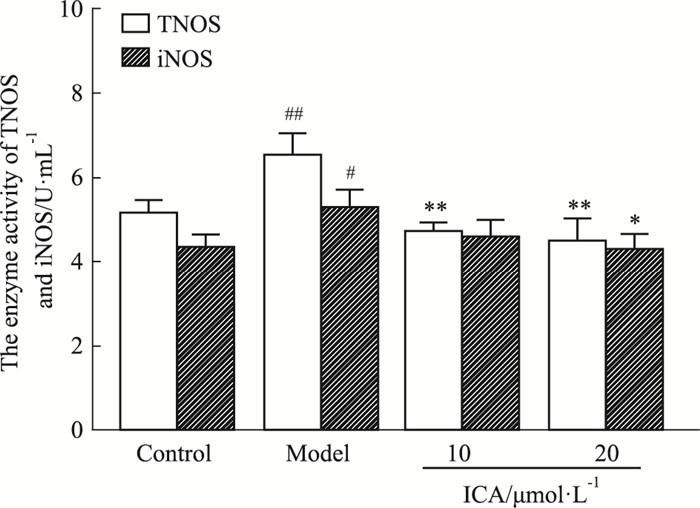
| Fig 8 Effects of ICA on enzyme activity of TNOS and iNOS of BMSCs injury induced by 5-FU (x±s, n=3) #P < 0.05, ##P < 0.01 vs control; *P < 0.05, **P < 0.01 vs 5-FU model |
从实验结果来看,和正常对照组相比,模型组细胞上清液iNOS活性明显高于正常对照组,分别加入10 μmol·L-1和20 μmol·L-1 ICA干预后,实验组iNOS活力与模型组比较显著下降(P < 0.05)。TNOS呈现相同的变化趋势,提示5-FU化疗损伤是可能是通过激活NOS引起NO的增加,从而通过NO通路促使BMSCs的凋亡。而ICA是降低了NOS的表达,抑制NO生成,从而达到保护BMSCs损伤的效果。
4 讨论5-FU是目前在临床上使用非常广泛的抗嘧啶药物,对消化道癌症等实体瘤具有非常好的效果,在肿瘤的医学治疗里面发挥着重要作用。但是其毒性呈剂量依赖性,高剂量化疗不仅能杀死肿瘤细胞,而且还能出现骨髓抑制的副作用,它不只是损害造血细胞,还损害BMSCs。BMSCs的损伤会影响化疗后受抑骨髓的造血恢复,增加患者的临床风险。中药作为一种辅助化疗药物,在肿瘤治疗中拥有特殊的优势,特别是在减轻化疗药物的毒副作用、提升化疗药物的疗效与患者化疗前后的生活品质等方面具有显著的效果。联合用药可以有效降低化疗药物给身体带来的影响。
本研究MTT实验结果初步表明,一定浓度的ICA可促进大鼠BMSCs增殖对5-FU抑制BMSCs增殖有明显的拮抗作用。Hoechst 33258荧光染色和Annexin V-FITC凋亡检测结果显示:用ICA处理过的BMSCs,凋亡细胞以及凋亡率相比模型组有明显的降低,初步说明ICA可抑制5-FU化疗损伤诱导的BMSCs凋亡的发生,对BMSCs具有保护作用。caspase-3是细胞凋亡过程中最关键的执行分子之一,caspase-3的激活常被作为细胞凋亡的一个重要指标。模型组的Cleaved caspase-3的蛋白表达水平比加ICA干预实验组的caspase-3明显要高。由此实验结果表明,5-FU通过激活caspase-3来实现诱导BMSCs凋亡从而造成化疗损伤,ICA可通过抑制caspase-3的活化,从而起到保护BMSCs的作用。
一氧化氮(nitric oxide,NO)是人体内细胞间信息传递的重要调节因子,它能够调节体内能量代谢、细胞凋亡、炎症和其他的关键途径[12]。在体内,NOS是体内催化L-精氨酸生成NO的关键酶。目前已知的NOS主要类型有4种,介导NO合成的限速酶是iNOS[13]。在正常条件中iNOS并不会表达或者少量表达,不过,在病理或者药物作用下,细胞能够诱导它们的合成,iNOS一旦合成,即可大量生成NO。这些NO能导致大量的ROS产生,ROS可以引起脂质过氧化[14],造成细胞的氧化损伤,这说明NOS的表达和活性与细胞的增殖凋亡有关。ICA是一种异黄酮化合物,其抗氧化作用主要与其清除活性氧自由基有关。本研究结果显示:5-FU可诱导BMSCs细胞内TNOS、iNOS活性升高,而ICA共处理组细胞内TNOS、iNOS酶活性相比模型组降低,表明ICA具有抑制BMSCs细胞内TNOS、iNOS酶活性的作用,从而减少NO的生成,抑制细胞凋亡,保护BMSCs的作用。综上所述,本研究表明一定浓度的ICA可促进BMSCs增殖,拮抗5-FU引起的BMSCs增殖抑制作用,这种拮抗作用可能是通过降低BMSCs细胞内NOS活性,减少NO的生成,抑制caspase-3的激活,从而抑制5-FU诱导的细胞凋亡的发生,达到保护BMSCs的作用。
| [1] |
Ohishi M, Schipani E. Bone marrow mesenchymal stem cells[J]. J Cell Biochem, 2010, 109(2): 277-82. |
| [2] |
Prata Kde L, Orellana M D, De Santis G C, et al. Effects of high-dose chemotherapy on bone marrow multipotent mesenchymal stromal cells isolated from lymphoma patients[J]. Exp Hematol, 2010, 38(4): 292-300. doi:10.1016/j.exphem.2010.01.006 |
| [3] |
王力, 吴鑫, 卢新政, 等. 人参皂苷Rg1对培养大鼠骨髓间充质干细胞增殖影响的机制研究[J]. 中国药理学通报, 2007, 23(1): 1480-4. Wang L, Wu X, Lu X Z, et al. The mechanisms of Ginsenosides Rg1 on the proliferation of bone marrow stromal cells[J]. Chin Pharmacol Bull, 2007, 23(1): 1480-4. |
| [4] |
李庆双, 郑关毅, 张碧琴, 等. 毛冬青甲素对大鼠骨髓间充质干细胞增殖及迁移的影响[J]. 中国药理学通报, 2018, 34(3): 358-64. Li Q S, Zheng G Y, Zhang B Q, et al. Effect of ilexonin A on proliferation and migration of bone mesenchymal stem cells in rats[J]. Chin Pharmacol Bull, 2018, 34(3): 358-64. doi:10.3969/j.issn.1001-1978.2018.03.013 |
| [5] |
翟远坤, 王鸣刚, 李志忠, 等. 淫羊藿苷含药血清对体外培养骨髓间充质干细胞增殖及成骨性分化的影响[J]. 中华中医药杂志, 2012, 27(2): 480-4. Zhai Y k, Wang M G, Li Z Z, et al. Effects of the serum of rats administered icariin on the proliferation and osteogenic differentiation of rBMSCs in vitro[J]. Chin J Tradit Clin Med Pharm, 2012, 27(2): 480-4. |
| [6] |
武密山, 赵素芝, 任立中, 等. 川续断皂苷Ⅳ诱导大鼠骨髓间充质干细胞向成骨细胞方向分化的研究[J]. 中国药理学通报, 2012, 28(2): 222-6. Wu M S, Zhao S Z, Ren L Z, et al. Experimental study of akebia saponin D on the differentiation of rat bone marrow derived mesenchymal stem cells to osteoblasts in vitro via induction[J]. Chin Pharmacol Bull, 2012, 28(2): 222-6. doi:10.3969/j.issn.1001-1978.2012.02.017 |
| [7] |
方健康, 周轶平, 李玛琳. 中药对骨髓间充质干细胞增殖、凋亡及分化的影响研究进展[J]. 中国中药杂志, 2014, 39(15): 2834-7. Fang J K, Zhou Y P, Li M L. Research progress on effects of traditional chinese medicines on proliferation, apoptosis and differentiation of bone marrow mesenchymal stem cells[J]. Chin J Chin Mater Med, 2014, 39(15): 2834-7. |
| [8] |
盛华刚. 淫羊藿苷对细胞增殖作用的研究进展[J]. 化工时刊, 2013, 27(8): 32-4. Sheng H G. Advances in research of icariin on cell proliferation[J]. Chem Ind Times, 2013, 27(8): 32-4. doi:10.3969/j.issn.1002-154X.2013.08.011 |
| [9] |
张黎声, 韩小晶, 罗志荣, 等. 淫羊藿苷对大鼠骨髓间充质干细胞迁移作用的影响[J]. 中国中医药信息杂志, 2017, 24(2): 44-8. Zhang L S, Han X J, Luo Z R, et al. Effects of icariin on migration of mesenchymal stem cells of rat bone marrow[J]. Chin J Inform Tradit Clin Med, 2017, 24(2): 44-8. doi:10.3969/j.issn.1005-5304.2017.02.013 |
| [10] |
刘韶英.淫羊蕾苷对骨髓间充质干细胞增殖及向心肌细胞分化的影响[D].北京: 北京中医药大学, 2008. Liu S Y. Effects of icariin on proliferation and differentiation of cardiomyocytes from bone marrow mesenchymal stem cells[D].BeiJing: Beijing Univ Chin Med, 2008. |
| [11] |
杨智洋.淫羊藿苷联合四环素对糖皮质激素诱导的大鼠骨髓间充质干细胞损害的保护作用[D].辽宁: 辽宁医学院, 2012. Yang Z Y. Protection of icariin and tetracycline on the impairment of rat bone mesenchymal stem cells induced by glucocorticoid in vitro[D] LiaoNing: Liaoning Med College, 2012. http://cdmd.cnki.com.cn/Article/CDMD-10160-1013132323.htm |
| [12] |
Mayhan W G, Anick D M, Sharpe G M, et al. Nitric oxide synthase dependent responses of the basilar artery during acute infusion of nicotine[J]. Nicotine Tob Res, 2009, 11(3): 270-7. doi:10.1093/ntr/ntn025 |
| [13] |
Higashi Y, Noma K, Yoshizumi M, et al. Endothelial function and oxidative stress in cardiovascular diseases[J]. Circ J, 2009, 73(3): 411-8. doi:10.1253/circj.CJ-08-1102 |
| [14] |
Zakizadeh E, aghihimani E, Saneei P, et al. The effect of purslane seeds on biomarkers of oxidative stress in diabetic patients: A randomized controlled cross-over clinical trial[J]. Int J Prev Med, 2015, 6(1): 95. doi:10.4103/2008-7802.166505 |

