

亚健康是指人体处于健康和疾病之间的状态,已成为公共卫生的重要问题之一。疲劳是其最常见的临床表现,因而疲劳性亚健康是亚健康的主要类型[1]。疲劳性亚健康是指以疲劳为主要表现,持续或反复发作达3个月,并排除其他如癌症、抑郁症等可能使机体疲劳的疾病,表现为处于生理性和病理性的中间状态。目前认为,此种状态的发生与工作生活失衡、心理压力大和生活方式不良等多种因素有关,可表现出失眠多梦、精力不足、情绪紊乱等,严重影响个体的生活质量与工作状态[2]。
疼痛与许多递质有关。作为一种重要的神经递质,5-羟色胺(5-hydroxytryptamine, 5-HT)在中枢和外周神经系统的疼痛信息调制过程中起着重要作用。研究表明,5-羟色胺2 A受体参与疼痛的发生、发展[3];糖皮质激素皮质醇(glucocorticoid, GC)可以通过减少与痛觉信息传递相关的神经肽,抑制痛觉信息传递,从而起到镇痛、提升痛阈的作用[4];Kim等[5]发现,通过移除一种产生多巴胺(dopamine, DA)的A 11神经元,慢性疼痛会明显减轻,说明了DA可以促进慢性疼痛。而疲劳状态会引起这些与疼痛有关的递质发生一定变化:5-HT含量明显增高;下丘脑-垂体-肾上腺轴功能亢进,直接促使GC含量增高;DA含量明显降低[6]。综上所述,在疲劳性亚健康状态下,递质的变化可以影响机体的疼痛敏感性,但缺乏具体定论。本研究采用疲劳性亚健康小鼠为实验动物模型,通过动物行为学实验,观察疲劳性亚健康对机械痛敏和热痛敏的影响。
1 材料与方法 1.1 材料 1.1.1 实验动物清洁昆明种小鼠40只,♀♂不拘,体质量(25±5)g,由徐州医科大学实验动物中心提供,生产许可证号:SCXK(苏)2015-0009。
1.1.2 仪器YSL-500疲劳转棒仪(上海软隆公司);血细胞计数仪(深圳迈瑞生物医疗公司);Von Frey测痛毛刷(West Coast公司);IITC series8型热辐射刺激仪(美国IITC公司)。
1.2 实验分组与疲劳性亚健康模型的制备随机将小鼠分为2组,正常对照组(control组)和疲劳性亚健康组(fatigue组),每组10只。为避免相互影响,分批次测定小鼠机械缩足反射阈值(paw withdrawal mechanical threshold, PWMT)与热缩足潜伏期(paw withdrawal thermal latency, PWTL)。采用小鼠水中站立的方法,强迫疲劳性亚健康组小鼠在水中连续站立9 d,每天8 h,建立疲劳性亚健康模型[7]。
1.3 生理状态观察模型建立前(d 0)、模型建立完成(d 9)以及恢复1周后(d 16),观察小鼠皮毛光泽与情绪状态。
1.4 转棒运动功能实验(Rota-rod test)d 0、9、16时,分别将小鼠放置于疲劳棒上,调节转棒速度为40周/分,测定小鼠跌落或被动连续旋转2周的时间,每只实验动物重复3次,每次间隔5 min,取平均值为结果。测试前,小鼠提前3 d以10周/分进行运动适应训练,每天20 min[8]。
1.5 血常规检查模型建立完成后,各组小鼠尾静脉采血,检测白细胞计数(WBC)、红细胞计数(RBC)、血红蛋白(HGB)、血细胞比容(HCT)、平均红细胞体积(MCV)、平均红细胞血红蛋白含量(MCH)、平均红细胞血红蛋白浓度(MCHC)、血小板数(PLT)、血小板平均体积(MPV)、血小板体积分布宽度(PDW)、血小板压积(PCT)等指标。
1.6 小鼠疼痛行为学测定 1.6.1 PWMT的测定d 0、9、16时,通过粗细不同的Von Frey细丝,根据Chen等[9]描述的方法,从0.16 g Von Frey探针开始,垂直刺激小鼠的右后足底。当小鼠受刺激出现缩足、抬腿,记做1次阳性反应。每组测量5次,当出现3次及以上阳性反应记做X,下一组测试更换为相邻细的Von Frey细丝,阳性反应出现小于3次记做O,下一组测试更换为相邻粗的细丝,完成各组测试后,根据公式得出阳性反应克数,为小鼠的PWMT。
1.6.2 PWTL的测定d 0、9、16时,用热痛刺激仪照射小鼠后足部,记录小鼠出现缩足回避时间。实验过程中保持热刺激强度不变,为防止对小鼠足底的损伤,设定截止时间为30 s,同侧足底照射间隔10 min。每只小鼠测5次,去掉最大值和最小值,计算3次的平均值为PWTL[10]。
1.7 统计学处理采用SPSS 16.0软件进行统计分析,各实验组数据采用t检验进行两样本均数间的比较,数据以x±s表示。
2 结果 2.1 小鼠生理状态变化d 0两组小鼠皮毛亮白,行为自如,情绪正常。d 9发现疲劳性亚健康组小鼠皮毛暗淡,情绪明显焦躁,易怒。d 16发现疲劳性亚健康组小鼠皮毛光亮,情绪平稳,与实验d 1无异;正常对照组小鼠行为情绪正常。
2.2 疲劳性亚健康对小鼠转棒运动功能的影响如Fig 1所示,d 0、16时,与正常对照组相比,疲劳性亚健康组小鼠在转棒上停留时间无明显差异;d 9时,与正常对照组相比,疲劳性亚健康组小鼠在转棒上停留时间明显缩短(P < 0.01),提示疲劳性亚健康组小鼠疲劳程度增加。

|
| Fig 1 Effects of fatigue-predominant subhealth on fatigue in mice(x±s, n=10) **P < 0.01 vs control group |
Tab 1结果显示,与正常对照组相比,疲劳性亚健康组小鼠各项血常规指标均无明显异常,即非疾病状态。
| Blood routine indicator | Control | Fatigue |
| WBC/109·L-1 | 10.86±1.00 | 10.75±0.95 |
| RBC/1012·L-1 | 8.65±0.77 | 8.91±0.54 |
| HGB/g·L-1 | 140.75±12.49 | 143.25±8.20 |
| HCT/% | 46.76±5.03 | 47.42±5.80 |
| MCV/fL | 53.19±1.79 | 54.44±1.88 |
| MCH/pg | 16.33±0.69 | 16.12±1.08 |
| MCHC/g·L-1 | 305.10±7.59 | 299.35±15.15 |
| PLT/109·L-1 | 556.90±116.06 | 499.65±122.50 |
| MPV/fL | 5.63±0.37 | 5.69±0.38 |
| PDW/% | 15.20±0.33 | 15.15±0.29 |
| PCT/% | 0.37±0.15 | 0.28±0.07 |
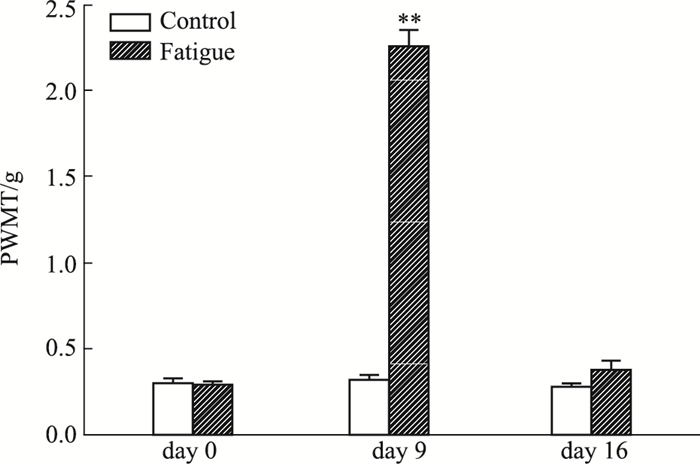
Fig 2结果显示,d 0、16时,与正常对照组相比,PWMT数值无明显差异;d 9时,与正常对照组相比,疲劳性亚健康组小鼠PWMT明显增加(P < 0.01),提示疲劳性亚健康组小鼠机械痛敏明显降低。
|
| Fig 2 Effects of fatigue-predominant subhealth on PWMT in mice(x±s, n=10) **P < 0.01 vs control group |
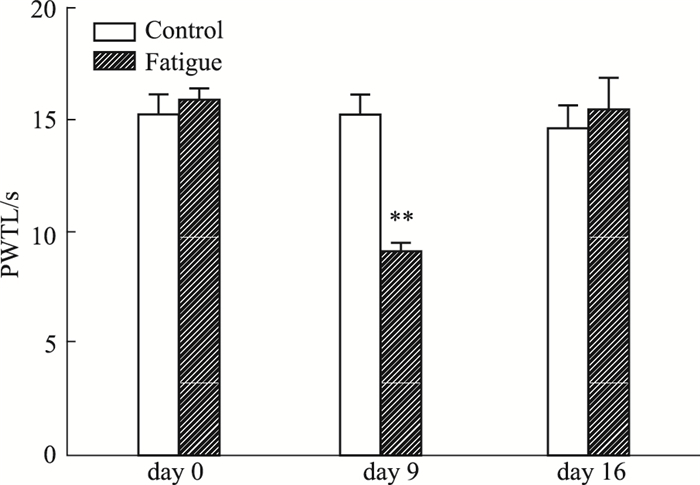
Fig 3结果显示,d 0、16时,与正常对照组相比,疲劳性亚健康组小鼠PWTL数值无明显差异;d 9时,与正常对照组相比,疲劳性亚健康组小鼠PWTL明显降低(P < 0.01),提示疲劳性亚健康组小鼠热痛敏增加。
|
| Fig 3 Effects of fatigue-predominant subhealth on PWTL in mice(x±s, n=10) **P < 0.01 vs control group |
本实验采用小鼠水中站立的方法,强迫疲劳性亚健康组小鼠在水中连续站立9 d,每天8 h,建立疲劳性亚健康模型。简便地模拟了疲劳性亚健康状态下机体生物节律改变、精力不足等形成因素。我们发现,与正常对照组小鼠相比,可见疲劳性亚健康组小鼠皮毛暗淡、情绪焦躁。模型建立完成后,疲劳性亚健康组小鼠疲劳程度与正常对照组有明显差异,而血常规检查显示,小鼠WBC、RBC、HGB、HCT、MCV、MCH、MCHC、PLT、MPV、PDW、PCT各项指标均正常。提示机体处于疲劳但仍健康的状态,符合对疲劳性亚健康的定义,表明本实验的疲劳性亚健康模型建立成功。
本实验测定PWMT和PWTL,通过小鼠耐受Von Frey纤维所致机械痛而产生不同的缩足时间,以及耐受同一光强所致热痛而产生不同的缩足时间,客观地反映实验对象的机械痛敏和热痛敏,同时,分批次检测以避免机械痛与热痛测定过程中的相互影响。结果显示,疲劳性亚健康组与正常对照组小鼠PWMT、PWTL基础值无明显差异,在模型建立成功后,疲劳性亚健康组小鼠PWMT明显高于正常对照组,而PWTL明显低于正常对照组。提示疲劳性亚健康组小鼠机械痛阈值升高,而热痛阈值降低,可以认为疲劳性亚健康使得机体机械痛敏降低,而热痛敏增高。同时,d 16时,即停止造模1周后,与正常对照组相比,疲劳性亚健康组小鼠PWMT和PWTL无明显异常,提示机械痛敏和热痛敏恢复正常,表明疲劳性亚健康可以通过1周恢复为正常状态,与已知研究结果相符[11]。
对于机械痛敏与热痛敏变化不同步的情况,Robson等[12]研究发现,硫喷妥钠使热痛阈值升高的同时,会通过降低胫骨的压力使机械痛阈值降低,由此提出热刺激与胫骨压力所诱发的疼痛神经起源不同。同时,近年也有实验证明,在切口痛中,吗啡可使机械痛敏增加,而热痛敏无变化[13]。综合考虑现实情况,提出几种假设:一方面,疲劳性亚健康模型和其他的疼痛模型相比,可能导致了机体内5-HT、DA等多种递质共同作用,较为复杂多样,因此造成机械性刺激和热刺激不同的痛反应;另一方面,脊髓背角神经元存在着不同阈值的神经元,会对触压刺激和热刺激产生不一样的反应,从而产生不同的行为学结果。另外,疲劳性亚健康可能影响了机械痛和热痛相关的不同通路,如分别对小鼠的机械痛和热痛的传导有着重要作用的酸敏感离子通道亚基3[14]和香草酸瞬时受体亚型Ⅰ基因[15]。因此,本实验结果出现的具体原因与作用机制还需进一步研究来确定。
实验表明,疲劳性亚健康状态影响机体疼痛敏感性,使得对机械痛的敏感性降低,而对热痛的敏感性增高,提示在现代生活中,不良的生活方式、较大工作压力等所致的疲劳性亚健康虽非疾病状态,但能够通过改变对疼痛的敏感等,进一步降低个体的生活质量。同时,研究结果支持在一定时间内,疲劳性亚健康可以恢复为健康状态,为临床诊治提供一定的指导意义。
| [1] |
Liao Y, Lin Y, Zhang C, et al. Intervention effect of baduanjin exercise on the fatigue state in people with fatigue-predominant subhealth: a cohort study[J]. J Altern Complement Med, 2015, 21(9): 554-62. doi:10.1089/acm.2014.0395 |
| [2] |
Wang W, Russell A, Yan Y. Traditional Chinese medicine and new concepts of predictive, preventive and personalized medicine in diagnosis and treatment of suboptimal health[J]. EPMA J, 2014, 5(1): 4. doi:10.1186/1878-5085-5-4 |
| [3] |
黄思婷, 姬宁宁, 杜雷, 等. 腹腔注射5-HT2A受体拮抗剂MDL11939对小鼠急性及慢性疼痛的影响[J]. 中国药理学通报, 2017, 33(2): 223-7. Huang S T, Ji N N, Du L, et al. Effects of intraperitoneal injection of 5-HT2A receptor antagonist MDL11939 on acute and chronic pain in mice[J]. Chin Pharmacol Bull, 2017, 33(2): 223-7. doi:10.3969/j.issn.1001-1978.2017.02.016 |
| [4] |
Rodríguez V J, Rodríguez V L, Guzmán N M. Pharmaceutical technology can turn a traditional drug, dexamethasone into a first-line ocular medicine. A global perspective and future trends[J]. Int J Pharm, 2017, 516(1-2): 342-51. doi:10.1016/j.ijpharm.2016.11.053 |
| [5] |
Kim J Y, Tillu D V, Quinn T L, et al. Spinal dopaminergic projections control the transition to pathological pain plasticity via a D1/D5-mediated mechanism[J]. J Neurosci, 2015, 35(16): 6307-17. doi:10.1523/JNEUROSCI.3481-14.2015 |
| [6] |
徐孝平, 潘永明, 刘瑞敏, 等. 亚健康状态大鼠的神经-免疫-内分泌机制的研究[J]. 中国比较医学杂志, 2012, 22(8): 33-9. Xu X P, Pan Y M, Liu R M, et al. Study on the mechanism of neuro-immuno-endocrine system of rats in sub-health state[J]. Chin J Comparative Med, 2012, 22(8): 33-9. |
| [7] |
刘艳艳, 程静茹, 余克强, 等. 疲劳型亚健康小鼠模型的研制[J]. 广东医学, 2012, 33(1): 21-4. Liu Y Y, Cheng J R, Yu K Q, et al. Construction of fatigue-type sub-health mouse model[J]. Guangdong Med J, 2012, 33(1): 21-4. doi:10.3969/j.issn.1001-9448.2012.01.013 |
| [8] |
Tung V W, Burton T J, Dababneh E, et al. Behavioral assessment of the aging mouse vestibular system[J]. J Vis Exp, 2014, 89: 1-11. |
| [9] |
Chen G, Tanabe K, Yanagidate F, et al. Intrathecal endothelin-1 has antinociceptive effects in rat model of postoperative pain[J]. Eur J Pharmacol, 2012, 697(1-3): 40-6. doi:10.1016/j.ejphar.2012.09.035 |
| [10] |
Hargreaves K, Dubner R, Brown F, et al. A new and sensitive method for measuring thermal nociception in cutaneous hyperalgesia[J]. Pain, 1988, 32(1): 77-88. doi:10.1016/0304-3959(88)90026-7 |
| [11] |
Tanaka M, Nakamura F, Mizokawa S, et al. Establishment and assessment of a rat model of fatigue[J]. Neurosci Lett, 2003, 352(3): 159-62. doi:10.1016/j.neulet.2003.08.051 |
| [12] |
Robson J G, Davenport H T, Sugiyama R. Differentiation of two types of pain by anesthetics[J]. Anesthesiology, 1965, 26: 31-6. doi:10.1097/00000542-196501000-00006 |
| [13] |
Sun Y, Sahbaie P, Liang D, et al. Opioids enhance CXCL1 expression and function after incision in mice[J]. J Pain, 2014, 15(8): 856-66. doi:10.1016/j.jpain.2014.05.003 |
| [14] |
Yen L T, Hsu Y C, Lin J G, et al. Role of ASIC3, Nav1.7 and Nav1.8 in electroacupuncture-induced analgesia in a mouse model of fibromyalgia pain[J]. Acupunct Med, 2018, 36(2): 110-6. doi:10.1136/acupmed-2016-011244 |
| [15] |
Wang C, Gu L, Ruan Y, et al. Pirt together with TRPV1 is involved in the regulation of neuropathic pain[J]. Neural Plast, 2018, 2018: 4861491. |

