


2. 河北中医学院基础医学院生物化学与生物学教研室,河北省心脑血管中医药防治重点实验室,河北 石家庄 050200
2. Dept of Biochemistry and Biology, Basic Medical College, Hebei University of Chinese Medicine and Hebei Key Lab of Chinese Medicine Research on Cardiocerebrovascular Diseases, Shijiazhuang 050200, China
随着社会的老龄化,动脉粥样硬化性疾病的发病率逐年升高。目前,临床上常用血管旁路移植、动脉球囊扩张术、支架置入术等血管重建术作为此类疾病治疗方法,但术后的再狭窄大大降低了其治疗效果,寻找一种安全有效、用药简便的药物一直是血管再狭窄研究的热点。血管平滑肌细胞(vascular smooth muscle cells,VSMC)是构成血管壁结构的主要细胞成分,同时还具有维持血管张力的作用,VSMC异常增生是动脉粥样硬化、血管重建术后再狭窄、高血压等心血管疾病的共同病理基础[1-2]。在一些因素的刺激下,VSMC能够表现出与肿瘤细胞类似的生物学行为[3],因此,应用抗肿瘤药物防治血管再狭窄作为一种新的治疗策略正在被大量研究。
Roscovitine是一种细胞周期蛋白依赖性激酶(cyclin-dependent kinase,CDK)抑制剂,能够抑制肿瘤细胞增殖,具有低毒、高效的特点,目前处于非小细胞肺癌、血液病等癌症的Ⅱ期临床研究。越来越多的研究表明,Roscovitine具有抗炎、抗增殖、抗凋亡、神经保护等多种药理功能,预示了Roscovitine可作为防治血管再狭窄的潜在药物[4-5]。在本实验中,我们采用肿瘤坏死因子α(tumor necrosis factor α,TNF-α)诱导体外VSMC增殖,观察Roscovitine对VSMC增殖及细胞周期的影响,为临床上血管再狭窄防治提供实验支持。
1 材料与方法 1.1 实验动物健康SD♂大鼠,体质量80~100 g,SPF级,购自北京维通利华实验动物技术有限公司,合格证号:SCXK(京)2012-0001。动物饲养于屏障环境,光照12 h·d-1,温度(20~26) ℃,相对湿度40%~70%,自由摄食和饮水。
1.2 试剂CDK抑制剂Roscovitine购自Gibco公司;TNF-α购自Sigma公司;Annexin V-FITC/PI双染细胞凋亡检测试剂盒,购自上海博谷生物科技有限公司;反转录RT-PCR反应试剂盒购自大连宝生物有限公司;蛋白定量分析试剂盒购自美国Pierce公司;引物购自上海生工生物技术公司;兔抗Cyclin A、Cyclin B、Cyclin D、Cyclin E多克隆抗体,兔抗CDK4、CDK5多克隆抗体,兔抗p53蛋白、p21蛋白、p27蛋白多克隆抗体,增殖细胞核抗原(proliferating cell nuclear antigen,PCNA)抗体,均购自美国Abcam公司。
1.3 仪器SpectraMax M2酶标分析仪(美国分子仪器公司);Epics XL流式细胞仪(美国Beckman Coulter公司);7300荧光定量PCR仪(美国ABI公司);Gel Doc XR+凝胶成像分析仪(美国Bio-Rad公司);DYY-Ⅲ型稳压稳流定时电泳仪、DYY-Ⅲ40B型转膜槽(北京六一仪器厂)。
1.4 细胞培养及分组健康SD大鼠,戊巴比妥钠45 mg·kg-1注射麻醉,取大鼠的胸腹主动脉血管,采用贴块法培养VSMC。具体培养过程:VSMC培养于含胎牛血清的DMEM培养液中,常规胰蛋白酶消化,显微镜下细胞呈典型的"峰谷"样生长,取3~6代细胞用于实验。将同步于静止期的VSMC分为正常对照组、TNF-α组(100 μg·L-1 TNF-α)、Roscovitine组(加入5、10、15、30 μmol·L-1 Roscovitine预处理15 h的VSMC,后加入终浓度为100 μg·L-1 TNF-α),不同处理组作用24 h后,收集细胞。
1.5 MTT法检测细胞增殖收集细胞前4 h,96孔板各孔加入10 μL MTT,于37 ℃孵育4 h,弃去孔中上清液,加入100 μL DMSO至充分溶解为蓝紫色溶液,采用酶标仪测定细胞各孔的吸光度(absorbance,A)值,测定波长为570 nm,实验重复3次,A值的大小可反映VSMC增殖程度。
1.6 流式细胞术检测细胞周期处理后的细胞,PBS洗涤后离心,制备单细胞悬液,采用Annexin V-FITC/PI双染法上机检测,用自带软件分析10 000个细胞周期时相。
1.7 Real-time RT-PCR测定目的基因mRNA的表达收集细胞,加入TRIzol试剂,提取总RNA,反转录cDNA,然后按试剂盒说明顺序加样进行体系反应,将β-actin设为内参上机检测,扩增结束,PCR仪分析软件进行分析,以相对表达量(relative quantity,RQ)值反映目的基因mRNA相对表达水平。引物序列见Tab 1。
| Gene | Sequence(5′-3′) | Product length/bp |
| Cyclin A | F:GCTGATGGAGGTGTGTGAAG | 80 |
| R:AAGTCCTGTGCCAAGTAGAATG | ||
| Cyclin B | F:CTGTGCTACTTCCCGAACTG | 94 |
| R:GAGGTGCTTTGTCCAGGTATG | ||
| Cyclin D | F:TAGGGACACCGACTGAGGAA | 62 |
| R:GCACGACATTCACCAAGGAT | ||
| Cyclin E | F:TTTGAGGTGCGTGTTTGTG | 63 |
| R:CCCTTTCTTGCGGAGATTC | ||
| CDK4 | F:ATGTCCGACCTGTTCCACA | 95 |
| R:CGAAGTCAAAGTTCCACCG | ||
| CDK5 | F:GCTTGCCCGAGTTCTACTACA | 100 |
| R:GAGTTTGCCTGAGACCCAA | ||
| p53 | F:GCTGATGGAGGTGTGTGAAG | 72 |
| R:AAGTCCTGTGCCAAGTAGAATG | ||
| p21 | F:CTGTGCTACTTCCCGAACTG | 141 |
| R:GAGGTGCTTTGTCCAGGTATG | ||
| p27 | F:TAGGGACACCGACTGAGGAA | 127 |
| R:GCACGACATTCACCAAGGAT | ||
| β-actin | F:GGTCATCACCATTGGCAA | 105 |
| R:GAGTTGAAGGTAGTTTCGTGGA |
收集细胞,加入细胞裂解液,提取总蛋白,电泳,半干法转移至PVDF膜,加入稀释浓度的PCNA、Cyclin A、Cyclin B、Cyclin D、Cyclin E、CDK4、CDK5、p53、p21、p27一抗孵育,后加入对应反应的二抗,化学发光法显影。测定条带的光密度值,β-actin做为内参,以目的条带光密度值和β-actin光密度值的比值即为目的蛋白的相对表达水平。
1.9 统计学分析采用SPSS 11.5软件进行处理,结果以x±s表示,用单因素方差分析ANOVA和Dunnett检验进行统计。
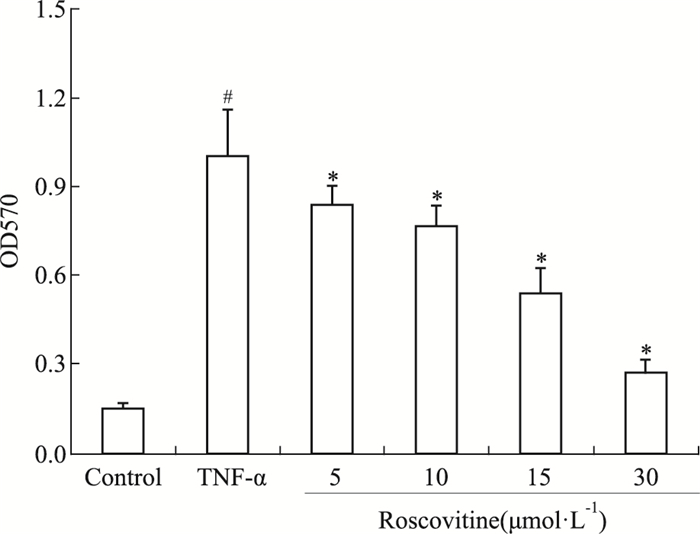
2 结果 2.1 Roscovitine对大鼠VSMC增殖的影响如Fig 1所示,与正常对照组比较,TNF-α组细胞A值明显升高(P < 0.05),Roscovitine (5、10、15、30 μmol·L-1)组比TNF-α组A值明显降低(P < 0.05)。Fig 2结果显示,与正常对照组比较,TNF-α组PCNA蛋白表达明显升高(P < 0.05),Roscovitine (5、10、15、30 μmol·L-1)组比TNF-α组PCNA蛋白表达明显降低(P < 0.05)。表明Roscovitine能抑制VSMC增殖。
|
| Fig 1 Effect of roscovitine on cell proliferation induced by TNF-α(x±s, n=6) #P < 0.05 vs control group; *P < 0.05 vs TNF-α group |

|
| Fig 2 Effect of roscovitine on protein expression of PCNA(x±s, n=3) #P < 0.05 vs control group; *P < 0.05 vs TNF-α group |
如Fig 3所示,TNF-α组G0/G1期细胞数量明显低于正常对照组,S期细胞数量高于对照组(P < 0.05),Roscovitine (5、10、15、30 μmol·L-1)组比TNF-α组G0/G1期细胞数量升高,S期细胞数量降低(P < 0.05)。表明Roscovitine抑制细胞周期从G0/G1期向S期转化。

|
| Fig 3 Effect of roscovitine on cell cell cycle(x±s, n=6) #P < 0.05 vs control group; *P < 0.05 vs TNF-α group |
如Fig 4所示,与正常对照组比较,TNF-α组Cyclin A、Cyclin B、Cyclin D、Cyclin E mRNA和蛋白表达明显升高(P < 0.05);Roscovitine处理后,能明显降低TNF-α诱导的细胞周期蛋白表达(P < 0.05)。

|
| Fig 4 Effect of roscovitine on protein(A) and mRNA(B) expression of cell cycle protein(x±s, n=3) #P < 0.05 vs control group; *P < 0.05 vs TNF-α group |
如Fig 5所示,TNF-α组比正常对照组CDK4、CDK5表达明显升高(P < 0.05),Roscovitine (5、10、15、30 μmol·L-1)组比TNF-α组CDK4、CDK5表达下降(P < 0.05)。

|
| Fig 5 Effect of roscovitine on protein(A) and mRNA(B) expression of cyclin-dependent kinase(x±s, n=3) #P < 0.05 vs control group; *P < 0.05 vs TNF-α group |
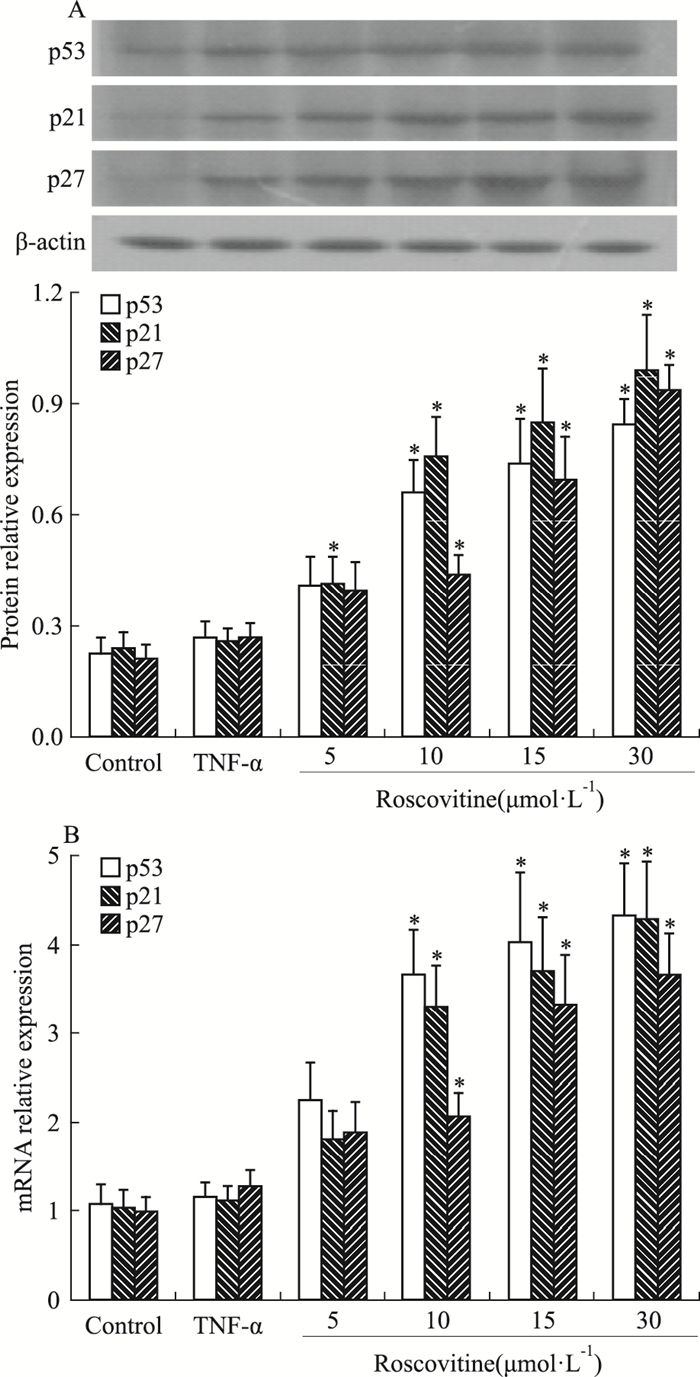
如Fig 6所示,Roscovitine 5、10、15、30 μmol·L-1组比TNF-α组p53、p21、p27 mRNA和蛋白表达明显上升(P < 0.05)。
|
| Fig 6 Effect of roscovitine on protein(A) and mRNA(B) expression of cell cycle inhibitory protein(x±s, n=3) #P < 0.05 vs control group; *P < 0.05 vs TNF-α group |
Roscovitine是嘌呤类似物,具有毒性低、活性高的特点,作为一种新型的抗肿瘤药物被大量研究。Roscovitine能抑制多种肿瘤细胞的增殖,而对正常细胞几乎无影响,例如,有研究报道Roscovitine能够抑制乳腺癌细胞、神经母细胞瘤细胞等增殖[6-7]。研究表明,刺激能够使VSMC增殖,呈现与肿瘤细胞相似的生物学行为,且二者许多信号转导途径一致[3],将抗肿瘤药物用于治疗血管增生性疾病可能是一种新的治疗策略。Roscovitine与其衍生物能明显抑制血小板衍生生长因子诱导的VSMC增殖[8]。我们在前期研究中也发现,Roscovitine能明显抑制血管紧张素II诱导的大鼠VSMC增殖[9]。本研究中,我们采用TNF-α诱导体外VSMC增殖,结果显示,TNF-α诱导的VSMC增殖活力明显增加,同时还观察到PCNA表达异常升高,给予Roscovitine干预后,能使VSMC增殖及PCNA表达降低,表明Roscovitine能明显抑制TNF-α诱导的大鼠VSMC增殖。
大量研究表明,VSMC增生与多种调节基因相关,但细胞周期调控是增生的最终共同途径[10],细胞周期抑制剂应用于临床也已成为现阶段的研究热点[11-12]。我们观察到Roscovitine能够抑制VSMC细胞周期从G0/G1期向S期转化,表明Roscovitine能够使VSMC细胞周期阻滞在S期,调控VSMC细胞周期。
Cyclins-CDKs-细胞周期素依赖性蛋白激酶抑制因子(cyclin-dependent-kinase inhibitor, CDKI)的网络调控系统在细胞生长和分化中备受关注,不同类型Cyclins在细胞细胞周期内有不同的作用,其水平也会发生变化。Cyclin A和B参与细胞周期中的S或M期,与DNA复制密切有关,而Cyclin D和E类型属细胞中的G1期,参与G1/S周期转换[13]。Cyclins和CDKs结合,不同的Cyclin/CDK复合物在细胞周期的特异位点组装,发挥相应的作用。同时,CDK活性还要受CDKIs抑制,CDKI可以与Cyclin/CDK复合物结合,也可以通过与CDK单体结合,阻断复合物的生成。我们观察到TNF-α诱导VSMC后,Cyclins-CDKs-CDKIs系统平衡被打破,Roscovitine能降低细胞周期蛋白Cyclin A、Cyclin B、Cyclin D、Cyclin E蛋白表达,降低细胞周期蛋白依赖激酶CDK4、CDK5蛋白表达,升高细胞周期抑制蛋白p53、p21、p27蛋白表达,表明Roscovitine能调控大鼠VSMC的增殖,调节Cyclins-CDKs-CDKIs系统,进一步验证了Roscovitine可与ATP竞争结合CDK的活性位点,调控VSMC细胞周期。
( 致谢:本研究在河北省人民医院代谢病重点实验室完成,感谢对实验给予指导和帮助的老师和同学。)
| [1] |
Lacolley P, Regnault V, Segers P, et al. Vascular smooth muscle cells and arterial stiffening: relevance in development, aging, and disease[J]. Physiol Rev, 2017, 97(4): 1555-617. doi:10.1152/physrev.00003.2017 |
| [2] |
Uryga A K, Bennett M R. Ageing induced vascular smooth muscle cell senescence in atherosclerosis[J]. J Physiol, 2016, 594(8): 2115-24. doi:10.1113/JP270923 |
| [3] |
Welt F G, Rogers C. Inflammation and restenosis in the stent era[J]. Arterioscler Thromb Vasc Biol, 2002, 22(11): 1769-76. doi:10.1161/01.ATV.0000037100.44766.5B |
| [4] |
Cicenas J, Kalyan K, Sorokinas A, et al. Roscovitine in cancer and other diseases[J]. Ann Transl Med, 2015, 3(10): 135-47. |
| [5] |
Xie T, Hu G, Dong B, et al. Roscovitine protects murine Leydig cells from lipopolysaccharide-induced inflammation[J]. Exp Ther Med, 2017, 13(5): 2169-76. doi:10.3892/etm.2017.4239 |
| [6] |
Arisan E D, Obakan P, Coker A, et al. Inhibition of ornithine decarboxylase alters the roscovitine-induced mitochondrial-mediated apoptosis in MCF-7 breast cancer cells[J]. Mol Med Rep, 2012, 5(5): 1323-9. |
| [7] |
Pizarro J G, Folch J, Junyent F, et al. Antiapoptotic effects of roscovitine on camptothecin-induced DNA damage in neuroblastoma cells[J]. Apoptosis, 2011, 16(5): 536-50. doi:10.1007/s10495-011-0583-3 |
| [8] |
Sroka I M, Heiss E H, Havlicek L, et al. A novel roscovitine derivative potently induces G1-phase arrest in platelet-derived growth factor-bb-activated vascular smooth muscle cells[J]. Mol Pharmacol, 2010, 77(2): 255-61. doi:10.1124/mol.109.060327 |
| [9] |
赵京山, 孙佳欢, 于琨, 等. Roscovitine通过影响核因子κB活化抑制大鼠颈动脉内膜损伤导致的炎性增生[J]. 中国病理生理杂志, 2017, 33(2): 233-8. Zhao J S, Sun J H, Yu K, et al. Roscovitine inhibits inflammatory hyperplasia of carotid artery intima in rats via suppressing nuclear factor-KB activation[J]. Chin J Pathophysiol, 2017, 33(2): 233-8. |
| [10] |
杨冬梅, 阳巍, 邱飞, 等. 姜黄素烟酸酯对血管平滑肌细胞增殖及ERK1/2信号通路的影响[J]. 中国药理学通报, 2016, 32(11): 1526-30. Yang D M, Yang W, Qiu F, et al. Effects of Cur Tn on proliferation of VSMC[J]. Chin Pharmacol Bull, 2016, 32(11): 1526-30. doi:10.3969/j.issn.1001-1978.2016.11.010 |
| [11] |
Liu Y, Li Y F, Chang H, et al. Roscovitine protects from arterial injury by regulating the expressions of c-Jun and p27 and inhibiting vascular smooth muscle cell proliferation[J]. J Cardiovasc Pharmacol, 2017, 69(3): 161-9. doi:10.1097/FJC.0000000000000453 |
| [12] |
李敬美, 丁圆媛, 潘夕春, 等. 细胞周期调节因子基因在H9c2心肌细胞肥大过程中的时相性表达变化[J]. 中国药理学通报, 2017, 33(1): 63-8. Li J M, Ding Y Y, Pan X C, et al. Temporal expressions of cell cycle regulators mRNA during hypertrophic process of H9c2 rat cardiomyocytes induced by angiotensin Ⅱ[J]. Chin Pharmacol Bull, 2017, 33(1): 63-8. doi:10.3969/j.issn.1001-1978.2017.01.012 |
| [13] |
Ingham M, Schwartz G K. Cell-cycle therapeutics come of age[J]. J Clin Oncol, 2017, 35(25): 2949-59. doi:10.1200/JCO.2016.69.0032 |

