


2. 军事医学科学院放射与辐射医学研究所,北京 100850
2. Institute of Radiation Medicine Academy of Military Medical Sciences,Beijing 100850,China
人参为五加科草本植物人参Panax ginseng C.A. Meyer的根,是我国传统的补益中药,具有大补元气、益气固脱、生津养血、安神益智之功效,是目前中医临床常用中药之一。人参皂苷(ginsenoside)在人参中含量约为4%,是人参主要有效成分之一[1]。根据皂苷元结构的不同,人参皂苷被分为原人参二醇类皂苷,如人参皂苷Rb1-3、Rc、Rd、Rg3等;原人参三醇类皂苷,如人参皂苷Re、Rf、Rg1、Rh,以及齐墩果酸类皂苷,如人参皂苷Ro和Ri等。人参皂苷中的二醇型与三醇型皂苷数量较多,被认为是人参的最重要活性成分。现代药理学研究显示,人参皂苷具有改善机体免疫力[2]、增强记忆力[3]、抗衰老[4]、抗氧化[5]、促进烧伤面愈合[6]和降血糖[7]等作用。随着其研究的逐渐深入,参附注射液、参麦注射液、生脉饮注射液、人参健脾丸和人参归脾丸等多种含有人参及其主要成分的制剂大量运用于临床的疾病治疗,且在临床用药过程中,其多与其他化学药物联合使用。在联合用药时,中药往往因其富含多样的天然活性成分而容易发生药物间相互作用[8],这种相互作用是指两种及两种以上药物同时或先后用药时,在代谢环节上产生相互作用。课题组前期研究发现临床剂量的参附注射液中的主要成分红参对大鼠 CYP1A2 在 mRNA 转录水平与肝微粒体酶活性水平具有上调作用,该上调作用可能会加速药物代谢酶的代谢,从而对其他合用药物产生影响[9]。细胞色素P450(CYP450)酶,简称CYP,主要参与药物体内代谢,药物对代谢酶可产生诱导或抑制作用,此改变是导致相互作用发生的主要原因。CYP是其基因超家族(superfamily)编码形成的一群蛋白酶[10]。课题组前期研究发现人参皂苷对CYP3A4具有一定的调控作用[11-12],但对CYP其他亚型研究较少。CYP1A1是细胞色素P450家族成员之一,其表达的诱导机制属于核受体介导型[13]。AhR是一种公认的配体激活转录因子,未与配体结合的AhR为一种胞浆蛋白,与配体结合后的AhR转移至细胞核内,并与核内芳香烃受体核转位蛋白(aryl hydrocarbon nuclear translocator,ARNT)形成异源二聚体,形成的二聚体识别并结合靶基因的外源性反应元件(xenobiotic response element,XRE),调控CYP1A1转录,影响酶活性,从而改变蛋白质功能[14]。CYP450酶系统在药物相互作用方面具有重要意义,其中一个重要表现是P450酶的诱导可增加生物转化率,从而降低药物浓度,使药效降低;若代谢形成活性药物则增加了药物作用或毒性。所以在药物代谢过程中,药物与药物代谢酶之间的作用以及联合用药时产生的相互作用,已经引起广泛关注[15]。
目前,人参皂苷类成分对于CYP1A1作用的研究报道较少。本文利用前期构建含有CYP1A1启动子序列的报告基因质粒pGL4.17-CYP1A1、含有hAhR编码区序列的pcDNA3.1-hAhR表达质粒和内参质粒pRL-TK瞬时转染HepG2细胞,在细胞水平上建立基于hAhR介导的CYP1A1药物诱导剂的体外筛选模型,并利用此体外筛选模型对人参皂苷Rc、Re、Rf和Rg1进行AhR转录激活特性筛选,筛选结果显示人参皂苷Rc、Re、Rf和Rg1均能不同程度地提高AhR转录活性。进一步检测了人参皂苷Rc、Re、Rf和Rg1对LS174T细胞中CYP1A1 mRNA表达和蛋白表达的影响,为人参及人参皂苷与其他药物联合用药时产生相互作用的可能性进行预测,有助于为临床中西医联合用药和合理化用药提供有参考价值的实验依据,从而提高临床应用人参的安全性与有效性。
1 材料 1.1 药品与试剂人参皂苷Rc,20 mg,批号:11641-200802;人参皂苷Re,20 mg,批号:110754-201324;人参皂苷Rg1,20 mg,批号:110703-201529,人参皂苷Rf,20 mg,批号:111719-201104,购于中国药品生物制品检定所。TCDD(2,3,7,8-tetrachlorodibenzo-p-dioxin),10 mg,批号:ED-901-A,购自美国Cerillant 公司。二甲基亚砜(DMSO)(美国Sigma公司);质粒pGL4.17-CYP1A1、pcDNA3.1-hAhR和pRL-TK本实验室保存;胎牛血清、磷酸盐缓冲液(PBS)、DMEM高糖培养基和Opti-MEM培养基(美国Hyclone公司);转染试剂TransIT-X2(美国Mirus公司);反转录与Real time-PCR试剂盒(北京全式金公司);无内毒素质粒小量提取试剂盒(德国Qiagen公司);双荧光素酶报告基因检测试剂盒(Dual luciferase reporter Kit)(美国Promega公司);BCA 蛋白定量试剂盒(北京普利莱公司);Western blot试剂盒(美国Promega公司);一抗 CYP1A1兔抗人(美国Proteintech公司);二抗辣根酶标记山羊抗兔IgG抗体(美国Cell Signaling Technology公司);其他试剂均为国产分析纯。
1.2 主要仪器细胞培养箱(日本SANYO公司);倒置显微镜(日本Nikon公司);Microfuge 22R型离心机(美国Beckman公司); GeneAmp PCR System 2400型PCR仪(美国Applied Biosystem公司);VICTOR X 型多标记酶标仪(美国 Perkin Elmer公司); Step one plus型Real-time PCR仪(美国Applied Biosystem 公司);Western blot电泳仪(瑞典Amersham公司);转膜仪(美国Bio-Rad公司);转移脱色摇床(海门市其林贝尔仪器制造有限公司);显影照相仪(美国GE公司)。
2 方法 2.1 细胞系和细胞培养细胞系HepG2和LS174T购自中国医学科学院基础医学研究所,由本实验室保存提供。HepG2和LS174T细胞均生长于含有体积分数为0.1的特级胎牛血清、100 mg·L-1青霉素和链霉素的DMEM培养液中,在37℃,饱和湿度为0.05 CO2的条件下贴壁培养,并取对数生长期的细胞用于实验。
2.2 质粒的扩增及纯化将实验室甘油冻存分别含有pGL4.17-CYP1A1报告基因质粒、pcDNA3.1-hAhR表达质粒和pRL-TK内参质粒的菌液在LB培养基中37℃摇床培养过夜,按质粒提取说明书分别提取pGL4.17-CYP1A1、pcDNA3.1-hAhR和pRL-TK 3种质粒,经紫外分光光度仪测定A260 nm值,4℃保存待用。
2.3 细胞瞬时转染与双荧光素酶活性检测瞬时转染实验前1 d取对数生长期HepG2细胞,以每孔5×105细胞接种于24孔板中,每组做4个复孔,培养至细胞密度约为0.8,弃培养液,用PBS洗细胞2次。用无抗生素的培养液稀释质粒,按照转染试剂TransIT-X2说明书,将250 ng pGL4.17-CYP1A1,500 ng pcDNA3.1-hAhR以及作为对照的50 ng pRL-TK内参质粒共转染HepG2细胞。按1 ∶50比例加入TransIT-X2转染试剂,室温孵育30 min后加入HepG2细胞中,100 μL每孔。37℃,饱和湿度为0.05 CO2的培养箱孵育12 h后,分别加入含有20 μmol·L-1 Rc、Re、Rf和Rg1的无血清培养基,同时设置2 nmol·L-1 TCDD作为阳性对照组。培养24、48 h后,弃去24孔板中的培养基,用PBS洗涤细胞1次,每孔加入100 μL报告基因裂解缓冲液,离心12 000 r·min-1,5 min,取上清。取20 μL上清液与100 μL萤火虫萤光素酶检测缓冲液混合后,采用多功能酶标仪检测萤火虫萤光素酶(firefly luciferase)的活性;再加入100 μL海肾荧光素酶检测缓冲液,检测海肾荧光素酶(Renilla luciferase)活性,计算两种荧光素酶活性的比值。
2.4 Real-timePCR检测人参皂苷对CYP1A1 mRNA水平变化 不同浓度的人参皂苷Rc、Re、Rf和Rg1(5、10、20、50 μmol·L-1)与完全激动剂TCDD(2 nmol·L-1)分别处理LS174T细胞,药物处理24、48 h后,TRIzol提取细胞总RNA,紫外分光光度计检测总RNA浓度和纯度。逆转录成cDNA后进行实时荧光定量PCR检测,PCR反应条件为94℃ 30 s,94℃ 5 s,55℃ 30 s,72℃ 30 s,共40个循环。以各目标基因2-△△Ct值表示各目标基因mRNA相对表达水平。用于扩增的特异性引物序列见表 1(Tab 1)。
| Gene | Forward primer(5′→3′) | Reverse primer(5′→3′) |
| CYP1A1 | CCATGACCAGAAGCTATGGGT | GCTCTCAAGCACCTAAGAGCG |
| β-Actin | TCATGAAGTGTGACGTGGACATC | CAGGAGGAGCAATGATCTTGATCT |
blot检测人参皂苷对CYP1A1的蛋白水平变化 不同浓度的人参皂苷Rc、Re、Rf和Rg1(5、10、20、50 μmol·L-1)与完全激动剂TCDD(2 nmol·L-1)分别处理LS174T细胞,药物处理48 h后,胰酶消化后离心收集细胞,RIPA裂解液冰上裂解20 min提取细胞全蛋白,BCA法进行蛋白质测定,沸水浴煮10 min变性,50 μg蛋白经SDS-PAGE电泳分离,转膜,用质量浓度为0.5 g·L-1脱脂奶粉于室温下摇动封闭膜2 h,孵育一抗,洗膜,孵育二抗,洗膜,化学发光,显影,图像分析,用Image J软件计算灰度值,以目标蛋白条带的灰度值与内参蛋白的积分吸光度值比值表示待测蛋白的相对表达水平。
2.6 数据处理所有数据重复3次,每次设置3个复孔,收集数据进行统计学分析。实验数据用x±s表示。采用GraphPad Prism 5软件的t-test方法进行统计学分析。
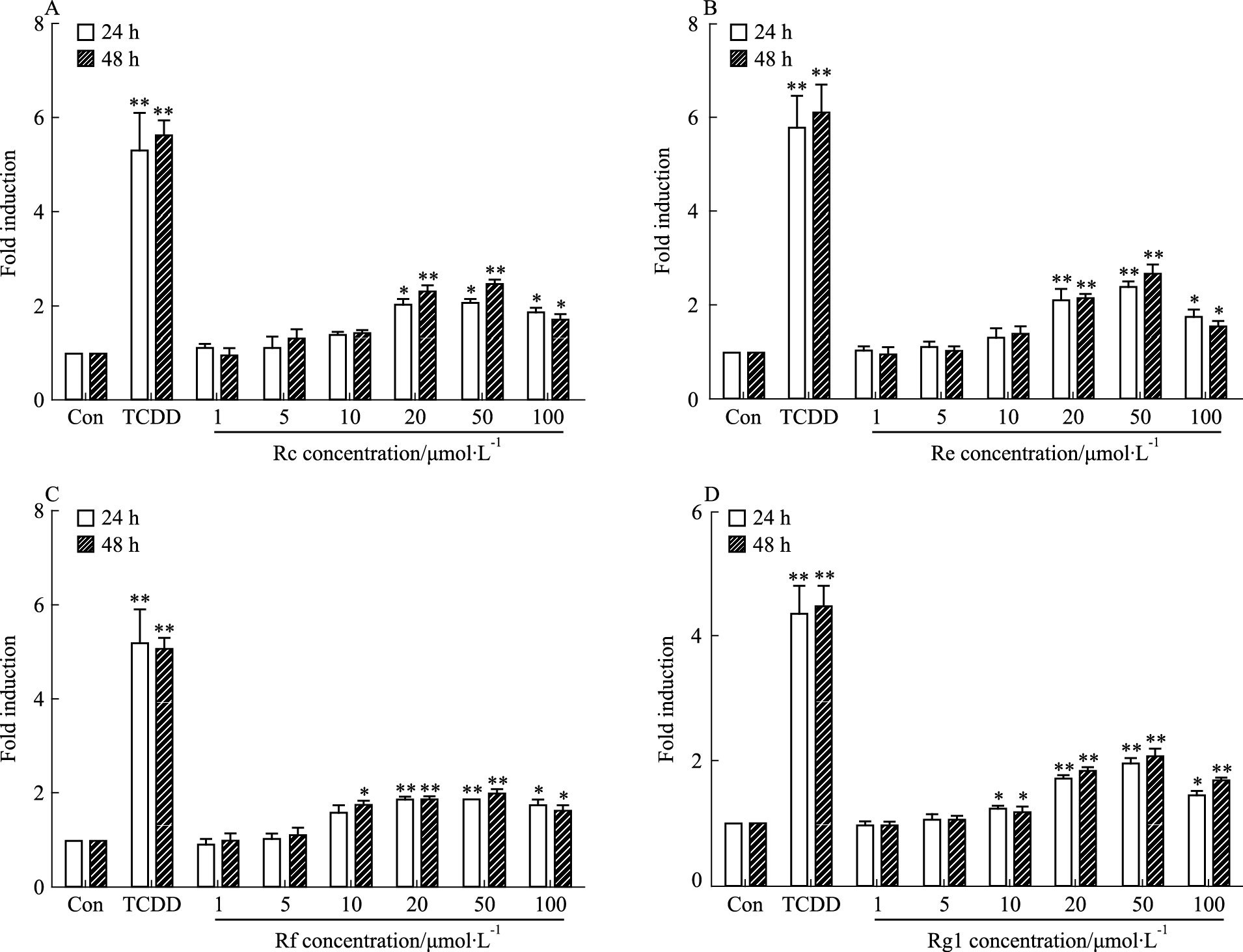
3 结果 3.1 基于报告基因技术对人参皂苷增强AhR转录活性作用筛选药物处理HepG2细胞24和48 h后,以DMSO(0.1%)作为溶剂对照,2 nmol·L-1 TCDD为阳性对照组,将各药物处理组荧光强度与溶剂对照组荧光强度比值为诱导倍数。双荧光素酶报告基因检测结果显示,人参皂苷Rc、Re、Rf和Rg1对报告基因激活效应趋势基本一致,在筛选浓度为20 μmol·L-1,处理时间为48 h时,人参皂苷Re激活效应明显(P<0.05),在筛选浓度为20 μmol·L-1,处理时间为24、48 h时,人参皂苷Rf对AhR产生了中等强度的激活效应(P<0.05),诱导倍数分别为2.1、2.4,结果如Fig 1所示。
|
| 图 1 Fold induction of relative CYP1A1 luciferase activity by ginsenosides for 24 h or 48 h at different concentrations(x±s,n=3) A: Ginsenoside Rc; B: Ginsenoside Re; C: Ginsenoside Rf; D: Ginsenoside Rg1,Con: Control group.*P<0.05,**P<0.01 vs control group |
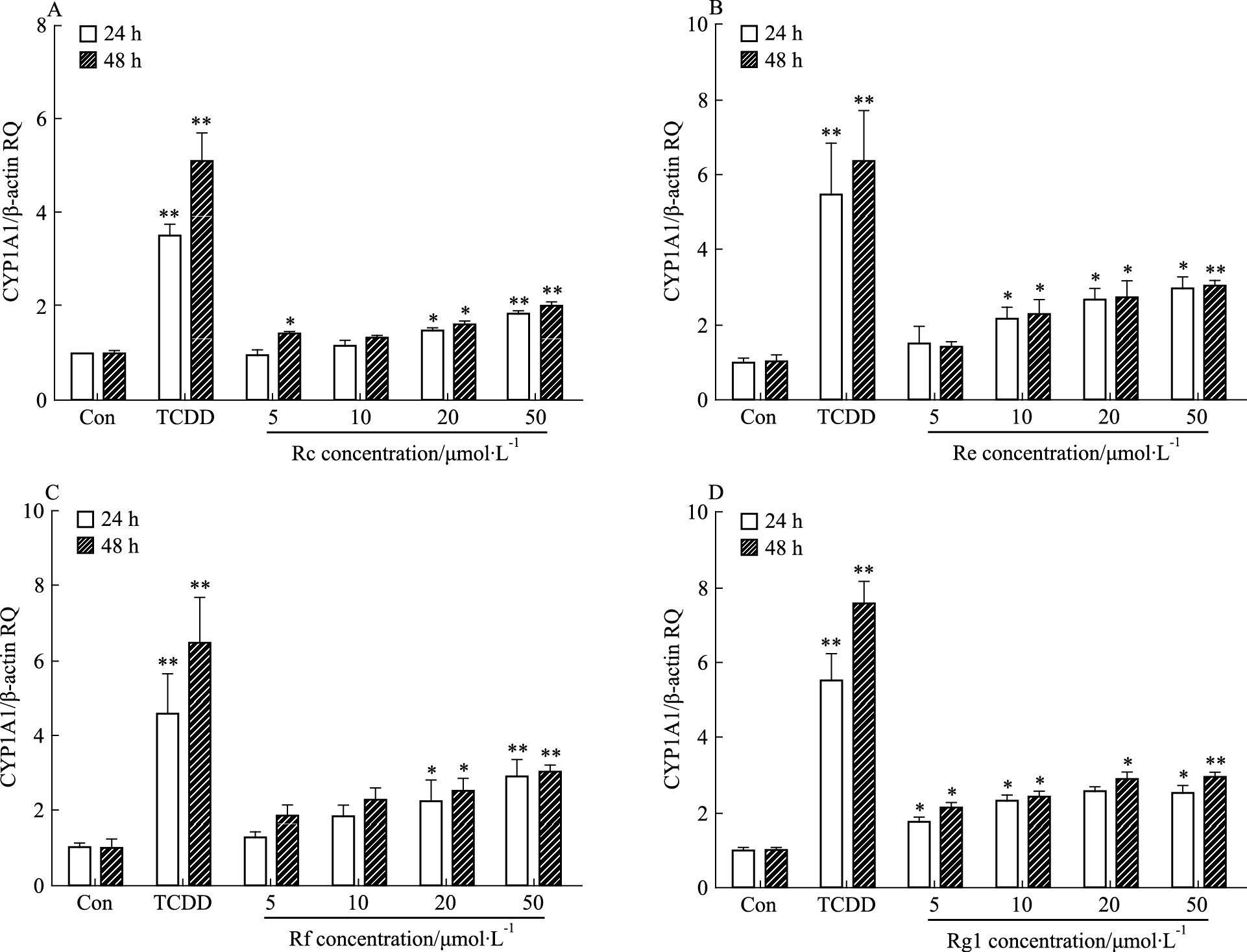
mRNA表达的影响 进一步利用实时荧光定量PCR检测人参皂苷对LS174T细胞CYP1A1 mRNA表达的影响,结果显示,与溶剂对照组相比,不同浓度的人参皂苷Rc、Re、Rf和Rg1(5、10、20、50 μmol·L-1)分别处理LS174T细胞24、48 h后,均能诱导CYP1A1 mRNA的表达,并呈现一定的浓度依赖性,结果如Fig 2所示。从剂量效应上分析显示,当人参皂苷浓度为50 μmol·L-1诱导作用最强(P<0.01);从时间效应上分析显示,48 h的诱导效应高于24 h。实时荧光定量PCR结果与双荧光素酶报告基因实验结果一致,表明人参皂苷Rc、Re、Rf和Rg1通过激活AhR受体,可进一步上调其调控靶基因CYP1A1 mRNA的表达,结果如Fig 2所示。
|
| 图 2 Fold induction of CYP1A1 mRNA expression relative to β-actin mRNA by the 4 kinds of ginsenoside at different concentrations in LS174T cells(x±s,n=3) A: Ginsenoside Rc; B: Ginsenoside Re; C: Ginsenoside Rf; D: Ginsenoside Rg1,Con: Control group.*P<0.05,**P<0.01 vs control group |
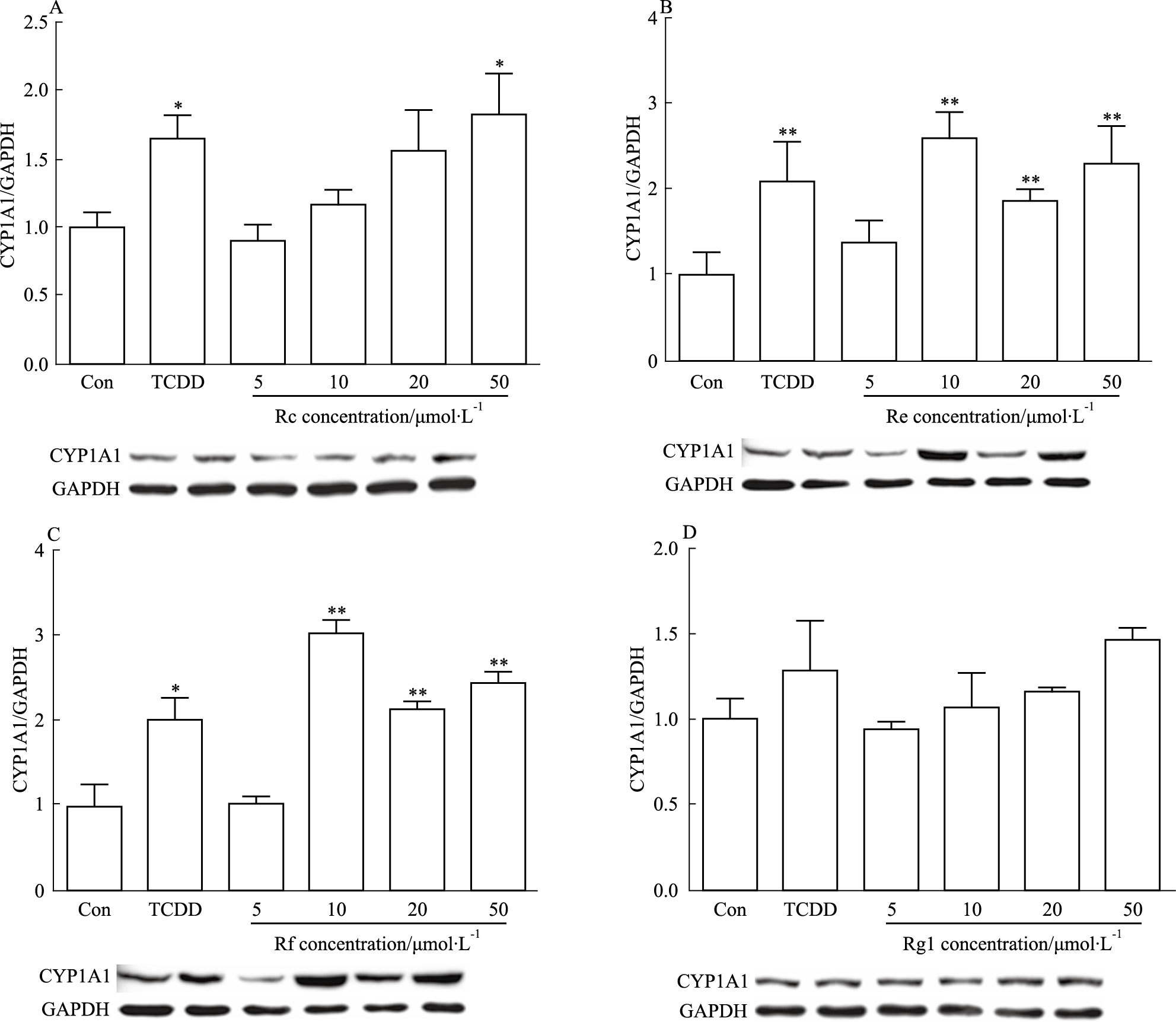
采用Western blot检测人参皂苷对LS174T细胞CYP1A1蛋白表达的影响,不同浓度的人参皂苷Rc、Re、Rf和Rg1(5、10、20、50 μmol·L-1)分别处理LS174T细胞48 h,Western blot检测结果显示,与溶剂对照组相比,人参皂苷Rc、Re、Rf和Rg1均能诱导CYP1A1蛋白表达,其中人参皂苷Re和Rf差异具有显著性(P<0.05),结果如Fig 3所示。
|
| 图 3 Fold induction of CYP1A1 protein expression relative to GAPDH by 4 kinds of ginsenoside at different concentrations in LS174T cells for 48 h(x±s,n=3) A: Ginsenoside Rc; B: Ginsenoside Re; C: Ginsenoside Rf; D: Ginsenoside Rg1,Con: Control group.*P<0.05,**P<0.01 vs control group |
人细胞色素P450是生物体内代谢的重要酶系,CYP1A1主要分布于肝外,在肝脏中含量很低,但其是具有主要诱导能力的代谢酶之一[16],AhR的下游靶基因众多,在AhR信号途径中,CYP1A1被认为是经典的下游靶位基因,此基因的转录激活也是AhR信号途径活化的重要标志之一[17]。CYP1A1可被多环芳烃类化合物诱导,并可催化一系列的多环芳烃化合物生成具有活性的代谢产物[18]。人参为我国传统名贵中草药材,素有“百药之王”的美誉,既作为药物也可作为食品补充剂,人参皂苷是人参的主要有效成分之一。中药中富含大量的天然活性成分,具有丰富的生理功能,越来越多应用于临床治疗,如用于高血压、抑郁症、糖尿病及心脏病等,但是因中药成分复杂,作用靶点较多,长期应用可能会影响肝脏药物代谢酶的活性或者表达,进而对其他联合应用药物的转运和代谢产生影响。因此,有必要对药物代谢酶与中药的相互作用关系进行深入研究。
报告基因法是将含有萤火虫荧光素酶的编码基因的质粒与目的基因的调控序列连接在一起构建报告基因质粒并导入细胞中。此方法可以在药物研发早期对化合物进行高通量、快速的相关核受体激活活性筛选,从而初步判断化合物是否具有潜在诱导CYP450的能力。本研究利用实验室前期构建的pGL4.17-CYP1A1报告基因质粒、pcDNA3.1-hAhR表达质粒与内参质粒pRL-TK共同转染HepG2细胞,在细胞水平上建立基于hAhR介导的CYP1A1药物诱导剂的体外筛选模型,并利用此体外筛选模型对人参皂苷Rc、Re、Rf和Rg1进行不同浓度与不同时间的筛选实验。结果显示,人参皂苷Rc、Re、Rf和Rg1能够激活AhR的转录活性,其中人参皂苷Rf对AhR产生了中等强度的激活效应。为了进一步验证人参皂苷Rc、Re、Rf和Rg1是否对CYP1A1表达产生影响,本实验选择了内源性核受体表达量较高的LS174T细胞,从CYP1A1的mRNA表达和蛋白表达两个方面进行进一步地确证。结果显示,在转录水平,人参皂苷Rc、Re、Rf和Rg1通过激活AhR,能明显地上调CYP1A1的mRNA表达,并呈现浓度依赖性;同时随着4种人参皂苷的浓度升高,CYP1A1的蛋白表达也呈现上升趋势,其中人参皂苷Re和Rf诱导表达差异具有显著性。以上结果提示,人参皂苷Rc、Re、Rf和Rg1能够对CYP1A1表达产生诱导作用,同时因为AhR作为CYP1A1的转录调控子,因此推测这种作用可能起始于AhR对 CYP1A1转录调控环节。
近年来,关于中药及有效成分与药物代谢酶相互作用的研究报道日益增多,现已发现多种中药可以对P450酶产生诱导或者抑制作用,例如葛根素或葛根提取物可以诱导大鼠CYP1A1/2、2A1和2C11的表达并抑制2B1、2E1和3A的活性[19];圣约翰草为治疗抑郁非处方药,其能诱导CYP3A4的表达,临床上与地高辛合用可降低地高辛的血药浓度,与华法林合用能够减弱华法林的抗凝作用[20];三七及其有效成分三七总皂苷对大鼠CYP1A1/2、2E1产生诱导作用,与一些主要由CYP1A2进行代谢的药物如雌二醇、非那西丁等,以及由CYP2E1进行代谢的药物,如氨苯砜、含氟麻醉药等合用时,可能引发潜在的相互作用[21]。因此,本研究考察了4种人参皂苷对AhR介导的CYP1A1的转录调控作用,进一步阐明人参及其有效成分与肝脏药物代谢酶之间的相互作用。此研究不仅能为潜在的药物相互作用提供一种预测方法,而且可为新药研发提供具有实际意义的理论数据。
( 致谢: 感谢军事医学科学院放射与辐射医学研究所高月研究员提供了良好的实验条件;感谢王宇光副研究员在实验细节方面的悉心指导。 )
| [1] | Liang Y, Zhao S. Progress in understanding of ginsenoside biosynthesis[J]. Plant Bology, 2008, 10 (4) : 415-21 doi:10.1111/j.1438-8677.2008.00064.x. |
| [2] | Attele A S, Wu J A, Yuan C S. Ginseng pharmacology: multiple constituents and multiple actions[J]. Biochem Pharmacol, 1999, 58 (11) : 1685-93 doi:10.1016/S0006-2952(99)00212-9. |
| [3] | Zhang G, Liu A, Zhou Y, et al. Panax ginsenoside Rg2 protects memory impairment via anti-apoptosis in a rat model with vascular dementia[J]. J Ethnopharmacol, , 2008, 115 (3) : 441-8 doi:10.1016/j.jep.2007.10.026. |
| [4] | 何方, 余丽梅. 人参皂苷Rg1对成体干细胞特性与功能的影响[J]. 中国药理学通报, 2016, 32 (3) : 319-22 . He F, Yu LM. Effects of ginsenoside Rg1 on characteristics and functions of adult stem cells[J]. Chin Pharmacol Bull, 2016, 32 (3) : 319-22 . |
| [5] | Chang M S, Lee S, Grho H M. Transcriptional activation of Cu/Zn super-oxide dismutase and catalase genes by panaxadiol ginsenosides extracted from Panax ginseng[J]. Phytoyther Rse,, 1999, 13 (8) : 641-4 doi:10.1002/(ISSN)1099-1573. |
| [6] | Kimura Y, Sumiyoshi M, Kawahira K. Effects of ginseng saponins isolated from red ginseng roots on burn wound healing in mice[J]. Br J Pharmacol, 2006, 148 (6) : 860-70 . |
| [7] | Tung N H, Song G Y, Park Y J, et al. Two new dammarane type saponins from the leaves of Panax ginseng[J]. Chem Pharm Bull, 2009, 57 (12) : 141-4 . |
| [8] | 肖红斌, 刘艳秋, 王莉, 等. 基于成分相互作用的中药复方组分配伍研究[J]. 世界科学技术-中医药现代化, 2011, 13 (2) : 240-3 . Xiao H B, Liu Y Q, Wang L, et al. Study on multi-component combination of chinese prescriptions based on component interaction[J]. World Sci Techol/Mod Trad Chin Med Mat Med, 2011, 13 (2) : 240-3 . |
| [9] | 李晗, 王宇光, 高月, 等. 基于临床用量的参附注射液对大鼠肝脏主要药物代谢酶的影响[J]. 药学学报, 2013, 48 (5) : 728-33 . Li H, Wang YG, Gao Y, et al. Effect of Shenfu injection on CYP450s of rat liver[J]. Acta Pharm Sin, 2013, 48 (5) : 728-33 . |
| [10] | Jin B, Park D W, Nam K W, et al. CpG methylation of the mouse CYP1A2 promoter[J]. Toxicol Lett, 2004, 152 (1) : 11-8 doi:10.1016/j.toxlet.2004.03.016. |
| [11] | 王宇光, 刘浩生, 高月, 等. 人参中皂苷成分的孕烷X受体激动特性筛[J]. 药学学报, 2013, 48 (1) : 144-8 . Wang Y G, Liu H S, Gao Y. Screening of pregnane X receptor activation from ginsenosides[J]. Acta Pharm Sin, 2013, 48 (1) : 144-8 . |
| [12] | 马增春, 赵佳伟, 高月, 等. 人参皂苷Re对H9c2心肌细胞CYP450酶的影响[J]. 中国药理学通报, 2016, 32 (4) : 494-8 . Ma Z C, Zhao J W, Gao Y, et al. Effcet of ginsenoside Re on cytochrome P450 in H9c2 cells[J]. Chin Pharmacol Bull, 2016, 32 (4) : 494-8 . |
| [13] | 陈卫平, 毕蕾. 药物代谢酶在中药配伍研究中的作用[J]. 中国中药杂志, 2007, 32 (2) : 96-8 . Chen W P, Bi L. Exploration on effect and significance of drug metabolic enzyme for studying on compatibility of Chinese herbs[J]. China J Chin Mat Med, 2007, 32 (2) : 96-8 . |
| [14] | Kikuchi Y, Ohsawa S, Mimura J, et al. Heterodimers of bHLH-PASprotein fragments derived from AhR, AhRR, and Arnt prepared by co-expression in Escherichia coli: characterization of their DNA binding activity and preparation of a DNA complex[J]. J Biochem, 2003, 134 (1) : 83-90 doi:10.1093/jb/mvg115. |
| [15] | Sevrioukova I F, Poulos T L. Understanding the mechanism of cytochrome P450 3A4: recent advances and remaining problems[J]. Dalton Trans, 2013, 42 (9) : 3116-26 doi:10.1039/C2DT31833D. |
| [16] | Coe K J, Nson S D, Ulrich R G. Profiling the hepatic effects of flutamide in rats: a microarray comparison with classical aryl hydrocarbon receptor ligands and atypical CYP1A inducers[J]. Drug Met, 2006, 34 (7) : 1266-75 doi:10.1124/dmd.105.009159. |
| [17] | Iba M M, Ngyyen T, Fung J. CYPlA1 idnuciton by piyrdine and its melabolites in HepG2 cells[J]. Arch Biochem Biophys, 2002, 404 (2) : 326-34 doi:10.1016/S0003-9861(02)00332-6. |
| [18] | Chiaro C R, Patel R D, Marcus C B, et al. Evidence for an aryl hydrocarbon receptor mediated cytochrome p450 auto regulatory pathway[J]. Mol Pharmacol, 2007, 72 (5) : 1369-79 doi:10.1124/mol.107.038968. |
| [19] | Zhang Z, Lam T N, Zuo Z. Radix Puerariae: an overview of its chemistry, pharmacology, pharmacokinetics, and clinical use[J]. J Clin Pharmacol, , 2013, 53 (8) : 787-811 . |
| [20] | Xie H G, Kim R B. St John′s Wort associated drug interactions: short-term inhibition and long-term induction[J]. Clin Pharmacol Ther, 2005, 78 (1) : 19-24 doi:10.1016/j.clpt.2005.04.002. |
| [21] | 陈艳进, 王宇光, 高月, 等. 三七总皂苷对大鼠肝脏药物代谢酶酶活性、mRNA及蛋白表达的影响[J]. 中国中药, 2014, 39 (19) : 3824-8 . Chen Y J, Wang Y G, Gao Y, et al. Effect of Panax notoginseng saponins on liver drug metablic enzyme activity, mRNA and protein expressions in rats[J]. China J Chin Mat Med, 2014, 39 (19) : 3824-8 . |
文章信息
-
文章历史
- 收稿日期: 2016-05-06
- 修订日期: 2016-06-05