


2. 安徽医科大学研究生学院, 安徽 合肥 230032;
3. 南京军区杭州疗养院海勤疗养区, 浙江 杭州 310002
高月(1963-), 女, 博士, 研究员, 研究方向:中药药理学, 通讯作者, E-mail:gaoyue@bmi.ac.cn
 , XIAO Yong1, ZHAO Jiao-wei1, 2, WANG Yu-guang1, TAN Hong-lin1, LIANG Qian-de1, TANG Xiang-lin1, XIAO Cheng-rong1, YANG Ling3
, XIAO Yong1, ZHAO Jiao-wei1, 2, WANG Yu-guang1, TAN Hong-lin1, LIANG Qian-de1, TANG Xiang-lin1, XIAO Cheng-rong1, YANG Ling3
 , GAO Yue1
, GAO Yue1

2. Graduate School of Anhui Medical University, Hefei 230032, China;
3. Hangzhou Convalescent Hospital, Hangzhou 310002, China
人参皂苷Re (ginsenoside Re)是中药人参中的主要有效成分,研究表明,人参皂苷Re具有较强的抗心肌缺血作用,可增加心肌供氧量,使心率明显降慢[1]。人参皂苷Re减少心肌细胞凋亡,对心肌缺血/再灌注损伤有防治作用[2]。细胞色素P450(cytochrome P450,CYP450) 酶是人体最重要的代谢酶,参与生物体内源性物质(如类固醇激素、花生四烯酸等) 和外源性物质( 如药物、环境致癌物等)的生物转化[3],CYP450酶包括表氧化酶和羟化酶两种,CYP2C和CYP2J两类CYP450表氧化酶可将花生四烯酸代谢生成环氧二十碳三烯酸(Epoxyeicosatrienoic acids,EETs)[4]。CYP4A和CYP4F两类CYP450羟化酶可将花生四烯酸代谢生成羟化环氧二十碳三烯酸(hydroxyeicosatrienoic acids,HETEs)[5]。EETs促血管生成、舒张血管,对心血管有着积极的保护作用[6]。而20-HETE的生物学效应与EETs相反,收缩冠脉血管,并通过抑制肌纤维膜ATP敏感性K+通道介导心肌损伤[7]。H9c2细胞常作为心肌损伤保护的体外研究模型,人参皂苷Re能否通过诱导或抑制CYP450酶的表达,以改变EETs和HETEs之间的体内代谢平衡,从而发挥其心肌保护作用。本文将通过检测人参皂苷Re对心肌细胞CYP450酶的影响来探讨其对心肌细胞的作用机制。
1 材料 1.1 细胞H9c2心肌细胞购于中国医学科学院协和细胞中心,由本实验室培养并保存。
1.2 药品与试剂人参皂苷Re,20 mg,批号:11179-200702。DMEM培养基、非必需氨基酸(NEAA)、胎牛血清(Hyclone公司);TRIzol和引物购于Invitrogen(Carlsbad,California,USA)。CYP4A1、CYP2J3抗体购自Santa Cruz Biotechnology公司,GAPDH抗体购自Cell Signaling公司,辣根过氧化物酶(HRP)标记的山羊抗兔IgG (H+L)为Santa Cruz Biotechnology公司产品。ECL检测系统为北京普利来公司产品。PVDF膜购自Millipore Biosciences。引物序列如Tab1所示。
| CYP gene | Forward primer(5′-3′) | Reverse primer(5′-3′) |
| CYP2C11 | CACCAGCTATCAGTGGATTTGG | GTCTGCCCTTTGCACAGGAA |
| CYP2J3 | CATTGAGCTCACAAGTGGCTTT | CAATTCCTAGGCTGTGATGTCG |
| CYP4A1 | TTGAGCTACTGCCAGATCCCAC | CCCATTTTTGGACTTCAGCACA |
| CYP4A3 | CTCGCCATAGCCATGCTTATC | CCTTCAGCTCAT TCATGG CAATC |
| CYP4F4 | CAGGTCTGAAGCAGGTAACTAAGC | CCGTCAGGGTGGCACAGAGT |
| ANP | GGAGCCTGCGAAGGTCAA | TATCTTCGGTACCGGAAGCTGT |
| GDPAH | CAAGGTCATCCATGACAACTTTG | GGGCCATCCACAGTCTTCTG |
购得H9c2心肌细胞后,倒掉原培养基,用PBS漂洗3次,加入0.25%胰酶室温消化约3 min,加入含10%胎牛血清的DMEM培养基终止消化,H9c2细胞培养瓶置37 °C,5% CO2,饱和湿度的恒温细胞培养箱培养。人参皂苷Re剂量效应处理浓度为0.1、1、10、50、100 μmol·L-1,检测时间为作用48 h。人参皂苷Re时间效应为作用后6、24、36、48及60 h,作用浓度为10 μmol·L-1。
2.2 实时定量PCR检测人参皂苷Re对CYP450 mRNA表达的影响取H9c2心肌细胞,以细胞数2×105/孔接种于6孔板中。同时设立0.1% DMSO的溶剂对照,药物处理H9c2大鼠心肌细胞不同时间点提取细胞总RNA。用紫外分光光度计(Beckman DU-600) 检测RNA浓度和纯度(OD260/OD280值为1.8~2.0)。按Real time PCR试剂盒说明书操作检测CYP450 mRNA及GDPAH。RT的反应条件为42 ℃ 30 min,99 ℃ 5 min,5 ℃ 5 min。PCR 的反应条件为94 ℃ 30 s,55 ℃ 30 s,72 ℃ 30 s,30个循环。
2.3 Western blot检测人参皂苷Re对CYP450蛋白表达的影响H9c2大鼠心肌细胞处于指数生长期,换0.1% FBS的DMEM培养24 h使细胞同步化,然后按实验分组,加入不同的处理因素继续孵育至所需时间。按说明书提取细胞总蛋白定量,每孔40 μg蛋白上样,进行电泳,半干式电转至 PVDF膜,5%脱脂牛奶室温封闭2 h后加一抗(CYP4A1为 1:2 000),4 ℃过夜后洗膜,再加入辣根过氧化物酶标记的二抗(1:2 000)室温下轻微摇晃孵育 1 h,暗室中进行压片、显影、定影,洗片晾干后用Alphalmager TM 2200进行图像分析,检测密度扫描值。
2.4 统计学方法数据用x±s表示,采用SPSS 13.0软件进行分析,两样本均数比较采用Dunmett-t检验。
3 结果 3.1 人参皂苷Re对H9c2心肌细胞CYP基因表达的影响人参皂苷Re剂量效应处理浓度为0.1、1、10、50、100 μmol·L-1,检测时间为作用48 h。人参皂苷Re时间效应为加药作用后6、24、36、48及60 h,作用浓度为10 μmol·L-1。与对照组比较,人参皂苷Re明显上调心肌细胞CYP2C11、CYP2J3 mRNA的表达至正常对照的1.6、1.8倍;人参皂苷Re对ω-羟化酶CYP4A1基因表达水平有明显下调作用,CYP4A1基因表达水平下调至正常对照的0.4倍。人参皂苷Re时间效应的研究结果表明,随着处理时间增加,人参皂苷Re对CYP2C11、CYP2J3基因表达水平明显上调至正常对照的2.5、2.7倍;然而,对CYP4A1基因表达水平明显下调至正常对照的0.45倍。
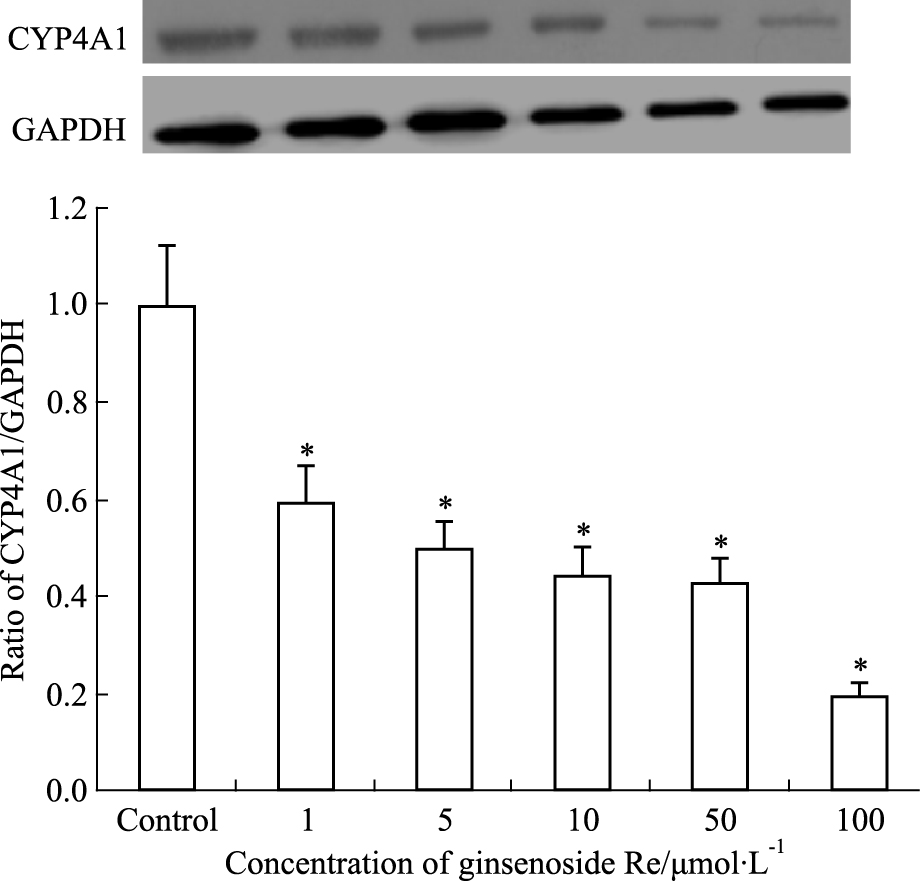
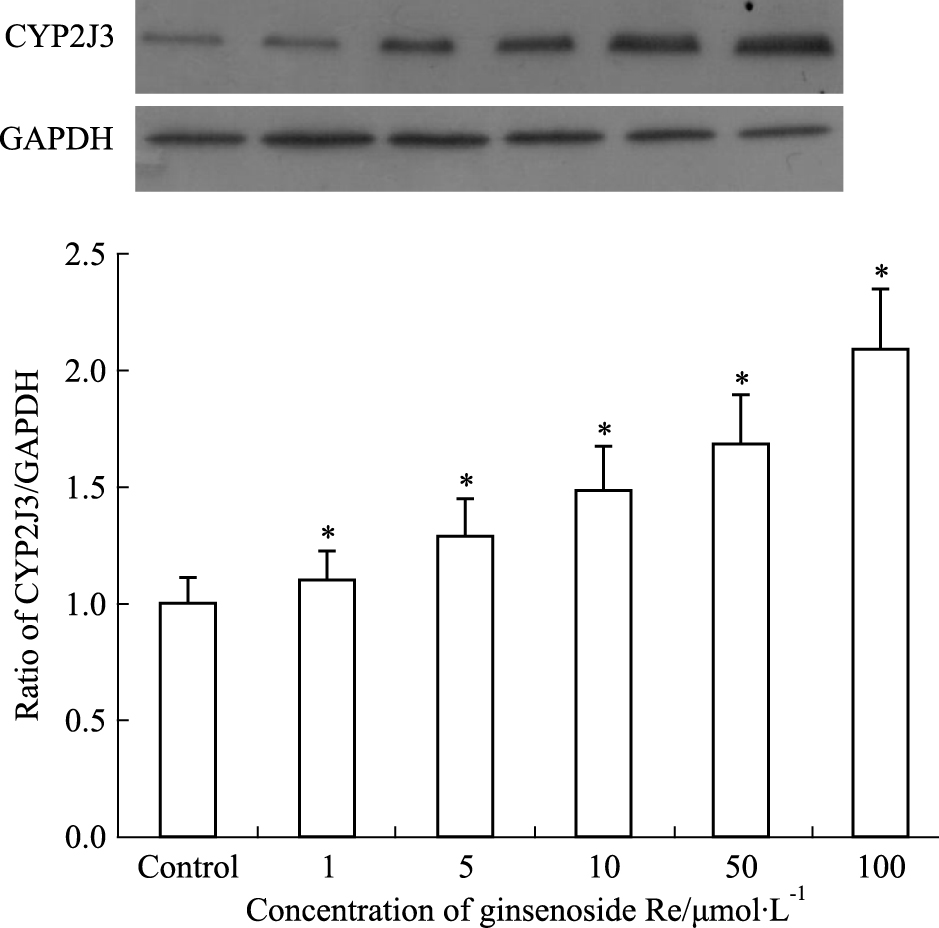
3.2 人参皂苷Re对H9c2细胞CYP450蛋白表达的影响人参皂苷Re处理的细胞样品CYP4A1蛋白表达水平的检测结果如Fig2所示,结果显示人参皂苷Re在浓度为1 μmol·L-1时CYP4A1 蛋白表达水平有所减少,而50 μmol·L-1与对照组比较,对CYP4A1 蛋白表达产生明显的下调效应,人参皂苷Re浓度依赖性下调CYP4A1的表达,在100 μmol·L-1时表达量达到最小。人参皂苷Re对CYP2J3蛋白表达的影响如Fig3所示,人参皂苷Re促进了CYP2J3蛋白的表达,且作用具有浓度依赖性。

|
| Fig 1 Effect of ginsenoside Re on cytochrome P450 mRNA in H9C2 cells (x±s, n=3)A: CYP2C11; B: CYP2J3; C: CYP4A1; D: CYP4A3; E: CYP4F4. (*P < 0.05, **P < 0.01 vs control) |
|
| Fig 2 Effect of ginsenoside Re on CYP4A1protein expression in H9c2 cells (x±s, n=3)*P < 0.05 vs control |
|
| Fig 3 Effect of ginsenoside Re onCYP2J3 protein expression in H9c2 cells (x±s, n=3)*P < 0.05 vs control |
|
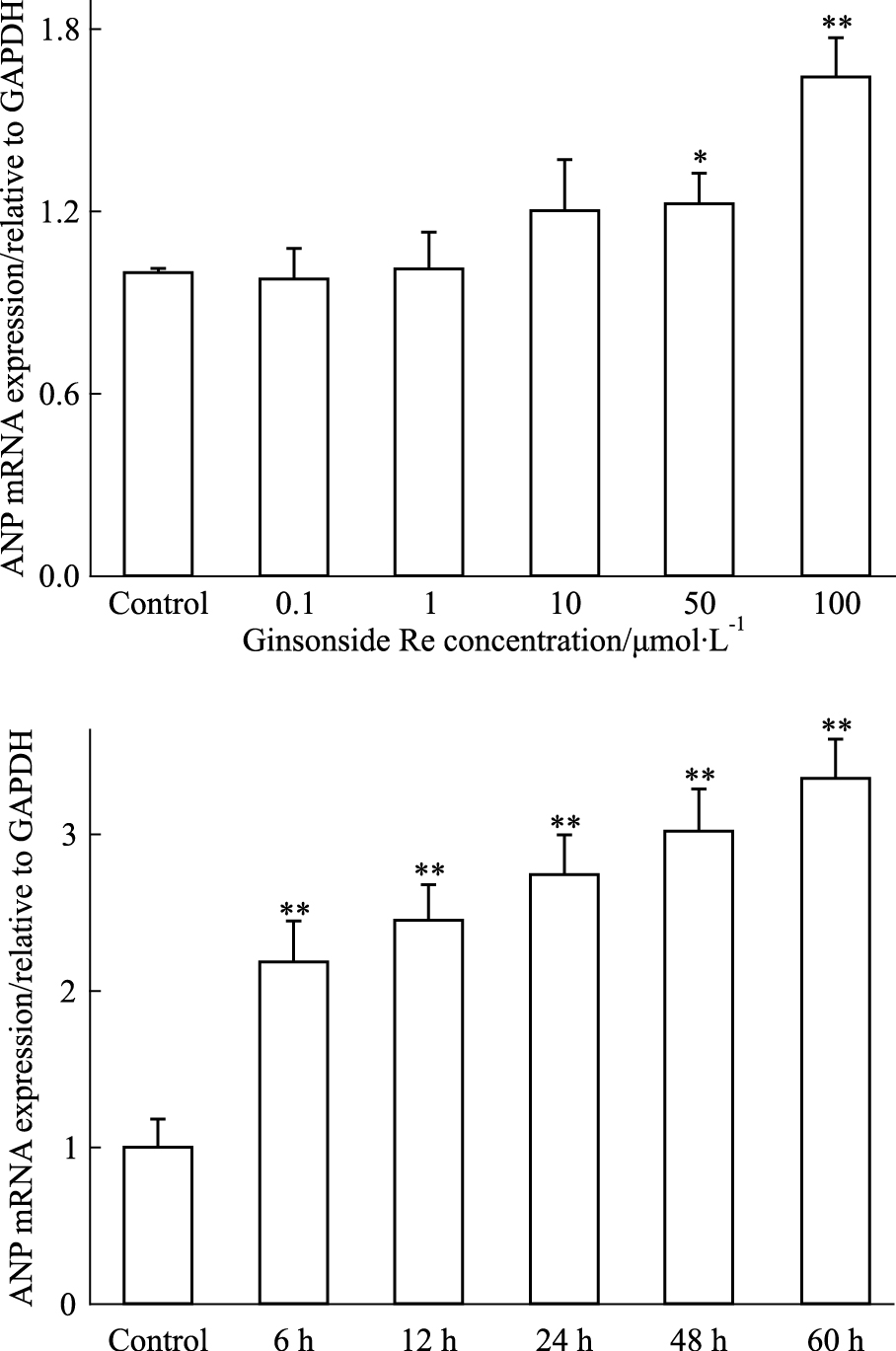
| Fig 4 Effect of ginsenoside Re onANP expression in H9c2 cells (x±s, n=3)*P < 0.05, **P < 0.01 vs control |
结果如Fig4显示,人参皂苷Re能够明显上调ANP基因表达至正常对照的3.2倍。提示人参皂苷Re可能促进心肌细胞释放ANP。
4 讨论CYP450酶通过调控Ca2+通道以及心肌细胞的收缩,CYP450酶可以参与心衰的发展过程。研究发现,心衰病人的心脏中CYP2J2和CYP2E1表达均增多[6]。EETs在心肌疾病中具有重要的生理病理作用,如抗心肌缺血、抗炎症反应、改善内皮功能、抗血小板黏附与聚集等作用,从而起到心肌保护作用。能代谢花生四烯酸产生EETs的CYP亚家族主要是CYP2家族,主要是2C和2J,分布于血管内皮和心肌细胞[8]。HETE是一种潜在的血管收缩剂,作为血管收缩剂的属性与它所作用的离子通道相关联,代谢花生四烯酸产生HETE的CYP亚家族主要是CYP4家族[9]。人参皂苷Re处理后能够明显上调CYP2C11和CYP2J3表达水平,与对照组相比,CYP2C11和CYP2J3 mRNA表达水平分别诱导至1.6和1.8倍;而人参皂苷Re对CYP4A1基因表达水平明显下调作用。进一步在蛋白水平研究了人参皂苷Re对CYP表氧化酶和羟氧化酶的影响,人参皂苷Re可以上调CYP450表氧化酶的表达水平,下调CYP450羟氧化酶的表达水平。特别是对于CYP4A1,人参皂苷Re在基因和蛋白表达水平都有明显的下调作用,而对CYP2J3在基因和蛋白表达水平都有明显的上调作用。人参皂苷Re改变了CYP2J3和CYP4A1的基因和蛋白水平,这可能是人参皂苷Re对心肌细胞作用的新靶点。
研究发现,EETs能够促进心肌细胞分泌内源性物质利钠肽(atrial natriuretic peptide,ANP),ANP通过钠盐调节体液平衡,降低后负荷,舒张血管,抑制心肌细胞肥大,减缓心室重构,发挥着重要的代偿作用[10]。对于ANP的检测结果显示,人参皂苷Re能够明显上调ANP基因表达水平。ANP对心脏有许多保护作用,如降低血压、扩张血管,抑制心肌肥厚和抗纤维化、抵制氧化应激反应、保护缺血/再灌注损伤等重要的生物学作用等[11]。人参皂苷Re对ANP的作用还需要进一步确证。
人参皂苷Re是人参最主要的有效成分,具有确切的疗效;其心肌保护作用也有初步研究,但发挥作用的分子机制并未得到真正的阐述。本研究将药物代谢酶CYP450酶引入心肌细胞作用研究中,人参皂苷Re可以调节心脏表达CYP450酶之间的不平衡,继而参与心脏发病机制HETE和EETs之间不平衡,从而产生心肌减毒作用。但现象背后的本质,还需观察人参皂苷Re对细胞损伤模型的作用,更要在动物水平进行药效学实验和作用机制研究。
(致谢:本实验在军事医学科学院放射与辐射医学研究所药理毒理研究室完成。)
| [1] | Peng L, Sun S, Xie L H, et al. Ginsenoside Re:pharmacological effects on cardiovascular system[J]. Cardiovasc Therap, 2012, 30(4):183-8. |
| [2] | Xie J T, Shao Z H, Vanden Hoek T L, et al. Antioxidant effects of ginsenoside Re in cardiomyocytes[J]. Eur J Pharmacol, 2006, 532(3):201-7. |
| [3] | 张红曦, 王宇光, 马增春, 等.参麦注射液对大鼠心脏细胞色素P450酶的调节作用[J].中国药理学通报, 2014, 30(4):484-90. Zhang H X, Wang Y G, Ma Z C, et al. Effects of Shenmai injection on the regulation of heart CYP450 isozymes in rats[J].Chin Pharmacol Bull, 2014, 30(4):484-90. |
| [4] | 胡东华, 王宇光, 陈志武, 等. 三七总皂苷对H9c2细胞P450酶mRNA表达的影响[J].中国药理学通报, 2013, 29(11):1563-7. Hu D H, Wang Y G, Chen Z W, et al. Effect of Panax notoginseng saponin on cytochrome P450 m RNA expression in H9c2 cell[J].Chin Pharmacol Bull, 2013, 29(11):1563-7. |
| [5] | Chaudhary K R, Batchu S N, Seubert J M.Cytochrome P450 enzymes and the heart[J]. Iubmb Life, 2009, 61(10):954-60. |
| [6] | Yu G G, Zeng X.Cytochrome P450 2J3/epoxyeicosatrienoic acids mediate the cardioprotection induced by ischaemic post-conditioning, but not preconditioning, in the rat[J].Clin Exp Pharmacol Physiol, 2011, 38(4):63-70. |
| [7] | Nebert D W, Russell D W. Clinical importance of the cytochromes P450[J]. Lancet, 2002, 360(9340):1155-62. |
| [8] | Nebert D W, Wikvall K, Miller W L. Human cytochromes P450 in health and disease[J]. Philos Trans R SocLond B Biol Sci, 2013, 368(9):1-24. |
| [9] | 张 迪, 霍洪亮, 张英妮, 等.20-羟二十烷四烯酸在机体生理及病理调节中的作用[J].生理科学进展, 2007, 38(2):120-4. Zhang D, Huo H L, Zhang Y N, et al. Roles of 20-HETE on Physiologic and pathologic regulation in organism[J]. Prog Physiol Sci, 2007, 38(2):120-4. |
| [10] | Oh Y B, Gao S, Shah A, et al. Endogenous angiotensin II suppresses stretch-induced ANP secretion via AT1 receptor pathway[J]. Peptides, 2011, 32(2):374-81. |
| [11] | Pfister R, Michels G.Lack of activation of the antihypertensive cardiac hormones ANP and BNP in human hypertension[J].J Am Coll Cardiol, 2013, 61(8):900-1. |