文章信息
- 张昱勤, 罗傲, 陈世瑞, 琚旭, 陈修远, 张王剑, 郝元涛.
- Zhang Yuqin, Luo Ao, Chen Shirui, Ju Xu, Chen Xiuyuan, Zhang Wangjian, Hao Yuantao
- 长期大气二氧化氮暴露与心脑血管住院风险的因果关联研究
- Causal links between long-term exposure to NO2 and the risk of cardiovascular hospitalization
- 中华流行病学杂志, 2023, 44(6): 885-890
- Chinese Journal of Epidemiology, 2023, 44(6): 885-890
- http://dx.doi.org/10.3760/cma.j.cn112338-20221122-00989
-
文章历史
收稿日期: 2022-11-22
2. 广东省疾病预防控制中心, 广州 511430;
3. 中山大学附属第八医院, 深圳 518033;
4. 北京大学公众健康与重大疫情防控战略研究中心, 北京 100191
2. Guangdong Provincial Center for Disease Control and Prevention, Guangzhou 511430, China;
3. The Eighth Affiliated Hospital, Sun Yat-sen University, Shenzhen 518033, China;
4. Peking University Center for Public Health and Epidemic Preparedness & Response, Beijing 100191, China
过去30年中,全球心脑血管疾病患者人数持续上升。2019年心脑血管疾病患者人数为5.23亿,是1990年(2.71亿)的近2倍[1]。据估计,我国2019年心脑血管疾病患者约3.3亿,造成了巨大的疾病负担[2-3]。随着社会经济发展,空气污染对人群心脑血管疾病危害受到关注。交通污染是城市空气污染的重要来源,而二氧化氮(NO2)已被确定为交通污染的标志物[4],且已有部分研究表明大气NO2与心脑血管疾病存在关联[5]。
现有研究多集中在欧美等发达国家,我国的相关研究较缺乏[6]。我国居民的暴露种类、暴露途径、生活方式和遗传背景与国外人群差异较大,并且我国气候类型复杂多样,具有更高的大气NO2污染浓度[7],无法直接引用国外的研究结论。同时,现有证据多集中在短期暴露的健康危害,缺乏队列研究提供长期暴露的健康危害证据[8],而多项研究显示大气污染的长期暴露危害更大[9-10]。此外,传统队列研究多采用关联性分析,难以提供因果解释。近年来,为了在观察性研究中进行因果推断研究,逐步发展出了基于逆概率加权的边际结构模型,其已被应用于流行病学领域,用于估计观察性研究中暴露与结局的因果关联[11-12]。本研究依托我国“基于社区人群的健康队列”广州市子队列,探讨大气NO2长期暴露与心脑血管住院的因果关联,为相关大气环境政策的制定和污染控制策略提供科学依据。
对象与方法1. 研究对象:来源于“基于社区人群的健康队列”。该队列为自然人群队列,在广东省示范区(深圳市、中山市、广州市)样本共计125万人[13]。本研究基于广州市子队列,于2015年1-12月,从广州市荔湾区和越秀区的35个社区随机招募36 271名成年参与者,进行了临床和实验室检查,由经过统一培训的社区医生对其进行面对面访谈,以获得基本人口学特征和行为方式数据,并随访至2020年12月31日,研究对象均签署知情同意书。
2. 资料来源:大气污染暴露数据来自于插值估计。从中国环境监测总站(http://www.cnemc.cn/)获取广东省60个污染监测站点2015-2020年NO2的每小时浓度数据,将其整合为各站点的年均NO2浓度,利用克里金插值法建模估计广州市空间分辨率为1 km2的NO2网格数据[14]。NO2插值的十折交叉验证R2和均方根误差分别为0.83和4.31 μg/m3。每个调查对象每年的大气NO2暴露根据家庭住址经纬度进行邻近匹配。
通过问卷调查收集研究对象的基本人口学特征(性别、年龄、民族、文化程度、婚姻状况及BMI)、行为方式(吸烟状况、饮酒状况、运动频率以及医疗费用支付方式)等。为进一步考虑土地利用因素[15]、相关环境污染因素及气象因素对NO2污染-健康效应的影响,本研究收集了归一化植被指数(NDVI)、PM2.5污染、气温和相对湿度等数据。
研究结局为心脑血管住院,该数据通过与广州市418家医疗机构(包括71家三级医疗机构、100家二级医疗机构、71家初级医疗机构及176家其他医疗机构)的电子住院记录联网获取。根据《国际疾病分类》第十版(ICD-10)对住院疾病进行编码,获取研究对象的总心脑血管疾病(ICD-10:I00~I99)、心血管疾病(ICD-10:I00~I59,I70~I99)以及脑血管疾病(ICD-10:I60~I69)入院结局信息。结局数据根据调查对象身份证号进行匹配。
3. 统计学分析:连续型资料采用x±s表示,分类资料采用频数、百分比描述。两类资料的单因素分析分别采用t检验和χ2。本研究绘制了因果关系图—有向无环图[16],筛选出需要调整的混杂变量,包括年龄、性别、民族、文化程度、婚姻状况、吸烟状况、运动频率、医疗费用支付方式、NDVI、气温以及相对湿度。
首先本研究采用序贯建模法构建传统的时依Cox模型[17],分别为仅纳入暴露变量NO2的单因素时依Cox模型(模型1)、在模型1基础上调整性别、年龄(模型2),及在模型2基础上调整因果图筛选的所有混杂变量(模型3)。其次构建了基于逆概率加权的边际结构时依Cox模型[18](模型4)。其中,时依变量包括NO2、NDVI、气温和相对湿度。模型中采用逆概率权重用于重加权原始观察单位,借此模拟随机对照试验构造出暴露分配与结局之间条件独立的“伪世界”,以消除观测到的混杂因素对暴露因素的影响。与实际人群不同,“伪世界”中虚拟人群的暴露变量不受混杂变量的影响,而各暴露组的结局发生率则与实际人群相同。基于“伪世界”的观察单位进行回归分析即可得到因果效应估计值[11, 18]。逆概率权重的构建基于线性混合效应模型和XGBoost算法,利用标准均值差(SMD)评价不同暴露浓度下的协变量平衡性,本研究SMD < 0.1表明平衡性良好,效应估计值具有因果解释性。基于此,最终主分析采用基于XGBoost算法的逆概率权重。最后,为排除暴露窗口、NDVI范围及PM2.5对结果稳定性的影响,本研究进行敏感性分析:①基于2~5年的暴露窗口分别进行累积滞后分析;②基于各调查对象居住地址250 m和1 000 m范围内的NDVI构建模型;③构建调整PM2.5的多污染模型。
为评估结果稳定性,本研究参考文献[19]将主分析和各敏感性分析的估计参数用于构建Meta回归,利用似然比检验评估结果稳定性,以P > 0.05表示结果稳健。为进一步评估未测量混杂因素对研究结论的潜在影响,本研究计算了E值,即未测量混杂与暴露和结局之间具有的最低关联强度,其大小表明如果有未测量混杂因素能够推翻研究结论,至少需要达到的与结局的关联强度大小[20]。采用R 4.1.3软件进行数据处理和分析。双侧检验,检验水准α=0.05。
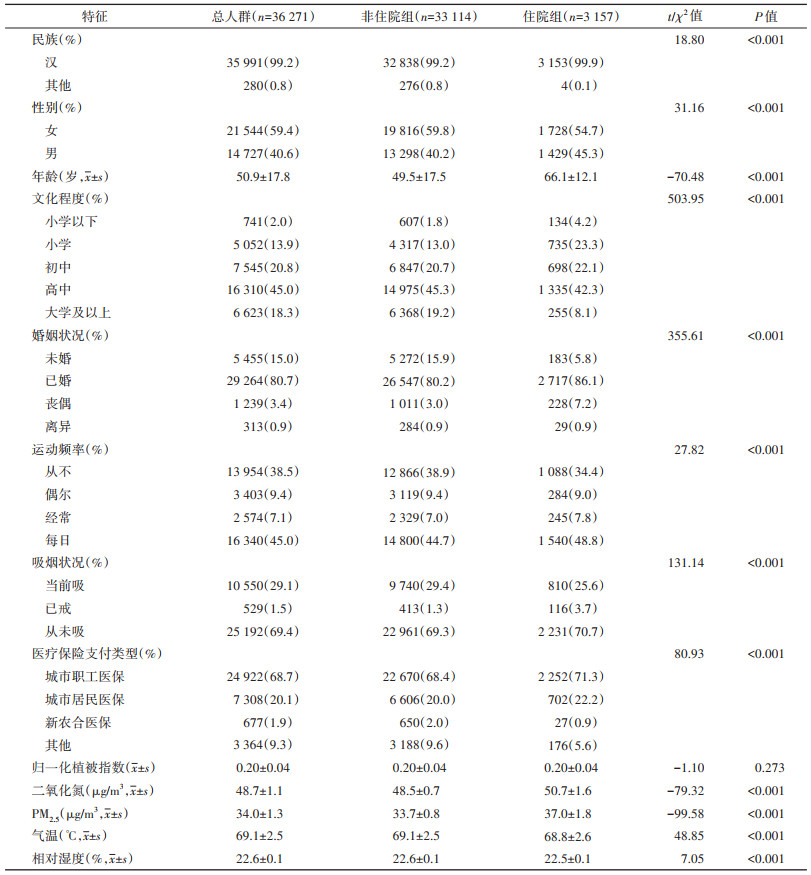
结果1. 基本特征:平均随访5.6年,总计随访203 822人年。36 271名基线调查对象中,汉族35 991名(99.2%),男性14 727名(40.6%),女性21 544名(59.4%),人群年龄为(50.9±17.8)岁,总心脑血管住院率为8.7%(3 157/36 271)。2015-2020年广州市NO2污染年均浓度呈下降趋势,研究对象年均NO2污染暴露为48.7 μg/m3。年均NO2暴露浓度较高时总心脑血管住院组与非住院组人群相比,差异有统计学意义(P < 0.001);相比于非住院组,住院组的平均年龄较高,占比较多为汉族、男性、已婚、文化程度较低、运动频率较高、从未吸烟和城市医保人群(均P < 0.001)。见表 1。
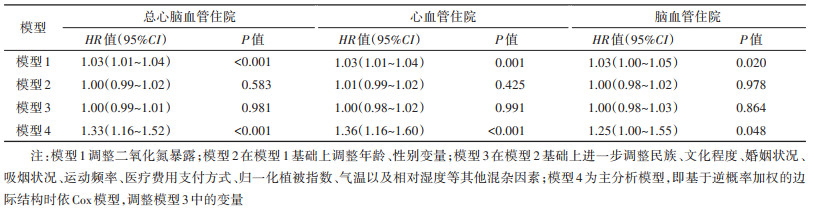
2. 大气NO2污染长期暴露对心脑血管住院的影响分析:主分析结果表明NO2长期暴露每增加10 μg/m3,总心脑血管、心血管和脑血管住院的风险比(HR)值(95%CI)分别为1.33(1.16~1.52)、1.36(1.16~1.60)及1.25(1.00~1.55)。见表 2。
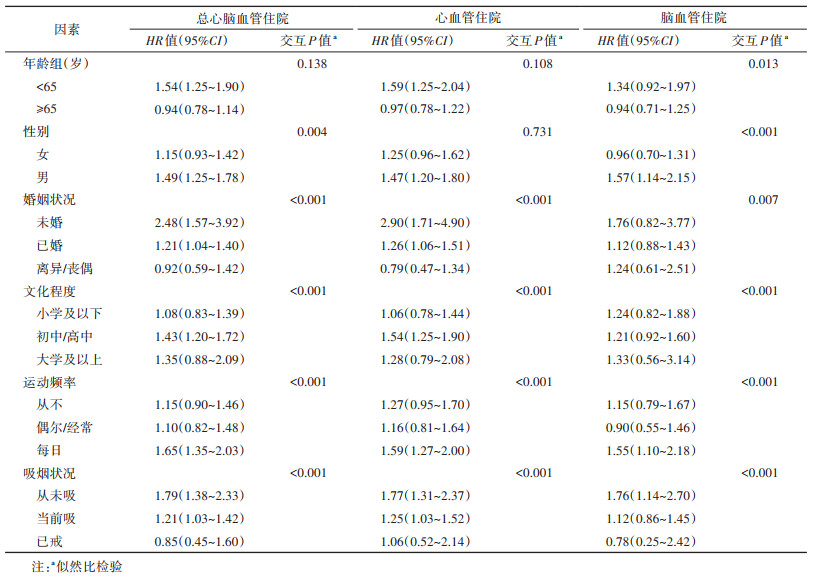
分层分析结果显示,未婚/已婚、文化程度为初中/高中、高运动频率、从未吸烟/当前吸烟人群亚组中,NO2年均暴露浓度与总心脑血管及其亚类住院风险的关联均有统计学意义(P < 0.05)。女性人群亚组中,NO2年均暴露浓度与总心脑血管和脑血管住院风险的关联均有统计学意义(P < 0.05);年龄 < 65岁人群亚组中,NO2年均暴露浓度仅与脑血管住院风险的关联有统计学意义(P=0.013),但性别和年龄各亚组间关联性在3种结局中均较为一致。见表 3。所有敏感性分析Meta回归提示本研究结果较稳健,同时,总心脑血管、心血管和脑血管住院的E值分别为1.98、2.07和1.81,反映研究结果的稳健性较好。
本研究依托“基于社区人群的健康队列”广州市子队列,利用逆概率加权的边际结构模型,探讨了长期NO2暴露与心脑血管住院的因果关联。结果显示,长期NO2暴露每增加10 μg/m3,所致心脑血管、心血管以及脑血管住院风险高达25%~36%,且提示未婚/已婚、文化程度为初中/高中、高运动频率以及从未吸烟/当前吸烟人群可能更加易感。
多项国外研究与本研究结果类似。一项关于空气污染对死亡和住院影响的系统综述研究结果显示,包括NO2在内的6种空气污染物都可增加一系列疾病的住院风险,其中常见的是心脑血管疾病[6]。美国2000-2016年医保参与者队列研究结果发现,年均NO2暴露每增加1 pbb,心脑血管住院风险HR值为1.03,且在低浓度时仍呈现有害作用[21]。此外,一项针对全美国不同地区老年人的区域性生态学研究表明,年均NO2暴露每增加10 ppb,将造成总心脑血管疾病死亡风险增加13.3%[22]。目前研究认为,空气污染物渗透到肺组织和全身循环,可造成血管收缩、高血压和斑块不稳定,导致炎症和氧化水平的增加,从而引起心血管和呼吸系统损害[23];另外,毒理学实验表明NO2可与呼吸道和/或肺部气道表面液中的成分发生反应,由此产生的高反应性蛋白质和脂质氧化产物随后可能通过二次反应损害上皮细胞,从而引起炎症,增加罹患心脑血管疾病的风险[24]。
目前,影响长期NO2暴露所致心脑血管住院风险的行为方式因素研究不足[8]。部分欧美国家研究表明,年龄、性别、文化程度、吸烟状况等因素对长期NO2暴露的心脑血管疾病风险有效应修饰作用[25-26]。年龄和运动频率的效应修饰作用也许并非生物学机制造成,而可能是相应的易感群体由于工作、生活方式等原因具有更长时间的职业或交通暴露[27]。目前已有研究表明,女性气道腔内径仅为相同肺容积男性的58%,可能造成女性每单位气道表面积中吸入的NO2浓度更高,易感性增大[28]。从未吸烟者相对而言可能具有更低的NO2耐受性,同时本研究中从未吸烟者多为女性(68.2%),也可能是造成吸烟效应修饰作用的原因之一。对于文化程度而言,文化程度越高的人群可能获得更好的工作生活条件,居住环境更接近市中心,因此更易发生NO2暴露所致心脑血管住院[29]。尽管本研究可能提示了部分易感人群,但研究结果还需结合进一步的毒理学与流行病学研究,深入探讨不同生活、行为因素的效应修饰作用及其机制。
本研究利用队列数据,采用边际结构模型探讨了NO2长期暴露对心脑血管住院的因果效应,识别出可能的易感人群,具有一定的公共卫生意义。本研究存在局限性。首先,研究中的环境暴露数据是基于国家监测站点数据的模型估计值,可能由于Berkson以及Classical误差造成暴露错分,导致研究结果的低估[30];其次,研究未纳入心脑血管疾病患病史信息作为协变量进行调整,结果可能存在偏倚,但通过E值的计算和多个敏感性分析说明结果具有一定的稳健性;最后,由于数据可及性的原因,研究尚未收集死因数据,因此无法探讨院外死亡的影响,未来将进一步收集相关数据进行深入研究。
利益冲突 所有作者声明无利益冲突
作者贡献声明 张昱勤:数据整理、统计学分析、论文撰写;罗傲:论文撰写;陈世瑞、琚旭:数据整理;陈修远:论文修改;张王剑:研究指导、论文修改、经费支持;郝元涛:研究指导、经费支持
志谢 感谢钟秉成、王馨苒对本研究的支持
| [1] |
Roth GA, Mensah GA, Johnson CO, et al. Global burden of cardiovascular diseases and risk factors, 1990-2019: update from the GBD 2019 Study[J]. J Am College Cardiol, 2020, 76(25): 2982-3021. DOI:10.1016/j.jacc.2020.11.010 |
| [2] |
The Writing Committee of the Report on Cardiovascular Health and Diseases in China. Report on cardiovascular health and diseases in China 2021: an updated summary[J]. Biomed Environ Sci, 2022, 35(7): 573-603. DOI:10.3967/bes2022.079 |
| [3] |
Yang BY, Guo YM, Markevych I, et al. Association of long-term exposure to ambient air pollutants with risk factors for cardiovascular disease in China[J]. JAMA Netw Open, 2019, 2(3): e190318. DOI:10.1001/jamanetworkopen.2019.0318 |
| [4] |
Deng QH, Lu C, Yu YC, et al. Early life exposure to traffic-related air pollution and allergic rhinitis in preschool children[J]. Respir Med, 2016, 121: 67-73. DOI:10.1016/j.rmed.2016.10.016 |
| [5] |
Yang BY, Qian ZM, Howard SW, et al. Global association between ambient air pollution and blood pressure: A systematic review and meta-analysis[J]. Environ Pollut, 2018, 235: 576-588. DOI:10.1016/j.envpol.2018.01.001 |
| [6] |
Al Ahad MA, Sullivan F, Demšar U, et al. The effect of air-pollution and weather exposure on mortality and hospital admission and implications for further research: A systematic scoping review[J]. PLoS One, 2020, 15(10): e0241415. DOI:10.1371/journal.pone.0241415 |
| [7] |
Deng WZ, Cohen JB, Wang S, et al. Improving the understanding between climate variability and observed extremes of global NO2 over the past 15 years[J]. Environ Res Lett, 2021, 16(5): 054020. DOI:10.1088/1748-9326/abd502 |
| [8] |
Huang SW, Li HM, Wang MR, et al. Long-term exposure to nitrogen dioxide and mortality: A systematic review and meta-analysis[J]. Sci Total Environ, 2021, 776: 145968. DOI:10.1016/j.scitotenv.2021.145968 |
| [9] |
Beverland IJ, Cohen GR, Heal MR, et al. A comparison of short-term and long-term air pollution exposure associations with mortality in two cohorts in Scotland[J]. Environ Health Perspect, 2012, 120(9): 1280-1285. DOI:10.1289/ehp.1104509 |
| [10] |
Kloog I, Coull BA, Zanobetti A, et al. Acute and chronic effects of particles on hospital admissions in New-England[J]. PLoS One, 2012, 7(4): e34664. DOI:10.1371/journal.pone.0034664 |
| [11] |
Robins JM, Hernán MÁ, Brumback B. Marginal structural models and causal inference in epidemiology[J]. Epidemiology, 2000, 11(5): 550-560. DOI:10.1097/00001648-200009000-00011 |
| [12] |
Xie DW, Yang W, Jepson C, et al. Statistical methods for modeling time-updated exposures in cohort studies of chronic kidney disease[J]. Clin J Am Soc Nephrol, 2017, 12(11): 1892-1899. DOI:10.2215/CJN.00650117 |
| [13] |
Ruan B, Yu ZX, Yang SG, et al. Establishment and development of national community-based collaborative innovation demonstration areas to achieve the control target of hepatitis B in China[J]. BMC Infect Dis, 2019, 19(1): 617. DOI:10.1186/s12879-019-4150-9 |
| [14] |
Zhang LC, An J, Tian X, et al. Acute effects of ambient particulate matter on blood pressure in office workers[J]. Environ Res, 2020, 186: 109497. DOI:10.1016/j.envres.2020.109497 |
| [15] |
Twohig-Bennett C, Jones A. The health benefits of the great outdoors: A systematic review and meta-analysis of greenspace exposure and health outcomes[J]. Environ Res, 2018, 166: 628-637. DOI:10.1016/j.envres.2018.06.030 |
| [16] |
郑卫军, 王晓燕, 王憓. 基于因果关系图进行多因素回归分析的变量筛选[J]. 中国卫生统计, 2014, 31(5): 908-910. DOI: CNKI:SUN:ZGWT.0.2014-05-056. Zheng WJ, Wang XY, Wang H. Variable selection of the multiple regression analysis based on DAGs[J]. Chin J Health Stat, 2014, 31(5): 908-910. DOI: CNKI:SUN:ZGWT.0.2014-05-056. |
| [17] |
Zhang ZH, Reinikainen J, Adeleke KA, et al. Time-varying covariates and coefficients in Cox regression models[J]. Ann Transl Med, 2018, 6(7): 121. DOI:10.21037/atm.2018.02.12 |
| [18] |
王振宇, 陈朔华, 赵欣宇, 等. Cox及其拓展模型在基于队列的依时暴露因素效应估计中的应用[J]. 中华流行病学杂志, 2020, 41(6): 957-961. DOI:10.3760/cma.j.cn112338-20200119-00046 Wang ZY, Chen SH, Zhao XY, et al. Application of Cox and extended regression models on modeling the effect of time-updated exposures in cohort studies[J]. Chin J Epidemiol, 2020, 41(6): 957-961. DOI:10.3760/cma.j.cn112338-20200119-00046 |
| [19] |
Han CL, Xu RB, Gao CX, et al. Socioeconomic disparity in the association between long-term exposure to PM2.5 and mortality in 2 640 Chinese counties[J]. Environ Int, 2021, 146: 106241. DOI:10.1016/j.envint.2020.106241 |
| [20] |
van der Weele TJ, Ding P. Sensitivity analysis in observational research: introducing the E-value[J]. Ann Intern Med, 2017, 167(4): 268-274. DOI:10.7326/M16-2607 |
| [21] |
Klompmaker JO, Hart JE, James P, et al. Air pollution and cardiovascular disease hospitalization - Are associations modified by greenness, temperature and humidity?[J]. Environ Int, 2021, 156: 106715. DOI:10.1016/j.envint.2021.106715 |
| [22] |
Eum KD, Kazemiparkouhi F, Wang BY, et al. Long-term NO2 exposures and cause-specific mortality in American older adults[J]. Environ Int, 2019, 124: 10-15. DOI:10.1016/j.envint.2018.12.060 |
| [23] |
Fiordelisi A, Piscitelli P, Trimarco B, et al. The mechanisms of air pollution and particulate matter in cardiovascular diseases[J]. Heart Fail Rev, 2017, 22(3): 337-347. DOI:10.1007/s10741-017-9606-7 |
| [24] |
Gamon LF, Wille U. Oxidative damage of biomolecules by the environmental pollutants NO2 and NO3[J]. Acc Chem Res, 2016, 49(10): 2136-2145. DOI:10.1021/acs.accounts.6b00219 |
| [25] |
Yazdi MD, Wang Y, Di Q, et al. Long-term association of air pollution and hospital admissions among Medicare participants using a doubly robust additive model[J]. Circulation, 2021, 143(16): 1584-1596. DOI:10.1161/CIRCULATIONAHA.120.050252 |
| [26] |
Atkinson RW, Carey IM, Kent AJ, et al. Long-term exposure to outdoor air pollution and incidence of cardiovascular diseases[J]. Epidemiology, 2013, 24(1): 44-53. DOI:10.1097/EDE.0b013e318276ccb8 |
| [27] |
Laurent O, Bard D, Filleul L, et al. Effect of socioeconomic status on the relationship between atmospheric pollution and mortality[J]. J Epidemiol Community Health, 2007, 61(8): 665-675. DOI:10.1136/jech.2006.053611 |
| [28] |
Kanner RE, Connett JE, Altose MD, et al. Gender difference in airway hyperresponsiveness in smokers with mild COPD. The Lung Health Study[J]. Am J Respir Crit Care Med, 1994, 150(4): 956-961. DOI:10.1164/ajrccm.150.4.7921469 |
| [29] |
Cramer J, Jørgensen JT, Hoffmann B, et al. Long-term exposure to air pollution and incidence of myocardial infarction: a Danish nurse cohort study[J]. Environ Health Perspect, 2020, 128(5): 057003. DOI:10.1289/EHP5818 |
| [30] |
Zhang WJ, Li S, Hopke PK, et al. Triggering of cardiovascular hospital admissions by fine particle concentrations in New York state: Before, during, and after implementation of multiple environmental policies and a recession[J]. Environ Pollut, 2018, 242: 1404-1416. DOI:10.1016/j.envpol.2018.08.030 |
 2023, Vol. 44
2023, Vol. 44