文章信息
- 从祥丰, 刘少博, 马吉祥, 王文绢, 陈波, 李剑虹.
- Cong Xiangfeng, Liu Shaobo, Ma Jixiang, Wang Wenjuan, Chen Bo, Li Jianhong
- 我国成年人自评健康状况与脑卒中发病风险的前瞻性研究
- Association between self-rated health status and risk of stroke in Chinese adults: a prospective study
- 中华流行病学杂志, 2021, 42(3): 513-519
- Chinese Journal of Epidemiology, 2021, 42(3): 513-519
- http://dx.doi.org/10.3760/cma.j.cn112338-20200103-00006
-
文章历史
收稿日期: 2020-01-03
2. 中国疾病预防控制中心慢病和老龄健康管理处, 北京 102206
2. Office of Non-Communicable Diseases and Ageing Health Management, Chinese Center for Disease Control and Prevention, Beijing 102206, China
2017年中国疾病负担研究结果显示[1],脑卒中是造成中国居民疾病负担最大的疾病。目前中国脑卒中现患病人数约为1 300万[2],且随着人口老龄化进程加速、肥胖率上升等因素影响,我国脑卒中发病率进一步上升[3-4]。加强脑卒中防控刻不容缓。尽早识别脑卒中潜在影响因素和预测因素,尤其是简单、易获得的因素,对防控工作具有重大意义。自评健康状况是一个简单、全面评价个人健康的因素,是心血管病死亡的独立预测因素[5-9]。但关于自评健康状况与脑卒中发病关系的研究较少,且研究结论不一[10-12]。本研究以前瞻性队列为基础,分析自评健康状况与脑卒中发病风险关联,为我国开展脑卒中预测和防治工作提供科学依据。
对象与方法1. 研究对象:2010年中国慢性病及其危险因素监测数据作为基线数据。从162个监测点(包括新疆生产建设兵团农二师)中选取11个省(河北、吉林、黑龙江、江苏、浙江、江西、河南、湖南、四川、贵州和陕西)的60个监测点(城市监测点25个、农村监测点35个)作为随访点。排除基线患有心血管病者(437人),共36 195人进入随访队列。2016- 2017年进行随访调查,实际完成随访者27 441人(包括死亡814人,其中死于脑卒中238人)。将失访人群和未失访人群重要特征(年龄、性别、糖尿病、TC、HDL-C)进行比较,显示两人群的年龄、性别分布和血脂水平略有差异,血糖水平无差异。排除恶性肿瘤者(68人)、年龄 < 20岁者(432人)、心血管病患病信息缺失者(147人)、心血管病确诊日期错误者(2010年以前)(52人)、BMI异常者(< 15 kg/m2或≥40 kg/m2)(43人),最终共26 699人纳入分析。本研究通过中国疾病预防控制中心慢性非传染性疾病预防控制中心伦理审查委员会的审查(审批号:201524B),所有调查对象均签署了知情同意书。
2. 研究内容:2010年基线调查内容包括问卷调查、体格测量和实验室检测。问卷调查以面对面询问方式进行调查,内容包括个人基本信息、生活方式(吸烟、饮酒、饮食、身体活动情况等)、慢性病患病情况等。体格测量包括身高、体重、腰围和血压。实验室检测指标包括FPG、餐后2 h血糖、TC、LDL-C、HDL-C和TG[13]。2016-2017年进行随访调查,通过问卷调查的形式调查个人基本信息(性别、身份证号码等)、死亡情况信息、心血管疾病发病信息(“2010年以来,您有没有被医生诊断患有脑卒中”“临床诊断依据”“影像辅助检查”“确诊时间”“确诊单位”等信息进行心血管病的确定)等。同时与死因库进行匹配,进一步获取死亡信息。
自评健康状况通过问卷获取,“您认为您的健康状况如何?”选项:①非常好,②好,③一般,④差,⑤非常差,5个等级。由于“非常差”人数较少,将“差”和“非常差”进行合并,分为①非常好,②好,③一般,④差4个等级。疾病分类采用国际疾病分类(第10版)(ICD-10)。本研究随访结局是发生脑卒中,包括蛛网膜下腔出血(I60)、脑内出血(I61)和缺血性卒中(脑梗死)(I63)。
3. 统计学分析:使用SAS 9.4软件进行数据清理和统计分析。比较自评健康组间研究对象人口学资料等基线特征差异,连续变量采用一般线性模型,用x±s表示;分类资料采用χ2检验,等级资料采用Kruskal-Wallis H检验,用n(%)表示;应用Schoenfeld residuals方法进行等比例风险假设验证,应用Cox比例风险模型进行单因素和多因素分析,计算风险比(HR)及其95%CI,评估自评健康状况与脑卒中发病风险的关联。交互检验采用似然比检验,比较有、无交互项模型间是否差异有统计学意义,采用Stata 14.0软件计算P值。敏感性分析,将死亡人群和基线患有糖尿病者剔除,重复上述Cox回归分析。双侧检验,以P < 0.05为差异有统计学意义。
结果1. 基本情况:共纳入26 699名研究对象,年龄(48.3±13.5)岁,男性占45.1%,自评健康差者占7.8%,文化程度高中及以上占20.5%,家庭年收入≥2万元占49.7%,城市居民占38.9%。与自评健康非常好者相比,自评健康差者年龄偏大、女性、文化程度低、家庭年收入低、患有慢性病以及农村地区居民所占比例高。见表 1。
2. 自评健康状况与脑卒中发病风险关联分析:研究对象随访(6.4±0.5)年,共计随访171 431.1人年。随访期间共观察到脑卒中发病1 332例(蛛网膜下腔出血32例、脑内出血197例、缺血性卒中1 149例,疾病重合46例),发病密度为7.77/1 000人年。
脑卒中分析中,经调整相关混杂因素后(模型2),与自评健康非常好者相比,自评健康差者脑卒中发病风险增加68%(HR=1.68;95%CI:1.22~2.30)。进一步调整糖尿病、高血压和地区后(模型3),自评健康差者脑卒中发病风险增加68%(HR=1.68;95%CI:1.22~2.32)。在脑卒中亚型缺血性卒中分析中,调整相关混杂因素后(模型2),以自评健康非常好者为参照,自评健康差者缺血性卒中发病风险增加57%(HR=1.57;95%CI:1.13~2.18)。进一步调整糖尿病、高血压和地区后,自评健康差者缺血性卒中发病风险为47%(HR=1.47;95%CI:1.05~2.05)。趋势性分析结果显示,自评健康每增加一个等级,脑卒中和缺血性卒中发病风险分别增加23%和22%。见表 2。
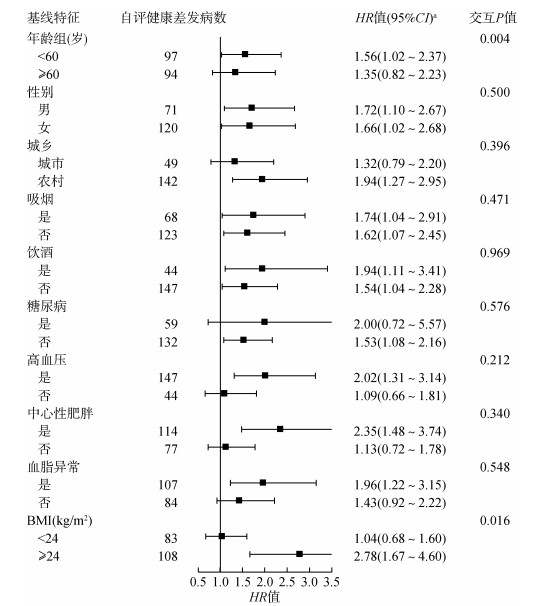
3. 亚组分析:性别、城乡、吸烟、饮酒、糖尿病、高血压、中心性肥胖、血脂异常对自评健康与脑卒中发病风险关联未见效应修饰作用(交互P > 0.05),年龄、BMI对自评健康与脑卒中发病风险关联具有效应修饰作用(交互P < 0.05),且年龄 < 60岁、BMI≥24 kg/m2人群中,自评健康差者与脑卒中发病风险的关联效应值更高。仅见年龄和血脂异常对自评健康与缺血性卒中发病风险关联具有效应修饰作用(交互P < 0.05),且年龄对缺血性卒中发生的修饰作用类似于脑卒中发病,血脂异常人群,自评健康差与缺血性卒中发病风险的关联效应值更高。见图 1。
|
| 注:a分析以自评健康非常好为参照,报告自评健康差者发生脑卒中风险的效应值;调整年龄、性别、文化程度、职业、婚姻状况、吸烟、饮酒、身体活动、血脂异常、糖尿病、高血压、BMI、地区、中心性肥胖,不包括分层因素 图 1 自评健康与脑卒中发病风险关联的基线特征亚组分析(n=26 699) |
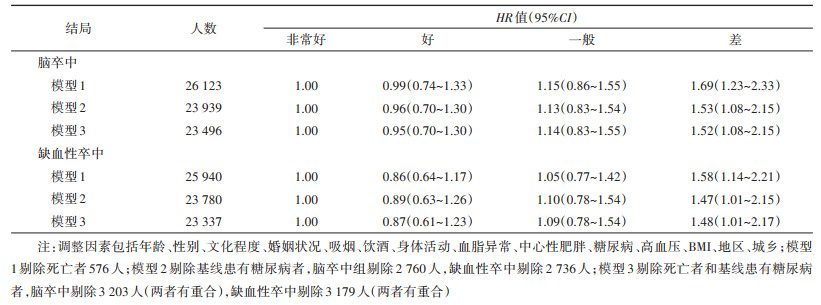
4. 敏感性分析:在脑卒中分析中,剔除死亡者,结果显示以自评健康非常好者为参照,自评健康差者脑卒中发病风险效应值为1.69(95%CI:1.23~2.33);剔除基线患有糖尿病者,自评健康差者风险效应值为1.53(95%CI:1.08~2.15);两者同时剔除,风险效应值为1.52(95%CI:1.08~2.15)。在缺血性卒中分析中,剔除死亡者发病风险效应值为1.58(95%CI:1.14~2.21);剔除基线患有糖尿病者,风险效应值为1.47(95%CI:1.01~2.15);两者同时剔除,风险效应值为1.48(95%CI:1.01~2.17)。敏感性分析总体结果显示,脑卒中结局风险效应值降低,缺血性卒中结局风险效应值未见明显变化。见表 3。
自评健康状况是一个简单、易获得的指标,被认为是不同人群心血管病死亡和全死因的有力预测因素[14-16]。尽管美国心脏协会推荐将自评健康作为心血管健康的一个重要指标[17],但关于自评健康与心血管发病的相关研究较少。本研究利用6年的前瞻性研究,揭示自评健康与脑卒中发病风险关联。
研究结果显示,脑卒中分析中,与自评健康非常好者相比,自评健康差者发生脑卒中的风险增加68%(HR=1.68,95%CI:1.22~2.32)。英国的一项纳入11 181名≥65岁人群的队列研究显示[18],与自评健康非常好/好者相比,自评健康一般/差者发生脑卒中的风险增加50%(HR=1.5,95%CI:1.1~1.9)。结果提示,在不同的人群中自评健康与脑卒中发生风险仍存在关联。中国慢性病前瞻性研究项目(China Kadoorie Biobank,CKB)研究显示[10],自评健康差者(参照是非常好者)发生脑卒中风险效应值为1.49(95%CI:1.42~1.56)。本研究风险效应值略高于CKB研究,可能原因是研究人群特征不同(如本研究人群年龄20~89岁,CKB人群30~79岁)。美国、巴西等研究也得出相似结论[19-20]。有学者研究显示[21-23],自评健康差的人群,C反应蛋白水平和纤维蛋白水平更高,这可能是自评健康与脑卒中发病风险存在关联的生物学机制之一。
目前关于自评健康与脑卒中亚型发病关联的研究较少。本研究仅对缺血性卒中进行了分析,出血性卒中未进行分析,因为出血性卒中样本量计算和分析结果均提示样本不足。在缺血性卒中分析中,剔除了随访结局是出血性卒中的人群。虽然卒中亚型生理机制不同,但它们具有一些共同的危险因素,如肥胖、高血压、吸烟等[24],因此考虑将其剔除。在调整相关混杂因素后,与自评健康非常好者相比,自评健康差者缺血性卒中发生风险值为1.47(95%CI:1.05~2.05),与一些研究相一致[10],如CKB研究风险值为1.45(95%CI:1.38~1.53)。该研究结果为自评健康与脑卒中亚型发病关系提供了一定的证据。进一步亚组分析显示,有些亚组自评健康与脑卒中发病风险未见关联。可能原因是有些亚组样本不足,或者可能在某些特征人群中确实存在无关联的结果,这有待今后进一步去研究。交互检验结果显示,不同年龄和BMI人群自评健康与脑卒中发病风险效应值不同,同时在缺血性卒中分析中发现,除年龄外,血脂异常和正常人群效应值也不同。这为我们今后进行针对性的人群干预提供了思路。
综上所述,自评健康与脑卒中和缺血性卒中发病风险均存在关联。有研究认为自评健康可以作为心血管事件的预测因素,它相较于传统危险因素(如高血压、糖尿病、吸烟)可能为脑卒中发病预测提供额外价值[10, 19]。但是否真正可以用于脑卒中发病的预测,还需要大量的队列研究进行证实,尤其是需要一些来自不同地区、人群的队列研究。
本研究存在局限性。首先,由于样本不足,未能对脑卒中亚型出血性卒中进行分析,今后还需扩大样本对该亚型进行研究。其次,自评健康是一个相对主观的指标,可能存在信息偏倚。但一般研究对象会根据客观的身体情况进行回答,因此影响可能有限。再次,本研究对一些因素未能考虑(如空气污染、焦虑抑郁等),可能存在残余混杂。但有研究认为,这些因素可能不会实质性的改变结果[10]。
利益冲突 所有作者均声明不存在利益冲突
| [1] |
Zhou MG, Wang HD, Zeng XY, et al. Mortality, morbidity, and risk factors in China and its provinces, 1990-2017:a systematic analysis for the Global Burden of Disease Study 2017[J]. Lancet, 2019, 394(10204): 1145-1158. DOI:10.1016/S0140-6736(19)30427-1 |
| [2] |
国家心血管病中心. 中国心血管病报告, 2018[M]. 北京: 中国大百科全书出版社, 2019. National Center for Cardiovascular Disease, China. Report on cardiovascular diseases in China, 2018[M]. Beijing: Encyclopedia of China Publishing House, 2019. |
| [3] |
Wang JH, An ZP, Li B, et al. Increasing stroke incidence and prevalence of risk factors in a low-income Chinese population[J]. Neurology, 2015, 84(4): 374-381. DOI:10.1212/WNL.0000000000001175 |
| [4] |
Guo YT, Wang H, Tian YC, et al. Multiple risk factors and ischaemic stroke in the elderly Asian population with and without atrial fibrillation. An analysis of 425600 Chinese individuals without prior stroke[J]. Thromb Haemost, 2016, 115(1): 184-192. DOI:10.1160/TH15-07-0577 |
| [5] |
Shen C, Schooling CM, Chan WM, et al. Self-rated health and mortality in a prospective Chinese elderly cohort study in Hong Kong[J]. Prev Med, 2014, 67: 112-118. DOI:10.1016/j.ypmed.2014.07.018 |
| [6] |
van der Linde RM, Mavaddat N, Luben R, et al. Self-rated health and cardiovascular disease incidence: results from a longitudinal population-based cohort in Norfolk, UK[J]. PLoS One, 2013, 8(6): e65290. DOI:10.1371/journal.pone.0065290 |
| [7] |
Kaplan GA, Goldberg DE, Everson SA, et al. Perceived health status and morbidity and mortality: evidence from the Kuopio ischaemic heart disease risk factor study[J]. Int J Epidemiol, 1996, 25(2): 259-265. DOI:10.1093/ije/25.2.259 |
| [8] |
Latham K, Peek CW. Self-rated health and morbidity onset among late midlife U.S. adults[J]. J Gerontol B, 2013, 68((1): 107-116. DOI:10.1093/geronb/gbs104 |
| [9] |
方向华, 孟琛, 刘向红, 等. 健康自评与老年人健康状况的前瞻性研究[J]. 中华流行病学杂志, 2003, 24(3): 184-188. Fang XH, Meng C, Liu XH, et al. Study on the relationship between self-rated health situation and health status in the elderly-an 8 year follow-up study from Multidimentional Longitudinal Study of Aging in Beijing[J]. Chin J Epidemiol, 2003, 24(3): 184-188. DOI:10.3760/j.issn:0254-6450.2003.03.006 |
| [10] |
Dong WH, Pan XF, Yu CQ, et al. Self-rated health status and risk of incident stroke in 0.5 million Chinese adults: the China Kadoorie Biobank study[J]. J Stroke, 2018, 20(2): 247-257. DOI:10.5853/jos.2017.01732 |
| [11] |
Hillen T, Davies S, Rudd AG, et al. Self ratings of health predict functional outcome and recurrence free survival after stroke[J]. J Epidemiol Community Health, 2003, 57(12): 960-966. DOI:10.1136/jech.57.12.960 |
| [12] |
Emmelin M, Weinehall L, Stegmayr B, et al. Self-rated ill-health strengthens the effect of biomedical risk factors in predicting stroke, especially for men: an incident case referent study[J]. J Hypertens, 2003, 21(5): 887-896. DOI:10.1097/00004872-200305000-00012 |
| [13] |
中国疾病预防控制中心, 中国疾病预防控制中心慢性非传染性疾病预防控制中心. 中国慢性病及其危险因素监测报告-2010[M]. 北京: 军事医学科学出版社, 2012. China CDC, National Center for Chronic and Non-communicable Disease Control and Prevention, China CDC. Report on chronic disease risk factor surveillance in China, 2010[M]. Beijing: Military Medical Science Press, 2012. |
| [14] |
Barger SD, Cribbet MR, Muldoon MF. Participant-reported health status predicts cardiovascular and all-cause mortality independent of established and nontraditional biomarkers: evidence from a representative US Sample[J]. J Am Heart Assoc, 2016, 5(9): e003741. DOI:10.1161/JAHA.116.003741 |
| [15] |
Feng QS, Zhu HY, Zhen ZH, et al. Self-rated health, interviewer-rated health, and their predictive powers on mortality in old age[J]. J Gerontol B, 2016, 71(3): 538-550. DOI:10.1093/geronb/gbu186 |
| [16] |
Sargent-Cox KA, Anstey KJ, Luszcz MA. The choice of self-rated health measures matter when predicting mortality: evidence from 10 years follow-up of the Australian longitudinal study of ageing[J]. BMC Geriatr, 2010, 10: 18. DOI:10.1186/1471-2318-10-18 |
| [17] |
Rumsfeld JS, Alexander KP, Goff DC, et al. Cardiovascular health: the importance of measuring patient-reported health status: a scientific statement from the American Heart Association[J]. Circulation, 2013, 127(22): 2233-2249. DOI:10.1161/CIR.0b013e3182949a2e |
| [18] |
Mavaddat N, van der Linde R, Parker R, et al. Relationship of self-rated health to stroke incidence and mortality in older individuals with and without a history of stroke: a longitudinal study of the MRC Cognitive Function and Ageing (CFAS) population[J]. PLoS One, 2016, 11(2): e0150178. DOI:10.1371/journal.pone.0150178 |
| [19] |
Rutledge T, Linke SE, Johnson BD, et al. Self-rated versus objective health indicators as predictors of major cardiovascular events: the NHLBI-sponsored Women's Ischemia Syndrome Evaluation[J]. Psychosom Med, 2010, 72(6): 549-555. DOI:10.1097/PSY.0b013e3181dc0259 |
| [20] |
de Arruda GO, Santos ADL, Teston EF, et al. Association between self-reported health and sociodemographic characteristics with cardiovascular diseases in adults[J]. Rev Esc Enferm USP, 2015, 49(1): 61-68. DOI:10.1590/S0080-623420150000100008 |
| [21] |
Shanahan L, Bauldry S, Freeman J, et al. Self-rated health and C-reactive protein in young adults[J]. Brain Behav Immun, 2014, 36: 139-146. DOI:10.1016/j.bbi.2013.10.020 |
| [22] |
Tanno K, Ohsawa M, Onoda T, et al. Poor self-rated health is significantly associated with elevated C-reactive protein levels in women, but not in men, in the Japanese general population[J]. J Psychosom Res, 2012, 73(3): 225-231. DOI:10.1016/j.jpsychores.2012.05.013 |
| [23] |
Fielding R, Lam TH, Ho SY, et al. Subjective health and fibrinogen in a healthy Chinese cohort[J]. Br J Health Psychol, 2004, 9(4): 523-532. DOI:10.1348/1359107042304533 |
| [24] |
Boehme AK, Esenwa C, Elkind MSV. Stroke risk factors, genetics, and prevention[J]. Circ Res, 2017, 120(3): 472-495. DOI:10.1161/CIRCRESAHA.116.308398 |
 2021, Vol. 42
2021, Vol. 42