文章信息
- 梁锐明, 殷鹏, 王黎君, 李镒冲, 刘江美, 刘韫宁, 由金玲, 齐金蕾, 周脉耕.
- Liang Ruiming, Yin Peng, Wang Lijun, Li Yichong, Liu Jiangmei, Liu Yunning, You Jinling, Qi Jinlei, Zhou Maigeng.
- 中国7个城市大气PM2.5对人群心血管疾病死亡的急性效应研究
- Acute effect of fine particulate matters on daily cardiovascular disease mortality in seven cities of China
- 中华流行病学杂志, 2017, 38(3): 283-289
- Chinese journal of Epidemiology, 2017, 38(3): 283-289
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2017.03.003
-
文章历史
收稿日期: 2016-10-11
2. 100050 北京, 中国疾病预防控制中心综合防控与评价室;
3. 100050 北京, 中国疾病预防控制中心慢性非传染性疾病预防控制中心
2. Division of Integrated Prevention and Evaluation, National Center for Chronic and Non-communicable Disease Control and Prevention, Chinese Center for Disease Control and Prevention, Beijing 100050, China;
3. National Center for Chronic and Non-communicable Disease Control and Prevention, Chinese Center for Disease Control and Prevention, Beijing 100050, China
近年来,大气中空气动力学直径≤2.5 μm颗粒物(Particulate matters with an aerodynamic diameter less than 2.5 μm,PM2.5)污染问题已成为备受关注的公共卫生问题。2013年,在亚洲及太平洋地区发展中国家,生活在PM2.5年平均浓度10 μg/m3以上的人口比例高达92%[1]。2014年,中国心血管疾病死亡率位于疾病死亡构成首位[2]。PM2.5的急性暴露与心血管疾病的发病、住院甚至死亡密切相关,影响不容小觑。近十余年,国外许多大型多城市空气污染研究为PM2.5的急性心血管疾病效应提供了证据[3-4],但是国内的相关研究多局限于北京、上海[5]、广州[6-7]、西安[8]等单个城市,仅少数研究为多城市研究[9-10]。单城市研究时,不同研究的分析模型、参数设置及分析时间范围不尽一致,可比性较差;我国和发达国家的暴露水平、污染物成分、疾病谱等情况不完全一致,不宜直接引用国外的多城市研究成果[9-11]。因此,开展符合我国国情的多城市PM2.5急性心血管疾病效应研究非常必要。本文采用统一的分析方法和参数设置,结合2013-2015年的每日心血管疾病死亡人数和环境数据,定量分析中国7个城市PM2.5对于居民心血管疾病死亡的急性影响,为多城市大气PM2.5的心血管疾病死亡急性效应研究提供科学依据。
资料与方法1.资料来源:
(1)研究地点:心血管疾病的发生以及空气污染的严重程度受地域、气候和饮食习惯等因素影响,从全国7大区域各选择一个典型城市作为研究现场,分别为石家庄(华北)、哈尔滨(东北)、上海(华东)、武汉(华中)、广州(华南)、成都(西南)以及西安(西北)。
(2)居民死亡资料:7个城市2013年1月1日至2015年12月31日的死亡数据来源于中国疾病预防控制中心死因监测系统。依据死亡日期和死亡原因,分别对各个城市的死亡人数进行分类汇总。根本死因分类参照《国际疾病分类》第十版(ICD-10),心血管疾病的ICD编码为I00~I99。为了鉴别PM2.5对心血管疾病死亡影响的易感人群,本文按照性别(男、女),年龄(5~64岁,65~74岁,≥75岁)进行分层。5岁以下儿童心血管疾病死亡数量较少,不纳入分层分析。
(3)环境监测资料:7个城市2013-2015年的环境监测资料来源于全国城市空气质量实时发布平台(http://106.37.208.233:20035/),包括PM2.5、NO2、SO2等污染物的实时浓度。根据环境空气质量标准(GB 3095-2012),每天至少有20 h浓度时,才可以计算日均浓度,否则被视为缺失日。如果某个监测站有超过25%的日均值缺失,则排除该监测站数据。本次分析中,某个城市的污染物日均值浓度为该城市的全部有效监测站的有效日均值浓度的算术平均值。
(4)气象监测资料:7个城市2013-2015年的气象资料来源于中国气象数据网(http://data.cma.cn/),包括日平均气温(℃)和日平均相对湿度(%)。
2.研究方法:
(1)基本模型:将各城市每天的心血管疾病死亡人数、大气污染数据以及气象数据按日期关联,在分城市水平和7个城市平均水平上定量分析PM2.5对每日心血管疾病死亡率的影响。分城市分析的核心模型为广义相加模型(Generalized Additive Model,GAM)。相对于总人口而言,居民每日因心血管疾病死亡为小概率事件,服从泊松分布。考虑到日死亡人数的过分散问题,采用半泊松分布和GAM模型相连接。公式:
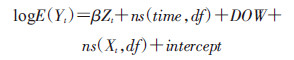 (1)
(1)
E(Yt)是t日各城市心血管疾病死亡人数的期望值,β为回归模型估计得到的系数,即PM2.5浓度每升高一个单位所引起的日心血管疾病死亡率增长值;Zt是t日某城市PM2.5日均浓度;ns为自然平滑样条函数,df为其自由度;time为日期变量,用于控制长期波动和季节性波动趋势;DOW为星期几变量,控制死亡率在一周内的自然波动;Xt是t日的气象条件,包括平均气温和平均相对湿度,用于调整气象因素对死亡的影响。本次分析中,日期变量的自然平滑样条函数自由度为7/年,气象因素中平均气温和相对湿度分别采用6和3为自由度,“星期几”变量以哑变量的形式进入模型。估计每个城市PM2.5的健康效应之后,利用随机效应模型估计了多城市的合并效应[9]。
(2)敏感性分析:①考虑到PM2.5浓度的不同滞后天数对效应估计值的影响,本次分析采用单日滞后模式[当天 (lag0),滞后1 d (lag1),滞后2 d (lag2)]以及多日移动平均滞后模式(单日和前一日的移动平均值,表示为lag01)两种方式,在分城市水平和多个城市平均水平估计PM2.5对心血管疾病死亡的影响。②考虑到共存污染物对效应估计值的影响,在模型中分别引入NO2和SO2,拟合了双污染物模型,估计分城市和多个城市的合并效应。③考虑到不同人群对PM2.5的敏感性不同,本研究按照年龄、性别、文化程度、死亡地点进行分层,估计各城市不同分层的效应值以及多个城市不同分层下的合并效应。采用公式2计算层间差别的95%CI,区间不包括0则说明两层间的效应差异有统计学意义[12]。
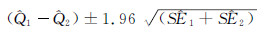 (2)
(2)
(3)暴露-反应关系曲线分析:建立基于我国国情的PM2.5与心血管疾病死亡的暴露-反应关系,对于我国的环境空气质量日均值标准意义重大。先对各个城市建立暴露-反应关系模型,再采用Meta分析的方法合并多个城市的暴露-反应关系图[13]。
3.统计学分析:采用R3.3.1软件,应用mgcv软件包。结果为PM2.5浓度每升高10 μg/m3引起居民心血管疾病日死亡率增加的百分比,包括均值和95%CI。
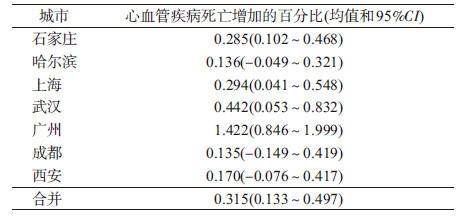
结果1.基本情况:2013-2015年,石家庄、哈尔滨、上海、武汉、广州、成都及西安市平均每日心血管疾病死亡人数分别为85(38~194)例、91(48~154)例、79(37~141)例、25(7~53)例、49(22~92)例、58(28~114)例、56(14~163)例。7个城市的PM2.5日均最低浓度为46 μg/m3(广州),最高浓度为117 μg/m3(石家庄),平均浓度为74 μg/m3。不同区域的城市,日平均气温和相对湿度差别较大(表 1)。
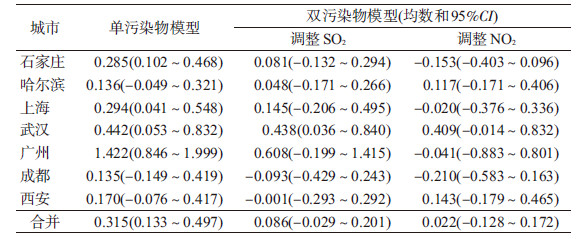
2.单污染物模型:在单污染物模型中,不同城市间PM2.5浓度(lag01)和日心血管疾病死亡率的关联强度差异较大(表 2)。PM2.5在广州市的效应最强,每10 μg/m3的PM2.5浓度升高会增加1.422%(95%CI:0.846%~1.999%)的心血管疾病日死亡率。在石家庄、上海和武汉3个城市,PM2.5对居民日心血管疾病死亡率的影响低于广州市,但仍具有统计学意义。但是,在哈尔滨、成都和西安3个城市的PM2.5的效应为正向但无统计学意义。采用随机效应模型合并各城市的效应值,发现在7个城市平均水平上,PM2.5浓度(lag01)每升高10 μg/m3能引起居民心血管疾病死亡率增加0.315%(95%CI:0.133%~0.497%)。
3.敏感性分析:
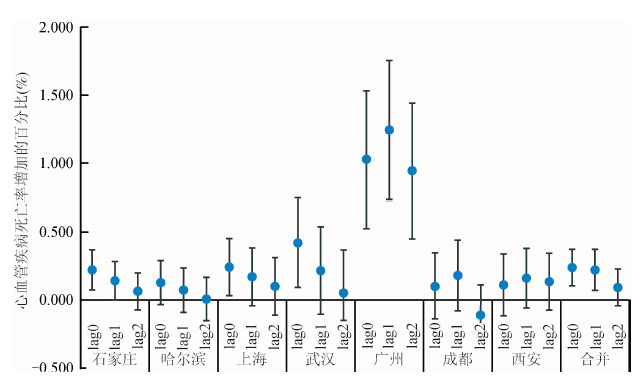
(1)不同滞后天数:在单污染物模型中,不同滞后天数下PM2.5浓度对心血管疾病的日死亡率影响强度不同(图 1)。对单日滞后而言,7个城市平均水平下PM2.5对心血管疾病死亡影响的效应分别为0.239%(95%CI:0.105%~0.372%)、0.221%(95%CI:0.070%~0.372%)、0.092%(95%CI:-0.043%~0.227%),从lag0到lag2递减,且在lag2时无统计学意义。分城市及多城市合并效应均为lag01时最强,这是本研究结果采用的主要滞后天数。
|
| 图 1 不同滞后天数下,PM2.5浓度每升高10 μg/m3引起我国7个城市居民心血管疾病死亡率增加的百分比(均值和95%CI) |
(2)双污染物模型:在双污染物模型中,加入SO2或NO2之后,各城市PM2.5对心血管疾病死亡率影响的效应值均有所降低,并且合并效应无统计学意义,提示PM2.5和其他污染物之间可能存在相互影响,PM2.5可能不具有独立的健康效应(表 3)。
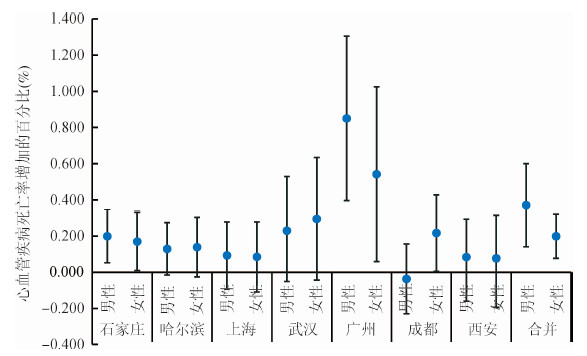
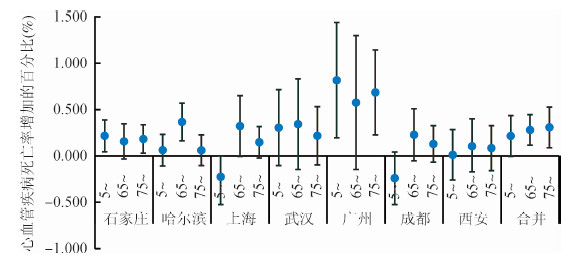
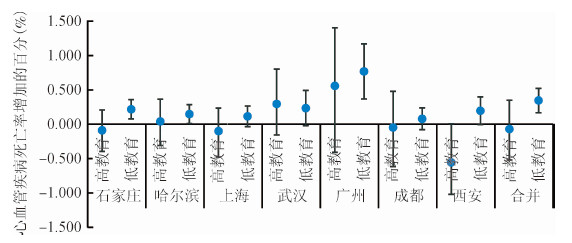
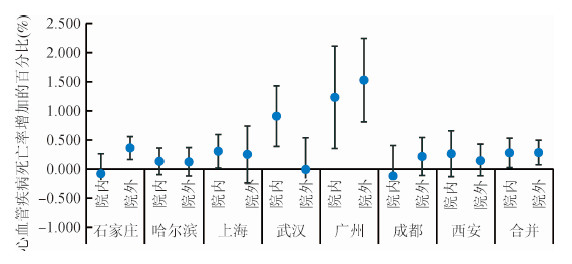
(3)分层分析:根据7个城市合并效应的结果,PM2.5对男性每日心血管疾病死亡率影响的效应值高于女性,分别为0.371%(95%CI:0.141%~0.600%)、0.199%(95%CI:0.077%~0.321%)。随着年龄的增长,PM2.5对心血管疾病死亡的影响逐渐增强,在65~74岁和≥75岁两个年龄组的效应具有统计学意义,而5~64岁年龄组的效应值无统计学意义。PM2.5对文化程度较低人群的效应高于文化程度高的人群,分别为0.347%(0.170%~0.524%),-0.070%(-0.489%~0.349%)。在不同死亡地点下,PM2.5对心血管疾病死亡影响的效应值相当。尽管如此,经统计学检验后,不同性别、年龄组、文化程度、死亡地点的人群中PM2.5的效应差异无统计学意义(图 2~5)。
|
| 图 2 不同性别下,PM2.5(lag01)浓度每升高10 μg/m3引起我国7个城市居民心血管疾病死亡率增加的百分比(均值和95%CI) |
|
| 图 3 不同年龄下,PM2.5(lag01)浓度每升高10 μg/m3引起我国7个城市居民心血管疾病死亡率增加的百分比(均值和95%CI) |
|
| 图 4 不同教育水平下,PM2.5(lag01)浓度每升高10 μg/m3引起我国7个城市居民心血管疾病死亡率增加的百分比(均值和95%CI) |
|
| 图 5 不同死亡地点下,PM2.5(lag01)浓度每升高10 μg/m3引起我国7个城市居民心血管疾病死亡率增加的百分比(均值和95%CI) |
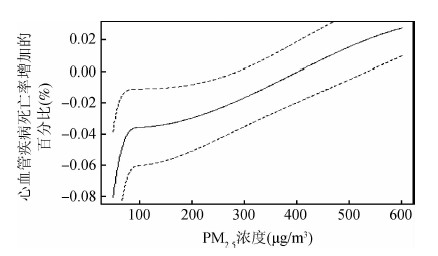
4.暴露-反应关系曲线:采用Meta分析随机效应模型,合并7个城市的PM2.5与心血管疾病死亡的暴露-反应关系曲线(图 6)。合并后的曲线表明,随着污染物的浓度升高,心血管疾病死亡率增加的百分比呈上升趋势,但污染物浓度相对较低时(污染物浓度界值约为100 μg/m3)的曲线斜率大于高污染物浓度时的曲线斜率。PM2.5与日心血管疾病死亡率的暴露-反应关系曲线无明显阈值。
|
| 图 6 经Meta分析合并后,7个城市PM2.5(lag01)浓度与每日心血管疾病死亡的暴露反应关系 |
本研究对7个城市进行研究,探讨PM2.5对心血管疾病死亡的急性效应。在不同城市、不同滞后天数下,PM2.5的效应存在一定的差异。PM2.5的升高会增加心血管疾病的死亡风险,且lag01时死亡风险最大。
分城市的分析结果提示PM2.5的效应具有地区差异性:华南(广州)、华中(武汉)、华北(石家庄)的效应值差异具有统计学意义,且华南地区的效应值远高于其他区域。这与国内同类研究结果一致[5-6, 8-9]。广州市的日平均PM2.5浓度稍低于其他6个城市,但是效应值却远高于其他。其原因如下:首先,不同城市内部的PM2.5暴露-反应关系系数不同。有研究表明南方城市(如广州)的暴露-反应关系系数大于北方城市[13],暴露-反应关系系数大,在同等情况下污染物浓度每升高一个单位所引起的疾病死亡率增加百分比较大;污染物浓度较高时,暴露-反应关系曲线反而趋于平坦[14];此外,颗粒物对死亡率的影响与居民在室内暴露于室外源性的颗粒物浓度有关,而室内暴露量又与居民室内外活动时间、室内外空气交换(如空调使用、开关窗通风的行为习惯)、建筑物特征等有关[15-16]。有研究表明,南方城市的颗粒物暴露系数较北方城市大[15]。虽然广州市的大气PM2.5日均浓度稍低,但南方城市的气温相对较高,建筑特征和北方不同,开窗通风较多,从室外渗透到室内的颗粒物较多,因此居民实际暴露量较大,从而导致了相同单位的PM2.5颗粒物浓度增加所对应的心血管疾病死亡增加百分比大于其他城市。
在7个城市平均水平上,PM2.5浓度(lag01)每升高10 μg/m3能引起居民心血管疾病死亡率增加0.315%(95%CI:0.133%~0.497%)。该值低于发达国家的多城市研究PM2.5效应值[3-4, 17]。美国一项针对112个城市进行的分析显示,PM2.5浓度每升高10 μg/m3对应的心血管疾病死亡效应值为0.85%[4]。可能原因为中国的PM2.5污染物浓度远高于发达国家,污染物浓度较高时暴露-反应关系曲线反而趋于平坦,而且国内外的人口年龄构成不同、污染物毒性不同、研究时段不同[4, 14]。本研究中合并7个城市PM2.5与心血管疾病死亡的暴露-反应关系曲线后未看到明显阈值,但污染物浓度较高时暴露-反应关系曲线相对于低污染浓度时平坦,与文献报道一致,也能一定程度上解释了我国效应值低于国外效应值的原因[18]。两项针对中国人群的Meta分析结果显示,PM2.5浓度每升高10 μg/m3对应的超额危险度分别为0.63%[19]和0.44%[20],而Chen等[9]在中国3城市的研究结果中,心血管疾病效应值为0.51%。本文结果略低于上述研究,造成效应值差别的可能原因是国内不同研究纳入分析的城市不同,而且分析的城市数量都较少,结果的可比性较差。
多污染物模型中,引入NO2或SO2后,在7城市平均水平下,PM2.5和心血管疾病死亡之间的关系无统计学意义,并未发现显著且稳健的PM2.5效应。这一结果与宁波市研究结果一致,这可能源于不同污染物之间的强相关关系对效应值的影响[21]。本研究中,细颗粒物对男性的心血管疾病死亡影响大于女性,但差异无统计学意义。同类研究中性别差异的结果不完全一致[8, 13, 22-23]。男性的效应值较大,可能由于男性工作环境相关的污染物累积暴露量大于女性[22];在我国,男性吸烟率高于女性[24],空气污染对吸烟者的效应大于非吸烟者[25]。细颗粒物对心血管疾病死亡的影响随年龄增加而增强,与同类研究结果一致,可能是由于老年人心血管基础疾病较多,且呼吸道和心血管对污染物的清除能力较差,暴露于PM2.5之后容易加重病情而导致死亡[26]。本文将文化程度作为社会经济状况的替代指标,发现文化程度较低的人更容易受PM2.5污染的影响,发生心血管疾病死亡事件,但差异无统计学意义。同文化程度较高的人相比,文化程度较低的人可能处于更恶劣的工作环境,暴露PM2.5的浓度更高,时间更长;自我防护意识及措施较差;医疗可及性可能低于文化程度较高的人,因此发生心血管疾病死亡的风险更高[13]。
本研究存在一定的局限性。首先,全国死因监测系统的漏报情况不可避免,死亡数据的漏报可能会对结果产生一定影响。但我国死因登记系统经过数十年的发展已逐渐成熟,质控体系已趋于完善。尽管我们不能完全排除漏报的情况,但本研究纳入分析的几个大城市死因监测工作都执行得很好,漏报情况较为少见,因此影响不大。其次,本研究用城市的平均暴露水平代替个体真实暴露水平,会导致一定的暴露测量误差[9, 15-16]。而且我国幅员辽阔,不同地区的气候特征、污染状况、人群易感性差异较大。本文虽在7个区域各选择了一个大城市作为典型城市,考虑了区域差异,但限于数据可获得性,未考虑区域内不同城市的差异,难以精确量化我国不同地区人群的PM2.5污染所造成的不同心血管疾病死亡风险。另外,不同城市、不同季节的空气PM2.5成分差异对PM2.5的健康效应影响不同,但是受限于污染数据的可获得性,本研究无法分析不同PM2.5成分对健康效应的影响。
本研究利用2013-2015年死亡和环境数据对我国7个典型城市的分析,提示PM2.5短期升高可以增加心血管疾病死亡率。这是对国内多城市PM2.5急性效应研究结果的更新和补充,可为不同城市的结果比较提供参考,并为相关环境政策的研究制定提供依据。
利益冲突: 无
| [1] | Brauer M, Freedman G, Frostad J, et al. Ambient air pollution exposure estimation for the global burden of disease 2013[J]. Environ Sci Technol, 2016, 50(1): 79–88. DOI:10.1021/acs.est.5b03709 |
| [2] |
国家心血管病中心.中国心血管病报告2015[M]. 北京: 中国大百科全书出版社, 2016.
National Center for Cardiovascular Diseases.Report on cardiovascular diseases in China 2015[M].Beijing: Encyclopedia of China Publishing House, 2016. |
| [3] | Dai LZ, Zanobetti A, Koutrakis P, et al. Associations of fine particulate matter species with mortality in the United States:a multicity time-series analysis[J]. Environ Health Perspect, 2014, 122(8): 837–842. DOI:10.1289/ehp.1307568 |
| [4] | Zanobetti A, Schwartz J. The effect of fine and coarse particulate air pollution on mortality:a national analysis[J]. Enviro Health Perspect, 2009, 117(6): 898–903. DOI:10.1289/ehp.0800108 |
| [5] | Huang W, Tan JG, Kan HD, et al. Visibility, air quality and daily mortality in Shanghai, China[J]. Sci Total Environ, 2009, 407(10): 3295–3300. DOI:10.1016/j.scitotenv.2009.02.019 |
| [6] | Yang CX, Peng XW, Huang W, et al. A time-stratified case-crossover study of fine particulate matter air pollution and mortality in Guangzhou, China[J]. Int Arch Occup Environ Health, 2012, 85(5): 579–585. DOI:10.1007/s00420-011-0707-7 |
| [7] |
冯文如, 刘世强, 黄勇, 等.
广州市PM2.5浓度与人群每日死亡风险的空间分布特征[J]. 环境卫生学杂志, 2015, 5(6): 512–519.
Feng WR, Liu SQ, Huang Y, et al. Spatial distribution characteristics of PM2.5 in air and daily mortality in Guangzhou[J]. J Environ Hyg, 2015, 5(6): 512–519. DOI:10.13421/j.cnki.hjwsxzz.2015.06.006 |
| [8] | Huang W, Cao JJ, Tao YB, et al. Seasonal variation of chemical species associated with short-term mortality effects of PM2.5 in Xi'an, a Central city in China[J]. Am J Epidemiol, 2012, 175(6): 556–566. DOI:10.1093/aje/kwr342 |
| [9] | Chen RJ, Li Y, Ma YJ, et al. Coarse particles and mortality in three Chinese cities:the China Air Pollution and Health Effects Study (CAPES)[J]. Sci Total Environ, 2011, 409(23): 4934–4938. DOI:10.1016/j.scitotenv.2011.08.058 |
| [10] | Lee H, Honda Y, Hashizume M, et al. Short-term exposure to fine and coarse particles and mortality:a multicity time-series study in East Asia[J]. Environ Pollut, 2015, 207: 43–51. DOI:10.1016/j.envpol.2015.08.036 |
| [11] | HEI. Outdoor Air pollution and health in the developing countries of Asia:a comprehensive review[R]. Special Report 18. Boston, MA:International Scientific Oversight Committee Health Effects Institute, 2010. |
| [12] | Zeka A, Zanobetti A, Schwartz J. Individual-level modifiers of the effects of particulate matter on daily mortality[J]. Am J Epidemiol, 2006, 163(9): 849–859. DOI:10.1093/aje/kwj116 |
| [13] |
陈仁杰. 复合型大气污染对我国17城市居民健康效应研究[D]. 上海: 复旦大学, 2013.
Chen RJ. The health effects of complex air pollution in 17 Chinese cities[D]. Shanghai:Fudan University, 2013. |
| [14] | Katsouyanni K, Touloumi G, Spix C, et al. Short term effects of ambient sulphur dioxide and particulate matter on mortality in 12 European cities:results from time series data from the APHEA project[J]. BMJ, 1997, 314(7095): 1658. DOI:10.1136/bmj.314.7095.1658 |
| [15] | Zhou B, Zhao B, Guo XF, et al. Investigating the geographical heterogeneity in PM10-mortality associations in the China Air Pollution and Health Effects Study (CAPES):a potential role of indoor exposure to PM10 of outdoor origin[J]. Atmos Environ, 2013, 75: 217–223. DOI:10.1016/j.atmosenv.2013.04.044 |
| [16] | Chen RJ, Zhou B, Kan HD, et al. Associations of particulate air pollution and daily mortality in 16 Chinese cities:an improved effect estimate after accounting for the indoor exposure to particles of outdoor origin[J]. Environ Pollut, 2013, 182: 278–282. DOI:10.1016/j.envpol.2013.07.024 |
| [17] | Dominici F, Wang Y, Correia AW, et al. Chemical composition of fine particulate matter and life expectancy:in 95 US counties between 2002 and 2007[J]. Epidemiology, 2015, 26(4): 556–564. DOI:10.1097/EDE.0000000000000297 |
| [18] | Xie WX, Li G, Zhao D, et al. Relationship between fine particulate air pollution and ischaemic heart disease morbidity and mortality[J]. Heart, 2015, 101(4): 257–263. DOI:10.1136/heartjnl-2014-306165 |
| [19] | Lu F, Xu DQ, Cheng YB, et al. Systematic review and Meta-analysis of the adverse health effects of ambient PM2.5 and PM10 pollution in the Chinese population[J]. Environ Res, 2015, 136: 196–204. DOI:10.1016/j.envres.2014.06.029 |
| [20] | Shang Y, Sun ZW, Cao JJ, et al. Systematic review of Chinese studies of short-term exposure to air pollution and daily mortality[J]. Environ Int, 2013, 54: 100–111. DOI:10.1016/j.envint.2013.01.010 |
| [21] |
钱旭君, 沈月平, 贺天锋, 等.
宁波市大气颗粒物与人群因心脑血管疾病死亡的时间序列研究[J]. 中华流行病学杂志, 2016, 37(6): 841–845.
Qian XJ, Shen YP, He TF, et al. Relationship between particulate matters and cardio-cerebrovascular mortality in Ningbo:a time-series study[J]. Chin J Epidemiol, 2016, 37(6): 841–845. DOI:10.3760/cma.j.issn.0254-6450.2016.06.020 |
| [22] | Clougherty JE. A growing role for gender analysis in air pollution epidemiology[J]. Environ Health Perspect, 2010, 118(2): 167–176. DOI:10.1289/ehp.0900994 |
| [23] | Middleton N, Yiallouros P, Kleanthous S, et al. A 10-year time-series analysis of respiratory and cardiovascular morbidity in Nicosia, Cyprus:the effect of short-term changes in air pollution and dust storms[J]. Environ Health, 2008, 7: 39. DOI:10.1186/1476-069X-7-39 |
| [24] | Gu DF, Kelly TN, Wu XG, et al. Mortality attributable to smoking in China[J]. N Eng J Med, 2009, 360(2): 150–159. DOI:10.1056/NEJMsa0802902 |
| [25] | Pope CA Ⅲ, Burnett RT, Turner MC, et al. Lung cancer and cardiovascular disease mortality associated with ambient air pollution and cigarette smoke:shape of the exposure-response relationships[J]. Environ Health Perspect, 2011, 119(11): 1616–1621. DOI:10.1289/ehp.1103639 |
| [26] | Bell ML, Zanobetti A, Dominici F. Evidence on vulnerability and susceptibility to health risks associated with short-term exposure to particulate matter:a systematic review and Meta-analysis[J]. Am J Epidemiol, 2013, 178(6): 865–876. DOI:10.1093/aje/kwt090 |
 2017, Vol. 38
2017, Vol. 38