文章信息
- 郑阳, 王全意.
- Zheng Yang, Wang Quanyi.
- 利巴韦林和干扰素-α联合应用治疗中东呼吸综合征冠状病毒感染的生物信息学分析
- Bioinformatics analysis on molecular mechanism of ribavirin and interferon-α in treating MERS-CoV
- 中华流行病学杂志, 2016, 37(2): 291-293
- Chinese Journal of Epidemiology, 2016, 37(2): 291-293
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2016.02.028
-
文章历史
- 投稿日期: 2015-07-31
2015年5月20日韩国确诊了一名中东呼吸综合征冠状病毒(Middle East Respiratory Syndrome Coronavirus,MERS-CoV)感染病例,随后由该病例引发的病例数量迅速上升,造成自2012年MERS- CoV发现以来中东以外地区的最大暴发疫情[1],并且其中有一例病例输入到我国境内。截至2015年6月30日,全球共确诊MERS-CoV感染病例1 357例,死亡486例,该病确诊病例数量仍然在不断增加。由于缺乏有效治疗手段,对于MERS病例的管理和救治仅限于支持治疗和抗微生物治疗。有科研人员认为联合使用利巴韦林和干扰素-α可能对治疗MERS-CoV感染病例有效,本研究拟通过生物信息学的方法,从基因层面探讨利巴韦林和干扰素-α联合应用与MERS-CoV感染之间的联系,从而为临床治疗提供一定的参考信息。
资料与方法1. 药物靶基因和MERS-CoV相关基因芯片数据检索:在比较毒理基因组学数据库(Comparative Toxicogenomics Database,CTD)中分别以干扰素-α和利巴韦林为关键词,搜索其靶基因。2种药物对应靶基因的总和,即代表干扰素-α和利巴韦林联合治疗的生物学靶点。在Array Express数据库里搜索与MERS-CoV有关的基因芯片数据库。
2. 基因芯片数据分析:利用Agilent GeneSpring GX软件对基因芯片数据进行分析,计算芯片上每一个探针的荧光值在不同时间点变化的标准差,按照数值大小排序,确定表达水平出现显著变化的基因。然后利用这些显著变化的基因进行非监督层次聚类分析(unsupervised hierarchical clustering)。
3. 生物信息学分析:利用PANTHER TOOL对药物靶基因和芯片数据进行GO(gene ontology,GO)富集分析,分析基因主要参与的生物学过程(biological process,BP)及所占百分比。利用DAVID平台,获取基因群显著富集的KEGG通路(P<0.05)。
结 果1. 数据搜索:截至2015年6月10日,在CTD中检索到干扰素-α和利巴韦林的靶基因分别为7个和26个,其中有6个相同基因,因此,利巴韦林和干扰素-α的靶基因共计27个。在ArrayExpress数据库中搜索到MERS-CoV感染相关的mRNA表达谱基因芯片数据集1个(编号:E-GEOD-56677),该芯片数据是比较MERS-CoV感染人类呼吸道上皮细胞后0、3、7、12、18和24 h基因表达的变化情况。按照同一芯片探针表达量在不同时间点的标准差由大到小排序,取前500个基因进行后续分析,其中与上述药物靶基因相同的基因共3个,分别是OAS1,IL6,ICAM1。
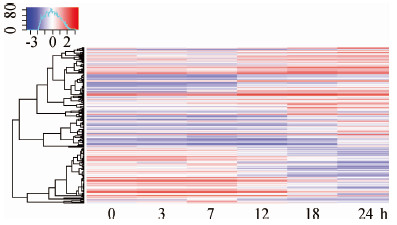
2. MERS-CoV感染人类呼吸道上皮细胞的基因表达谱的非监督层次聚类分析:为了解基因芯片数据中所有基因按照时间序列的表达模式,以及这些基因的群组划分,对芯片数据进行聚类分析(图 1),按照病毒刺激后基因表达随时间发生的变化,将基因主要分为两组,第一组基因在病毒感染后随时间的变化表达水平逐渐升高,包含药物靶基因OAS1,IL6;第二组则随时间变化而表达水平逐渐降低,包含药物靶基因ICAM1。
|
| 图 1 MERS-CoV感染细胞后6个时间点mRNA 非监督层次聚类分析 |
3. 生物信息学分析:
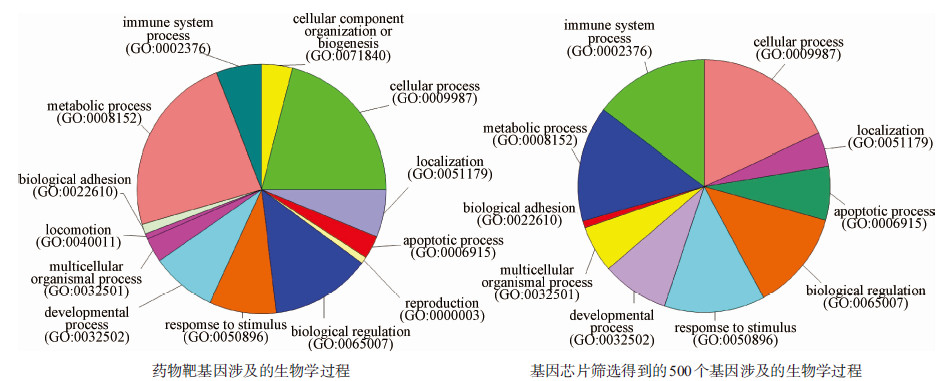
(1)差异表达基因的功能注释:利用PANTHER TOOL对27个药物靶基因和基因芯片筛选得到的500个基因分别进行GO注释。结果显示,药物靶基因和基因芯片数据涉及的生物学过程分别为10个和13个,见图 2。
|
| 图 2 MERS-CoV感染相关基因的GO注释 |
(2)信号通路分析与比较:利用DAVID平台进行信号通路分析,基因芯片第一组和第二组基因富集的信号通路分别为9个和3个(P<0.05);27个药物靶基因富集的信号通路共有23个(P<0.05)。药物靶基因与第一组基因群共同作用的信号通路有7条,主要与识别病原体,促进细胞因子释放,生成自身免疫反应等有关;药物靶基因与第二组基因群无共同作用的信号通路。
讨 论MERS-CoV感染病例的疾病谱较为广泛,病死率高,且目前尚无特异性治疗方法。由于MERS与SARS病毒高度同源,因此认为在治疗MERS-CoV感染时可借鉴SARS的治疗经验,其中包括利巴韦林和干扰素-α的联合使用[2]。有研究者将这两种药物加入感染MERS-CoV的恒河猴肾细胞系中,证实联合应用这两种药物比单独使用能够更为有效的抑制MERS-CoV的生长,并且在恒河猴动物模型中也证实了其对预后的促进作用[3, 4],提示联合应用利巴韦林和干扰素-α确实有助于机体对抗MERS-CoV的感染。为了解这两种药联合使用与人体感染MERS- CoV后基因表达变化的关联性,本研究通过生物信息学方法对公共数据平台的数据进行了分析。
利用公共数据,方便快捷,能够节省资源及成本,并能充分利用已知的科研结果,得到对疾病研究有价值的信息。本研究利用CTD和ArrayExpress平台,分别发现27个利巴韦林和干扰素-α在人体中作用的靶基因,1个与MERS-CoV感染相关的mRNA表达谱芯片数据。通过对基因芯片数据进行层次聚类分析,发现与病毒感染相关的基因主要有两大类,即基因表达在病毒感染细胞后随时间逐渐增高或逐渐降低。GO功能注释显示,芯片数据中显著变化的基因与药物靶基因涉及的生物学过程基本一致,且通过信号通路分析发现,芯片数据中的第一组基因与药物靶基因参与的信号通路有7条相同。综合这两个分析结果,提示利巴韦林和干扰素-α联合应用可能与MERS-CoV感染有关的基因相互作用,通过激活或抑制芯片数据中表达水平显著变化的基因,来改变病毒感染相关的信号通路的作用,从而达到抵抗病毒,抑制疾病发展的目的。一项关于MERS重症病例的研究显示,使用利巴韦林和干扰素-α联合治疗的患者与不使用该治疗的对照组相比,用药14 d时治疗组的生存率明显高于对照组,但是截止到用药28 d时,却未观察到显著差异[5],提示这两种药物组合对于治疗MERS的效果有限。本研究中第二组基因参与的信号通路与药物靶基因完全不同,也说明利巴韦林和干扰素-α在对抗病毒感染过程的局限性,与上述的抗病毒作用有限性相对应。同时,这一结果也提示后续研究中可以将这些通路涉及的基因作为药物作用靶基因,反向推导与其相互作用的化合物,为探索的新的治疗药物提供线索。
利益冲突 无| [1] Petersen E, Hui DS, Perlman S, et al.Middle East Respiratory Syndrome-advancing the public health and research agenda on MERS-lessons from the South Korea outbreak[J].Int J Infect Dis, 2015, 36:54-55.DOI:10.1016/j.ijid.2015.06.004. |
| [2] 郑阳, 杨鹏.中东呼吸综合征冠状病毒研究现况[J].国际病毒学杂志, 2013, 20(3):97-99.DOI:10.3760/cma.j.issn.1673-4092.2013.03.001.Zheng Y, Yang P.Current research on Middle East respiratory syndrome coronavirus[J].Inter J Virol, 2013, 20(3):97-99.DOI:10.3760/cma.j.issn.1673-4092.2013.03.001. |
| [3] Falzarano D, de Wit E, Martellaro C, et al.Inhibition of novel β coronavirus replication by a combination of interferon-α2b and ribavirin[J].Sci Rep, 2013, 3:1686.DOI:10.1038/srep01686. |
| [4] Falzarano D, de Wit E, Rasmussen AL, et al.Treatment with interferon-α2b and ribavirin improves outcome in MERS-CoV-infected rhesus macaques[J].Nat Med, 2013, 19(10):1313-1317.DOI:10.1038/nm.3362. |
| [5] Omrani AS, Saad MM, Baig K, et al.Ribavirin and interferon alfa-2a for severe Middle East respiratory syndrome coronavirus infection:a retrospective cohort study[J].Lancet Infect Dis, 2014, 14(11):1090-1095.DOI:10.1016/S1473-3099(14)70920-X. |
 2016, Vol. 37
2016, Vol. 37


