文章信息
- 李斌, 刘海灿, 王兆芬, 马永成, 苏效东, 蒋明霞, 万康林, 刘寿, 赵秀芹, 瞿述根.
- Li Bin, Liu Haican, Wang Zhaofen, Ma Yongcheng, Su Xiaodong, Jiang Mingxia, Wan Kanglin, Liu Shou, Zhao Xiuqin, Qu Shugen.
- 青海省结核分枝杆菌临床分离株可变数目串联重复序列基因多态性研究
- Study on VNTR diversity of clinical Mycobacterium tuberculosis isolates from Qinghai
- 中华流行病学杂志, 2015, 36(10): 1158-1161
- Chinese Journal of Epidemiology, 2015, 36(10): 1158-1161
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2015.10.026
-
文章历史
- 投稿日期: 2015-03-03
2. 中国疾病预防控制中心传染病预防控制所传染病预防控制国家重点实验室;
3. 青海省疾病预防控制中心传染病预防控制所
2 State Key Laboratory for Communicable Disease Prevention and Control, Institute for Communicable Disease Control and Prevention, Chinese Center for Disease Control and Prevention;
3 Institute for Communicable Disease Control and Prevention, Qinghai Provincial Center for Disease Control and Prevention
多位点数目可变串联重复序列分析(MLVA)是基于PCR的DNA指纹技术,利用基因组中特定位点上可变数目串联重复序列(VNTR)的多态性进行基因分型的研究[1],被检测菌株根据不同位点的VNTR重复单元的拷贝数进行数字化编码,然后利用相关软件通过计算机对检测菌株进行自动分型[2]。结核分枝杆菌的全基因组序列中存在许多VNTR位点,但其侧翼序列具有高度保守性。为此本研究采用15个VNTR位点对青海省251株结核分枝杆菌临床分离株进行基因分型研究,初步了解其基因多态性。
材料与方法1. 菌株来源:251株结核分枝杆菌临床分离株为2009-2012年青海省疾病预防控制中心从结核病患者痰标本分离培养及鉴定后获得。对照标准菌株H37Rv由中国疾病预防控制中心传染病预防控制所(传染病所)结核病实验室提供。
2. 主要试剂:2×Taq Master Mix、100 bp DNA Ladder、琼脂糖均购自北京康为世纪生物科技有限公司。
3. DNA提取:用生理盐水从L-J培养基的斜面上洗脱菌体,80 ℃孵育30 min灭活,12 000 r/min离心3 min,弃上清收集菌体,用500 μl生理盐水充分悬浮,100 ℃水浴1 h,12 000 r/min离心5 min取上清即为PCR扩增模板。-20 ℃保存备用。
4. MLVA检测:①引物设计与合成:15个位点(表 1)[3, 4]的引物序列由传染病所提供,生工生物工程(上海)股份有限公司合成。②PCR反应体系及反应条件:采用25 μl反应体系,其中含上、下游引物各0.5 μl,2×Taq Master Mix 12.5 μl,DNA模板1 μl,灭菌水10.5 μl。PCR反应条件:预变性94 ℃ 5 min;变性94 ℃ 30 s,退火62 ℃ 30 s,延伸72 ℃ 45 s,35个循环;终延伸72 ℃ 10 min。③琼脂糖凝胶电泳:取10 μl PCR扩增产物在2%琼脂糖凝胶上电泳,用100 bp DNA Marker确定其相对分子质量,以标准株H73Rv作为对照。
5. 结果分析:根据成像DNA片段的大小,与标准株H37Rv对比,从而得出每个检测菌株15个位点的重复拷贝数。应用Hunter-Gaston指数(HGI)分析各位点的多态性[5],再用BioNumerics 5.0软件对菌株进行聚类分析。
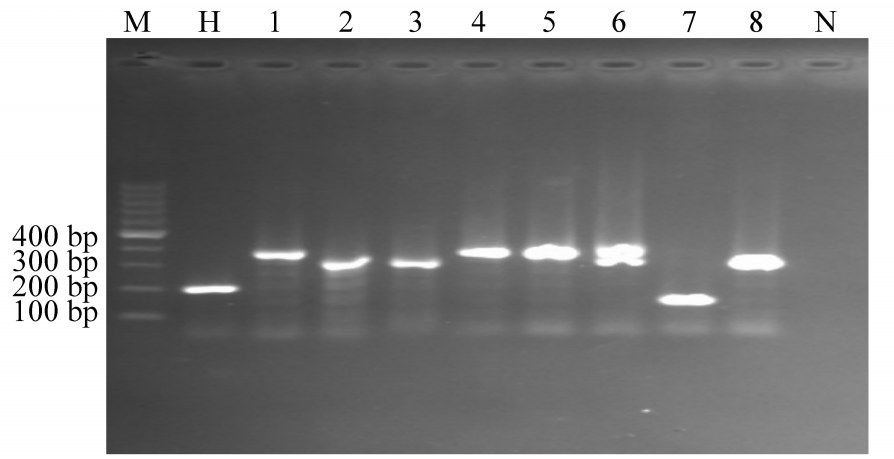
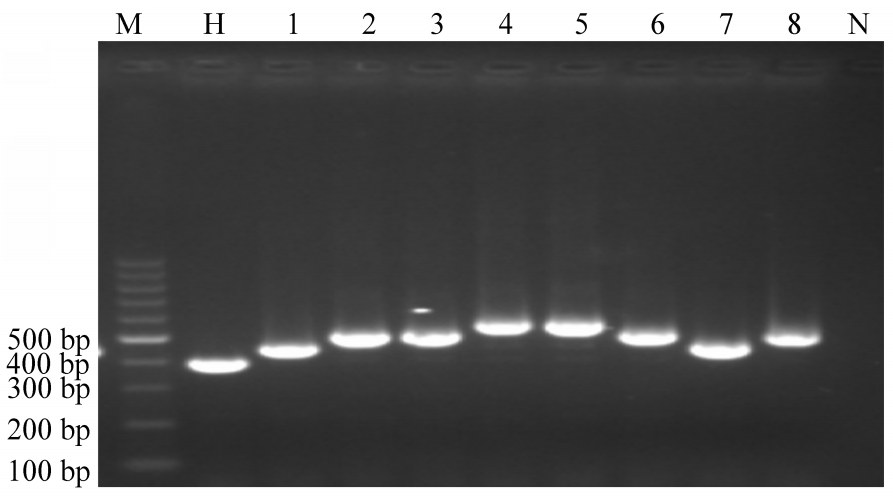
结果1. VNTR位点检测:251株结核分枝杆菌的PCR产物凝胶电泳均可观察到15个位点。图 1和图 2分别为8株结核分枝杆菌临床分离株的Mtub21和MIRU40位点的PCR产物凝胶电泳结果。位点PCR产物长度不同说明位点重复次数不同,表明该位点存在基因多态性。
|
| 注:M:DNA Marker(100~1 000 bp); H:H37Rv; N:阴性对照; 1~8:被检测菌株(QH81~QH88) 图 1 8株结核分枝杆菌临床分离株的Mtub21位点基因多态性检测 |
|
| 注:M:DNA Marker(100~1 000 bp); H:H37Rv; N:阴性对照; 1~8:被检测菌株(QH193~QH200) 图 2 8株结核分枝杆菌临床分离株的MIRU40位点基因多态性检测 |
2. VNTR位点的多态性:为了比较不同位点的多态性,应用HGI对各个位点的分辨能力进行分析。15个VNTR位点HGI有较大差异,HGI为0.122~0.768,其中分辨率>0.6的VNTR位点有6个,表明这些位点具有较高的分辨率,且不同位点显示不同的分辨率(表 2)。
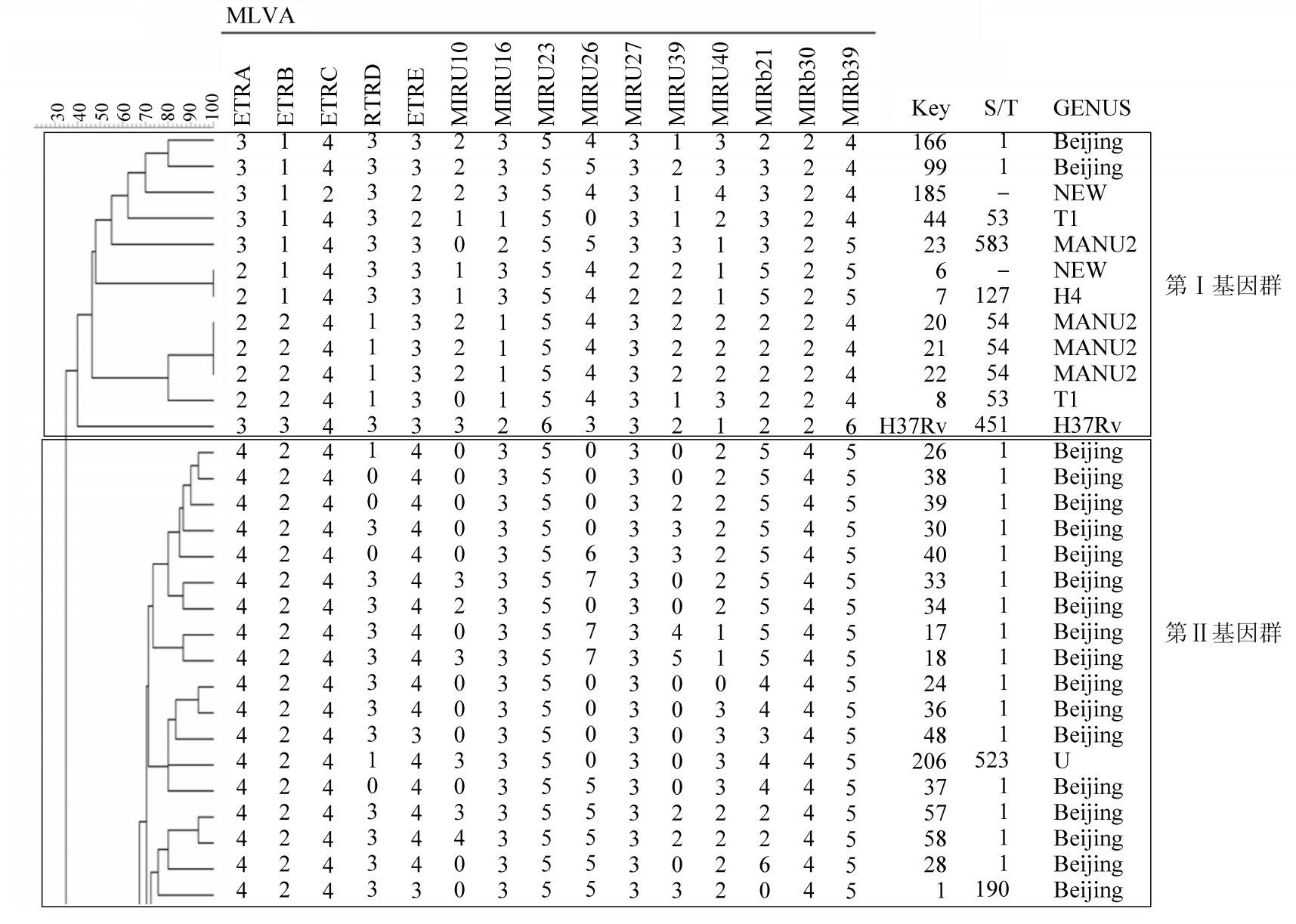
3. 基因分型聚类分析:经BioNumberics 5.0软件聚类分析(图 3),251株结核分枝杆菌分为4个基因群,238个基因型。4个基因群分别占4.9%、91.9%、1.6%和1.6%。所有的基因型与标准株H37Rv基因型均不相同。
|
| 图 3 部分结核分支杆菌菌株BioNumberics聚类分析 |
本研究采用青海省分离培养的251株结核菌,选取15个VNTR位点进行MLVA分型,并计算15个位点的分辨率,应用HGI比较各位点分辨能力。结果显示各位点HGI存在较大差异,仅3个位点(MIRU16、MIRU23和Mtub30)HGI未超过0.3,有6个VNTR位点(ETRE、MIRU10、MIRU26、MIRU39、MIRU40和Mtub21)HGI>0.6,表明这些位点适宜青海地区全部菌株的基因分型。分辨能力最强的是MIRU26,这与李卓林等[3]报道的一致。而Sun等[6]对分离自新加坡291名患者的303株结核分枝杆菌应用标准MIRU-VNTR分型方法检测基因多样性,发现12个MIRU位点中,MIRU-10、26、31、39具有较高的分辨能力。Mazars等[7]也发现12个MIRU位点中分别具有不同的分辨能力,其中6个(MIRU-10、16、23、26、31、40)是带有高度多样性的位点,提示MIRU26位点在分辨能力上起到重要作用。本文251株结核菌临床分离株可分为4个基因群、238个基因型,所有基因型与标准株H37Rv基因型均不相同。车洋等[8]对我国江苏省168株结核分枝杆菌分型显示,Ⅷ型为主要流行型。提示在不同地区结核分枝杆菌具有独特的分子特征。而青海省临床分离株则以第Ⅱ群为优势流行菌型,该菌群主要分布于西宁及海西两地区,为当地主要流行菌型。
| [1] Cowan LS, Diem L ,Monson T, et al. Evaluation of a two-step approach for large-scale,prospective genotyping of Mycobacterium tuberculosis isolates in the United States[J]. J Clin Microbiol,2005,43(2):688-695. |
| [2] Lv B,Liu M,Li ZN,et al. Analysis on genotyping of 159 strains of Mycobacterium tuberculosis isolated clinically in some areas of China with MLVA-19-Loci[J]. Dis Surveill,2009,24(5):359-362. (in Chinese)吕冰,刘梅,李兆娜,等. 中国部分地区159株结核分枝杆菌临床分离株MLVA-19分型分析[J]. 疾病监测,2009,24(5):359-362. |
| [3] Li ZL,Wang LL,Liu RH,et al. MLVA analysis of 110 clinical isolates of Mycobacterium tuberculosis from Jilin province[J]. J Jilin Univ:Med Ed,2013,39(2):308-312. (in Chinese)李卓林,王璐璐,刘日辉,等. 吉林省110株结核分枝杆菌临床分离株MLVA基因分型[J]. 吉林大学学报:医学版,2013,39(2):308-312. |
| [4] Liu ZW,Lv B,Wang XM,et al. Analysis on the genotyping of 71 Mycobacterium tuberculosis clinical strains isolated from Zhejiang province with MLVA[J]. Chin Prev Med,2008,9(12):1017- 1020. (in Chinese)柳正卫,吕冰,王晓萌,等. 71株浙江省结核分枝杆菌临床分离株MLVA基因分型研究[J]. 中国预防医学杂志,2008,9(12):1017-1020. |
| [5] Wan KL,Liu JH,Hauck Y,et al. Investigation on Mycobacterium tuberculosis diversity in China and the origin of the Beijing clade[J]. PLoS One,2011,6(12):e29190. |
| [6] Sun YJ, Bellamy R, Lee ASG, et al. Use of mycobacterial interspersed repetitive unit-variable-number tandem repeat typing to examine genetic diversity of Mycobacterium tuberculosis in Singapore[J]. J Clin Microbiol,2004,42(5):1986-1993. |
| [7] Mazars E,Lesjean S,Banuls AL,et al. High-resolution minisatellite- based typing as a portable approach to global analysis of Mycobacterium tuberculosis molecular epidemiology[J]. Proc Natl Aad Sci USA,2001,98(4):1901-1906. |
| [8] Che Y,Dong HJ, Yu M. MIRU genotyping technology research progress in the molecular epidemiology of tuberculosis[J]. Chin J Public Health Manage,2011,27(5):472-474. (in Chinese)车洋,董红军,于梅. MIRU基因分型技术在结核病分子流行病学中的研究进展[J]. 中国公共卫生管理,2011,27(5):472-474. |
 2015, Vol. 36
2015, Vol. 36