2. 中国药科大学, 南京 210009
2. China Pharmaceutical University, Nanjing 210009, China
黄杨宁片以环维黄杨星D为原料研制,具有行气活血,通络止痛的功能,用于气滞血瘀所致的胸痹心痛、脉结代;冠心病、心律失常见上述证候者。制剂及其原料均收载于《中华人民共和国药典》(以下简称《中国药典》)2000至2015年版一部[1-4]。黄杨宁片作为一种口服固体制剂,2015年版《中国药典》中并没有溶出度的检查项目,也未见黄杨宁片溶出度检查方法研究的文献报道。溶出度会影响药物的吸收也反映制剂的工艺,2015年版《中国药典》二部对化药固体制剂一般都规定溶出度检查,但一部鉴于中药的复杂因素如流浸膏或有效部位或生药投料,复杂基质下多成分共同作用难以用某一种成分作为溶出指标,溶出和测定方法也难以建立,因此对中药固体制剂基本都没有规定溶出度检查。黄杨宁片原料“环维黄杨星D”是2015年版《中国药典》一部收载的第1个接近于化药的中药原料药,主成分明确,纯度也较高,因此可以尝试采用溶出度来考察制剂工艺和评价药物质量。本文参考文献[5-16]建立了黄杨宁片溶出度测定方法,并对5个生产厂家的产品进行了溶出曲线考察,方法简便可靠,可望为2015年版《中国药典》一部收录第1个药物溶出度检查项标准提供依据。
1 仪器与试药 1.1 仪器SOTAX公司Sotax AT 7 Smart自动溶出仪;岛津公司LC-20AB高效液相色谱仪(LC-20AB泵,SIL-20AC自动进样器,CTO-20AC柱温箱,SPDM20A二极管阵列PDA检测器、Lab-solution工作站)。
1.2 试药5个厂家的27批黄杨宁片样品由国家药品评价性抽样中各省药监局提供;环维黄杨星D对照品(批号110888-200503)来自中国食品药品检定研究院。庚烷磺酸钠为分析纯,东京化成工业株式会社;磷酸二氢钾为分析纯,南京化学试剂一厂;乙腈为色谱纯,Fisher Scientific公司;水为超纯水,其余试剂均为分析纯。
2 方法与结果 2.1 色谱条件色谱柱:Agela Durashell RP C18(4.6 mm×250 mm,5 μm);流动相:0.01 mol·L-1庚烷磺酸钠与0.01 mol·L-1磷酸二氢钾等量混合水溶液(含0.2%三乙胺,用磷酸调节pH至3.5)-乙腈(77:23);流速:1.0 mL·min-1;检测波长:206 nm;进样量:对照品溶液20 μL,供试品溶液80 μL;柱温:40 ℃。
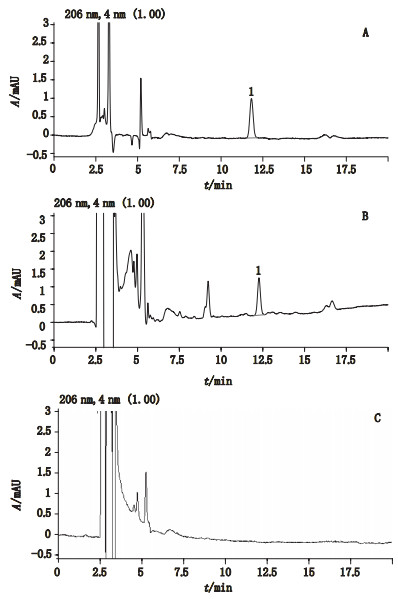
2.2 溶出度测定 2.2.1 测定方法取本品,照溶出度与释放度测定法(《中国药典》2015年版通则0931第三法),以0.1 mol·L-1盐酸溶液150 mL为溶出介质,转速为75 r·min-1,依法操作,经60 min时,取溶液5 mL,滤过,取续滤液作为供试品溶液。另取环维黄杨星D对照品适量,精密称定,加流动相制成约10 μg·mL-1的对照品溶液。按“2.1”项下色谱条件,取对照品溶液20 μL和供试品溶液80 μL,分别注入液相色谱仪,测定,计算每片的溶出度。结果见图 1。
|
1.环维黄杨星(cyclovirobuxine D) A.对照品溶液(reference substance solution)B.供试品溶液(sample solution)C.空白溶液(blank solution) 图 1 样品溶出度测定HPLC色谱图 Fig.1 Chromatogram of dissolution test |
精密称取环维黄杨星D对照品适量,用流动相制成浓度分别为1.25、2.5、5、10、15、25、50、100、200 μg·mL-1的系列对照品溶液,按“2.1.1”项下色谱条件,精密吸取20 μL,分别进样测定。以进样量X(μg)为横坐标,峰面积值Y为纵坐标计算回归方程:
| $Y=63\;993 X+35.064\;70 \quad r=0.999\;9 $ |
环维黄杨星D进样量在0.025 5~4.084 8 μg范围内线性关系良好。
2.2.2.2 检测下限和定量下限取环维黄杨星D对照品,按“2.2.1”项下方法制备溶液,并稀释至信噪比约为10和3时浓度的溶液,连续进样5次。结果检测下限为0.02 μg(RSD=5.6%,n=5),定量下限为0.05 μg(RSD=2.5%,n=5)。
2.2.2.3 回收率精密称取已知含量的样品细粉适量(相当于环维黄杨星D 0.5 mg),6份,分别置100 mL量瓶中,各精密加入质量浓度为0.5 mg ·mL-1的环维黄杨星D对照品溶液1.0 mL,再加溶出介质约70 mL,振摇使环维黄杨星D溶解,加流动相稀释至刻度,摇匀,过滤,取续滤液即得供试溶液,测定并计算。结果平均回收率为97.6%(RSD=1.5%,n=6)。
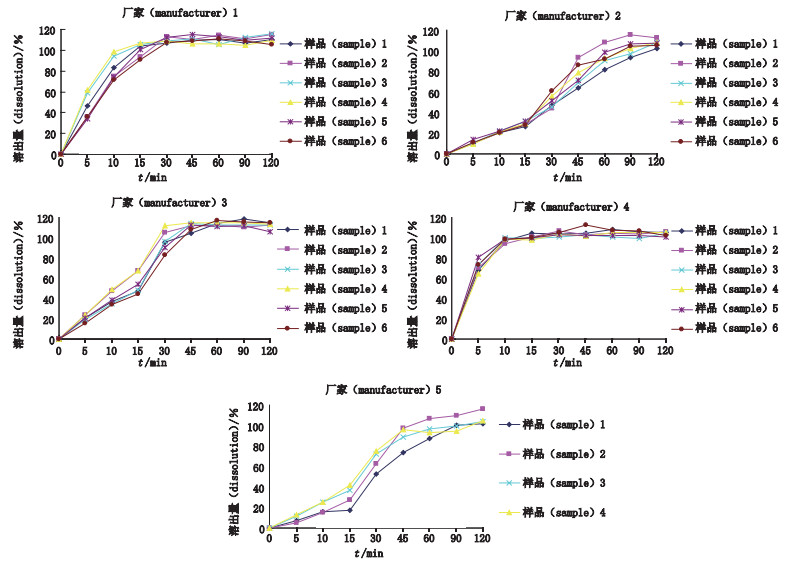
2.3 溶出曲线比较取黄杨宁片样品(厂家1,批号15121701;厂家2,批号1605062;厂家3,批号1502001;厂家4,批号160301;厂家5,批号151001 083,样1、样2为薄膜衣片,样3、样4为素片),以0.1 mol·L-1盐酸溶液150 mL为溶出介质,转速为75 r·min-1,依法操作,在5、10、15、30、45、60、90、120 min取样,并同时补充溶出介质,滤过,取续滤液作为供试品溶液。按“2.1”项下色谱条件进行测定,绘制溶出曲线,结果见图 2。
|
图 2 不同厂家黄杨宁片样品的溶出曲线 Fig.2 Dissolution curves of samples from different manufacturers |
取黄杨宁片样品27批,按“2.2.1”项下方法测定溶出度,结果见表 1。故拟设置溶出度限度为标示量的90%。
|
|
表 1 黄杨宁样品溶出度测定结果 Tab.1 The results of dissolution of Huangyangning tablets |
取样品(厂家2,批号1605063),采用小杯法,转速为75 r·min-1,分别以水、0.1 mol·L-1盐酸溶液、pH 4.0醋酸盐缓冲液、pH 6.8磷酸盐缓冲液为溶出介质,按“2.2”的方法测定溶出曲线,结果0.1 mol·L-1盐酸溶液溶出效率较高,且均一性良好,故采用0.1 mol·L-1盐酸溶液为溶出介质。
3.1.2 转速的选择取样品(厂家2,批号1605063),采用小杯法,以0.1 mol·L-1盐酸溶液为溶出介质,分别以50、75、100 r·min-1为转速,按“2.3”的方法测定溶出曲线,结果表明,转速为50 r·min-1时溶出度低;转速为75 r·min-1和100 r·min-1时,60 min取样可基本保证完全溶出。因此选择转速75 r·min-1。
3.1.3 测定方法的确定由于溶出需采用0.1 mol·L-1盐酸溶液,为使溶出溶液中主成分浓度最大化, 选择采用小杯法150 mL,最终供试品溶液为主成分浓度较稀的酸性水溶液,规格1(每片含总黄杨生物碱0.5 mg,环维黄杨星D 0.375 mg)的溶液质量浓度为2.5 μg·mL-1。在已报道的环维黄杨星D的HPLC测定方法中,离子对色谱分离末端检测反相HPLC法在溶液的兼容性和方法灵敏度上能满足溶出度测定要求,在所有HPLC法中最为合适,但供试品溶液需进样80 µL,此时色谱行为仍保持优良且满足定量要求。
3.2 溶出曲线考察结果5个厂家样品的溶出曲线差异明显,方法具有较好的区分度,厂家1、4的样品溶出曲线显示整个溶出过程相对较快;而厂家2、3、5的样品溶出行为相对缓慢。厂家3、5的产品溶出度在批间的差异较大。
3.3 溶出度的计算5个厂家的27批黄杨宁片样品,采用HPLC法测定环维黄杨星D的含量,结果为原标准标示量的60%~84%。环维黄杨星D原料以及黄杨宁片原标准的含量测定法为滴定法和紫外可见分光光度法,测定的实际均为总黄杨生物碱含量。在新拟定上报的标准中,修改成HPLC法,测定的是环维黄杨星D单体化合物,拟将原标准中的“规格1:每片含环维黄杨星D 0.5 mg;规格2:每片含环维黄杨星D 1mg”改为“规格1:每片含总黄杨生物碱0.5 mg,环维黄杨星D 0.375 mg;规格2:每片含总黄杨生物碱1 mg,环维黄杨星D 0.75 mg”。本文溶出度测定法为HPLC色谱测定法,测定的也是环维黄杨星D单体化合物,故应按新拟定的标示量来计算溶出度。
3.4 结果与建议本文建立的HPLC溶出度测定方法简单、灵敏、可靠,可用于黄杨宁片溶出度的测定,为其质量控制和标准制定提供了依据。
| [1] |
中华人民共和国药典2000年版.一部[S]. 2000: 153, 575 ChP 2000. Vol Ⅰ[S]. 2000: 153, 575 |
| [2] |
中华人民共和国药典2005年版.一部[S]. 2005: 276, 591 ChP 2005. Vol Ⅰ[S]. 2005: 276, 591 |
| [3] |
中华人民共和国药典2010年版.一部[S]. 2010: 575, 1065 ChP 2010. Vol Ⅰ[S]. 2010: 575, 1065 |
| [4] |
中华人民共和国药典2015年版.一部[S]. 2015: 406, 1472 ChP 2015. Vol Ⅰ[S]. 2015, 406, 1472 |
| [5] |
陈勇, 樊雪君, 龚青. HPLC梯度洗脱法测定黄杨宁片中环维黄杨星D的含量[J]. 中国中药杂志, 2006, 31(14): 1155. CHEN Y, FAN XJ, GONG Q. Determination of cyclovirobuxine-D in Huangyangning tablets by RP-HPLC with gradient elution[J]. China J Chin Mater Med, 2006, 31(14): 1155. DOI:10.3321/j.issn:1001-5302.2006.14.006 |
| [6] |
郭青, 吕霞, 孙姗, 等. 黄杨宁原料及片中环维黄杨星D含量及含量均匀度测定[J]. 药物分析杂志, 2009, 29(10): 1651. GUO Q, LÜ X, SUN S, et al. Determination and uniformit yexamination of cyclovirobuxine D in Huangyangning materials and its tablets[J]. Chin J Pharm Anal, 2009, 29(10): 1651. |
| [7] |
吕霞, 胡明通, 杨春, 等. HPLC-ELSD法测定黄杨宁片中环维黄杨星D的含量[J]. 现代中药研究与实践, 2014, 28(3): 52. LÜ X, HU MT, YANG C, et al. Determination of cyclovirobuxine D in Huangyangning tablets by HPLC-ELSD[J]. Chin Med J Res Pract, 2014, 28(3): 52. |
| [8] |
盛龙生, 安登魁, 徐新军, 等. HPLC/MS法与柱前衍生化HPLC/UV法测定环维黄杨星D有关物质比较[J]. 中国药科大学学报, 2002, 33(5): 408. SHENG LS, AN DK, XU XJ, et al. The comparison of determinating cyclovirobuxine D related substances by HPLC/MS and precolumn derivation on RP HPLC using l-phenyl-isocyanate[J]. J China Pharm Univ, 2002, 33(5): 408. DOI:10.3321/j.issn:1000-5048.2002.05.013 |
| [9] |
徐新军, 张正行, 安登魁, 等. 环维黄杨星D对照品的建立[J]. 中药新药与临床药理, 2004, 15(2): 110. XU XJ, ZHANG ZX, AN DK, et al. Establishment of the control of cyclovirobuxine D[J]. Tradit Chin Drug Res Clin Pharmacol, 2004, 15(2): 110. DOI:10.3321/j.issn:1003-9783.2004.02.012 |
| [10] |
柯仲成, 周亚球, 方超. 黄杨宁片质量标准的改进[J]. 中成药, 2007, 29(5): 3. KE ZC, ZHOU YQ, FANG C. Improvement on the standard of Huangyangning tablets[J]. Chin Tradit Pat Med, 2007, 29(5): 3. |
| [11] |
杨晨, 郭青, CHRISTIANWolf, 等. 柱前衍生化RP-HPLC法对黄杨宁片原料中环维黄杨星D和杂质的定性定量研究[J]. 药物分析杂志, 2017, 37(6): 1013. YANG C, GUO Q, CHRISTIAN Wolf, et al. Qualitative and quantitative analysis of cyclovirobuxine D and impurities in active pharmaceutical ingredient of Huangyangning tablets by RP-HPLC with pre-column derivatization[J]. Chin J Pharm Anal, 2017, 37(6): 1013. |
| [12] |
谢昀, 于治国, 徐新盛, 等. 反相离子对色谱法测定环维黄杨星D含量[J]. 药物分析杂志, 2006, 26(7): 888. XIE Y, YU ZG, XU XS, et al. Determination of cyclovirobuxine D by ion pair RP-HPLC[J]. Chin J Pharm Anal, 2006, 26(7): 888. |
| [13] |
刘洁, 杭太俊, 张正行. HPLC法测定黄杨宁中环维黄杨星D和有关生物碱检查[J]. 药物分析杂志, 2006, 26(4): 446. LIU J, HANG TJ, ZHANG ZX. HPLC determination of cyclovirobuxine D and its related alkaloids in Huangyangning[J]. Chin J Pharm Anal, 2006, 26(4): 446. |
| [14] |
胡国强, 许启泰, 张保国, 等. 环维黄杨星D分离方法改进[J]. 中国天然药物, 2004, 2(3): 155. HU GQ, XU QT, ZHANG BG, et al. An improved separation method of cyclovirobuxine D from the total alkaloids of Buxus[J]. Chin J Nat Med, 2004, 2(3): 155. |
| [15] |
郭青, 吕霞, 伍乃英, 等. 黄杨宁片及原料中环维黄杨星D含量测定的3种HPLC方法评价[J]. 中国现代应用药学, 2009, 26(11): 929. GUO Q, LÜ X, WU NY, et al. Evaluation on three HPLC methods on the determination of cyclovirobuxine D in Huangyangning tablets and raw materials[J]. Chin J Mod Appl Pharm, 2009, 26(11): 929. |
| [16] |
黄勤安, 黄海燕, 鲁静, 等. 高效液相色谱法测定黄杨宁片中环维黄杨星D的含量和含量均匀度[J]. 药物分析杂志, 2007, 27(2): 264. HUANG QA, HUANG HY, LU J, et al. HPLC determination of content and uniformity of cyclovirobuxine D in Huangyangning tablets[J]. Chin J Pharm Anal, 2007, 27(2): 264. |
 2019, Vol. 39
2019, Vol. 39 
