2. 浙江省医学科学院 安全性评价研究中心, 杭州 310013;
3. 绍兴市中医院, 绍兴 312499
2. Zhejiang Academy of Medical Sciences, Center of Safety Evaluation, Hangzhou 310013, China;
3. Shaoxing Hospital of Traditional Chinese Medicine, Shaoxing 312499, China
参麦注射液由古方生脉饮衍变而来,处方由红参和麦冬等药材构成。传统医学认为,参麦注射液具有益气固脱和养阴生津的功效;现代药理学证实,参麦方剂具有抗心肌缺血、去除氧自由基等药理学功效,临床上被广泛用于心血管疾病、免疫功能低下及各种慢性疾病治疗[1-2]。
大量研究表明,人参皂苷是参麦注射液中最主要的有效成分[3-6]。现有的参麦注射液含量测定通过检测制剂中的人参皂苷实现,其中参麦注射液含量测定方法现用国家标准为WS3-B-3428-98,有人参皂苷Rg1、Re和Rb1及人参总皂苷的含量测定,但难以全面控制参麦注射液的质量[7]。目前文献多采用HPLC同时测定参麦注射中多种人参皂苷[8-9],但由于HPLC本身的分离度和灵敏度问题,导致分析时间较长,分离效果也不甚理想。近年来也有利用超高效液相色谱(UHPLC)测定参麦注射液中人参皂苷的报道[10-11]。本实验通过方法学优化,应用UHPLC同时测定参麦方剂中11个人参皂苷的含量,并应用于参麦注射液中人参皂苷的测定。结果表明,该方法灵敏度高,分析时间短,稳定可靠,能够比较全面地检测麦注射液中人参皂苷类的含量,为参麦注射液的质量控制研究提供参考依据。
1 仪器与试药 1.1 仪器安捷伦1290 infinity超高效液相色谱仪(包含四元梯度泵、自动进样器、柱温箱和DAD检测器,安捷伦科技公司);MS105DU型电子天平(0.01 mg梅特勒-托利多(常州)测量技术有限公司);KQ-300DA型数控超声波清洗器,昆山市超声仪器有限公司。
1.2 试药参麦注射液由杭州正大青春宝有限公司提供(批号1706271、1611071、1611081、1611082,规格10 mL·支-1,每1 mL含红参0.1 g)。
对照品人参皂苷Rg1(批号Z26S7X21730)、人参皂苷Re(批号B10M8S35243)、人参皂苷Rf(批号P09M8F31017)、20(S)-人参皂苷Rh1(批号Z12M8X35790)、20(S)-人参皂苷Rg2(批号M27N8S49074)、人参皂苷Rb1(批号Z06M8L30693)、人参皂苷Rc(批号P24F8F30057)、人参皂苷Rb2(批号P09M8F35575)、人参皂苷Rd(批号Z27F8X30060)、20(S)-人参皂苷Rg3(批号Z01D7X25885)含量均为98%,均购于上海源叶生物科技有限公司。
乙腈(色谱纯)和超纯水(色谱纯)购自默克公司。
2 方法与结果 2.1 色谱条件色谱柱:Aglient Eclipse Plus C18(2.1 mm×50 mm,1.8 μm);乙腈(A)-水(B)为流动相,采用二元梯度洗脱(0~10 min,19%A;10~32 min,19%A→28%A,32~39 min,28%A→36%A,39~49 min,36%A→45%A),流速0.3 mL·min-1;柱温30 ℃;检测波长203 nm;进样量1 μL。
2.2 溶液配制 2.2.1 对照品储备液精密称取对照品人参皂苷Rg1 3.80 mg、人参皂苷Re 2.20 mg、人参皂苷Rf 0.99 mg、20(S)-人参皂苷Rh1 0.19 mg、20(S)-人参皂苷Rg2 0.22 mg、人参皂苷Rb1 6.26 mg、人参皂苷Rc 2.68 mg、人参皂苷Rb2 2.34 mg、人参皂苷Rb3 0.31 mg、人参皂苷Rd 1.30 mg、20(S)-人参皂苷Rg3 0.28 mg,分别置1 mL量瓶中,加20%乙腈水溶解并稀释至刻度,制成单一对照品储备液。
2.2.2 混合对照品溶液分别精密吸取上述单一对照品储备液人参皂苷Rg1 761 μL、人参皂苷Re 441 μL、人参皂苷Rf 499 μL、20(S)-人参皂苷Rh1 192 μL、20(S)-人参皂苷Rg2 221 μL、人参皂苷Rb1 782 μL、人参皂苷Rc 536 μL、人参皂苷Rb2 470 μL、人参皂苷Rb3 310 μL、人参皂苷Rd 654 μL、20(S)-人参皂苷Rg3 285 μL,置10 mL量瓶中,加初始比例流动相至刻度,制成人参皂苷Rg1、Re、Rf、Rh1、Rg2、Rb1、Rc、Rb2、Rb3、Rd、Rg3的质量浓度分别为0.380、0.220、0.099、0.019、0.022、0.626、0.268、0.234、0.031、0.130、0.028 mg·mL-1的混合对照品储备液。
2.2.3 供试品溶液取参麦注射液,过0.22 μm微孔滤膜,收集续滤液,即得。
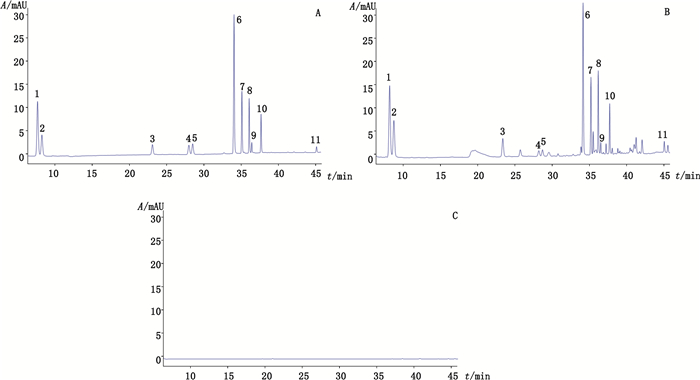
2.3 方法学考察 2.3.1 系统适用性和专属性试验分别取流动相溶液(空白对照)、混合对照品溶液和供试品溶液,按“2.1”项下色谱条件进样测定,记录色谱图,见图 1。结果显示,混合对照品溶液与供试品溶液中各指标成分色谱峰的理论塔板数均大于5 000,分离度均大于1.5,拖尾因子在0.9~1.0之间,表明系统适用性良好。在样品色谱图中,分别有与对照品保留时间一致的特征峰,表明各化合物之间分离度好,无干扰,专属性良好。
|
1.人参皂苷Rg1(ginsenosides Rg1) 2.人参皂苷Re(ginsenosides Re) 3.人参皂苷Rf(ginsenosides Rf) 4. 20(S)-人参皂苷Rh1(20(S)-ginsenosides Rh1) 5. 20(S)-人参皂苷Rg2(20(S)-ginsenosides Rg2) 6.人参皂苷Rb1(ginsenosides Rb1) 7.人参皂苷Rc(ginsenosides Rc) 8.人参皂苷Rb2(ginsenosides Rb2) 9.人参皂苷Rb3(ginsenosides Rb3) 10.人参皂苷Rd(ginsenosides Rd) 11. 20(S)-人参皂苷Rg3(20(S)-ginsenosides Rg3) 图 1 11个混合对照品(A)、参麦注射液样品(B)和空白对照(C)色谱图 Fig.1 UHPLC chromatograms of eleven reference substances(A), the Shenmai injection sample(B)and blank control(C) |
精密吸取“2.2.2”项下混合对照品储备液0、0.8、0.5、0.4、0.25 mL,分别置1 mL量瓶中,加流动相定容,摇匀,即得系列浓度的的混合对照品溶液。在上述色谱条件下进样测定,以测定的峰面积为纵坐标(Y),相应对照品的浓度为横坐标(X),绘制标准曲线。结果11个成分的线性关系良好,回归方程和相关系数见表 1。
|
|
表 1 11个对照品线性关系考察 Tab.1 Linear relationship of eleven reference substances |
精密吸取“2.2.2”项下混合对照品溶液,按上述色谱条件连续进样6次,记录峰面积。结果显示,11个人参皂苷峰面积的RSD均小于2%,说明仪器精密度良好。
2.3.4 稳定性试验取参麦注射液样品,按“2.2.2”项下方法制备供试品溶液,按上述色谱条件分别于0、2、4、8、12、24 h进样分析,11个人参皂苷峰面积的RSD均小于3%,表明供试品溶液在24 h内稳定性良好。
2.3.5 重复性试验取同一批次的参麦注射液,平行制备6份供试品溶液,进样测定并计算各人参皂苷成分含量。结果显示,样品中人参皂苷Rg1、Re、Rf、Rh1、Rg2、Rb1、Rc、Rb2、Rb3、Rd、Rg3平均含量分别为0.136 8、0.081 3、0.040 1、0.097 6、0.098 8、0.179 7、0.096 5、0.083 5、0.012 7、0.052 3、0.012 6 mg·mL-1,RSD分别为0.44%、0.57%、2.2%、1.2%、1.3%、0.33%、1.8%、1.1%、4.2%、0.52%、3.9%,表明该方法重复性良好。
2.3.6 加样回收率试验取已知含量的供试品溶液(批号1706271)0.5 mL,按已知含量的100%水平加入混合对照品0.5 mL,充分混匀,平行制备6份,过0.22 μm微孔滤膜后,进样测定。结果见表 2。
|
|
表 2 加样回收率实验结果(n=6) Tab.2 Results of recovery |
取4个批次的供试品各3份,依法进样测定,计算含量,结果见表 3。
|
|
表 3 参麦注射液含量测定结果(mg·mL-1,n=3) Tab.3 Average results of Shenmai injection determination |
考察了不同流动相系统(乙腈-水、0.05%磷酸二氢钾缓冲盐-乙腈等)对分离效果的影响,同时考察不同柱温(20、25、30、35、40 ℃)和流速(0.1、0.2、0.3、0.4、0.5 mL·min-1)对分离度的影响,结果显示,柱温30 ℃,流速为0.3 mL·min-1时各色谱峰分离度最优,并且能保持柱压在合理范围内;考察了进样量对分离度的影响,结果进样量为1 μL时峰形最佳,大于1 μL时,色谱峰峰形不好,小于1 μL时,峰面积太小影响积分。综合考虑,最终确定了“2.1”项的色谱条件。
3.2 与HPLC比较本实验采用1.8 μm小颗粒填料色谱柱,相比于HPLC使用的常规色谱柱,这一基于小粒径的分析法具有更高的效率、更佳的数据质量,能够显著地缩短分析时间,45 min内即可同时测定参麦注射液中11个成分。同时,在保证所测定皂苷成分含量结果一致[8, 12-15]的情况下,时间节省了近50 min。
4 结论近年来,随着人们对传统中药的安全及质量需求的不断提升,企业对中药质量控制的加速投入,药品分析检测的工作量急剧增加,也带来了提升分析检测效率的现实需求。本实验采用UHPLC,可在45 min内对参麦注射液中11个活性成分同时进行测定,方法稳定可靠,操作简单,为快速全面控制中药注射剂提供了实验依据。
| [1] |
朱利洁, 于佳慧, 曹文杰, 等. 参麦注射液对心肌保护作用的临床和基础研究[J]. 时珍国医国药, 2015, 26(5): 1216. ZHU LJ, YU JH, CAO WJ, et al. Clinical and basic research of Shenmai injection on myocardial protection[J]. Lishenzhen Med Mater Med Res, 2015, 26(5): 1216. |
| [2] |
LU LY, ZHENG GQ. An overview of systematic reviews of Shenmai injection for healthcare[J]. Evid Based Complement Alternat Med, 2014, 2014(8): 840650. |
| [3] |
YU J, GU LQ, XIN YF, et al. Potential accumulation of protopanaxadiol-type ginsenosides in six-months toxicokinetic study of Shenmai injection in dogs[J]. Regul Toxicol Pharmacol, 2017, 83(2): 5. |
| [4] |
杨柳, 刘奕明, 曾星, 等. HPLC/MS/MS法测定参麦注射液及人血浆中的人参皂苷Rg1[J]. 药物分析杂志, 2005, 25(8): 905. YANG L, LIU YM, ZENG X, et al. HPLC/MS/MS determination ginsenoside Rg1 in Shenmai injection and in human plasma[J]. Chin J Pharm Anal, 2005, 25(8): 905. |
| [5] |
ZHANG HJ, WU YJ, CHENG YY. Analysis of "SHENMAI" injection by HPLC/MS/MS[J]. J Pharm Biomed Anal, 2003, 31(1): 175. DOI:10.1016/S0731-7085(02)00565-4 |
| [6] |
FAN XH, WANG Y, CHENG YY. LC/MS fingerprinting of Shenmai injection:A novel approach to quality control of herbal medcines[J]. J Pharm Biomed Anal, 2006, 40(3): 591. DOI:10.1016/j.jpba.2005.10.036 |
| [7] |
中华人民共和国卫生部药品标准.中药成方制剂第十八册[S]WS3-B-3428-98.Z18-170 Drug standards of the Ministry of Health of the People's Republic of China.The 18th Volume of Traditional Chinese Medicine Prescriptions[S].WS3-B-3428-98.Z18-170 |
| [8] |
陈闽军, 吴永江, 程翼宇. 高效液相色谱用于参麦注射液人参皂苷的含量测定和批次一致性考察[J]. 中国药学杂志, 2003, 38(8): 63. CHEN MJ, WU YJ, CHENG YY. Determination of ginsenosides and assessment of the batch-to batch consistency of Shenmai injection by HPLC[J]. Chin Pharm J, 2003, 38(8): 63. |
| [9] |
郝海群, 雷洋. 高效液相色谱法测定不同厂家参麦注射液中人参皂苷Rg1和人参皂苷Re的含量[J]. 河南中医, 2015, 35(6): 1445. HAO HQ, LEI Y. The content determination of ginseng-saponin Rg1 and Re in ginseng and ophiopognis injection produced by different manufacturers by using high performance liquid chromatography[J]. Henan Tradit Chin Med, 2015, 35(6): 1445. |
| [10] |
曹树萍, 聂黎行, 王钢力, 等. UPLC法用于参麦注射液及其中间体的皂苷含量研究[J]. 药物分析杂志, 2014, 34(7): 1264. CAO SP, NIE LX, WANG GL, et al. Study on ginsenosides contents of Shenmai injection and its intermediates by UPLC[J]. Chin J Pharm Anal, 2014, 34(7): 1264. |
| [11] |
林苏娜, 余楚钦, 林华庆, 等. UPLC测定参麦注射液中人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1的含量[J]. 中国实验方剂学杂志, 2014, 20(8): 48. LIN SN, YU CQ, LIN HQ, et al. Content determination of ginsenoside Rg1, ginsenoside Re and ginsenoside Rb1 in Shenmai injection by UPLC[J]. Chin J Exp Tradit Med Form, 2014, 20(8): 48. |
| [12] |
曹树萍, 聂黎行, 王钢力, 等. HPLC法同时测定参麦注射液中9个人参皂苷的含量[J]. 药物分析杂志, 2011, 31(3): 476. CAO SP, NIE LX, WANG GL, et al. HPLC simultaneous determination of nine ginsenosides in Shenmai injection[J]. Chin J Pharm Anal, 2011, 31(3): 476. |
| [13] |
董礼, 干建伟, 李梅, 等. HPLC法快速测定参麦注射液指纹图谱[J]. 中成药, 2016, 38(3): 599. DONG L, GAN JW, LI M, et al. Rapid determination of Shenmai injection fingerprint by HPLC[J]. Chin Tradit Pat Med, 2016, 38(3): 599. |
| [14] |
吴茵, 魏欣, 张黎媛, 等. HPLC-MS/MS法同时测定参麦注射液7种主要有效成分[J]. 中草药, 2014, 45(18): 2625. WU Y, WEI X, ZHANG LY, et al. Simultaneous determination of seven components in Shenmai injection by HPLC-MS/MS[J]. Chin Tradit Herb Drugs, 2014, 45(18): 2625. DOI:10.7501/j.issn.0253-2670.2014.18.010 |
| [15] |
刘燕, 聂黎行, 陈方军, 等. 高分离度快速液相色谱-离子阱质谱分析参麦注射液化学成分[J]. 药物分析杂志, 2011, 31(9): 1672. LIU Y, NIE LX, CHEN FJ, et al. Analysis on chemical constitutes of Shenmai injection by RRLC-ion trap mass spectrometry[J]. Chin J Pharm Anal, 2011, 31(9): 1672. |
 2019, Vol. 39
2019, Vol. 39 
