过氧化氢是一种具有强氧化性、腐蚀性的无色透明液体,作为漂白剂和氧化剂被广泛地应用于染发、烫发类化妆品中,由于其较强的氧化性,过量使用会对皮肤、毛发产生严重损害[1]。已报道的文献中有关过氧化氢检测的方法有很多,主要有下述几类:电位滴定法[2]、常规滴定法[3]、高效液相色谱法[4-6]、基于傅里叶近红外光谱法[7]、荧光光度法[8-9]、生物传感分析法[10]和分光光度法[11-14]等检测方法,少量文献涉及染发剂中过氧化氢含量的测定[1]。
卫生部颁布的《化妆品卫生规范》(2007年版)对过氧化氢的使用限量做了规定,但缺少相应的检验方法。《化妆品安全技术规范》(2015年版)对过氧化氢的限定值不作改动,同时增加了高效液相柱前衍生检测方法。高效液相柱前衍生检测方法是人工进行衍生操作,人工衍生的缺点是衍生反应时间一致性不能保证,导致衍生产物的量和保留时间由于反应时间的不同而变化,同时每进一针样品需要重新配制溶液,且衍生物不稳定,需衍生后立即进样分析,操作较为烦琐。而且笔者发现按照《化妆品安全技术规范》(2015年版)过氧化氢测定的方法,衍生后用水定容的步骤中,溶液会有白色沉淀析出,所以进行了修改,将用水定容改成用乙腈定容,避免了白色沉淀的析出。
本研究采用自动进样器完成三苯基膦在线衍生后直接进样,将不能被液相色谱直接检出的过氧化氢与三苯基膦进行衍生化反应,生成的氧化三苯基膦可以很好地被高效液相色谱仪检出和分离,用二极管阵列检测器在225 nm波长下测定[1]。参考《化妆品安全技术规范》(2015年版)化妆品中过氧化氢检测方法设定仪器自动衍生进样程序,并与人工衍生方法进行方法学比较,来验证仪器自动衍生进样程序的检测结果,同时测定3种市售不同品牌染发剂中过氧化氢的含量。
1 材料与方法 1.1 仪器、试剂及供试品仪器:1200高效液相色谱仪,配置DAD检测器(安捷伦公司);ZORBAX SB-C18(4.6 mm× 250 mm,5 μm)(安捷伦公司);AE-163电子天平(梅特勒公司)。
试剂:三苯基膦(Sigma公司,批号WXBC3325U);三苯基氧化膦(百灵威公司,批号LJ70Q19);过氧化氢(国药公司,30%,批号10011208);高锰酸钾(杭州萧山化学试剂厂,批号20130502)。硫酸(杭州化学试剂公司,批号20160625,分析纯);乙腈(默克公司,批号JA077230,色谱纯);Mini-Q水纯化系统(Millipore公司);其余试剂均为分析纯。
供试品:共收集3个品牌的染发剂(国家级、省本级抽检化妆品样品)。
1.2 供试品溶液的制备取染发剂供试品Ⅰ,准确称取约0.1 g,置于50 mL棕色量瓶,超纯水溶解,振摇,定容,取上清液,0.45 μm滤膜过滤,即得。临用现配,避光操作。
1.3 标准溶液标定[15]临用前标定。移取30%过氧化氢溶液25.0 mL于250 mL量瓶中,超纯水定容,作为待标定过氧化氢溶液。称取溶液待标定过氧化氢约0.3 g于250 mL锥形瓶中,加入超纯水约30 mL,振摇,超纯水定容,加入硫酸溶液(取10 mL硫酸缓慢加入150 mL超纯水中,摇匀)100 mL,振摇用高锰酸钾标准溶液(称取约高锰酸钾1.0 g,置于大烧杯中,加超纯水至300 mL,煮沸约1 h,静置冷却后用微孔玻璃漏斗或玻璃棉漏斗过滤,1周后标定,C=0.099 45 mol·L-1)滴定至微红色,半分钟不褪色为终点。记录消耗高锰酸钾标准溶液的体积,平行测定3次。
1.4 标准溶液制备精密称取标定后的过氧化氢溶液1.500 8 g,于25 mL棕色量瓶中,超纯水定容,作为对照品储备液。用水配制成线性浓度约分别为2.4~192.7 μg·mL-1和9.6~192.7 μg·mL-1的标准溶液,分别作为柱前在线自动衍生法和人工衍生法的标准曲线溶液,临用现配,全程避光操作。
1.5 色谱条件色谱柱:ZORBAX SB-C18(4.6 mm×250 mm,5 μm);流动相:乙腈-超纯水(60:40);流速:1.0 mL·min-1;检测波长:225 nm;进样量:10 μL;柱温:35 ℃。
2 结果与讨论 2.1 柱前在线自动衍生程序参照《化妆品安全技术规范》(2015年版)[15]中过氧化氢的衍生顺序和反应体积,并适当修改,设定进样程序(见表 1)。同时按相同条件制备空白溶液。
|
|
表 1 在线衍生程序表 Tab.1 On-line derivatization program |
人工衍生:准确移取人工衍生法的标准溶液1.0 mL(或供试品溶液)于10 mL棕色量瓶,加入1.0 mL三苯基膦乙腈溶液,振摇,加入乙腈定容,振摇,暗处室温反应30 min。同时按相同条件制备空白溶液。
衍生化反应是一种利用化学变换把化合物转化成类似化学结构的物质,以便将难于分析的物质转化为与其化学结构相似但易于分析的物质。不同的衍生反应所需加入的试剂种类和顺序会有所不同。《化妆品安全技术规范》(2015年版)标准中测定过氧化氢的原理是将被测样品中的过氧化氢与三苯基膦进行衍生化反应,生成能被高效液相色谱仪分离并且检出的氧化三苯基膦。本实验建立柱前在线自动衍生法需验证仪器自动衍生进样程序进行的衍生化反应是否充分,所以同时按照《化妆品安全技术规范》(2015年版)标准人工衍生操作实验。《化妆品安全技术规范》(2015年版)中的衍生步骤中最后一步用水定容后溶液会有白色沉淀析出,本文改为用乙腈定容。
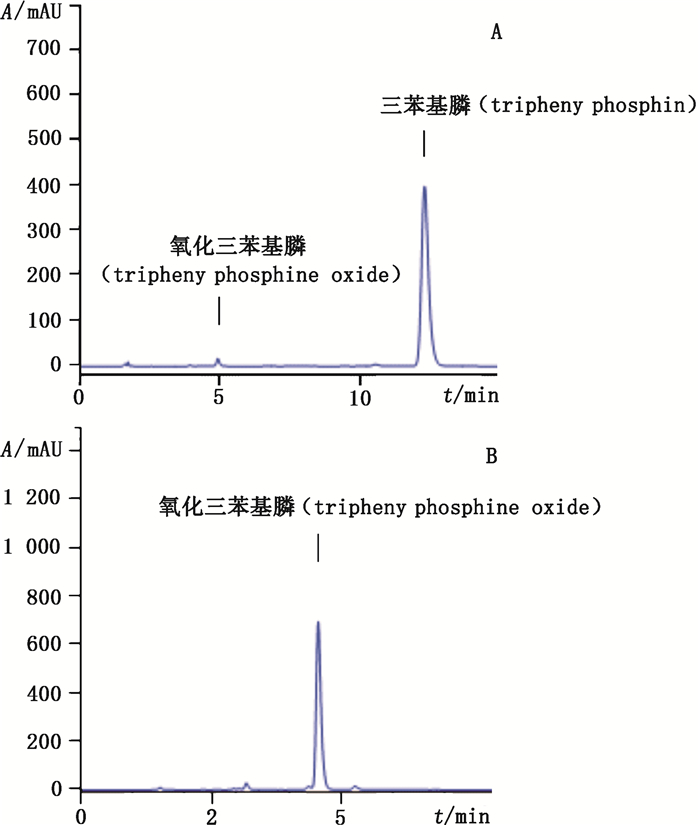
2.3 线性关系考察三苯基膦的活性较强,在原始的三苯基膦试剂中由于纯度或者其他原因,其中已经含有一定的氧化三苯基膦,所以空白图谱在氧化三苯基膦的保留时间处也有峰(见图 1)。本文通过高效液相软件将所得图谱的峰面积扣除空白即为最后图谱。
|
图 1 试剂空白(A)和对照品(B)色谱图 Fig.1 Chroma to grams of reagent blank(A)and reference substance(B) |
分别取“1.4”项下的柱前在线自动衍生法和人工衍生法的标准曲线溶液,按照“1.5”项下色谱条件进行测定,以对照品峰面积(Y)为纵坐标,溶液浓度(X,μg·mL-1)为横坐标,绘制标准曲线,求得线性回归方程。柱前在线自动衍生法和人工衍生法的标准溶液线性范围分别为2.4~192.7 μg·mL-1和9.6~192.7 μg·mL-1,线性回归方程分别为:
Y=38.19X-187.9 r=0.999 6
Y=43.15X-160.8 r=0.999 7
以信噪比(S/N)为3:1时的为检测下限,检测下限分别为18.1 μg·g-1和23.5 μg·g-1;以信噪比(S/N)为10:1时的为定量下限,定量下限分别为60.2 μg·g-1和78.2 μg·g-1。实验结果表明,柱前在线自动衍生法测得的检测下限和定量下限更低。
2.4 精密度试验取同一浓度标准溶液,按照“1.5”项下方法连续进样6次,记录对照品峰面积及RSD,柱前在线自动衍生法和人工衍生法峰面积的RSD分别为0.70%和0.30%,表明仪器精密度均良好。
2.5 重复性试验分别精密称定供试品Ⅰ6份,每份约0.1 g,按“1.2”项下方法制备供试品溶液,按照“1.5”项下色谱条件进行测定,记录峰面积,计算样品含量及RSD。结果柱前在线自动衍生法和人工衍生法测得供试品中的过氧化氢含量分别为5.82%和5.72%,RSD分别为2.7%和3.3%。表明2种方法的重复性良好。
2.6 稳定性试验取同一浓度标准溶液,分别在1.0、3.0、5.0、8.0、23.0、24.0 h进样,以峰面积为指标,测定其稳定性。计算柱前在线自动衍生法和人工衍生法峰面积的RSD分别为1.4%和2.1%。表明标准溶液在24 h内均稳定。
2.7 加样回收率试验精密称定9份供试品Ⅰ,每份约0.1 g,分别添加3个不同质量浓度标准溶液,按“1.2”项下方法制备供试溶液,按照“1.5”项下色谱条件进行测定,结果见图 2。计算加样回收率,结果见表 2。柱前在线自动衍生法和人工衍生法的回收率范围分别为92.7%~99.5%和91.4%~99.0%,表明2种方法在不同添加水平均有良好的回收率,方法准确度均良好。
|
|
表 2 加样回收率比较(n=3) Tab.2 Comparison of recoveries |
对市售抽检的3种不同品牌染发剂中的过氧化氢进行测定,与《化妆品安全技术规范》(2015年版)高效液相衍生法测定结果对比。精密称定3种不同品牌染发剂适量,每个样品平行测定2份,按“1.2”项下方法制备供试品溶液,按照“1.5”项下色谱条件进行测定,记录峰面积,计算含量及RSD。由表 3可知,柱前在线自动衍生法和人工衍生法测得3种不同品牌染发剂中的过氧化氢含量的RSD为1.6%~2.8%,2种衍生方法的检测结果RSD均小于5%。
|
|
表 3 不同品牌染发剂中的过氧化氢的含量(n=2) Tab.3 The content of H2O2 in different hair dye products |
本实验建立柱前在线自动衍生-高效液相色谱法快速测定化妆品中过氧化氢的含量,并与《化妆品安全技术规范》(2015年版)高效液相色谱柱前衍生法进行了方法学的比较,同时比较3种不同品牌染发剂中过氧化氢的含量,并且将《化妆品安全技术规范》(2015年版)中的衍生步骤中最后一步用水定容改为用乙腈定容。
很多分析实验室并没有充分利用高效液相色谱仪的自动进样器,只是单纯地进行样品进样[16],本实验充分利用自动进样器的程序进行自动在线衍生,样品只需简单溶解,即可上机检测。同时每次衍生时只需要少量衍生剂,并且克服了手工衍生时的缺点,RSD小于5%,符合定量分析的要求。柱前在线自动衍生-高效液相色谱法得到理想的线性、精密度、重现性和稳定性,灵敏性较好。通过考察加标回收对方法进行了验证,得到了较好的准确度。同时柱前在线自动衍生-高效液相色谱法的操作性有较大的优越性,大大节省了人工操作,同时消除烦琐的人工衍生过程及引入的误差,且测得的检出下限和定量下限比人工衍生要低。综上所述,利用柱前在线自动衍生-高效液相色谱法快速测化妆品中的过氧化氢,结果可靠,方法可行,适于在化妆品检验工作中应用。
| [1] |
胡俊明, 石文鹏, 林少彬. 高效液相色谱法测定化妆品中过氧化氢的方法研究[J]. 中国卫生检验杂志, 2003, 13(5): 593. HU JM, SHI WP, LIN SB. Study on method for determination of H2O2 in cosmetics by HPLC[J]. Chin J Health Lab Technol, 2003, 13(5): 593. DOI:10.3969/j.issn.1004-8685.2003.05.023 |
| [2] |
柳鑫, 董砺节. 基于全自动电位滴定仪的食品中过氧化值测定方法[J]. 食品安全质量检测学报, 2016, 7(3): 1289. LIU X, DONG LJ. Determination of peroxide values of food products by autopotentiometric titrator[J]. J Food Saf Qual, 2016, 7(3): 1289. |
| [3] |
GB/T23499-2009食品中过氧化氢的测定方法[S].2009 GB/T23499-2009 The determination methods of hydrogen peroxide in the food[S].2009 |
| [4] |
孙佳, 毛燕, 李刚, 等. 应用亲水作用液相色谱法测定食品中过氧化氢[J]. 食品安全质量检测学报, 2013, 4(6): 1878. SUN J, MAO Y, LI G, et al. Application of hydrophilic interaction liquid chromatography to determine hydrogen peroxide in food[J]. J Food Saf Qual, 2013, 4(6): 1878. |
| [5] |
徐金荣, 陈忠明. 高效液相色谱-荧光检测法环境样品中的过氧化物[J]. 色谱, 2005, 23(4): 366. XU JR, CHEN ZM. Determination of peroxides in environmental samples by high performance liquid chromatography with fluorescence detection[J]. Chin J Chromatogr, 2005, 23(4): 366. DOI:10.3321/j.issn:1000-8713.2005.04.008 |
| [6] |
张倩, 付时雨, 李海龙, 等. 一种快速测定过氧化氢浓度的方法[J]. 光谱学与光谱分析, 2014, 34(3): 767. ZHANG Q, FU SY, LI HL, et al. A rapid method for the determination of hydrogen peroxide concentration[J]. Spectroscopy Spectra Anal, 2014, 34(3): 767. DOI:10.3964/j.issn.1000-0593(2014)03-0767-04 |
| [7] |
陈易晖, 刘艳, 周建立. 高效液相色谱-紫外检测法测定食品中的过氧化氢[J]. 光谱实验室, 2009, 26(2): 414. CHEN YH, LIU Y, ZHOU JL. Determination of peroxides in food samples by high performance liquid chromatography with variable wavelength detector[J]. Chin J Spectrosc Lab, 2009, 26(2): 414. DOI:10.3969/j.issn.1004-8138.2009.02.064 |
| [8] |
高媛, 王宁, 于修烛, 等. 基于傅里叶近红外光谱的食用油过氧化值间接检测研究[J]. 中国粮油学报, 2015, 30(5): 138. GAO Y, WANG N, YU XZ, et al. Indirect determination of peroxide value of edible oils by fourier transform near infrared spectrum spectroscopy[J]. J Chin Cereals Oils Associ, 2015, 30(5): 138. DOI:10.3969/j.issn.1003-0174.2015.05.026 |
| [9] |
邹昀, 张德新. 荧光分析法测定水发食品中过氧化氢残留量[J]. 公共卫生与预防医学, 2009, 20(6): 64. ZHOU Y, ZHANG DX. Determination of hydrogen peroxide in water-soaked foodstuffs by fluorescence analysis[J]. J Pub Health Prev Med, 2009, 20(6): 64. |
| [10] |
盛丽, 朱金林, 韩小茜. 碱性藏花红T荧光猝灭法测定痕量过氧化氢[J]. 光谱实验室, 2008, 25(6): 1075. SHENG L, ZHU JL, HAN XQ. Determination of hydrogen peroxide based on fluorescence quenching with safraninet system[J]. Chin J Spectrosc Lab, 2008, 25(6): 1075. DOI:10.3969/j.issn.1004-8138.2008.06.015 |
| [11] |
童志强, 袁如, 柴雅琴, 等. 基于二氧化锆/纳米金溶胶凝胶膜固定辣根过氧化物酶的H2O2生物传感器的研制[J]. 西南师范大学学报, 2006, 31(5): 102. TONG ZQ, YUAN R, CHAI YQ, et al. A biosensor for hydrogen peroxide based on horseradish peroxidase immobilized in ZrO2/Au So-l gel matrix[J]. J Southwest China Normal Univ, 2006, 31(5): 102. DOI:10.3969/j.issn.1000-5471.2006.05.021 |
| [12] |
姜成春, 庞素艳, 马军, 等. 钛盐光度法测定Fenton氧化中的过氧化氢[J]. 中国给水排水, 2006, 22(4): 88. JIANG CC, PANG SY, MA J, et al. Spectrophotometric determination of hydrogen peroxide in fenton reaction with titanium oxalate[J]. China Water Wastewater, 2006, 22(4): 88. DOI:10.3321/j.issn:1000-4602.2006.04.025 |
| [13] |
张薇薇, 杨怡, 陈培超. 钼酸铵分光光度法测定水发产品中过氧化氢残留量[J]. 现代预防医学, 2008, 35(8): 1556. ZHANG WW, YANG Y, CHEN PC. Determination of hydrogen peroxide in water-soaked foodstuffs by ammonium molybdate tetrahydrate spectrophotometry[J]. Mod Prevent Med, 2008, 35(8): 1556. DOI:10.3969/j.issn.1003-8507.2008.08.066 |
| [14] |
张瑛洁, 马军, 张亮. 钛盐分光光度法测定酸性染料体系中的过氧化氢[J]. 工业水处理, 2008, 28(11): 72. ZHANG YJ, MA J, ZHANG L. Spectrophotometric determination of hydrogen peroxide in acidic dye system with titanium oxalate[J]. Ind Water Treat, 2008, 28(11): 72. |
| [15] |
化妆品安全技术规范2015年版[S].2016: 363 Safety and Technical Standards for Cosmetics[S].2016: 363 |
| [16] |
林玉宙, 黄耀铕, 丛骁, 等. 柱前在线自动衍生-高效液相色谱法快速测定乳粉中牛磺酸[J]. 乳业科学与技术, 2015, 38(5): 23. LIN YZ, HUANG YY, CONG X, et al. Rapid determination of taurine in milk powder by high performance liquid chromatography with on-line automated pre-column derivatization[J]. J Dairy Sci Technol, 2015, 38(5): 23. |
 2019, Vol. 39
2019, Vol. 39 