三黄泻心汤为商朝伊尹所创,首载于东汉张仲景所撰之《金匮要略·惊悸吐衄下血胸满瘀血病脉证治第十六》,主治疗热盛吐衄证,包括大黄、黄连、黄芩3个药味[1]。依据刘昌孝院士提出的中药质量标志物(Q-Marker)控制中药产品质量的理论[2],按经方的制剂方法制备样品,测得三黄泻心汤的生物碱类-黄酮类-蒽醌类质量标志物体系中16种质量标志物组合的含量:盐酸药根碱-盐酸表小檗碱-盐酸黄连碱-盐酸巴马汀-盐酸小檗碱-黄芩苷-汉黄芩苷-黄芩素-汉黄芩素-番泻苷A-番泻苷B-芦荟大黄素-大黄酸-大黄素-大黄酚-大黄素甲醚,其含量)依次为1.800、5.400、7.700、4.500、18.800、47.800、9.400、3.600、1.100、0.423、3.540、0.069、0.112、0.365、0.111、0.033 mg·mL-1[3]。质量标志物组合成分药理作用明确且与临床疗效相关[4-5],采用生物检定方法验证三黄泻心汤与其质量标志物配比的等效性。
清热解毒药药理作用广泛,主要的药理作用为抗菌、抗炎等[6]。三黄泻心汤为经典清热解毒方剂,具有明显的抑菌作用,其质量标志物均具有明确的生物活性[7-9]。目前生物活性评价方法已逐渐受到国内外学者的关注,尤其是FDA发布的《植物药研发行业指南》对植物药及制剂的质量评控明确提出[10]:在只靠化学检验不足以确保质量和疗效一致性的情况下,应在质量标准和稳定性方案中纳入生物检定。肖小河等[11]指出生物活性检测方法联合多组分化学表征将是中药及中药相关产品质量评控的重要发展方向。生物检定在合理的供试品溶液制备的情况下,选择体外的试验方法较为适宜,如体外抑菌。所以本实验选取了体外抑菌[12-13]作为生物效价评价指标,测定了三黄泻心汤质量标志物抑菌生物效价。
1 材料 1.1 药物药材饮片:饮片黄芩(批号120101)、黄连(批号120101)、大黄(批号120101)购自安国市路路通饮片厂,经北京中医药大学张贵君教授鉴定依次为唇形科植物黄芩Scutellaria baicalensis Georgi的干燥根,毛茛科植物黄连Coptis chinensis Franch.的干燥根茎,寥科植物大黄Rheum palmatum L.的干燥根。
对照品:盐酸药根碱(批号201011)、盐酸表小檗碱(批号110426)、盐酸黄连碱(批号107917)、盐酸巴马汀(批号110732)、盐酸小檗碱(批号110713)、黄芩苷(批号110329)、汉黄芩苷(批号110702)、黄芩素(批号100810)、汉黄芩素(批号110404)、芦荟大黄素(批号100729)、大黄酸(批号111201)、大黄素(批号111106)、大黄酚(批号110802)、大黄素甲醚(批号100328)、番泻苷A(批号110714)、番泻苷B(批号110908),纯度均≥ 98%,购自四川省维克奇生物科技有限公司。
阳性对照物:亚胺培南(批号810121,规格4万U),购自重庆赛普那斯科技有限公司。
1.2 试验菌金黄色葡萄球菌(批号260143)、乙型链球菌(批号321304)、大肠杆菌(批号14153)、痢疾杆菌(批号513502)、伤寒杆菌(批号50071-8)、白色念珠菌(批号CMCC(F)98001),均购自中国食品药品检定研究院,由本室传代保存。
1.3 培养基胎牛血清(中国农业科学院哈尔滨兽医研究所,批号0607);营养肉汤(北京奥博星生物技术有限责任公司生产,规格为250 g,批号20120316);营养琼脂(北京奥星生物技术有限责任公司生产,规格为250 g,批号20130105);沙氏培养基(自制,蛋白胨10 g,葡萄糖40 g,蒸馏水1 000 mL配成液体培养基)。
1.4 仪器电热鼓风箱:DFG801型,湖北省黄石市医疗器械厂;电热恒温培养箱:DNP-9162型,上海精密实验设备有限公司;高压蒸汽灭菌器:AstellScientific,AMA440N,英国;冰箱:Electrolux,BCD-211E,伊莱克斯电器有限公司(中国)。
2 方法 2.1 复方水煎液和质量标志物组的制备取三黄泻心汤(黄芩5 g,黄连5 g,大黄10 g),加水煎煮2次。第1次加10倍水,常温浸泡30 min,煎煮,水沸后回流提取30 min,4层纱布趁热滤过,药渣再加10倍水,煎煮20 min,同法过滤,合并2次滤液,浓缩,冷至常温后,调节浓度至每毫升提取液含药量1 g。
三黄泻心汤质量标志物组:盐酸药根碱-盐酸表小檗碱-盐酸黄连碱-盐酸巴马汀-盐酸小檗碱-黄芩苷-汉黄芩苷-黄芩素-汉黄芩素-番泻苷A-番泻苷B-芦荟大黄素-大黄酸-大黄素-大黄酚-大黄素甲醚,其含量依次为1.800、5.400、7.700、4.500、18.800、47.800、9.400、3.600、1.100、0.423、3.540、0.069、0.112、0.365、0.111、0.033 mg·g-1,三黄泻心汤泻火解毒质量标志物组的含量为104.153 mg·g-1。按照16种质量标志物比例56:163:232:136:571:1 448:283:110:32:107:13:2:3:11:3:1混合均匀,得到三黄泻心汤质量标志物组。按照盐酸药根碱-盐酸表小檗碱-盐酸黄连碱-盐酸巴马汀-盐酸小檗碱比例(1:3:4.28:2.5:10.44)混合均匀得到黄连质量标志物组,按照黄芩苷-汉黄芩苷-黄芩素-汉黄芩素比例(43.45:8.55:3.27:1)混合均匀得到黄芩质量标志物组,按照番泻苷A-番泻苷B-芦荟大黄素-大黄酸-大黄素-大黄酚-大黄素甲醚比例(12.82:107.27:2.09:3.39:11.06:3.36:1)混合均匀得到大黄质量标志物组。用无菌0.9%氯化钠溶液配制成一定浓度的药液,煮沸灭菌于4 ℃保存备用。试验时,用培养液将药物对倍稀释,制成不同浓度梯度。
2.2 试验菌液和培养基的配制金黄色葡萄球菌、痢疾杆菌、伤寒杆菌、大肠埃希菌接种于MH肉汤,置普通培养箱37 ℃、24 h培养;白色念珠菌接种于沙保弱氏肉汤,置普通培养箱37 ℃、48 h培养;乙型链球菌接种于5%小牛血清肉汤,5% CO2培养箱37 ℃、48 h培养。比浊法进行细菌计数,转种于平板测定菌液中活菌数,即菌落形成单位(CFU·mL-1)。用稀释液调配成1.5×108 CFU·mL-1菌液备用。沙保弱氏培养基、5%小牛血清肉汤、MH培养基、MH肉汤均按《现代微生物培养基和试剂手册》制备。
2.3 最小抑菌浓度(minimal inhibitory concentration,MIC)和最小杀菌浓度(minimal bactericidal concentration,MBC)测定方法参照《卫生部药政局新药临床前研究指导原则》中“抗菌药体外抗菌试验原则”和《微生物学检验技术》,采用二倍稀释法测定MIC,平板转染法测定MBC(表 1、2)。
|
|
表 1 各药物体外抑菌MIC结果(mg·mL-1) Tab.1 The MIC results of each group in vitro |
|
|
表 2 各药物体外抑菌MBC结果 Tab.2 The MBC results of each group in vitro |
根据以上结果选择金黄色葡萄球菌和乙型链球菌2种标准菌株(中国食品药品检定研究院提供)。分别选择对金黄色葡萄球菌和乙型链球菌MIC的2、4、8倍作为试验浓度,按照《中华人民共和国药典》2010年版二部附录Ⅺ规定的培养基和培养条件进行抑菌试验,测定抑菌圈直径(表 3)。
|
|
表 3 对2种标准菌株的平均抑菌圈直径(mm) Tab.3 Average bacteriostasis diameter of two standard strains |
可见,复方水煎液对乙型链球菌2倍MIC(浓度为125 mg·mL-1)的抑菌圈大小较合适,故选择乙型链球菌为测定菌株,确定生药125 mg·mL-1中心浓度。亚胺培南对乙型链球菌4倍MIC(浓度为1 mg·mL-1)的抑菌圈大小较合适,故选择乙型链球菌为测定菌株,确定1 mg·mL-1为中心浓度。
2.5 生物效应标准曲线的确定以生药0.125 g·mL-1、1 mg·mL-1为中心浓度,1:0.8为剂距,用蒸馏水配制一组不同浓度的三黄泻心汤水煎液与亚胺培南标准液,在规定的培养基和培养条件下培养16 h,取出,用游标卡尺测量抑菌圈直径,以对数浓度(lgCk)Y为纵坐标,抑菌圈直径X(mm)为横坐标,应用Excel软件得到三黄泻心汤及亚胺培南的直线方程式。
2.6 标准曲线回归数据及β的可信限率测定精密移取对照(三黄泻心汤、亚胺培南)溶液,用蒸馏水稀释成各浓度Ck(k1-k8);同时配制对照溶液的中心浓度溶液。取备妥的双碟24只,分为8组,每组3只。每组各碟内间隔的3只牛津杯内分别滴满对照溶液Ck(k1-k8),即0.40~2.50 U·mL-1溶液;另3只牛津杯内均滴满对照溶液的中心浓度溶液。在规定的培养基和培养条件下培养16 h后,逐一测量每个抑菌圈直径。根据测得值,应用Excel软件计算出标准曲线的回归数据及β的可信限率。
2.7 抑菌生物效价的测定按照《中华人民共和国药典》2005年版二部附录Ⅺ规定的培养基和培养条件进行抑菌试验,测定药效组分抑菌圈直径。代入计算公式lgR = (yt-ys)/b,求出R值,即为相应生物效价。
2.8 试验结果三黄泻心汤对金黄色葡萄球菌、乙型链球菌、伤寒杆菌、痢疾杆菌敏感,其药效组分对金黄色葡萄球菌、乙型链球菌、痢疾杆菌、白色念珠菌敏感,且质量标志物配比的抑菌效果明显优于三黄泻心汤水煎液。因此选择金黄色葡萄球菌和乙型溶血性链球菌进行抑菌效价计算,质量标志物组抑菌效果明显优于复方水煎液,见表 1。
据上述抑菌结果,选取金黄色葡萄球菌和乙型链球菌2种标准菌株(中国食品药品检定研究院提供)。采用二倍稀释法测定三黄泻心汤水煎液及亚胺培南对2种标准菌株的MIC,结果三黄泻心汤水煎液对上述2种标准菌株的MIC依次为125 mg·mL-1和62.5 mg·mL-1。亚胺培南对上述4种标准菌株的MIC依次为0.5 mg·mL-1和0.25 mg·mL-1(表 4、5)。
|
|
表 4 不同浓度三黄泻心汤和亚胺培南对乙型链球菌的抑菌圈直径(mm) Tab.4 Diameter of bacteriostasis of different concentrations of Sanhuang Xiexin decoction |
|
|
表 5 质量标志物组供试品测定记录表 Tab.5 Record table for test products of Q-marker group |
复方水煎液对乙型链球菌2倍MIC(浓度为125 mg·mL-1)的抑菌圈大小较合适。故选择乙型链球菌为测定菌株,确定生药125 mg·mL-1中心浓度。亚胺培南对乙型链球菌4倍MIC(浓度为1 mg·mL-1)的抑菌圈大小较合适。故选择乙型链球菌为测定菌株,确定1 mg·mL-1为中心浓度。
以对数浓度Y(lgCk)为纵坐标,抑菌圈直径X(mm)为横坐标,得出三黄泻心汤和亚胺培南的直线方程式分别为
| $ \begin{array}{ll}{Y = 0.1252 X-2.978} & {R^{2} = 0.9882} \\ {Y = 0.1606 X-2.6672} & {R^{2} = 0.9886}\end{array} $ |
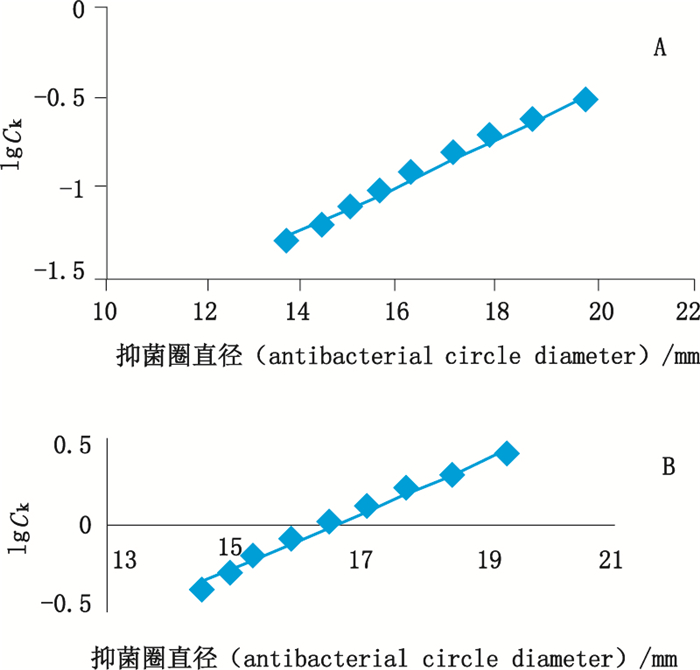
表明复方水煎液生药在0.051~0.305 g · mL-1时,对数浓度与抑菌圈直径线性关系良好,因此,选定生药0.125 g · mL-1作为中心浓度;亚胺培南在0.41~2.44 mg · mL-1时,对数浓度与抑菌圈直径线性关系良好,因此,选定1.00 mg · mL-1作为中心浓度(图 1)。
|
图 1 三黄泻心汤水煎液(A)和亚胺培南(B)对乙型链球菌抑菌生物效应曲线 Fig.1 Biological effect curves of Sanhuang Xiexin decoction(A) and imipenem (B) to Streptococcus B |
复方水煎液-乙型链球菌β = b±t0.05×Sb = 7.704±2.45×0.800 3 = 5.743 3~9.664 7,可信限率(FL) = (9.664 7-5.743 3)/(7.704×2)×100% = 25.45%。亚胺培南-乙型链球菌β = b±t0.05×Sb = 6.026 6±2.45×0.609 3 = 7.519 5~4.533 7,可信限率(FL) = (7.519 5-4.533 7)/(6.026 6×2)×100% = 24.77%(表 5)。
质量标志物配比相对三黄泻心汤的效价为lgR = (yt-ys)/b = 14.13/7.704 = 1.834 6,R = PT/PS = 74.92;即1 g质量标志物配比所产生的生物效价相当于74.92 g的复方药材。
质量标志物组相对亚胺培南的效价为lgR = (yt-ys)/b = 3.87/6.026 6 = 0.642 2,R = PT/PS = 4.387 3;即1 mg质量标志物组所产生的生物效应相当于4.387 3 μg的亚胺培南。
3 结论与讨论 3.1 质量标志物的选择三黄泻心汤为临床常用经典方剂,其抑菌作用已被广泛证实[7-8,14-15]。其处方组成为黄连、黄芩、大黄三味药。其中黄连、黄芩、大黄均为临床常用药材,其化学成分及活性研究较为深入。从文献报道来看,黄连抗菌活性主要由盐酸药根碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱等生物碱类成分提供;黄芩抗菌活性主要由黄芩苷、汉黄芩苷、黄芩素、汉黄芩素等黄酮类成分提供;大黄抗菌活性主要由番泻苷A、番泻苷B、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚等蒽醌类成分提供[16-20]。上述成分也是这些药材活性及质量控制研究的重点关注成分。因此在三黄泻心汤的研究中,也选择上述16个成分作为其质量标志物。从实验结果来看,这16个成分的混合物已能代表甚至超过原汤剂的抑菌活性,表明上述标志物的选择具有一定合理性。
3.2 生物效价测定方法在实验菌种选择中,依据上呼吸道感染的常见参考细菌包括金黄色葡萄球菌、乙型溶血性链球菌、伤寒杆菌、白色念珠菌、大肠杆菌、痢疾杆菌[21-25],故选择上述6种菌对原汤剂和质量标志物进行等效性试验。前期预试验中对亚胺培南、庆大霉素作为对照药物进行比较,结果表明亚胺培南抑菌更广谱且敏感,选为阳性对照物。
生物效价测定试验与化学分析相比,重复性较差。为此,在正式试验前,专门进行了预试验,在预试验中所得抑菌抑菌圈直径线性方程与正式试验结果稍有差异,但试验最终结论基本一致,表明本试验结果重复性较好。
三黄泻心汤的原汤剂与其质量标志物组的抑菌实验数据显示,乙型溶血性链球菌的抑菌圈直径更适宜,表现出更佳的敏感度,与报道溶血性链球菌最常见[26]相符,因此选为计算效价的菌种。三黄泻心汤的原汤剂与其质量标志物组均有较强的抗菌作用,且质量标志物组效果明显优于复方水煎液。另发现单味药质量标志物组抑菌效果:黄连 > 黄芩 > 大黄,此方中黄连抑菌效果最佳且更广谱。3个单味药均有抑菌作用的是金黄色葡萄球菌和乙型溶血性链球菌。三黄泻心汤水煎剂及质量标志物组对金黄色葡萄球菌、乙型溶血性链球菌抑制作用明显,这与单味药的抑菌结论相符。
3.3 质量标志物生物效价评价的意义本实验选择与三黄泻心汤泻火解毒作用密切相关的抑菌生物效应指标来反映原方及质量标记物组的作用效果[27-31]。首次采用抑菌生物效应评价方法,在已初步确定疗效的质量标志物组研究的基础上,对三黄泻心汤原方及质量标志物组的生物效价进行测定。选择性较高,作用较强,灵敏度较好,从抑菌角度评价三黄泻心汤的质量标志物组的药效作用,得出1 g质量标志物组所产生的生物效价相当于74.92 g的复方药材,1 mg质量标志物组所产生的生物效应相当于4.387 3 μg的亚胺培南。质量标志物组药效明显优于原汤剂,为中药制剂新品的研发提供了探讨的方向,方法简便,可操作性强。
中药的质量控制和评价一直以来都是中药新药研发的难点,尤其是在中药国际化研究中,更是极大的挑战。三黄泻心汤质量标志物组是中药新药研发的一种新思路,本实验将抗生素与质量标志物进行效价换算,确定三黄泻心汤质量标志物组及其生物效价分析方法为中药质量控制提供了一种新的研究模式,通过对质量标记物及生物效价的深入研究和实施,将药物品质评价和质量控制有机地结合,探索出一条用于中药产品质量一致性评价和质量控制的可行性模式。
| [1] |
范永升. 金匮要略[M]. 北京: 中国中医药出版社, 2003. FAN YS. Synopsis of Golden Chamber[M]. Beijing: China Traditional Chinese Medicine Publishing House, 2003. |
| [2] |
刘昌孝, 陈士林, 肖小河, 等. 中药质量标志物(Q-Marker):中药产品质量控制的新概念[J]. 中草药, 2016, 47(9): 1443. LIU CX, CHEN SL, XIAO XH, et al. New concept on quality marker of Chinese materia medica:quality control for Chinese medicinal products[J]. Chin Tradit Herb Drugs, 2016, 47(9): 1443. |
| [3] |
刘晶晶, 张贵君, 彭慧, 等. 三黄泻心汤药效组分分析[J]. 中国实验方剂学杂志, 2013, 19(18): 103. LIU JJ, ZHANG GJ, PENG H, et al. Analysis of active components alignments of classic recipe of Chinese medicine Sanhuang Xiexin Tang[J]. Chin J Exp Tradit Med Form, 2013, 19(18): 103. |
| [4] |
李颜, 郭澄. 三黄泻心汤的现代药理研究进展[J]. 中国药房, 2010, 11(12): 1045. LI Y, GUO C. The modern pharmacological research progress of Sanhuang Xiexin decoction[J]. China Pharm, 2010, 11(12): 1045. |
| [5] |
赖先荣, 张艺, 郑海杰, 等. 三黄方及其单味药药效物质基础的血清药物化学研究[J]. 世界科学技术-中医药现代化, 2012, 19(5): 520. LAI XR, ZHANG Y, ZHENG HJ, et al. Three serum pharmacochemistry of Sanhuangfang and its single medicinal ingredients[J]. World Sci Technol Mod Tradit Chin Med, 2012, 19(5): 520. |
| [6] |
李瑞奇, 白明, 苗明三. 清热药的特点及现代研究[J]. 中医学报, 2013, 1(7): 1003. LI RQ, BAI M, MIAO MS. Modern research and relationship of heat-clearing traditional Chinese medicine[J]. Acta Chin Med, 2013, 1(7): 1003. |
| [7] |
魏晓芬, 李静华, 郭玉成. 三黄泻心汤不同剂型的体外抑菌作用观察[J]. 承德医学院学报, 2006, 23(1): 14. WEI XF, LI JH, GUO YC. The bacteriostatic effects of Sanhuang Xiexin Decoction of different dosage forms of the observation[J]. J Chengde Med Coll, 2006, 23(1): 14. |
| [8] |
谭波, 于丽华, 韩志芬, 等. 泻心汤的抗菌作用研究[J]. 上海中医药大学学报, 2007, 21(2): 48. TAN B, YU LH, HAN ZF, et al. Antibacterial effect of Xiexin decoction[J]. J Shanghai Univ Tradit Chin Med, 2007, 21(2): 48. DOI:10.3969/j.issn.1008-861X.2007.02.016 |
| [9] |
US.Department of Health and Human Services, Food and Drug Administration Center for Drug Evaluation and Research (CDER).Botanical Drug Development Guidance for Industry(Draft Guidance)[S].2015
|
| [10] |
秦亚东, 席先蓉, 梁光义, 等. 高效液相色谱法测定泻心汤不同煎液中黄芩苷的含量及体外抗菌作用比较[J]. 时珍国医国药, 2006, 17(12): 2387. QIN YD, XI XR, LIANG GY, et al. Determination of baicalin in different decoctions of Xiexin Tang by HPLC and comparson of the antibacterial effects in vitro[J]. Lishizhen Med Mater Med Res, 2006, 17(12): 2387. DOI:10.3969/j.issn.1008-0805.2006.12.005 |
| [11] |
肖小河, 王伽伯, 鄢丹. 生物评价在中药质量标准化中的研究与应用[J]. 世界科学技术-中医药现代化, 2014, 16(3): 514. XIAO XH, WANG JB, YAN D. Studies and application of biological evaluation in the quality standardization of Chinese medicines[J]. World Sci Technol Mod Tradit Chin Med, 2014, 16(3): 514. |
| [12] |
孙婷婷, 马晓慧, 李欣欣, 等. 中药生物效价研究现状及开发思路探讨[J]. 中草药, 2017, 48(9): 1906. SUN TT, MA XH, LI XX, et al. Discussion on research status and development ideas of biopotency for Chinese materia medica[J]. Chin Tradit Herb Drugs, 2017, 48(9): 1906. |
| [13] |
徐蓓蕾, 文春先, 张贵君, 等. 葛根芩连汤药效组分抑菌生物效价测定[J]. 中华中医药杂志, 2013, 28(1): 230. XU BL, WEN CX, ZHANG GJ, et al. Determination of biological titers of active components alignments in Gegen Qinlian decoction on bacteriostasis[J]. China J Tradit Chin Med Pharm, 2013, 28(1): 230. |
| [14] |
白羽, 徐广宇. 三黄泻心汤合煎和分煎样品的抑菌活性研究[J]. 健康之路, 2016, 15(3): 203. BAI Y, XU GY. Study on antimicrobial activity of Sanhuang Xiexin decoction and Fenjian decoction samples[J]. Health Way, 2016, 15(3): 203. |
| [15] |
孙涛, 张洪峰, 刘璐. 三黄泻心汤不同提取溶媒抑菌活性研究[J]. 中国医院用药评价与分析, 2015, 15(6): 711. SUN T, ZHANG HF, LIU L. Antibacterial activity of different extracts from Sanhuang Xiexin decoction[J]. Eval Anal Drug Use Hosp China, 2015, 15(6): 711. |
| [16] |
王育红, 张志清, 李仲兴, 等. 8种中药水煎剂与免煎颗粒剂对临床菌株的体外抑菌作用研究[J]. 时珍国医国药, 2005, 23(8): 734. WANG YH, ZHANG ZQ, LI ZX, et al. 8 kinds of Chinese herbal medicine decoction and free decoction on clinical strains of the bacteriostatic action[J]. Lishizhen Med Mater Med Res, 2005, 23(8): 734. DOI:10.3969/j.issn.1008-0805.2005.08.010 |
| [17] |
毛理纳, 罗予, 孟林敏, 等. 黄连合用头孢菌素类抗生素的抑菌作用研究[J]. 中医药学刊, 2004, 22(11): 2033. MAO LN, LUO Y, MENG LM, et al. Antibacterial effect of Coptis chinensis cephalosporins[J]. J Tradit Chin Med, 2004, 22(11): 2033. DOI:10.3969/j.issn.1673-7717.2004.11.031 |
| [18] |
唐金凤, 李莉, 左国营. 51种常见中草药抗菌活性筛选[J]. 时珍国医国药, 2016, 27(4): 788. TANG JF, LI L, ZUO GY. 51 kinds of common herbal medicine antibacterial activity in screening[J]. Lishizhen Med Mater Med Res, 2016, 27(4): 788. |
| [19] |
罗海燕, 邝枣园, 黄雅丽, 等. 黄芩颗粒和黄芩煎剂体外抗菌试验的比较[J]. 临床合理用药杂志, 2011, 4(1): 69. LUO HY, KUANG ZY, HUANG YL, et al. Comparison of in vitro antibacterial test between Scutellaria baicalensis granules and Scutellaria baicalensis[J]. J Clin Rat Drug Use, 2011, 4(1): 69. DOI:10.3969/j.issn.1674-3296.2011.01.057 |
| [20] |
宋丽琴. 大黄不同炮制品的体外抑菌作用[J]. 海峡药学, 2011, 23(5): 55. SONG LQ. In vitro bacteriostasis of different artillery products of rhubarb[J]. Strait Pharm J, 2011, 23(5): 55. DOI:10.3969/j.issn.1006-3765.2011.05.021 |
| [21] |
张晓艳, 易绍琼, 陈薇. 金黄色葡萄球菌疫苗的研究进展[J]. 微生物学免疫学进展, 2009, 37(2): 74. ZHANG XY, YI SQ, CHEN W. Advances in the research of Staphylococcus aureus vaccine[J]. Prog Microbiol Immunol, 2009, 37(2): 74. DOI:10.3969/j.issn.1005-5673.2009.02.019 |
| [22] |
王倩, 褚云卓, 邓宇欣. 连续5年监测乙型溶血性链球菌的临床分布及耐药性分析[J]. 中国现代医学杂志, 2004, 14(20): 67. WANG Q, CHU YZ, DENG YX. Analysis of clinical distribution and drug resistance of Streptococcus hemolytic streptococci for 5 consecutive years[J]. Chin J Mod Med, 2004, 14(20): 67. DOI:10.3969/j.issn.1005-8982.2004.20.021 |
| [23] |
尹秀玲, 牛发良. 大肠杆菌耐药机制的研究进展[J]. 河北北方学院学报, 2007, 23(2): 49. YIN XL, NIU FL. Research progress in the mechanism of drug resistance of Escherichia coli[J]. J Hebei North Univ, 2007, 23(2): 49. |
| [24] |
王亚霞, 魏琴, 刘亚新. 医院内白色念珠菌感染原因探讨及预防[J]. 中华医院感染学杂志, 2003, 13(9): 885. WANG YX, WEI Q, LIU YX. Study on the causes of Candida albicans infection in hospital and prevention[J]. Chin J Nosocomiol, 2003, 13(9): 885. DOI:10.3321/j.issn:1005-4529.2003.09.033 |
| [25] |
张麦利. 痢疾杆菌菌型分布及其耐药性分析[J]. 医技与临床, 2009, 11(13): 1022. ZHANG ML. Shigella serotype distribution and drug resistance analysis[J]. Clin Med Technol, 2009, 11(13): 1022. |
| [26] |
陈哲杰, 李文, 何瑶, 等. 三黄泻心汤研究现状及其关键技术与核心问题分析[J]. 中草药, 2016, 39(11): 4111. CHEN ZJ, LI W, HE Y, et al. Research status of Sanhuang Xiexin decoction and analyses of key technologies and core issues[J]. Chin Tradit Herb Drugs, 2016, 39(11): 4111. |
| [27] |
刘晶晶, 张贵君, 彭慧, 等. 与大黄功能对应的7种药效组分分析[J]. 天津中医药, 2014, 31(1): 202. LIU JJ, ZHANG GJ, PENG H, et al. Analysis of active components alignments in rhubarb on the basis of functions of purging fire of detoxification eliminating stagnant and treating jaundice[J]. Tianjin Tradit Chin Med, 2014, 31(1): 202. |
| [28] |
刘晶晶, 张贵君, 彭慧, 等. 黄芩清热燥湿和泻火解毒药效组分分析[J]. 辽宁中医药大学学报, 2013, 15(11): 89. LIU JJ, ZHANG GJ, PENG H, et al. Analysis of active components alignments in Scutellaria on the basis of functions of clearing away heat and eliminating dampness purging fire and toxic material[J]. J Liaoning Univ Tradit Chin Med, 2013, 15(11): 89. |
| [29] |
刘晶晶, 张贵君, 彭慧, 等. 与黄连功能对应的5种药效组分分析[J]. 辽宁中医药大学学报, 2013, 15(10): 56. LIU JJ, ZHANG GJ, PENG H, et al. Analysis of the five active component alignment corresponding to the function of Rhizoma Coptidis[J]. J Liaoning Univ Tradit Chin Med, 2013, 15(10): 56. |
| [30] |
谭正怀, 唐大轩, 李杭翼. 泻心汤配伍理论实验研究[J]. 中国实验方剂学杂志, 2010, 16(4): 99. TAN ZH, TANG DX, LI HY. Study on interactions among drugs in Xiexin decoction[J]. Chin J Exp Tradit Med Form, 2010, 16(4): 99. DOI:10.3969/j.issn.1005-9903.2010.04.035 |
| [31] |
耿慧春, 辛颖, 艾凤伟, 等. 三黄泻心汤HPLC指纹图谱研究[J]. 中草药, 2008, 39(4): 524. GENG HC, XIN Y, AI FW, et al. Fingerprint research of Sanhuang Xiexin decoction by HPLC[J]. Chin Tradit Herb Drugs, 2008, 39(4): 524. DOI:10.3321/j.issn:0253-2670.2008.04.015 |
 2019, Vol. 39
2019, Vol. 39 