2. 北京市药品检验所, 北京 102206;
3. 中国药学会, 北京 100022
2. Beijing Institute for Drug Control, Beijing 102206, China;
3. Chinese Pharmaceutical Association, Beijing 100022, China
复方利血平片(曾用名复方降压片)临床常用于治疗早期和中期高血压病,含有利血平、氢氯噻嗪、硫酸双肼屈嗪、盐酸异丙嗪、维生素B1、维生素B6、泛酸钙、氯化钾和三硅酸镁等成分,其中治疗高血压的主要药物为肾上腺素能神经阻滞药利血平,血管扩张药硫酸双肼屈嗪及利尿降压药氢氯噻嗪,三药联合应用有显著的协同作用。复方利血平片目前已收载于《中华人民共和国药典》2015年版第二部[1],分别采用梯度洗脱HPLC法与等度HPLC法测定利血平、氢氯噻嗪、盐酸异丙嗪、硫酸双肼屈嗪、维生素B1和维生素B6。也有研究人员采用计算紫外分光光度法测定6个组分[2],或采用等度HPLC法测定部分组分[3-9]。梯度洗脱较等度洗脱更为复杂,存在仪器间差别较大、分析时间更长及容易出现基线漂移等缺点[10],而本文通过大量的实验研究,结合各组分的化学特性,建立2个流动相组成相同、比例不同的等度HPLC系统,用于6个主要成分(硫酸双肼屈嗪、氢氯噻嗪、维生素B1、维生素B6、利血平和盐酸异丙嗪)的含量均匀度测定。该法简便快捷,耐用性好,重复性好,可用于控制复方利血平片的质量。
1 仪器、试药和药品岛津LC -10Avp高效液相色谱仪,安捷伦Agilent1200,试验中所用色谱柱如表 1所示。
|
|
表 1 试验所用色谱柱 Table 1 The chromatographic columns used in the test |
对照品氢氯噻嗪(批号100309-200702,纯度100%)、硫酸双肼屈嗪(批号100309-200702,纯度100%)、维生素B1(批号100392-200301,纯度100%)、维生素B6(批号100116-200502,纯度100%)、盐酸异丙嗪(批号100422-200501,纯度100%)、利血平(批号100041-200311,纯度100%)均购自中国食品药品检定研究院。复方利血平片由北京双鹤制药有限公司生产,批号100510、100511、100512;空白片由北京双鹤制药有限公司提供。三硅酸镁(化学纯,批号F20071207)购于国药集团化学试剂有限公司。乙腈为色谱纯,磷酸为优级纯,庚烷磺酸钠为色谱纯。
2 色谱条件 2.1 硫酸双肼屈嗪、氢氯噻嗪、维生素B1和维生素B6色谱柱:Phenomenex Gemini C18(250 mm×4.6 mm,5 μm);流动相:0.14%庚烷磺酸钠溶液(用5%磷酸溶液调节pH至3.5)-乙腈(82: 18)为流动相,检测波长为256 nm,柱温40℃,流速1.0 mL·min-1,进样量20 μL。
2.2 利血平和盐酸异丙嗪色谱柱:Phenomenex Gemini C18(250 mm×4.6 mm,5 μm);流动相:0.14%庚烷磺酸钠溶液(用5%磷酸溶液调节pH至3.5)-乙腈(60: 40)为流动相,检测波长为220 nm,柱温40 ℃,流速1.0 mL·min-1,进样量20 μL。
3 溶液的制备 3.1 硫酸双肼屈嗪、氢氯噻嗪、维生素B1和维生素B6供试品溶液:取本品1片,置50 mL量瓶中,加0.1%磷酸溶液适量,超声处理(功率250 W,频率40 kHz)30 min(每5 min振摇1次)使溶解,放冷,用0.1%磷酸溶液稀释至刻度,摇匀,2 000 r·min-1离心10 min后取上清液作为供试品溶液。
对照品溶液:取氢氯噻嗪对照品约31 mg,精密称定,置50 mL量瓶中,加乙腈4 mL,超声(功率50 W,频率40 kHz)使溶解,放冷,用0.1%磷酸溶液稀释刻度,摇匀,即为氢氯噻嗪储备液;再取硫酸双肼屈嗪对照品约21 mg,精密称定,置25 mL量瓶中,用0.1%磷酸溶液超声使溶解并稀释刻度,摇匀,即为硫酸双肼屈嗪储备液;取三硅酸镁约30 mg,精密称定,置50 mL量瓶中,分别精密加入氢氯噻嗪储备液与硫酸双肼屈嗪储备液5 mL,加0.1%磷酸溶液适量,超声处理30 min(每5 min振摇1次),放冷,用0.1%磷酸溶液稀释刻度,摇匀,离心后取上清液作为对照品溶液。
空白辅料溶液:取1片空白片(含除氢氯噻嗪与硫酸双肼屈嗪外的其他成分),置50 mL量瓶中,与供试品溶液同法操作。
3.2 利血平和盐酸异丙嗪供试品溶液:避光操作。取本品1片,置10 mL量瓶中,加乙腈-0.1%磷酸溶液(50: 50)适量,超声振摇20 min使溶解,放冷,用乙腈-0.1%磷酸溶液(50: 50)稀释至刻度,摇匀,滤过,取续滤液作为供试品溶液。
对照品溶液:避光操作。取利血平对照品约11 mg,精密称定,置200 mL量瓶中,加乙腈溶解并稀释至刻度,作为利血平对照品储备液;再取盐酸异丙嗪约11 mg,精密称定,置50 mL量瓶中,加乙腈-0.1%磷酸溶液(50: 50)适量,超声使溶解,放冷,精密加入上述利血平对照品储备液3 mL,并用乙腈-0.1%磷酸溶液(50: 50)稀释至刻度,摇匀,作为对照品溶液。
空白辅料溶液:取1片空白片(含除盐酸异丙嗪与利血平外的其他成分),置10 mL量瓶中,与供试品溶液同法操作。
4 方法与结果 4.1 系统适用性取“3.1”项下的对照品溶液,按“2.1”项下色谱条件试验,理论板数按硫酸双肼屈嗪或氢氯噻嗪计算,均不低于8 000;氢氯噻嗪峰、硫酸双肼屈嗪峰与其他色谱峰的分离度应符合要求;且2个色谱峰的拖尾因子均不得过1.5。
取“3.2”项下的对照品溶液,按“2.2”项下色谱条件试验,理论板数按盐酸异丙嗪计算不低于2 500,盐酸异丙嗪色谱峰与前面相邻峰的分离度不小于1.0,各主峰与其他色谱峰的分离度应符合要求。
4.2 专属性试验分别对复方利血平片进行了光照、高温和高热的破坏实验,实验条件分别为:取复方利血平片开口放在紫外光灯(254 nm和365 nm)下,照射72 h;取复方利血平片开口在60 ℃条件下放置10 d;取复方利血平片开口置相对湿度92.5%的恒湿密闭容器中,放置30 d。取样品分别照“3.1”项下配制供试品溶液,加0.1%磷酸溶液适量,超声处理30 min(每5 min振摇1次),放冷,用0.1%磷酸溶液稀释刻度,摇匀,离心后取上清液进样,同时进行二极管检测器峰纯度分析。
结果经高湿破坏后,硫酸双肼屈嗪降解产物峰增加,与硫酸双肼屈嗪峰的分离度约为2.5,盐酸异丙嗪分解较多,但也能与主成分峰分离;经高温破坏后,降解产物略有增加,各测定成分峰均能与降解产物分离,且其色谱峰纯度符合规定;经光照破坏后,维生素B6降解产物增加,能与主成分峰分离,其他成分的降解产物无明显增加。表明本法专属性能满足检测需要。
4.3 线性关系分别取三硅酸镁30 mg 5份,置50 mL量瓶中,分别精密加入“3.1”项下的氢氯噻嗪储备液与硫酸双肼屈嗪储备液各3、4、5、6和7 mL,加0.1%磷酸溶液稀释至刻度,加0.1%磷酸溶液适量,超声处理30 min(每5 min振摇1次),放冷,用0.1%磷酸溶液稀释刻度,摇匀,离心后取上清液,照“2.1”项下色谱条件试验,记录色谱图,以浓度X(mg·mL-1)为横坐标,峰面积Y为纵坐标,绘制标准曲线,氢氯噻嗪、硫酸双肼屈嗪、维生素B1、维生素B6回归方程分别为
Y=28.00X+0.000 4 r=0.999 9
Y=16.84X-0.131 6 r=0.999 6
Y=368.1X-0.496 9 r=0.999 4
Y=42.02X+0.006 r=0.999 6
氢氯噻嗪、硫酸双肼屈嗪、维生素B1、维生素B6质量浓度分别在0.036 88~0.086 04 mg·mL-1、0.050 95~0.118 9 mg·mL-1、0.011 69~0.027 27 mg·mL-1、0.013 10~0.030 58 mg·mL-1范围内与峰面积线性关系良好。
照“3.2”项下方法,分别制备2.1 mg·mL-1的盐酸异丙嗪储备液和0.031 2 mg·mL-1的利血平储备液。分别精密量取上述2个储备液各2、3、4、5、6和7 mL,置50 mL量瓶中,加乙腈-0.1%磷酸溶液(50: 50)稀释至刻度,照“2.2”项下色谱条件试验,记录色谱图,以浓度X(mg·mL-1)为横坐标,峰面积Y为纵坐标,绘制标准曲线,盐酸异丙嗪和利血平回归方程分别为:
Y=18.67X+ 0.095 1 r=1.000
Y=0.547 8X-0.006 5 r=1.000
盐酸异丙嗪和利血平质量浓度分别在0.082 65~0.289 3 mg·mL-1和1.221~4.273 μg·mL-1范围内与峰面积线性关系良好。
4.4 精密度取各成分对照品溶液连续进样5次,氢氯噻嗪、硫酸双肼屈嗪、维生素B1、维生素B6、盐酸异丙嗪及利血平峰面积的RSD分别为0.08%、1.0%、0.31%、0.28%、0.70%及0.57%。
4.5 定量下限取各对照品储备液,分别稀释,所得稀释液主峰与噪音峰信号强度比不低于10,按氢氯噻嗪计定量下限为1.6 ng,按硫酸双肼屈嗪计定量下限为2.7 ng;按维生素B1计定量下限为7.8 ng,按维生素B6计定量下限为26.2 ng;按盐酸异丙嗪计定量下限为1.7 ng,按利血平计定量下限为0.7 ng。
4.6 回收率试验 4.6.1 硫酸双肼屈嗪、氢氯噻嗪、维生素B1和维生素B6按高、中、低浓度,分别精密称取氢氯噻嗪、硫酸双肼屈嗪、维生素B1及维生素B6原料适量,置200 mL量瓶中,加0.1%磷酸溶液180 mL,振摇,再加4片空白片(含除氢氯噻嗪与硫酸双肼屈嗪外的其他成分),超声30 min,放冷,加0.1%磷酸溶液至刻度,4 000 r·min-1离心10 min,取上清液,照“2.1”项下色谱条件试验,记录色谱图。氢氯噻嗪3个浓度回收率的平均值分别为99.9%、100.2%和99.5%,RSD为0.4%(n=9);硫酸双肼屈嗪3个浓度回收率的平均值分别为99.2%、101.6%和101.2%,RSD为1.4%(n=9);维生素B1 3个浓度回收率的平均值分别为100.3%、100.7%和100.5%,RSD为0.3%(n=9);维生素B6 3个浓度回收率的平均值分别为100.5%、101.5%和101.7%,RSD为1.5%(n=9)。
4.6.2 利血平和盐酸异丙嗪取利血平原料约15.6 mg,精密称定,置500 mL量瓶中,用乙腈配制储备液。按高、中、低浓度,精密称取盐酸异丙嗪适量,并加入适量利血平储备液,置50 mL量瓶中,再加5片空白片(含除盐酸异丙嗪与利血平外的其他成分),加乙腈-0.1%磷酸溶液(50: 50)40 mL,超声20 min,放冷,加乙腈-0.1%磷酸溶液(50: 50)至刻度,滤过,取续滤液,照“2.2”项下色谱条件试验,记录色谱图。盐酸异丙嗪3个浓度回收率的平均值分别为100.2%、100.6%和100.9%,RSD为0.5%(n=9);利血平3个浓度回收率的平均值分别为99.7%、99.6%和100.5%,RSD为0.7%(n=9)。
4.7 稳定性试验 4.7.1 硫酸双肼屈嗪、氢氯噻嗪、维生素B1和维生素B6取氢氯噻嗪、硫酸双肼屈嗪、维生素B1和维生素B6供试品溶液及对照品溶液,在0~8 h内进样,结果供试品溶液中氢氯噻嗪、硫酸双肼屈嗪、维生素B1、维生素B6峰峰面积的RSD分别为0.2%、1.4%、0.4%、1.4%;对照品溶液中氢氯噻嗪、硫酸双肼屈嗪、维生素B1、维生素B6峰峰面积的RSD分别为0.1%、1.0%、0.3%、1.2%。表明氢氯噻嗪、硫酸双肼屈嗪、维生素B1和维生素B6供试品溶液与对照品溶液至少在8 h内稳定。
4.7.2 利血平和盐酸异丙嗪取盐酸异丙嗪和利血平供试品溶液及对照品溶液避光保存,在0~8 h内进样,结果供试品溶液中盐酸异丙嗪峰、利血平峰峰面积的RSD分别为0.1%和0.04%;对照品溶液中盐酸异丙嗪峰峰和利血平峰峰面积的RSD均为0.1%。表明在避光条件下,盐酸异丙嗪和利血平供试品溶液与对照品溶液至少在8 h内稳定。
4.8 耐用性考察按照“2.1”项下色谱条件,考察了4个品牌的色谱柱,结果除Phenomenex Geminis色谱柱外,其他色谱柱均不能将维生素B6峰与氢氯噻嗪峰分离。分别在同品牌的2根色谱柱上实验,结果3根色谱柱均可使4个成分有较好分离,所以色谱柱推荐使用Phenomenex公司Gemini(5 μm,4.6 mm×250 mm,110A)色谱柱,或使用相当的色谱柱。
按照“2.2”项下色谱条件试验,试用了2个品牌的色谱柱(详见表 1的2~3),并在不同仪器上实验,结果盐酸异丙嗪峰与前面峰的分离度基本一致,保留时间均可接受,表明方法对于色谱柱与仪器有较强的耐用性。
4.9 样品测定取3批样品,分别测定6个成分的含量均匀度,取各成分含量均匀度平均值为含量结果,见表 2。含量均匀度色谱图见图 1~2。
|
|
表 2 6个成分的含量均匀度测定结果 Table 2 The results of content uniformity for the six components |
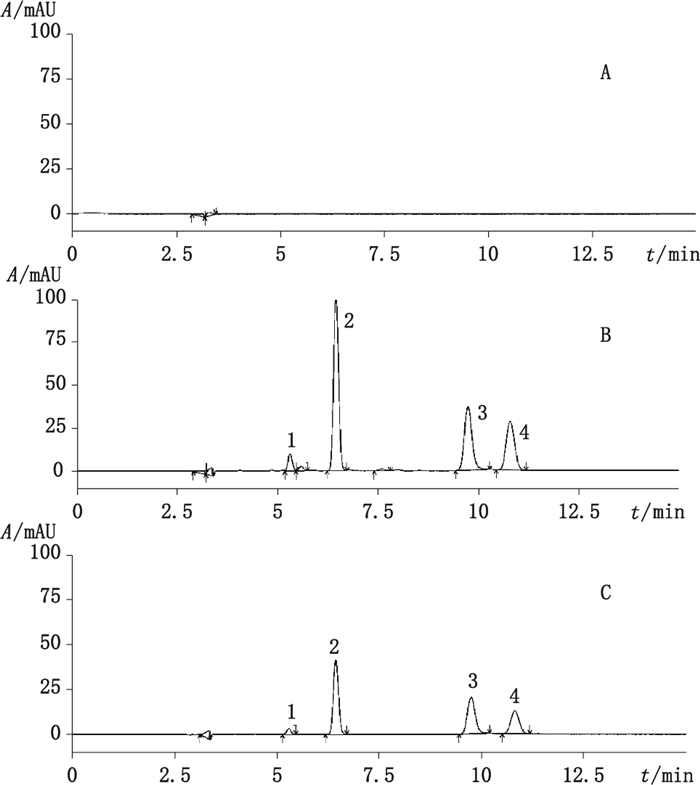
|
1.维生素B6(vitamin B6)2.氢氯噻嗪(hydrochlorothiazide)3.硫酸双肼屈嗪(dihydralazine sulfate)4.维生素B1(vitaminB1) A.阴性溶液(negative solution)B.供试品溶液(sample solution)C.对照品溶液(reference substance solution) 图 1 硫酸双肼屈嗪、氢氯噻嗪、维生素B1和维生素B6鉴别、含量均匀度色谱图 Figure 1 HPLC chromatograms of identification and the content uniformity for hydrochlorothiazide, dihydralazine sulfate, vitamin B1, vitamin B6 |
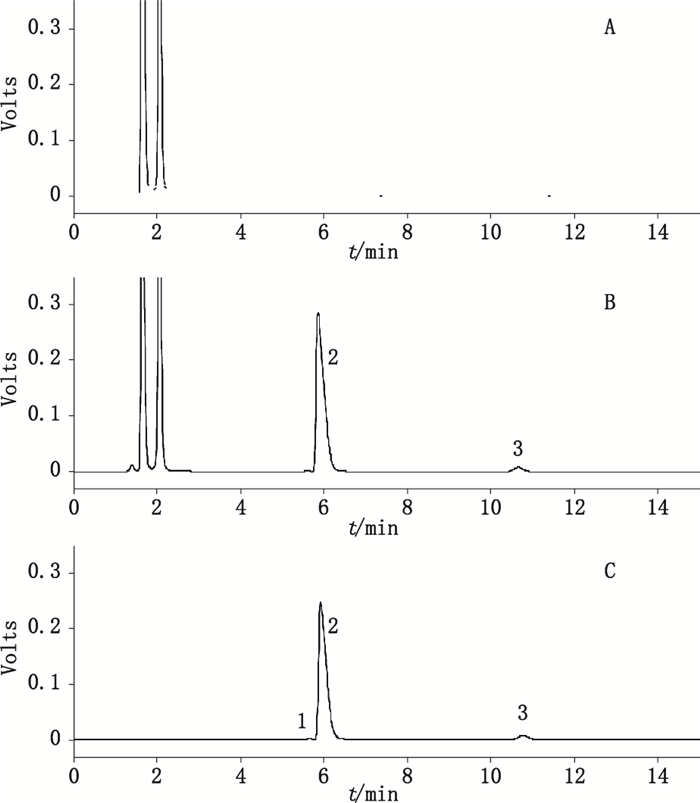
|
1.盐酸异丙嗪杂质(impurity of promethazine hyrochloride)2.盐酸异丙嗪(promethazine hydrochloride)3.利血平(reserpine) A.阴性溶液(negative solution)B.供试品溶液(sample solution)C.对照品溶液(reference solution) 图 2 异丙嗪与利血平鉴别、含量均匀度色谱图 Figure 2 HPLC chromatograms of identification and the content uniformity for promethazine hydrochloride and reserpine |
参考文献[11-13],筛选了6种不同流动相,考察了水相庚烷磺酸钠浓度、磷酸氢铵浓度、pH及流动相比例,并经过多次微调,最终确定氢氯噻嗪、硫酸双肼屈嗪、维生素B1和维生素B6含量均匀度测定方法流动相。并基于上述流动相的水相与有机相,经试验确定利血平和盐酸异丙嗪含量均匀度测定方法流动相。
5.2 检测波长选择氢氯噻嗪在226 nm与271 nm处有最大吸收,在242 nm处有最小吸收;硫酸双肼屈嗪除在220 nm有最大吸收外,在250 nm附近也有较强吸收。考虑到220 nm或226 nm靠近系外末端,而在256 nm处2个化合物吸收值基本相当,且维生素B1和维生素B6的吸收值也能满足测定要求,所以选择检测波长为256 nm。
盐酸异丙嗪在300 nm与250 nm处有最大吸收,在218 nm处有最小吸收;利血平在266 nm与216 nm有最大吸收,在244 nm处有最小吸收。考虑到本品中盐酸异丙嗪的含量远远大于利血平,为了提高利血平检测灵敏度,选择检测波长220 nm。
5.3 色谱柱温度因流动相中含有离子对试剂庚烷磺酸钠,为了便于流动相的平衡,色谱柱温度定为40 ℃。
5.4 溶剂的选择溶剂的选择贯穿了整个研究过程,最终主要依据测定组分的溶解性、供试品溶液与对照品溶液的稳定性,选择相应的溶剂。
5.5 供试品溶液配制方法因本品在选择的2种溶剂中均较易崩解,因此未采用研磨转移方法。因氢氯噻嗪与利血平在选择的2种溶剂中溶解度略差,为了保证其全部溶解,经实验确定采用超声振摇方法助溶。配制的氢氯噻嗪与硫酸双肼屈嗪供试品溶液经滤膜过滤后,峰面积分别比离心操作减少约3.3%与2.8%,所以采取离心操作。又因利血平和盐酸异丙嗪对光均不稳定,所以盐酸异丙嗪与利血平含量均匀度检查采用避光操作。
5.6 盐酸异丙嗪测定方法在“2.2”项色谱条件下,供试品溶液与对照品溶液色谱图中,盐酸异丙嗪峰前均有一杂质峰,两者分离度小于1.5,且随流动相中乙腈比例的减少,其分离度改善不大,推测该杂质的结构与盐酸异丙嗪可能极为相似。此杂质峰在盐酸异丙嗪色谱峰前面出峰,其峰面积仅为盐酸异丙嗪峰面积的0.5%~0.8%,在强力破坏条件下盐酸异丙嗪色谱峰的纯度因子均能满足测定要求,因此确定系统适用性实验要求。
5.7 硫酸双肼屈嗪测定方法测定硫酸双肼屈嗪时,回收率较低,经实验发现与本品中含有三硅酸镁有关。虽尝试更换溶剂,改变具体操作方法,但未能改变三硅酸镁对硫酸双肼屈嗪的影响。因有文献报道三硅酸镁对药物有吸附作用[14-15],结合实验结果,认为三硅酸镁可能对硫酸双肼屈嗪产生吸附,故为避免三硅酸镁干扰,参考复杂制剂含量测定方法,采用对照品溶液中加入三硅酸镁的方法。在配制储备液时为保证氢氯噻嗪对照品的溶解加入了乙腈2 mL,同时为避免乙腈对硫酸双肼屈嗪稳定性的影响,硫酸双肼屈嗪储备液与氢氯噻嗪储备液需分别配制。
| [1] |
中华人民共和国药典2015年版.二部[S].2015: 803 ChP 2015.Vol Ⅱ[S].2015: 803 |
| [2] |
王缨, 王唯红, 聂磊. 复方利血平片6个组分含量的偏最小二乘法测定[J]. 中国医药工业杂志, 2009, 40(10): 776. WANG Y, WANG WH, NIE L. Determination of six components in compound reserpine tablets by partial least square method[J]. Chin J Pharm, 2009, 40(10): 776. |
| [3] |
张莉, 田洪斌. HPLC法测定复方利血平片中利血平的含量[J]. 中国药事, 2008, 22(11): 997. ZHANG L, TIAN HB. Determination of reserpine in compound reserpine tablets by HPLC[J]. China Pharm Aff, 2008, 22(11): 997. |
| [4] |
王昕, 赵吉. HPLC法测定复方降压片中利血平及盐酸异丙嗪的含量[J]. 中国药品标准, 2005, 6(2): 13. WANG X, ZHAO Z. Determination of reserpine and promethazine hydrochloride in compound antihypertensive tables by HPLC[J]. Drug Stand China, 2005, 6(2): 13. DOI:10.3969/j.issn.1009-3656.2005.02.006 |
| [5] |
程正, 万庆, 管玉云, 等. HPLC法测定复方利血平片中氢氯噻嗪盐酸异丙嗪和利血平的含量[J]. 安徽医药, 2010, 14(1): 38. CHENG Z, WAN Q, GUAN YY, et al. Determination of hydrochlorothiazide promethazine hydrochloride and reserpine in compound reserpine tablets by HPLC[J]. Anhui Med Pharm J, 2010, 14(1): 38. DOI:10.3969/j.issn.1009-6469.2010.01.015 |
| [6] |
李运莉, 吴俊芳, 朱立伟, 等. 复方利血平片质量标准的研究[J]. 中国药品标准, 2006, 7(2): 58. LI YL, WU JF, ZHU LW, et al. Study on quality Standards for compound reserpine tablets[J]. Drug Stand China, 2006, 7(2): 58. DOI:10.3969/j.issn.1009-3656.2006.02.026 |
| [7] |
刘道杰, 王霞. 反相高效液相色谱同时测定复方降压药中三组分[J]. 分析实验室, 2002, 21(6): 87. LIU DJ, WANG X. Simultaneous determination of three components in hypotensive compound tablets by reversed phase high performance liquid chromatography[J]. Chin J Anal Lab, 2002, 21(6): 87. |
| [8] |
潘静岚. PLC法同时测定复方利血平氨苯蝶啶片中3组分的含量[J]. 广东药学院学报, 2008, 24(3): 238. PAN JL. Simultaneous determination of hydrochlorothiazide, dihydralazine sulfate and triamterene in compound hypoensive tablets by HPLC[J]. J Guangdong Coll Pharm, 2008, 24(3): 238. |
| [9] |
邱颖恒, 周敏贤, 李玉兰, 等. 反相高效液相色谱法测定盐酸肼屈嗪片的含量[J]. 中国药师, 2008, 11(11): 1305. QIU YH, ZHOU MX, LI YL, et al. Determination of hydralazine hydrochloride tablets by HPLC[J]. China Pharm Aff, 2008, 11(11): 1305. DOI:10.3969/j.issn.1008-049X.2008.11.017 |
| [10] |
SNYDER LR, GLAJCH JL, KIRKLAND JJ, 等.实用高效液相色谱的建立[M].王杰, 赵岚峰, 王树力, 等译.第2版.北京: 科学出版社, 2001: 370 SNYDER LR, GLAJCH JL, KIRKLAND JJ, et al.Practical HPLC Method Development[M].WANG J, ZHAO LF, WANG SL, et al(translation).2nd.Beijing: Science Press, 2001: 370 |
| [11] |
车宝泉. HPLC法测定复方降压片中5个成分的含量[J]. 药学学报, 2004, 39(8): 618. CHE BQ. Determination of five components in compound hypotensive tablets by HPLC[J]. Acta Pharm Sin, 2004, 39(8): 618. DOI:10.3321/j.issn:0513-4870.2004.08.010 |
| [12] |
陈鼎雄. HPLC法测定复方降压胶囊中氢氯噻嗪、地巴唑、氯氮和盐酸异丙嗪的含量[J]. 药物分析杂志, 2005, 25(4): 442. CHEN DX. HPLC determination of hydrochlorothiazide, dibazol, chlordiazepoxide and promethazine hydrochloride in compound diabazol capsules[J]. Chin J Pharm Anal, 2005, 25(4): 442. |
| [13] |
陆兴毅, 周泽良. HPLC法测定复方罗布麻片Ⅰ中氢氯噻嗪和硫酸双肼屈嗪的含量[J]. 中国药师, 2009, 12(4): 597. LU XY, ZHOU ZL. Detemination of hydrochlorothiazide and dihydralazine sulfuate in compound kendir leaves tabletsⅠby HPLC[J]. China Pharm, 2009, 12(4): 597. |
| [14] |
林如, 杨丽, 张汝华. 三硅酸镁、铝镁原粉对抗过敏药物-扑尔敏吸附作用的研究[J]. 齐齐哈尔轻工学院学报, 1988, 14(4): 44. LIN R, YANG L, ZHANG RH. The research of the adsorption of magnesium trisilicate and mixture of alumina magnesia and silica powder for chlophenamin[J]. J Qiqihaer Inst Light Ind, 1988, 14(4): 44. |
| [15] |
郑樑元, 平齐能, 刘国杰, 等. 辅料对四环素吸收影响的研究[J]. 南京药学院学报, 1982, 9(2): 51. ZHENG LY, PING QN, LIU GJ, et al. The Research of the influence of excipients for the tetracycline absorption[J]. J Nanjing Coll Pharm, 1982, 9(2): 51. |
 2018, Vol. 38
2018, Vol. 38 