2. 安徽省食品药品检验研究院, 合肥 230051
2. Anhui Institute for Food and Drug Control, Hefei 230051, China
复方罗布麻片Ⅰ是由罗布麻叶、野菊花、防己、氢氯噻嗪、硫酸双肼屈嗪以及盐酸异丙嗪等[1]11味中西药组成的复方制剂,药效协同[2-3],成分复杂[4],常用于治疗高血压,临床应用多年,疗效明显。现行标准为《国家药品标准》化学药品地方标准上升国家标准第十一册,现行标准只收载了氢氯噻嗪[5-8]的含量测定和盐酸异丙嗪的薄层鉴别。氢氯噻嗪作为高效的降压药[9],是作用于远曲小管的利尿剂[10],通过排钠利尿,造成体内Na+和水的负平衡,使细胞外液和血容量减少而降压。为了提高其降压效果,有些复合剂型中会加入一些低效的抗高血压药,如硫酸双肼屈嗪,从而提高疗效,因此复方罗布麻片Ⅰ的质量标准提高迫在眉睫。通过大量的实验摸索,并结合正交验证实验,用Spss 17.0软件对数据进行分析,从而得出最佳色谱系统,便于控制该药的质量标准,也为控制复方罗布麻片Ⅰ的内在质量研究提供了科学依据。
1 仪器与试药岛津LC-20AD高效液相色谱仪,LC-20AD紫外可见光度检测器,Kromasil C18色谱柱(250 mm×4.6 mm,5 μm);Elmasonic P超声仪;XS-105十万分之一电子分析天平(梅特勒-托利多仪器);BINDER电热干燥箱(BINDER)。
对照品泛酸钙(批号:100370-201402,纯度为97.5%)、氢氯噻嗪(批号:100309-201103,纯度为99.8%)、维生素B6(批号:100116-201103)、维生素B1(批号:100390-200502)、硫酸双肼屈嗪(批号:100514-201102,纯度为85.5%)和盐酸异丙嗪(批号:100422-201002,纯度为99.4%)均来自中国食品药品检定研究院,供含量测定用,复方罗布麻片Ⅰ由东芝堂药业(安徽)有限公司提供,批号分别为151001、151002和151003。乙腈、甲醇均为色谱纯,辛烷磺酸钠为离子对色谱用试剂,水为超纯水;其他试剂均为分析纯。
2 方法 2.1 色谱条件Kromasil C18柱(250 mm×4.6 mm,5 μm);流动相A为0.10%辛烷磺酸钠+0.40%磷酸二氢钾(磷酸调pH至3.0)-乙腈(96: 4),流动相B为乙腈,梯度洗脱(0~12 min,99%A;12~15 min,99%A→96%A;15~30 min,96%A;30~33 min,96%A→90%A;33~105 min,90%A;105~108 min,90%A→65%A;108~130 min,65%A;130~135 min,65%A→99%A;135~155 min,99%A);柱温:30 ℃;检测波长:泛酸钙200 nm,氢氯噻嗪、维生素B6、硫酸双肼屈嗪、维生素B1及盐酸异丙嗪均为271 nm;流速:1.0 mL·min-1;进样体积:40 μL。
2.2 溶液的制备 2.2.1 对照品储备液分别精密称取泛酸钙、氢氯噻嗪、维生素B6、维生素B1、硫酸双肼屈嗪和盐酸异丙嗪的对照品适量,加0.8%磷酸-乙腈(80: 20)混合溶液使溶解并稀释制成每1 mL含0.133 5、0.782 7、0.254 6、0.252 2、0.822 9、0.526 4 mg的混合溶液,作为对照品储备液。
2.2.2 对照品溶液精密量取“2.2.1”项下的对照品储备液5 mL,置100 mL量瓶中,加0.8%磷酸-乙腈(80: 20)混合溶液50 mL,用流动相A稀释至刻度,摇匀,即得对照品溶液。
2.2.3 供试品溶液取本品20片,精密称定,精密称取适量(约相当于氢氯噻嗪4.0 mg)置100 mL量瓶中,加0.8%磷酸-乙腈(80: 20)混合溶液50 mL,超声(功率1 kW,频率60 Hz)20 min使溶解,放至室温,用流动相A稀释至刻度,摇匀,即得供试品溶液。
2.2.4 阴性对照溶液按处方比例制备不含泛酸钙、氢氯噻嗪、维生素B6、维生素B1、硫酸双肼屈嗪及盐酸异丙嗪的溶液,按“2.2.3”项下方法处理,作为阴性对照溶液。
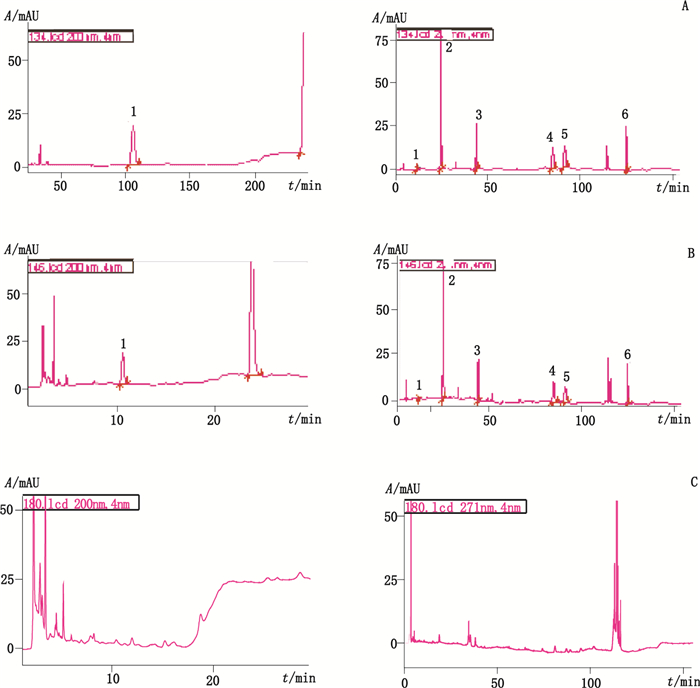
2.3 专属性试验分别取混合对照品溶液、供试品溶液和阴性对照溶液,按“2.1”项下色谱条件,分别进样40 μL,在色谱图中,混合对照品及供试品出峰位置,阴性对照溶液无干扰,色谱图如图 1。
|
1.泛酸钙(calcium pantothenate)2.氢氯噻嗪(hydrochlorothiazide)3.维生素B6(pyridoxine hydrochloride)4.维生素B1(thiamine hydrochloride)5.硫酸双肼屈嗪(sulfhydrazine sulfate)6.盐酸异丙嗪(promethazine hydrochloride) 图 1 混合对照品(A)、供试品(B)及阴性供试品(C)HPLC色谱图 Figure 1 HPLC chromatograms of mixed reference substances(A), samples(B)and negative samples(C) |
精密吸取“2.2.1”项下的对照品储备液各1、3、5、7、10 mL,分别置于100 mL量瓶中,加0.8%磷酸-乙腈(80: 20)混合溶液约50 mL,摇匀,分别用流动相A稀释至刻度,即得系列线性溶液,按“2.1”项下色谱条件,以对照品的峰面积Y为纵坐标、质量浓度X(μg·mL-1)为横坐标,进行线性回归,线性方程、r值和线性范围见表 1。以信噪比(S/N)为3: 1和10: 1为基准测得各成分的检测下限和定量下限,结果见表 1。
|
|
表 1 各被测成分的标准曲线方程、相关系数、线性范围和检测下限及定量下限(n=6) Table 1 Regressive equations, correlation coefficients, linear ranges of the investigated components and LOQ, LOD |
吸取“2.2.2”项下的对照品溶液40 μL,按照“2.1”项下色谱条件,连续进样6次,测定峰面积并计算RSD,结果泛酸钙、氢氯噻嗪、维生素B6、维生素B1、硫酸双肼屈嗪和盐酸异丙嗪峰面积的RSD(n=6)分别为0.27%、0.09%、0.11%、0.47%、1.0%和0.13%,表明仪器精密度良好。
2.6 稳定性试验取“2.2.3”项下同一供试品溶液,分别在0、3、6、9、12、18 h按“2.1”项下的色谱条件进样测定,记录峰面积。结果泛酸钙、氢氯噻嗪、维生素B6、维生素B1、硫酸双肼屈嗪和盐酸异丙嗪峰面积的RSD(n=6)分别为1.2%、0.09%、1.2%、1.5%、1.6%和0.43%,表明供试品溶液在18 h内稳定性良好。
2.7 重复性试验取同一批供试品(批号151003),按照“2.2.3”项下平行制备6份供试品溶液,按“2.1”项下的色谱条件进样测定,记录峰面积。结果泛酸钙、氢氯噻嗪、维生素B6、维生素B1、硫酸双肼屈嗪和盐酸异丙嗪含量百分比(n=6)分别为97.57%、101.18%、97.71%、100.86%、48.61%和89.19%,RSD分别为1.5%、0.54%、0.60%、1.2%、1.7%和0.57%,表明该方法重复性良好。
2.8 加样回收率试验精密称取已知含量的同一批样品,约相当于2.5片的量,置200 mL量瓶中,共9份,平均分为3组,分别精密加入对照品储备液4、5和6 mL,按“2.2.3”项下方法制备供试品溶液,按“2.1”项下的色谱条件测定,结果见表 2。
|
|
表 2 加样回收率实验结果(n=6) Table 2 Recoveries of six compounds |
分别取不同厂家的样品,按“2.2.3”项下方法制备供试品溶液,再按“2.1”项下的色谱条件进样测定,记录峰面积,计算样品含量,结果见表 3。
|
|
表 3 复方罗布麻片Ⅰ中6个成分的标示量含量(%) Table 3 Contents of six components in kendir leaves tablets Ⅰ to labelled amount |
本次研究显示流动相pH偏酸性,各化学成分具有较好的稳定性和峰形。考虑不同色谱柱的填料在分离效果上存在一定差异,选择3种不同品牌的色谱柱进行比较,型号均为250 mm×4.6 mm,5 μm,见表 4。本文运用Spss 17.0软件对实验结果进行方差分析[11],得到表 5,以分离度为优化指标。由表 5可知,因子A栏P=0.004,在显著水平α=0.05上有统计学意义;因子B栏P=0.030,在显著水平α=0.05上有统计学意义。也就是说因子A和因子B在显著水平α=0.05上显著。由表 6可见,A2B1为最佳条件,即pH为3.0,色谱柱为Kromasil C18。
|
|
表 4 正交实验的因素及水平 Table 4 Factors and levels of orthogonal test |
|
|
表 5 主体间效应的检验 Table 5 The test of inter-subjective effects |
|
|
表 6 A×B正交表 Table 6 A×B orthogonal |
参照2015年版《中华人民共和国药典》及相关文献[12-13],待测组分中除氢氯噻嗪和硫酸双肼屈嗪外,其余组分均在水中易溶。由于硫酸双肼屈嗪在酸性水溶液中溶解度较好且较稳定,实验分别考察了硫酸双肼屈嗪在0.6%、0.8%和1.0%的冰醋酸溶液以及0.6%、0.8%和1.0%的磷酸溶液中溶解及稳定性,结果显示0.8%的磷酸溶液最佳。由于氢氯噻嗪在乙腈中溶解度较好[14],笔者以0.8%磷酸溶液-乙腈不同比例约50 mL混合溶液(比例范围5: 45~45: 5)分别作为溶剂,考察拟定样品称样量中相关组分溶解情况,并用流动相A稀释至100 mL,在同一色谱条件进样测定,结果0.8%磷酸溶液-乙腈(40: 10)的混合溶液能确保样品溶解完全且溶液稳定。
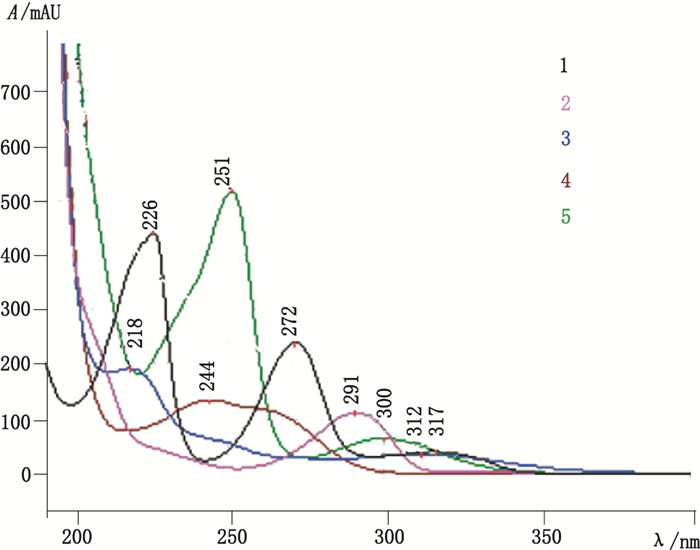
3.3 波长的选择泛酸钙在230 nm以上无紫外发色基团,通过测定泛酸钙的紫外吸收光谱,发现其最大吸收在195 nm。文献报道泛酸钙的检测波长多在210 nm[15],由于样品中泛酸钙含量低,在210 nm测定的峰面积较小,虽然满足定量限要求(约为定量限20倍),但200 nm处测定峰面积较200 nm测定值提高约4倍,略低于195 nm的测定值,能有效减少积分误差以及避免流动相和样品其他组分对泛酸钙测定的干扰,因此最终选择200 nm作为泛酸钙的测定波长。由于该药为典型的中西药复方制剂,中药成分对相关组分的液相测定仍有较大干扰,同时待测组分在不同波长处的紫外吸收也有差异,因此按处方比例配制混合对照品溶液,通过DAD检测得到相关组分光谱图(如图 2)。由光谱图可知,交点在270 nm左右有交点,而《中华人民共和国药典》2015版二部收载的氢氯噻嗪含量测定波长为271 nm,考虑含测的均衡性,尽可能保证待测组分在测定波长下均有较大吸收,同时避免低波长处中药成分对测定的干扰,最终确定为271 nm作为测定波长较为合理。因此,泛酸钙在200 nm处测定,氢氯噻嗪、维生素B6、维生素B1、硫酸双肼屈嗪及盐酸异丙嗪在271 nm处测定。
|
1.氢氯噻嗪(hydrochlorothiazide)2.维生素B6(pyridoxine hydrochloride)3.硫酸双肼屈嗪(dihydralazine sulfateand)4.维生素B1(thiamine hydrochloride)5.盐酸异丙嗪(promethazine hydrochloride) 图 2 各组分光谱图 Figure 2 The spectrum of different component |
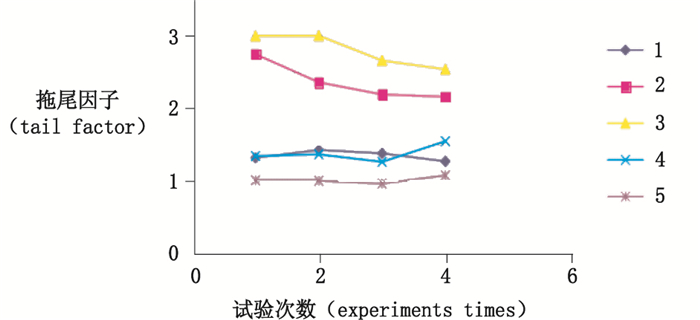
该复方制剂中的6个化学成分(泛酸钙、氢氯噻嗪、维生素B6、维生素B1、硫酸双肼屈嗪及盐酸异丙嗪)极性相近,单一的离子对试剂或磷酸盐流动相,难以达到系统适用性的要求,硫酸双肼屈嗪及盐酸异丙嗪峰形较差,拖尾严重,通过添加不同浓度的三乙胺能有一定改善。同时考虑在流动相中加入适量的磷酸盐以提高离子对试剂的缓冲能力,改善硫酸双肼屈嗪及盐酸异丙嗪的峰形。以硫酸双肼屈嗪为例,其拖尾因子与流动相种类关系如图 3。
|
1. 0.1%辛烷磺酸钠加1.0%三乙胺(0.10% octane sulfonic acid sodium with 1.0% triethylamine) 2. 0.1%辛烷磺酸钠加0.1%三乙胺(0.10% octane sulfonic acid sodium with 0.1% triethylamine) 3. 0.1%辛烷磺酸钠加0.5%三乙胺(0.10% octane sulfonic acid sodium with 0.5% triethylamine) 4. 0.1%辛烷磺酸钠无三乙胺(0.10% octane sulfonic acid sodium without triethylamine) 5. 0.1%辛烷磺酸钠加0.4%磷酸二氢钾(0.10% octane sulfonic acid sodium with 0.4% potassium dihydrogen phosphate) 图 3 流动相选择优化图 Figure 3 Optimize mobile phase selection |
复方罗布麻片Ⅰ现行标准含量测定项只对处方中氢氯噻嗪做了控制,影响复方制剂质量评价的合理性,本文建立了HPLC双波长法同时测定复方罗布麻片Ⅰ中6个成分组分,相对于其他文献,该复方制剂中化药成分的含量测定方法简便易行,可操作性强,重现性好。经研究表明,硫酸双肼屈嗪在酸性溶液中稳定性较好,且现行标准中未对其进行含量控制。实验中发现复方制剂中的硫酸双肼屈嗪含量较低,未能符合处方投料的配比,为后期该复方制剂的工艺优化及质量标准的建立和完善提供科学依据。
| [1] |
陆兴毅, 周泽良. HPLC法测定复方罗布麻片Ⅰ中氢氯噻嗪和硫酸双肼屈嗪的含量[J]. 中国药师, 2009, 12(5): 597. LU XY, ZHOU ZL. HPLC determination of hydrochlorothiazide and dihydralazine sulfate in compound kendir leaves tabletsⅠby HPLC[J]. China Pharm, 2009, 12(5): 597. DOI:10.3969/j.issn.1008-049X.2009.05.021 |
| [2] |
ANDRIEUX P, PATRIC F, KILINC T, et al. Pantothenic acid(vitamin b5)in fortified foods:comparison of a novel ultra-performance liquid chromatography-tandem mass spectrometry method and a microbiological assay(AOAC Official Method 992.07)[J]. Aoac Intl, 2012, 95(1): 143. DOI:10.5740/jaoacint.10-333 |
| [3] |
许会, 汤卫国, 黄春玉, 等. HPLC法测定复方氨氯地平缬沙坦氢氯噻嗪片剂溶出度[J]. 药物分析杂志, 2015, 35(1): 46. XU H, TANG WG, HUANG CY, et al. HPLC determination of the dissolution of compound amlodipine, valsartan and hydrochlorothiazide tablets[J]. Chin J Pharm Anal, 2015, 35(1): 46. |
| [4] |
刘海清. HPLC测定复方罗布麻片中罗布麻甲素的含量[J]. 中成药, 2004, 26(5): 91. LIU HQ. HPLC determination of isoquercitrin in compound kendir leaves tablets[J]. Chin Tradit Pat Med, 2004, 26(5): 91. |
| [5] |
王建平, 汪明志. HPLC测定珍菊降压片中氢氯噻嗪不确定度分析[J]. 中国执业药师, 2016, 13(8): 27. WANG JP, WANG MZ. Uncertainty for determination of hydrochlorothiazide in Zhenju Jiangya tablets by HPLC[J]. Chin Licens Pharm, 2016, 13(8): 27. DOI:10.3969/j.issn.1672-5433.2016.08.006 |
| [6] |
HISHAM H. High performance liquid chromatography for simultaneous determination of xipamide, triamterene and hydrochlorothiazide in bilk drug samples and dosage forms[J]. Acta Pharm, 2016, 66(10): 109. |
| [7] |
卢晓梅. HPLC法同时测定复方罗布麻片Ⅰ中氢氯噻嗪和盐酸异丙嗪的含量及含量均匀度[J]. 中国药师, 2014, 17(11): 1891. LU XM. Simultaneous determination of contents and content uniformity of hydrochlorohiazide and promethazine hydrochloride in compound kendir leaves tablets Ⅰ by HPLC[J]. China Pharm, 2014, 17(11): 1891. DOI:10.3969/j.issn.1008-049X.2014.11.032 |
| [8] |
李清艳, 乔湜, 刘国如, 等. 复方罗布麻片Ⅰ中7种成分的UPLC-MS/MS分段离子切换法测定[J]. 中国医药工业杂志, 2016, 47(11): 1450. LI QY, QIAO T, LIU GR, et al. Determination of seven components in Fufang LuobumaⅠtablets by UPLC-MS/MS combined with ion switching technology[J]. Chin J Pharm, 2016, 47(11): 1450. |
| [9] |
BHOIR SI. RP-HPLC method for simultaneous estimation of bisoprolol fumarate and hydrochlorothiazide in tablet formulation[J]. J Pharm Biomed Anal, 2010, 52. |
| [10] |
ZORICA V, NEDZAD M. Simultaneous analysis of irbesartan and hydrochlorothiazide:an improved HPLC method with the aid of a chemometric protocol[J]. Molecules, 2012, 17(10): 3461. |
| [11] |
耿银银, 许丽晓. 亲水作用色谱法测定阿卡波糖含量[J]. 药物分析杂志, 2017, 37(5): 818. GENG YY, XU LX. Determination of acarbose content by hydrophilic interaction liquid chromatography[J]. Chin J Pharm Anal, 2017, 37(5): 818. |
| [12] |
杨小林, 邱栋樑. HPLC梯度洗脱法测定硝苯地平氢氯噻嗪片中两组分的含量[J]. 海峡药学, 2015, 27(8): 57. YANG XL, QIU DL. Determination of two components in nifedipine hydrochlorothiazide tablets by HPLC gradient elution method[J]. Strait Pharm J, 2015, 27(8): 57. DOI:10.3969/j.issn.1006-3765.2015.08.022 |
| [13] |
钱忠义. HPLC法测定复方罗布麻片Ⅰ中3组分的含量[J]. 中国药师, 2009, 12(9): 1265. QIAN ZY. Detrmination of the contents of three components in compound kendir leaf tabletsⅠby HPLC[J]. Chin Pharm, 2009, 12(9): 1265. DOI:10.3969/j.issn.1008-049X.2009.09.042 |
| [14] |
翁水旺. RP-HPLC法测定复方三维右旋泛酸钙糖浆中维生素B1和维生素B6的含量[J]. 药物分析杂质, 2004, 24(6): 645. WENG SW. RP-HPLC determination of pyridoxine hydrochloride and thiamine hydrochloride in compound trivitamin and calcium pantothenate syrup[J]. Chin J Pharm Anal, 2004, 24(6): 645. |
| [15] |
祝莉莎, 刘君康, 吴鹏宇, 等. HPLC法同时测定复方利血平片中硫酸双肼屈嗪等5种成分[J]. 现代科学仪器, 2013(4): 193. ZHU LS, LIU JK, WU PY, et al. Simultaneous determination of dithydralazine sulfate in five components such as resetpine tablets by HPLC[J]. Mod Sci Instrum, 2013(4): 193. |
 2018, Vol. 38
2018, Vol. 38 
