银屑病是一种常见的易于复发的慢性炎症性皮肤病,特征性损害为红色丘疹或斑块上覆有多层银白色鳞屑[1-2]。该类病以关节炎、肌腱端炎、脊柱炎和银屑病皮疹为主要表现的疾病,临床表现和疾病进程多样化[3-5]。传统治疗银屑病的药物包括甲氨蝶呤、环孢素、维甲酸类药物等,这些药物各有不同程度的疗效,但不良反应也多[6-7]。此外,患有重度银屑病的患者多数有各种并发症,如非酒精性脂肪肝、缺血性心脏病等[8],这也一定程度上限制了治疗药物的选择范围。
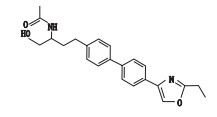
中国医学科学院药物研究所经多年研究,找到了全新结构的高选择性S1P1受体激动剂艾托莫德(SYL927)[9-10],化学结构及名称见表 1。SYL927体外药理实验表现出对S1P1受体显著的激动活性和选择性;在体内,该药物通过诱导外周循环淋巴细胞归巢作用,能够在不降低心率的同时有效降低大鼠外周血淋巴细胞水平,在自身免疫性疾病银屑病模型中发挥良好的治疗作用[11-13]。此外,与其他S1P受体激动剂相比,SYL927选择性激动S1P1受体,而对心肌细胞上分布较广的S1P3受体亚型作用微弱,对心脏副作用小;且其半衰期短,对淋巴细胞的转运展现出更为有效和快速可逆的抑制作用[14]。SYL927具有良好的药理活性和较低的毒副作用,代谢特性良好[15],作为用于治疗银屑病的1类新药,正在进行Ⅰ期临床研究。
|
|
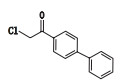
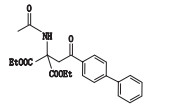
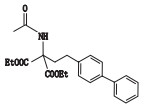
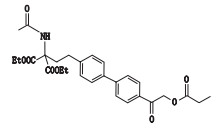
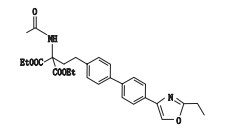
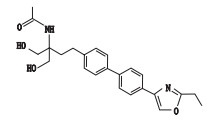
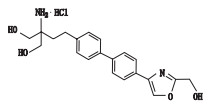
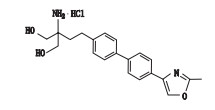
表 1 SYL927及有关物质的结构 Table 1 Structures of SYL927 and related substances |
为控制SYL927原料药在合成过程中可能存在的中间体、副产物等有关物质,本文建立了采用高效液相色谱法检测SYL927的有关物质的方法,对原料药合成工艺中的6种中间体(927-1、927-2、927-3、927-5、927-6、927-7,结构及名称见表 1)和3种副产物(Imp-A、Imp-C、Imp-F,结构及名称见表 1)进行了研究,通过专属性、破坏性、耐用性等试验及方法学验证,从而为监测原料药有关物质,保证药物的质量提供可靠的方法。
1 仪器与试药 1.1 仪器岛津高效液相色谱仪(岛津LC-20AT泵、SPD-M20A检测器、LC solution工作站),XP205十万分之一电子天平(METTLER公司)。
1.2 试药乙腈、甲醇均为HPLC级,百灵威公司;水为市售娃哈哈纯净水;三水合乙酸钠,分析纯,国药集团化学试剂有限公司;乙酸,分析纯,北京化工厂。艾托莫德(SYL927)原料药样品(批号SNT20140423、SNT20140424、SNT20140425),中国医学科学院药物研究所;SYL927,合成中间体927-1、927-2、927-3、927-5、927-6、927-7和副产物Imp-A、Imp-C、Imp-F的对照品,纯度均大于99%,由中国医学科学院药物研究所合成和标化。
2 方法与结果 2.1 色谱条件色谱柱:Agilent HC-C8(4.6 mm×250 mm,5 μm);流动相:A相为乙腈,B相为0.2%醋酸钠缓冲液(称取三水合醋酸钠20.4 g,加冰醋酸80 mL,加水至1 000 mL,加水稀释10倍,pH 3.6),进行梯度洗脱,梯度洗脱程序见表 2;流速:1.0 mL·min-1;柱温:40 ℃;检测波长:283 nm;进样量:20 μL。
|
|
表 2 梯度洗脱程序 Table 2 Gradient elution program |
取SYL927原料药样品约25 mg,准确称量,置25 mL量瓶中,加甲醇超声溶解并稀释至刻度,摇匀,制得质量浓度为1 mg·mL-1的溶液,即得。
2.3 混合对照溶液的制备精密量取供试品溶液1 mL,置于100 mL量瓶中,用甲醇稀释至刻度,摇匀,制得10 μg·mL-1的溶液,即得。
2.4 混合对照品溶液的制备分别称取SYL927及中间体927-1、927-2、927-3、927-5、927-6、927-7适量,加甲醇溶解并定量稀释制成10 μg·mL-1的混合对照品溶液Ⅰ。分别称取副产物Imp-A、Imp-C、Imp-F和中间体927-7,加甲醇溶解并定量稀释制成10 μg·mL-1的混合对照品溶液Ⅱ。
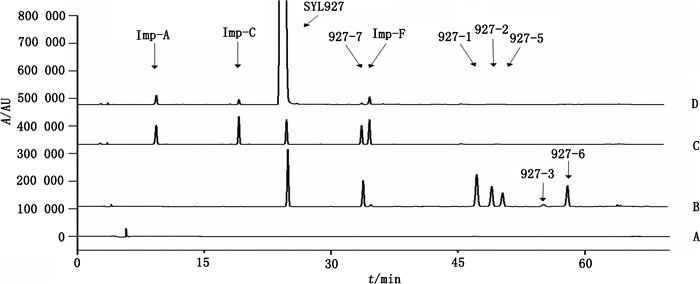
2.5 专属性试验量取空白溶剂、混合对照品溶液Ⅰ、混合对照品溶液Ⅱ、供试品溶液各20 μL,按“2.1”项的色谱条件进样测定。结果表明,溶剂不干扰各化合物的分离,SYL927与9个有关物质与各相邻峰均达到完全分离,分离度大于1.5,专属性好,见图 1。
|
A.空白溶剂(blank solvent)B.混合对照品溶液Ⅰ(mixed reference substance solution Ⅰ)C.混合对照品溶液Ⅱ(mixed reference substance solution Ⅱ)D.供试品溶液(analytical solution) 图 1 专属性色谱图 Figure 1 Chromatograms of specificity |
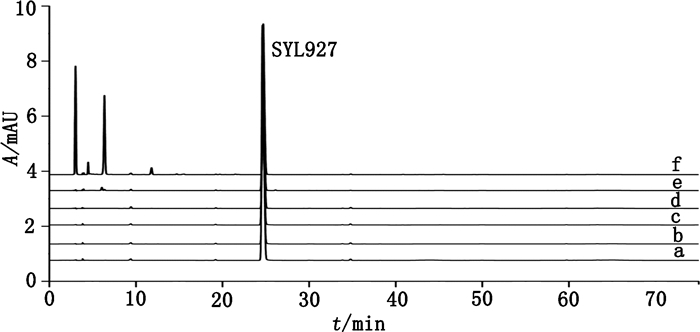
称取SYL927原料药样品约10 mg,共5份,分别进行光照[置于(4 500±500)lx,10 d]、高温加热(60 ℃,10 d)、碱破坏(加6 mol·L-1氢氧化钠溶液1 mL,在80 ℃水浴加热1 h,放冷至室温,加6 mol·L-1盐酸溶液中和)、酸破坏(加6 mol·L-1盐酸溶液1 mL,在80 ℃水浴加热1 h,放冷至室温,加6 mol·L-1氢氧化钠溶液中和)、氧化破坏(加入30%过氧化氢溶液1 mL,80 ℃水浴0.5 h),加甲醇制成0.2 mg·mL-1的破坏溶液,同法配制各破坏条件的空白溶液。分别精密量取上述破坏溶液各20 μL,按“2.1”项色谱条件测定,色谱图见图 2。
|
a.供试品溶液(analytical solution)b.高温破坏溶液(thermolytic condition solution)c.光破坏溶液(photolytic condition solution)d.碱破坏溶液(basic hydrolysis solution)e.酸破坏溶液(acidic hydrolysis solution)f.氧化破坏溶液(oxidative solution) 图 2 SYL927破坏试验色谱图 Figure 2 Chromatograms of stress condition test |
结果表明,SYL927在光照、高温加热、碱破坏条件下稳定,未产生新杂质;酸破坏分解产生少量杂质;在氧化条件下不稳定,氧化分解产生较多杂质。SYL927经过破坏所产生的杂质与主峰及各杂质峰之间也能完全分离,分离度大于1.5;证明建立的方法专属性好,可用于SYL927的有关物质测定。
2.7 线性关系考察及响应因子、检测下限与定量下限测定称取SYL927、6种中间体和3种副产物的对照品适量,分别加甲醇溶解并定量稀释制成0.1~22 μg·mL-1的6个系列浓度混合对照品溶液,在“2.1”项的色谱条件下进样测定;以质量浓度X为横坐标,峰面积Y为纵坐标,进行线性回归,10种化合物线性关系良好。计算各中间体和副产物相对SYL927的响应因子,以S/N=3时测得量为检测下限,S/N=10时测得量为定量下限。结果见表 3。
|
|
表 3 SYL927及9个有关物质的线性范围、回归方程、响应因子、检测下限(LOD)与定量下限(LOQ) Table 3 Linear ranges, regression equations, response factors, detection limits(LOD) and quantitation limits(LOQ)of SYL927 and 9 related substances |
称取SYL927、927-1、927-2、927-3、927-5、927-6、927-7、Imp-A、Imp-C、Imp-F的对照品各适量,加甲醇制成约10 μg·mL-1的混合溶液,按“2.1”项的色谱条件连续进样7次,记录色谱图,以峰面积计算精密度。结果SYL927、927-1、927-2、927-3、927-5、927-6、927-7、Imp-A、Imp-C、Imp-F的精密度(RSD)分别为0.41%、0.43%、0.40%、0.76%、0.48%、0.39%、0.41%、0.33%、0.34%和0.31%,均小于1.0%,表明精密度良好。
2.9 溶液稳定性试验取“2.2”项下供试品溶液及“2.3”项下对照溶液,按“2.1”项色谱条件于0、2.5、5、10、15、20和25 h进样测定,记录色谱图,SYL927及各杂质峰面积的RSD均小于1.0%,表明供试品溶液和对照溶液室温放置25 h稳定。
2.10 准确度试验称取SYL927原料药样品7份(每份10 mg),分别置于10 mL量瓶中,分别加入含各杂质20 μg·mL-1的混合对照品溶液5 mL,用甲醇溶解并稀释至刻度,测定有关物质的量,计算回收率。9个有关物质927-1、927-2、927-3、927-5、927-6、927-7及Imp-A、Imp-C、Imp-F的回收率平均值分别为100.7%、101.1%、100.4%、101.3%、100.8%、100.4%、100.2%、101.1%和101.4%,RSD分别为0.98%、0.93%、1.2%、0.95%、0.96%、0.98%、2.2%、0.84%和1.1%,表明回收率良好。
2.11 耐用性试验在Agilent HC-C8(4.6 mm×250 mm,5 μm)、CAPVELL PAK C8(4.6 mm×250 mm,5 μm)和Xtimata C8(4.6 mm×250 mm,5 μm)3款色谱柱上进行有关物质分离的考察;结果显示各色谱峰之间能够实现良好分离,分离度均大于1.5。同时也考察了不同柱流速(0.9 mL·min-1和1.1 mL·min-1)、不同流动相比例(乙腈-0.2%醋酸钠缓冲液起始比例19:81和乙腈-0.2%醋酸钠缓冲液起始比例21:79)、不同色谱柱温度(36 ℃和44 ℃)和不同的0.2%醋酸钠缓冲液pH(pH 3.5和pH 3.7)条件下的耐用性,结果表明,有关物质的分离度均可达到基线分离,分离度均大于1.5,方法耐用性较好。
2.12 有关物质的测定结果分别取供试品溶液及对照溶液各20 μL,注入液相色谱仪中,记录色谱图;如有杂质峰,按主成分自身对照法计算。3批原料药样品测定结果见表 4。
|
|
表 4 原料药有关物质测定结果(%) Table 4 The determination results of related substance in SYL927 drug substance |
对流动相各组分以及各组分之间比例的摸索和优化,考察了SYL927与中间体、副产物和破坏产生的降解杂质等有关物质的峰形、保留时间和分离度,确定以乙腈-0.2%醋酸钠缓冲液(pH 3.6)为流动相梯度洗脱,可以使SYL927及各有关物质色谱峰之间均达到完全分离,且峰形良好。
3.2 检测波长的选择SYL927和4个中间体(927-1、927-2、927-6、927-7)和3个副产物(Imp-A、Imp-C、Imp-F)均在281~289 nm有最大吸收;而中间体927-5在295 nm有最大吸收,在283 nm有较大吸收;中间体927-3在254 nm有最大吸收,在283 nm也有吸收。破坏性试验产生的杂质在283 nm均有较大吸收,具有足够的检测灵敏度。因此选择283 nm作为有关物质检测波长。
3.3 有关物质测定方法的选择多批SYL927原料药的研究表明,中间体927-1、927-2、927-3、927-5、927-6在合成工艺中可被除去,SYL927原料药只检出副产物Imp-A、Imp-C、Imp-F和合成前体927-7。杂质的响应因子分别为Imp-A为0.9,Imp-C为1.0,927-7为0.9,Imp-F为1.1,均在0.9~1.1之间,与主成分响应相当,因此SYL927原料药采用主成分自身对照法对SYL927有关物质进行测定。
4 结论本试验建立了高效液相色谱检测SYL927原料药有关物质的方法,并进行了方法学研究,方法灵敏度高,专属性强。对多批原料药的检测及工艺研究,表明该方法可有效地分离和检测SYL927原料药中潜在的有关物质。SYL927破坏性试验结果表明,在氧化条件下,易产生降解,生成4个杂质,提示SYL927在生产、运输、贮存时应避免接触氧化剂,保证药品质量稳定。
| [1] |
STERN RS, NIJSTEN T, FELDMAN SR, et al. Psoriasis is common, carries a substantial burden even when not extensive, and is associated with widespread treatment dissatisfaction[J]. J Investig Dermatol Symp Proc, 2004, 9(2): 136. DOI:10.1046/j.1087-0024.2003.09102.x |
| [2] |
FARLEY E, MENTER A. Psoriasis:comorbidities and associations[J]. G Ital Dermatol Venereol, 2011, 146(1): 9. |
| [3] |
邓雪蓉, 张卓莉. 银屑病和银屑病关节炎研究评价组发布2015银屑病关节炎治疗建议[J]. 中华风湿病学杂志, 2016, 20(9): 646. DENG XR, ZHANG ZL. The evaluation group of psoriasis and psoriasis arthritis research launched 2015 recommendations for treatment of psoriatic arthritis[J]. Chin J Rheumatol, 2016, 20(9): 646. |
| [4] |
JIANG S, HINCHLIFFE TE, WU T. Biomarkers of an autoimmune skin disease - psoriasis[J]. Genomics Proteomics Bioinformatics, 2015, 13(4): 224. DOI:10.1016/j.gpb.2015.04.002 |
| [5] |
PARISI R, SYMMONS DP, GRIFITHS CE, et al. Global epidemiology of psoriasis:a systematic review of incidence and prevalence[J]. J Invest Dermatol, 2013, 133(2): 377. DOI:10.1038/jid.2012.339 |
| [6] |
MENTER A, GRIFFITHS CE. Current and future management of psoriasis[J]. Lancet, 2007, 370(9583): 272. DOI:10.1016/S0140-6736(07)61129-5 |
| [7] |
CAMERON H, DAWE RS, YULE S, et al. A randomized, observer-blinded trial of twice vs. three times weekly narrowband ultraviolet B phototherapy for chronic plaque psoriasis[J]. Br J Dermatol, 2007, 147(5): 973
|
| [8] |
National Psoriasis Foundation Website. Psoriasis media kit[EB/OL]. (2016-02-25)[2017-05-16]. https://www.psoriasis.org/sites/default/files/for-media/MediaKit.pdf
|
| [9] |
XIAO Q, JIN J, WANG X, et al. Synthesis, identification, and biological activity of metabolites of two novel selective S1P1 agonists[J]. Bioorg Med Chem, 2016, 24(10): 2273. DOI:10.1016/j.bmc.2016.03.059 |
| [10] |
张婷婷, 金波, 李彤, 等. HPLC-MS/MS鉴定创新药物艾托莫德的有关物质[J]. 中国药学杂志, 2017, 52(1): 68. ZHANG TT, JIN B, LI T, et al. Identification of related substances in a new drug aituomode by HPLC-MS/MS[J]. Chin Pharm J, 2017, 52(1): 68. |
| [11] |
XIANG Y, ASMUSSEN G, BOOKER M, et al. Discovery of novel sphingosine kinase 1 inhibitors[J]. Bioorg Med Chem Lett, 2009, 19(21): 6119. DOI:10.1016/j.bmcl.2009.09.022 |
| [12] |
EVINDAR G, BERNIER SG, KAVARANA MJ, et al. Synthesis and evaluation of alkoxy-phenylamides and alkoxy-phenylimidazoles as potent sphingosine-1-phosphate receptor subtype-1 agonists[J]. Bioorg Med Chem Lett, 2009, 19(2): 369. DOI:10.1016/j.bmcl.2008.11.072 |
| [13] |
FOSS FW JR, MATHEWS TP, KHAREL Y, et al. Synthesis and biological evaluation of sphingosine kinase substrates as sphingosine-1-phosphate receptor prodrugs[J]. Bioorg Med Chem, 2009, 17(16): 6123. DOI:10.1016/j.bmc.2009.04.015 |
| [14] |
韩伟娟, 张海婧, 汪小涧, 等. 胺基丙二醇类衍生物、其制备方法和其药物组合物与用途: 中国, 103702973[P]. 2014-04-02 HANG WJ, ZHANG HJ, WANG XJ, et al. Amino-Propylene-Glycol Derivatives, Preparation Method and Pharmaceutical Composition and Use Thereof: China, 10370297. 3[P]. 2014-04-02 |
| [15] |
MI JQ, ZHAO MM, YANG S, et al. Pharmacokinetics of H002, a novel S1PR1 modulator, and its metabolites in rat blood using liquid chromatography-tandem mass spectrometry[J]. Acta Pharm Sin B, 2016, 6(6): 576. DOI:10.1016/j.apsb.2016.06.001 |
 2018, Vol. 38
2018, Vol. 38 

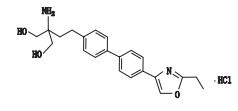
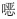 唑-4-基)-[1, 1′-联苯]-4-基)乙基}-1, 3-丙二醇盐酸盐2-amino-2-(2-(4′-(2-ethyloxazol-4-yl)-[1, 1′-biphenyl]- 4-yl)ethyl)-1, 3-propanediol hydrochloride
唑-4-基)-[1, 1′-联苯]-4-基)乙基}-1, 3-丙二醇盐酸盐2-amino-2-(2-(4′-(2-ethyloxazol-4-yl)-[1, 1′-biphenyl]- 4-yl)ethyl)-1, 3-propanediol hydrochloride