2. 和田维吾尔药业股份有限责任公司, 和田 848200;
3. 新疆第八师石河子市药品检验所, 石河子 832000
2. Xinjiang Uygur Pharmaceuticals Co., Ltd., Hetian 848200, China;
3. Xinjiang Eighth division of the Shihezi Institute of Drug Inspection, Shihezi 832000, China
维药伊木萨克片(国药准字Z65020144)是维吾尔民族治疗早泄的传统验方,由丁香、罂粟壳、马钱子、肉豆蔻等11味药材组成,具有补肾壮阳及益精固涩的功效。用于阳萎,早泄,滑精,遗尿及神经衰弱等[1]。本制剂收载于1998年版《中华人民共和国卫生部药品标准维吾尔药分册》中,标准仅采用薄层色谱法对罂粟壳和马钱子进行了定性鉴别,而对处方中的其他药材没有任何鉴别项。
伊木萨克片良好的功效依赖于处方各药材的相互作用。其中,罂粟壳、马钱子补充摄住力,增强机体对营养物质的保留,从而防止人体营养物质的流失[2-3],然罂粟壳所含的主要生物活性成分为吗啡、可待因、罂粟碱类生物碱,久服易成瘾[4-6],马钱子含有马钱子碱、士的宁等生物碱,由于毒性大,安全范围小,过量时会导致延髓麻痹,心脏和呼吸均被抑制而死于呼吸麻痹、窒息或心力衰竭[7-9]。因此,为确保制剂的安全性与有效性,本实验对制剂中的罂粟壳、马钱子、西红花、丁香、欧白及、肉豆蔻、乳香、高良姜8味药材进行了薄层色谱定性鉴别;对罂粟壳中的吗啡、可待因、罂粟碱,马钱子中的士的宁和马钱子碱进行了含量测定,可为完善该制剂的质量标准提供参考。
1 仪器与试药 1.1 仪器Waters e2695高效液相色谱仪(2998 PDA检测器,717自动进样器,Empower工作站),移液枪(Eppendorf公司),KH-300DE型数控超声波清洗器(昆山禾创超声仪器有限公司,功率500 W,频率40 kHz),BT125D十万分之一电子天平(德国赛多利斯公司),雷磁PHS-3C精密PH计(上海精密科学仪器有限公司)。
1.2 试药伊木萨克片(批号分别为20160601、20160701、20160801规格为0.5 g·片-1)由新疆和田维吾尔药业有限责任公司提供;对照品吗啡(批号171201-201123,纯度≥98%)、磷酸可待因(批号171203-201005,纯度≥98%)、盐酸罂粟碱(批号171214-201205,纯度≥98%)均购于中国食品药品检定研究院,对照品马钱子碱(批号CAS#357-57-3,纯度≥98%)、士的宁(批号CAS#57-24-9,纯度≥98%)均购于上海源叶生物科技有限公司;对照药材马钱子(批号121164-200302)、罂粟壳(批号120957-201507)、高良姜(批号121263-201304)、肉豆蔻(批号120926-201307)、乳香(批号120970-201305)、白及(批号121262-201104)、西红花(批号121009-200502)、丁香(批号121039-201004)均购于中国食品药品检定研究院,阴性样品药材均由新疆和田维吾尔药业有限责任公司提供。G型硅胶板(50×100 mm,批号20161005,青岛海洋化工分厂)。甲醇和乙腈为色谱纯,其余均为分析纯,双蒸水。
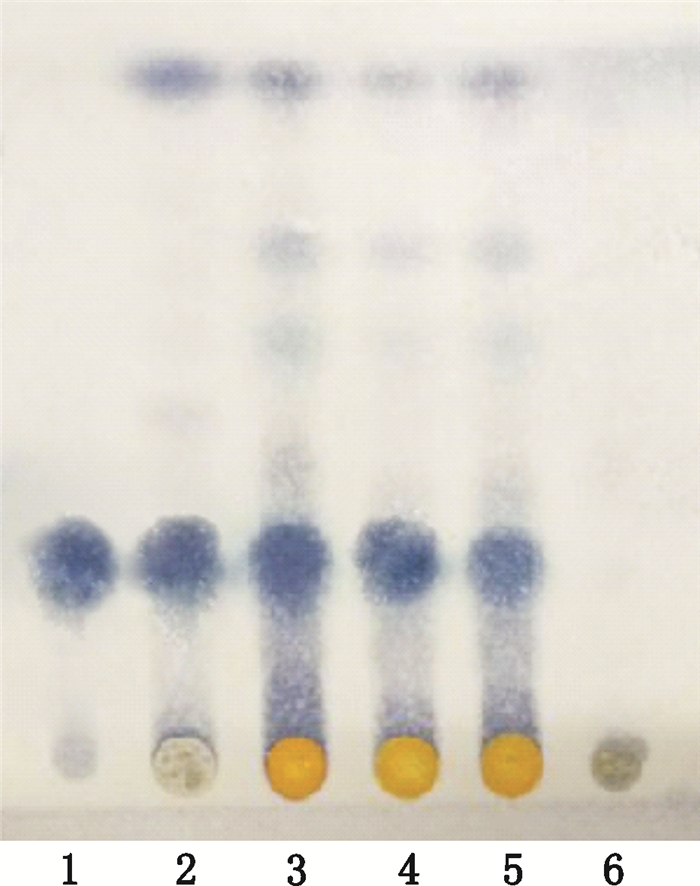
2 定性鉴别 2.1 丁香薄层色谱鉴别取伊木萨克片1.0 g,研细,加甲醇5 mL,超声30 min,过滤得滤液,旋转蒸发,蒸干后加1 mL甲醇溶解,即得供试品溶液。取丁香酚对照品适量,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。取按照处方工艺及比例制备缺丁香的阴性样品1.0 g,用相同方法制备阴性对照溶液。取丁香对照药材粉末0.5 g,同法制成对照药材溶液。吸取对照品溶液5 μL及对照药材溶液、供试品溶液、阴性对照溶液各10 μL,分别点于同一硅胶G薄层板上,以石油醚(60~90 ℃)-乙酸乙酯(15:1)为展开剂,展开,取出,晾干。喷以10%硫酸乙醇溶液后再喷以5%磷钼酸溶液,在105 ℃加热至斑点显色清晰。样品色谱中,在与对照品色谱和对照药材色谱相应的位置上,显相同颜色的斑点。见图 1。
|
1.丁香酚对照品(reference substance of eugenol) 2.丁香对照药材(reference crude drug of Sy zy gium aromaticuro(L.)Merr.L·M.Perry) 3. 20160601号样品(sample 20160601) 4. 20160701号样品(sample 20160701) 5. 20160801号样品(sample 20160801) 6.阴性样品(negative sample without Syzygium aromaticuro (L.)Merr. & L.M.Perry)) 图 1 丁香薄层色谱图 Figure 1 TLC chromatogram of Sy zy gium aromaticuro(L.)Merr.L·M.Perry |
取伊木萨克片1.0 g,研细,加甲醇5 mL,超声30 min,过滤得滤液,旋转蒸发,蒸干后加1 mL甲醇溶解,即得供试品溶液。取高良姜对照药材粉末0.5 g,同法制成对照药材溶液。取按照处方工艺及比例制备的缺高良姜的阴性样品1.0 g,用相同方法制备阴性对照溶液。吸取对照药材溶液、供试品溶液、阴性对照溶液各10 μL,分别点于同一硅胶G薄层板上,以正己烷-乙酸乙醋-甲醇-冰乙酸(10:1:1:0.5)为展开剂,展开,取出,晾干。喷以10%硫酸乙醇溶液后再喷以5%磷钼酸溶液,在105 ℃加热至斑点显色清晰。样品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点。见图 2。

|
1.高良姜素对照品(reference substance of galangin) 2.高良姜对照药材(reference crude drug of Alpinia officinarum Hance.) 3.20160601号样品(sample 20160601) 4.20160701号样品(sample 20160701) 5.20160801号样品(sample 20160801) 6.阴性样品(negative sample without Alpinia officinarum Hance.) 图 2 高良姜薄层色谱图 Figure 2 TLC chromatogram of Alpinia officinarum Hance. |
取伊木萨克片1.0 g,研细,加甲醇5 mL,超声10 min,过滤得滤液,旋转蒸发,蒸干后加1 mL甲醇溶解,即得供试品溶液。取西红花苷-Ⅰ、西红花苷-Ⅱ的对照品适量,加甲醇制成每1 mL含1 mg的溶液,作为混合对照品溶液。取西红花对照药材粉末0.5 g,同法制成对照药材溶液。取按照处方工艺及比例制备缺西红花的阴性样品1.0 g,用相同方法制备阴性对照溶液。吸取对照品溶液、对照药材溶液各5 μL,供试品溶液、阴性对照溶液各10 μL,分别点于同一硅胶G薄层板上,以乙酸乙酯-甲醇-水(5:1.5:0.6)为展开剂,展开,取出,晾干,置日光灯下检视。样品色谱中,在与对照品色谱和对照药材色谱相应的位置上,显相同颜色的斑点。见图 3。

|
1.西红花苷-Ⅰ、西红花苷-Ⅱ混合对照品(mixed reference substances of crocusⅠand crocusⅡ) 2.西红花对照药材(reference crude drug of Crocus sativus L.) 3.20160601号样品(sample 20160601) 4.20160701号样品(sample 20160701) 5.20160801号样品(sample 20160801)6.阴性样品(negative sample without Crocus sativus L.) 图 3 西红花薄层色谱图 Figure 3 TLC chromatogram of Crocus sativus L. |
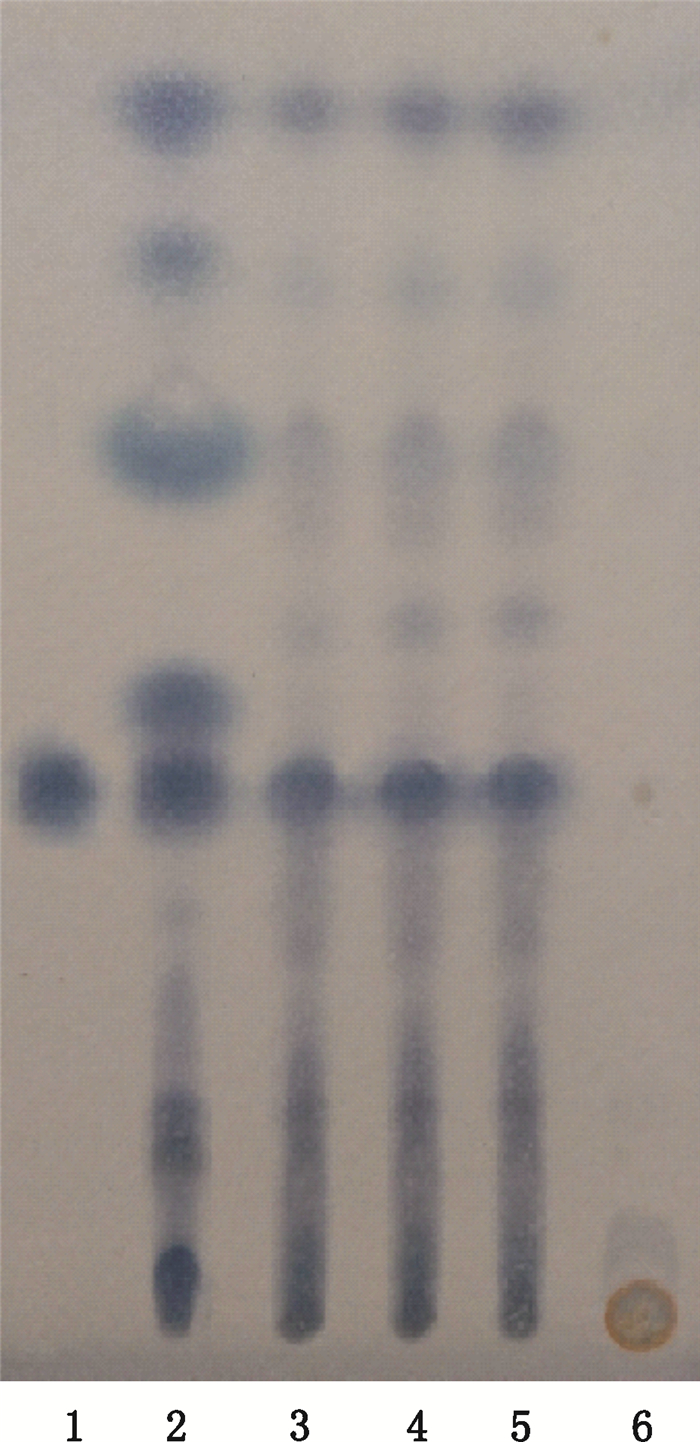
取伊木萨克片1.0 g,研细,取石油醚(60~90 ℃)5 mL,超声30 min,过滤液浓缩至2 mL,即得供试品溶液。取肉豆蔻对照药材粉末0.5 g,同法制成对照药材溶液。取按照处方工艺及比例制备缺肉豆蔻的阴性样品1.0 g,用相同方法制备阴性对照溶液。吸取对照药材溶液、供试品溶液、阴性对照溶液各10 μL,分别点于同一硅胶G薄层板上,以石油醚(60~90°)-乙酸乙酯(9:1)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液后再喷以5%磷钼酸溶液,在105 ℃加热至斑点显色清晰。见图 4。
|
1.去氢二异丁香酚对照品(reference substance of dehydrodiisoeugenol) 2.肉豆蔻对照药材(reference crude drug of Myristica fragrans Houtt.)3.20160601号样品(sample 20160601) 4.20160701号样品(sample 20160701) 5.20160801号样品(sample 20160801) 6.阴性样品(negative sample without Myristica fragrans Houtt.) 图 4 肉豆蔻薄层色谱图 Figure 4 TLC chromatogram of Myristica fragrans Houtt. |
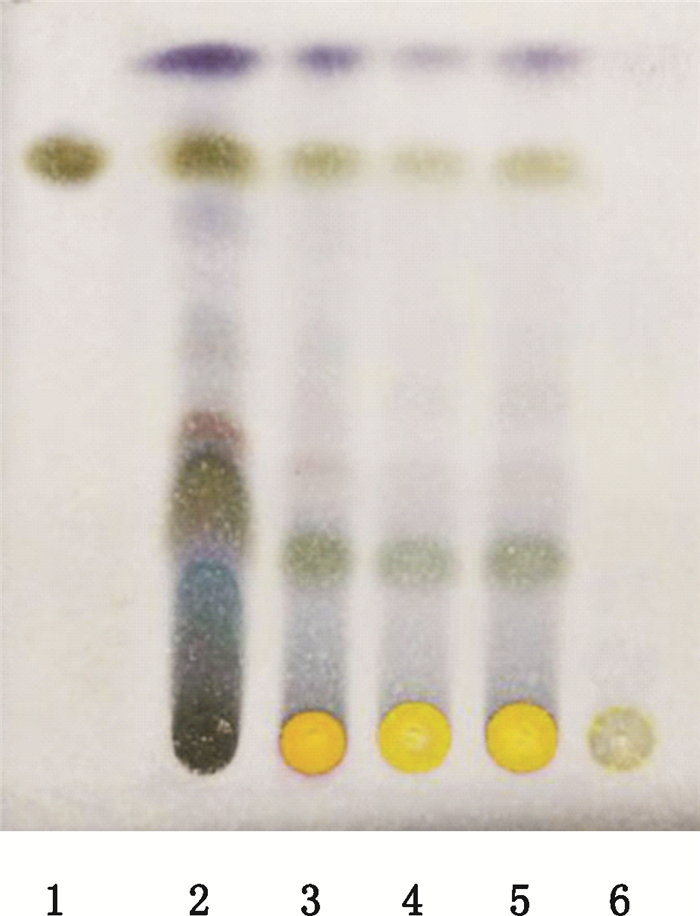
取伊木萨克片1.0 g,研细,加甲醇5 mL,超声30 min,过滤得滤液,旋转蒸发,蒸干后加1 mL甲醇溶解,即得供试品溶液。取乳香对照药材粉末0.5 g,同法制成对照药材溶液。取按照处方工艺及比例制备的缺乳香的阴性样品1.0 g,用相同方法制备阴性对照溶液。吸取对照药材溶液、供试品溶液、阴性对照溶液各10 μL,分别点于同一硅胶G薄层板上,以石油醚(60~90 ℃)-乙酸乙酯(10:1)为展开剂,展开,取出,晾干。喷以5%香草醛硫酸溶液,在105 ℃加热至斑点显色清晰。样品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点。见图 5。
|
1.11-羰基-β-乙酰乳香酸对照品(reference substance of acetyl-11-keto-β-boswellic acid) 2.乳香对照药材(reference crude drug of Boswelia Carterii Birdw.) 3.20160601号样品(sample 20160601) 4.20160701号样品(sample 20160701) 5.20160801号样品(sample 20160801)6.阴性样品(negative sample without Boswelia Carterii Birdw.) 图 5 乳香薄层色谱图 Figure 5 TLC chromatogram of Myristicae Boswelia Carterii Birdw. |
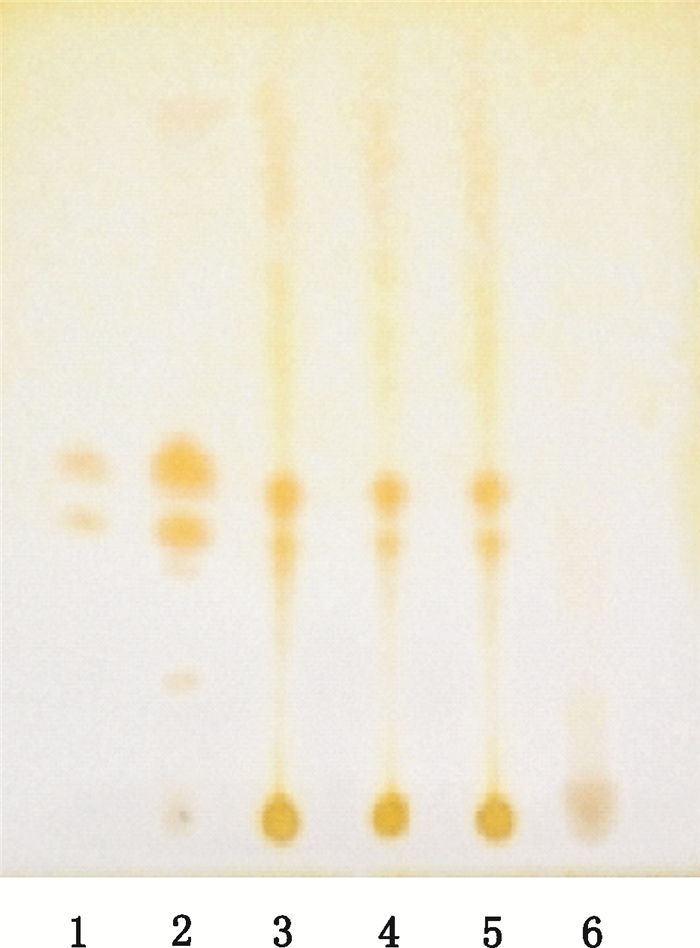
取伊木萨克片1.0 g,研细,加4 mL氨润湿后加三氯甲烷3 mL超声30 min后,滤液蒸干,残渣加甲醇1 mL溶解,即得供试品溶液。取马钱子碱、士的宁的对照品适量,加甲醇制成每1 mL含1 mg的溶液,作为混合对照品溶液。取马钱子对照药材粉末0.5 g,同法制成对照药材溶液。取按照处方工艺的比例制备缺马钱子的阴性样品1.0 g,用相同方法制备阴性对照溶液。吸取对照品溶液、对照药材溶液各5 μL,供试品溶液、阴性对照溶液各10 μL,分别点于同一硅胶G薄层板上,以甲苯-丙酮-浓氨试液(2:10:1)为展开剂,展开后喷碘化铋钾试液。见图 6。
|
1.马钱子碱和士的宁混合对照品(mixed reference substances of brucine and strychnine) 2.马钱子对照药材(reference crude drug of Strychnos nux-vomicaL.) 3.20160601号样品(sample 20160601) 4.20160701号样品(sample 20160701) 5.20160801号样品(sample 20160801)6.阴性样品(negative sample without Strychnos nux-vomicaL.) 图 6 马钱子薄层色谱图 Figure 6 TLC chromatogram of Strychnos nux-vomicaL. |
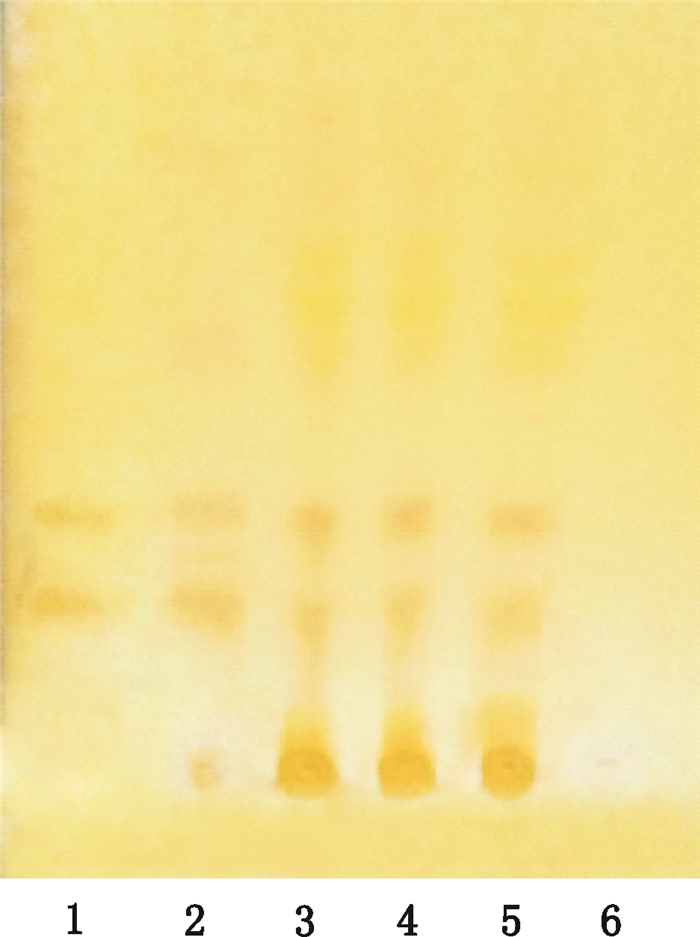
取伊木萨克片1.0 g,研细,加4 mL氨润湿后加三氯甲烷3 mL超声30 min后,滤液蒸干,残渣加甲醇1 mL溶解,即得供试品溶液。取吗啡对照品适量,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。取罂粟壳对照药材粉末0.5 g,同法制成对照药材溶液。取按照处方工艺及比例制备缺罂粟壳的阴性样品1.0 g,用相同的方法制备阴性对照溶液。吸取对照品溶液、对照药材溶液各5 μL,供试品溶液、阴性对照溶液各10 μL,分别点于同一硅胶G薄层板上,以甲苯-丙酮-乙醇-浓氨(10:10:1.5:1.5)为展开剂,展开后喷碘化铋钾试液。见图 7。
|
1.吗啡、磷酸可待因混合对照品(mixed reference substances of morphine and codeine phosphate) 2.罂粟壳对照药材(reference crude drug of Papaver Somniferum L.) 3.20160601号样品(sample 20160601) 4.20160701号样品(sample 20160701) 5.20160801号样品(sample 20160801) 6.阴性样品(negative sample without Papaver Somniferum L.) 图 7 罂粟壳薄层色谱图 Figure 7 TLC chromatogram of Papaver Somniferum L. |
取伊木萨克片1.0 g,研细,加甲醇5 mL,超声处理30 min,滤过,滤液蒸干,残渣加水5 mL使溶解,再加盐酸1 mL,超声30 min,待冷却后用乙醚分2次提取,每次5 mL,合并乙醚液,蒸干,残渣,加三氯甲烷2 mL使溶解,即得供试品溶液。另取白及对照药材0.5 g,同法制成对照药材溶液。取按照处方工艺及比例制备缺欧白及阴性样品1.0 g,用相同方法制备阴性对照溶液。吸取对照药材溶液、供试品溶液、阴性对照溶液各10 μL,分别点于同一硅胶G薄层板上,以石油醚(30~60 ℃)-甲酸乙酯-甲酸(15:5:1)为展开剂,展开,取出,晾干,喷以5%磷钼酸溶液,在105 ℃加热至斑点显色清晰。在与对照药材色谱相应的位置上,显相同颜色的斑点。见图 8。

|
1.1,4-二[4-(葡萄糖氧)苄基]-2-异丁基苹果酸酯对照品(reference substance of militarine) 2.白及对照药材(reference crude drug of Bletilla srriata (Thunb.)Reichb.f) 3.20160601号样品(sample 20160601) 4.20160701号样品(sample 20160701) 5.20160801号样品(sample 20160801) 6.阴性样品(negative sample without Bletilla srriata(Thunb.)Reichb.f) 图 8 欧白及薄层色谱图 Figure 8 TLC chromatogram of Orchis mascula L. |
精密称取吗啡对照品适量,用含5%醋酸的20%甲醇溶液溶于25 mL量瓶中,制成质量浓度为0.237 6 mg·mL-1的对照品溶液。避光保存在4 ℃下备用。
3.1.2 磷酸可待因、盐酸罂粟碱、马钱子碱和士的宁对照品溶液精密称取磷酸可待因、盐酸罂粟碱、马钱子碱和士的宁的对照品适量,分别加乙腈溶解,制成质量浓度分别为0.227 6、0.223 2、0.686和0.730 mg·mL-1的对照品溶液。各取对照品溶液适量,加乙腈定容至10 mL量瓶中,制得磷酸可待因、盐酸罂粟碱、马钱子碱和士的宁质量浓度分别为34.54、8.315、21.99和23.40 μg·mL-1的混合对照品储备液。避光保存在4 ℃下备用。
3.2 供试品溶液制备 3.2.1 吗啡供试品溶液取本品约1.0 g,精密称定,置具塞锥形瓶中,加氨水4 mL,充分湿润,放置10 min,加三氯甲烷30 mL超声30 min,取20 mL蒸干浓缩,加甲醇定容于10 mL量瓶中,摇匀,过滤,滤液经0.45 μm微孔滤膜滤过,即得。
3.2.2 可待因、罂粟碱、马钱子碱和士的宁供试品溶液取本品约1.0 g,精密称定,加75%乙醇溶于10 mL量瓶中,超声30 min,放至室温,用75%乙醇补足至刻度,过滤,滤液经0.45 μm微孔滤膜滤过,即得。
3.3 阴性对照溶液制备 3.3.1 吗啡阴性对照溶液按处方比例及工艺自制不含罂粟壳的阴性样品,按“3.2.1”项下供试品溶液的制备方法操作,即得。
3.3.2 可待因和罂粟碱阴性对照溶液按处方比例及工艺自制不含罂粟壳的样品,按“3.2.2”项下供试品溶液的制备方法制备,即得可待因和罂粟碱阴性对照溶液。
3.3.3 马钱子阴性对照溶液按处方比例及工艺自制不含马钱子的样品,按“3.2.2”项下供试品溶液的制备方法操作,即得。
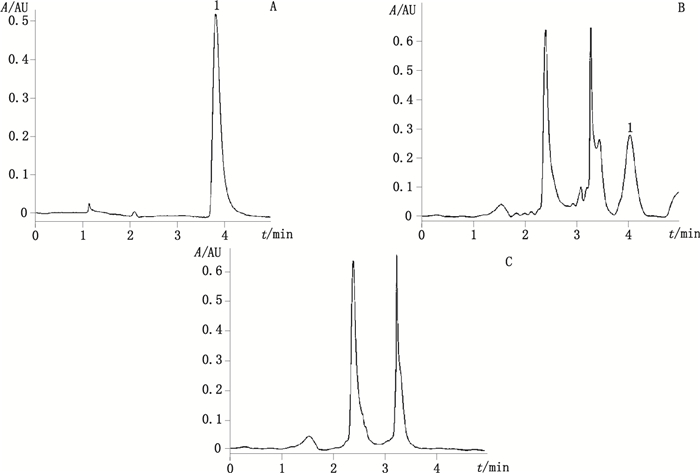
3.4 色谱条件与系统适用性试验 3.4.1 吗啡色谱条件与系统适用性试验采用Waters RP-C18(250 mm×4.6 mm,5 μm)色谱柱,以乙腈-0.01 mol·L-1磷酸二氢钾和0.05 mol·L-1庚烷磺酸钠混合溶液(pH=3.1)(2:98)为流动相,流速1 mL·min-1,检测波长220 nm,柱温25 ℃,进样体积10 μL。对照品、样品与阴性样品色谱图见图 9。在上述色谱条件下,吗啡理论塔板数为8 000,样品中所测成分色谱峰与相邻峰的分离度R > 1.5。
|
1.吗啡(morphine) 图 9 吗啡对照品(A)、样品(B)及阴性样品(C)色谱图 Figure 9 HPLC chromatograms of reference substance of morphine(A), sample(B), negative control(C) |
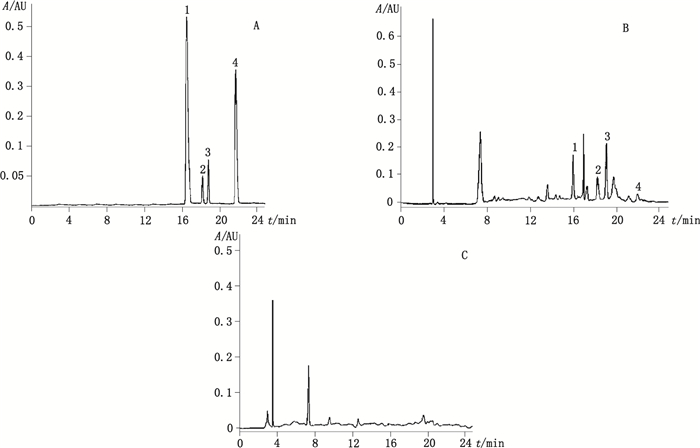
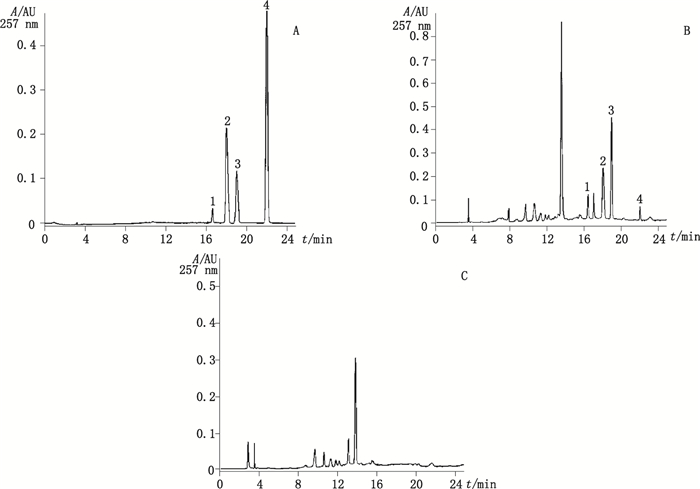
采用Waters RP-C18(250 mm×4.6 mm,5 μm)色谱柱,以乙腈(A)-0.01 mol·L-1磷酸二氢钾和0.05 mol·L-1庚烷磺酸钠混合溶液(B)(pH=3.8)为流动相,梯度洗脱(0~20 min,2%A→40%A;20~25 min,40%A→60%A), 流速1 mL·min-1,检测波长220 nm(可待因)、257 nm(马钱子碱、士的宁和罂粟碱),柱温25 ℃,进样体积10 μL。对照品溶液、供试品溶液与阴性对照溶液色谱图见图 10、11。在上述色谱条件下,各成分理论塔板数均大于4 000,样品中4个被测成分色谱峰与相邻峰的分离度R > 1.5。
|
1.可待因(codeine) 2.马钱子碱(brucine) 3.士的宁(strychnine) 4.罂粟碱(papaverine) 图 10 220 nm检测波长下混合对照品(A)、样品(B)及阴性样品(C)HPLC色谱图 Figure 10 HPLC chromatograms of mixture of reference substances(A), Yimusake tablet(B) and negative sample without Papaver somniferum L. and Strychnos nux-vomical(C)at the detection wavelength of 220 nm |
|
1.可待因(codeine) 2.马钱子碱(brucine) 3.士的宁(strychnine) 4.罂粟碱(papaverine) 图 11 257 nm检测波长下混合对照品(A)、样品(B)及阴性样品(C)HPLC色谱图 Figure 11 HPLC chromatograms of mixture of reference substances(A), Yimusake tablet(B) and negative sample without Papaveri Somniferrm L. and Strychnos nux-vomical(C)at the detection wavelength of 257 nm |
精密吸取混合对照品储备液0.05、0.1、0.2、0.3、0.4、0.5 mL,分别置于10 mL量瓶中,用乙腈稀释至刻度,摇匀,即得系列浓度的混合对照品溶液。分别精密吸取10 μL进样,记录色谱图。以峰面积Y为纵坐标,质量浓度X(μg·mL-1)为横坐标进行线性回归,同时以仪器的信噪比S/N为3时测定检测下限(LOD),S/N为10时测定定量下限(LOQ),结果见表 1。
|
|
表 1 5个化合物的回归方程、相关系数、线性范围和检测下限、定量下限(n=6) Table 1 Linear regression data, LODs and LOQs for five active compounds analyzed by HPLC |
精密吸取混合对照品储备液0.02、0.1、0.2、0.4、0.6、0.8 mL,分别置于10 mL量瓶中,用乙腈稀释至刻度,摇匀,即得系列浓度的混合对照品溶液。分别精密吸取10 μL进样,记录色谱图。以峰面积Y为纵坐标,质量浓度X(μg·mL-1)为横坐标进行线性回归,同时以S/N为3时测定检测下限(LOD),S/N为10时测定定量下限(LOQ),结果见表 1。
3.6 精密度试验取同一混合对照品溶液,在“3.4”项色谱条件下连续进样6次,记录色谱峰面积,结果吗啡、可待因、罂粟碱、士的宁和马钱子碱峰面积的RSD分别为0.81%、0.68%、0.71%、0.52%和0.60%。
3.7 重复性试验取同一批号伊木萨克片(20160701)供试品溶液6份,每份1.0 g,精密称定,按“3.2”项下方法平行制备供试品溶液,按“3.4”项色谱条件下进样分析,记录各色谱峰面积,结果吗啡、可待因、罂粟碱、士的宁和马钱子碱峰面积的RSD分别为1.4%、1.1%、1.1%、1.3%和1.2%。
3.8 稳定性试验将制备的伊木萨克片(20160701)供试品溶液,分别于0、2、4、6、8、12 h内进样6次,记录峰面积,结果吗啡、可待因、罂粟碱、士的宁和马钱子碱12 h内的峰面积的RSD分别为0.69%、0.72%、0.94%、1.3%和1.3%。
3.9 加样回收率试验取已测知5种成分准确含量的伊木萨克片(20160701)9份,每份0.5 g,精密称定,再分别精密加入相当于各待测成分含有量120%、100%、80%的吗啡、磷酸可待因、盐酸罂粟碱、马钱子碱和士的宁对照品溶液,按“3.2”项方法分别制备得到高、中、低不同浓度的供试溶液,按“3.4”项下色谱条件进样测定,计算各平均加样回收率和RSD,结果见表 2。结果表明该方法的加样回收率良好。
|
|
表 2 加样回收率实验结果(n=9) Table 2 Results of recovery test |
取伊木萨克片样品3批,分别按“3.2”项下方法制备供试品溶液,在“3.4”项色谱条件下进行测定,计算伊木萨克片中吗啡、可待因、罂粟碱、马钱子碱、士的宁的含量,结果见表 3。由测定结果可知,制剂中吗啡、可待因、罂粟碱、士的宁和马钱子碱的平均含量分别为0.483、0.618 7、0.061、2.485和1.124 mg·g-1。
|
|
表 3 3批样品含量测定结果(mg·g-1 n=3) Table 3 Results of content determination in three batches of samples |
通过前期预实验薄层色谱定性鉴别对欧白及的相关化学成分进行研究。发现维药欧白及的化学成分与中药材白及相似。由于维药欧白及无对照药材,因此本实验在薄层色谱定性鉴别实验中选择中药白及对照药材进行薄层色谱定性鉴别。
4.2 检测波长的选择据相关文献报道[10-14],吗啡、可待因、罂粟碱、马钱子碱、士的宁最大吸收波长分别为220、220、257、260和254 nm。本实验采用紫外检测器在190~600 nm进行全波长扫描,吗啡、可待因在220 nm处有最大吸收,罂粟碱、马钱子碱、士的宁在257 nm处有最大吸收;故选220 nm作为吗啡、可待因的检测波长,257 nm作为罂粟碱、马钱子碱、士的宁的检测波长。
4.3 提取溶剂的选择参考文献[10-14],分别以氨水湿润之后加三氯甲烷、甲醇、75%甲醇、无水乙醇、75%乙醇作为溶剂进行制剂提取。经比较,吗啡以氨水湿润之后加三氯甲烷做溶剂进行提取,提取率高;可待因、罂粟碱、马钱子碱、士的宁以75%乙醇作溶剂进行提取,提取率高;因此,吗啡以氨水湿润之后加三氯甲烷为提取溶剂,可待因、罂粟碱、马钱子碱、士的宁以75%乙醇为提取溶剂。
4.4 流动相的选择在预实验中选用不同溶剂系统[10-14],如乙腈-0.1%磷酸溶液(每100 mL加0.1 g庚烷磺酸钠)、乙腈-磷酸二氢钾溶液(磷酸调pH=4)、乙腈-0.5%乙酸铵(氨水调pH=7.5)、乙腈-0.01 mol·L-1磷酸二氢钾和0.05 mol·L-1庚烷磺酸钠混合溶液(磷酸调pH=3.8)、乙腈-0.01 mol·L-1磷酸二氢钾和0.05 mol·L-1庚烷磺酸钠混合溶液(磷酸调pH=3.1)等作为流动相进行实验。经优化,确定吗啡的流动相为乙腈-0.01 mol·L-1磷酸二氢钾和0.05 mol·L-1庚烷磺酸钠混合溶液(磷酸调pH=3.1),可待因、罂粟碱、马钱子碱和士的宁的流动相为乙腈-0.01 mol·L-1磷酸二氢钾和0.05 mol·L-1庚烷磺酸钠混合溶液(磷酸调pH=3.8)。
4.4 小结本实验所建立的定性定量实验方法能较好地分析伊木萨克片制剂中罂粟壳、马钱子、西红花、丁香、白及、肉豆蔻、乳香、高良姜。薄层色谱法重现性好,高效液相色谱法实验方法精密度、重复性和稳定性良好,结果稳定可靠。本实验所建立规范合理的方法,能控制伊木萨克片制剂的质量使之更规范,可充分保证伊木萨克片的安全性、有效性和稳定性。
| [1] |
中华人民共国卫生部药品标准. 维吾尔药分册[S]. 1998: 130 Drug Specifications Promulgated by the Ministry of Public Health, PR China. Uigher Medicine[S]. 1998: 130 |
| [2] |
孙中义, 李彦峰, 张荣贵, 等. 伊木萨克片治疗早泄的多中心临床研究[J]. 中国男科学杂志, 2010, 24(2): 46. SUN ZY, LI YF, ZHANG RG, et al. Clinical study on treatment of premature ejaculation with Yimusake Pian[J]. Chin J Androl, 2010, 24(2): 46. |
| [3] |
赵连明, 姜辉, 洪锴, 等. 维药伊木萨克片治疗早泄临床观察[J]. 中华男科学杂志, 2014, 20(11): 1033. ZHAO LM, JIANG H, HONG K, et al. Yimusake formula:safe and efficacious for premature ejaculation[J]. Chin J Androl, 2014, 20(11): 1033. |
| [4] |
王林, 傅先明, 钱若兵, 等. 吗啡成瘾性大鼠脑内核团神经细胞[Ca2+] i变化的研究[J]. 立体定向和功能性神经外科杂志, 2007, 20(12): 84. WANG L, FU XM, QIAN RB, et al. The changes of neuroal intracellular free calcium in brain regions of morphine-addicted rats[J]. Chin J Stereotactic Function Neurosurg, 2007, 20(2): 84. |
| [5] |
吕晓英. 麻醉中药罂粟壳的利用研究和处方分析[J]. 中医药临床杂志, 2005, 13(3): 245. LÜ XY. Study on the utilization and prescription analysis of Pericarpium Papaveris[J]. Clin J Chin Med, 2005, 13(3): 245. |
| [6] |
郝红艳, 郭济贤, 顺庆生, 等. HPLC和HPCE法测定罂粟壳中3种生物活性生物碱[J]. 药学学报, 2000, 35(4): 289. HAO HY, GUO JX, SHUN QS, et al. Determination of 3 biologically active alkaloids in Pericarpium Papaveris by HPLC and HPCE[J]. Acta Pharm Sin, 2000, 35(4): 289. |
| [7] |
杜贵友. 有毒中药现代研究与合理应用[M]. 北京: 人民卫生出版社, 2003, 305. DU GY. Modern Research and Rational Application of Poisonous Chinese Medicine[M]. Beijing: People's Medical Publishing House, 2003, 305. |
| [8] |
贾旋旋, 李文, 李俊松, 等. 马钱子的毒性研究进展[J]. 中国中药杂志, 2009, 34(18): 2396. JIA XX, LI W, LI JS, et al. Progress in study on toxicity of Semen Strychni[J]. China J Chin Mater Med, 2009, 34(18): 2396. DOI:10.3321/j.issn:1001-5302.2009.18.030 |
| [9] |
刘娟, 余翔. 马钱子的炮制和毒理研究进展[J]. 现代医院, 2006, 6(11): 52. LIU J, YU X. Research evolvement of semen strychni preparation and its toxicology[J]. Mod Hosp Nov, 2006, 6(11): 52. DOI:10.3969/j.issn.1671-332X.2006.11.032 |
| [10] |
中华人民共和国药典2015年版. 一部[S]. 2015: 369 ChP 2015. Vol Ⅰ[S]. 2015: 369, 50 |
| [11] |
杨红娟, 郭伟斌, 郑淑凤, 等. RP-HPLC同时测定复方甘草片中4个成分的含量[J]. 药物分析杂志, 2013, 33(1): 141. YANG HJ, GUO WB, ZHENG SF, et al. RP-HPLC simultaneous determination of four active components in compound liquorice tablets[J]. Chin J Pharm Anal, 2013, 33(1): 141. |
| [12] |
祝小静. RP-HPLC法测定二母安嗽片中的吗啡[J]. 药物评价研究, 2014, 37(5): 434. ZHU XJ. Determination of morphine in Ermu Ansou tablet by RP-HPLC[J]. Drug Eval Res, 2014, 37(5): 434. |
| [13] |
王瑶, 陆益红, 孟长虹, 等. 盐酸罂粟碱注射液含量测定及有关物质研究[J]. 药物分析杂志, 2011, 31(9): 1693. WANG Y, LU YH, MENG CH, et al. Study on determination of papaverine hydrochloride injection and its related substances[J]. Chin J Pharm Anal, 2011, 31(9): 1693. |
| [14] |
陈晓莉, 李永吉, 王录娜, 等. HPLC法测定马钱子缓释片中士的宁与马钱子碱[J]. 哈尔滨商业大学学报(自然科学版), 2013, 29(4): 391. CHEN XL, LI YJ, WANG LN, et al. Determination of content of strychnine and brucine in strychnos sustained-release tablets by HPLC[J]. J Harbin Univ Comm, 2013, 29(4): 391. |
 2018, Vol. 38
2018, Vol. 38 
