羊奶相比于牛奶,具有脂肪粒和蛋白微粒小,矿物质和维生素丰富,更容易被人体吸收的特点;且羊奶从基础结构到营养配比更接近于人奶,尤其适合婴幼儿食用[1],同时羊奶中αS-酪蛋白等异体蛋白含量较少,能大大降低过敏反应的发生[2]。随着物质水平的提高,营养价值更高的羊奶及奶制品受到越来越多的追捧,但随着养殖行业规模化发展,为治疗预防动物疾病,往往采用多种类药物同时使用或滥用的现象,甚者有的不法分子为达到非法获利的目的,添加违禁药物,导致羊奶及组织中禁限用药物残留问题频出[3],对婴幼儿及体弱人群身体健康造成潜在威胁。
为了预防和治疗动物疾病,保证动物生长,畜禽养殖行业常用兽药主要有磺胺类、喹喏酮类、大环内酯类、苯并咪唑类、镇静剂类、抗病毒和截短侧耳素类等药物,由于科学养殖知识的缺乏和经济利益的趋势,超剂量使用现象尤为突出,其次不法兽药生产企业为追求疗效,多种类兽药复方使用,加之不合理的休药期限,导致动物体内同时残留多种兽药;同时为促进动物生长,铤而走险添加违禁药物以谋取私利的现象也时有发生。但目前大多检测方法[4-7]和标准[8-10]主要检测单一种类药物,多种类多残留同时检测的方法也存在检测药物数量和种类少的缺点[11-14],八大类74种兽药同时检测的液相色谱-串联质谱方法还少有报道,因此为满足对奶及奶制品质量安全监管,建立更多种类、更多数量兽药同时检测的确证方法尤为迫切。
1 材料与仪器 1.1 试剂与耗材β-受体激动剂、磺胺、喹喏酮、大环内酯、苯并咪唑、镇静剂、抗病毒和截短侧耳素类共八类74种兽药对照品(具体药物见表 1)购于德国Dr. Ehrenstorfer公司和百灵威公司,纯度均在97%以上;甲醇、乙腈、甲酸等有机溶剂均为色谱纯,购自美国Fisher公司;Waters Oasis PRiME HLB SPE柱(60 mg,3 mL,填料:N-乙烯基吡咯烷酮-二乙烯苯共聚物)购于美国Waters公司。
|
|
表 1 v八大类74种禁限用药物的定性/定量离子对及其对应质谱参数及保留时间 Table 1 Qualitative ions, quantitative ions and relevant parameters of eight categories of seventy four kinds of forbidden and restricted drugs |
将上述对照品用甲醇配制成单标母液,并配制10 μg·mL-1混合储备液于-20 ℃保存,系列标准工作液现用现配;羊奶样品购于电商超市,选择经LC-MS/MS分析确认为阴性羊奶样本作为基质添加样本。
1.2 仪器设备超高效液相色谱仪(H-Class UPLC)串接三重四极杆质谱仪(xevo TO-XS),美国Waters公司;3K15型离心机,美国Sigma公司;纯水仪,美国Millipore公司。氮吹仪,美国Organomation公司。
2 方法 2.1 前处理过程提取:准确称取2 g(精确到0.01 g)羊奶于50 mL离心管中,加入0.5%甲酸乙腈溶液10 mL,9 500 r·min-1离心5 min,取上清液于一50 mL离心管中,重复提取1次,合并提取液,待过净化柱。
净化:将全部提取液转移至事先用85%乙腈溶液活化的Oasis PRiME HLB柱中,保持流速1~2滴·s-1,收集全部滤过液,50 ℃氮气吹至近干,用初始流动相定容至1 mL,12 000 r·min-1离心5 min,上液层使用0.22 μm滤膜过滤,待上机测定。
2.2 液相色谱条件色谱柱:Acquity UPLC BEH C18柱(100 mm×2.1 mm,1.7 μm,填料为十八烷基键合亚乙基桥杂化颗粒,Waters公司);流动相:甲醇(A),0.1%甲酸溶液(B),梯度洗脱(0~0.5 min,3%A保持不变;0.5~2.0 min,3%A线性变化至25%;2.0~3.5 min,25%A保持不变;3.5~3.6 min,25%A线性变化至40%;3.6~4.0 min,40%A保持不变;4.0~5.5 min,40%A线性变化至90%;5.5~8.0 min,90%A保持不变;8.0~8.1 min,90%A线性变化至3%;8.1~10.5 min,3%A保持不变);流速:0.3 ml·min-1。
2.3 质谱条件电离模式:ESI+;毛细管电压:3.0 kV;萃取锥孔电压:3 V;RF透镜电压:0.5 V;源温:150 ℃;脱溶剂温度:600 ℃;锥孔气流速:50 L·h-1;脱溶剂气流速:900 L·h-1;碰撞气流速:0.14 mL·min-1;采集模式:多通道多时段MRM采集;八大类74种药物优化质谱参数及保留时间见表 1。
3 结果与分析 3.1 质谱条件优化β-受体激动剂、磺胺、喹喏酮、大环内酯、苯并咪唑、镇静剂、抗病毒和截短侧耳素类共8类药物结构中均含有氨基结构,因此选用正离子模式采集数据,MS Scan模式下进行一级质谱分析,得到[M+H]+峰,并优化各自聚焦电压使其准分子离子峰响应最佳,然后在Daughter Scan模式下针对各自[M+H]+峰进行二级质谱扫描,获得丰富的碎片离子信息。通过文献[8]对比实验发现,各类化合物碎片离子和丢失离子存在一定共性,其中β-受体激动剂类羟甲基克仑特罗、克仑塞罗、克仑普罗和克仑特罗具有相同的碎片离子m/z 202.9,推测是各自准分子离子峰[M+H]+,脱去H2O分子后,经结构重排失去(2-甲基丙烯)得到的特征碎片;而沙丁胺醇、西布特罗、丙卡特罗、瑞普特罗、克仑普罗等丢失离子普遍为m/z 60.2、m/z 18.0、m/z 74.3分别为脱H2O+丙烯峰、脱H2O峰和脱H2O+2-甲基丙烯峰;喹诺酮类药物主要碎裂机理为喹诺酮化合物准分子离子峰[M+H]+的脱水峰([M+H-H2O]+)、脱羧峰([M+H-CO2]+)以及脱羧后哌嗪环断裂发生结构重排失去CHR的产物离子([M+H-CO2-CHR]+),如曲伐沙星m/z 399.4、莫西沙星m/z 384.4为([M+H-H2O]+),曲伐沙星m/z 330.2、加替沙星m/z 261.2峰为([M+H-CO2-CHR]+)造成。实验选择各自准分子离子和2对强度较高的子离子以满足欧盟2002/957/EC决议中关于质谱分析法定性定量不少于4分的要求,并优化碰撞电压使其响应强度最佳。
受仪器条件所限,单一通道无法一次性进行全部74种药物的同时扫描,因此实验采用多通道模式,同时因为药物种类较多,出峰时间较为集中在2~6 min内的现象,实验对不同通道进行时间分段,保证每一种药物具有充足的扫描频率,实验还对每种药物驻留时间在0.005~0.05 ms之间进行优化,保证各色谱峰上都能达到10~12个数据采集点,确保每种药物都能得到较高的灵敏度和准确定量。
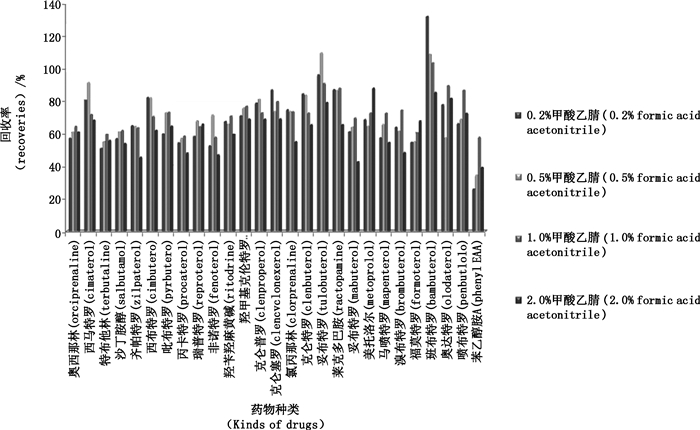
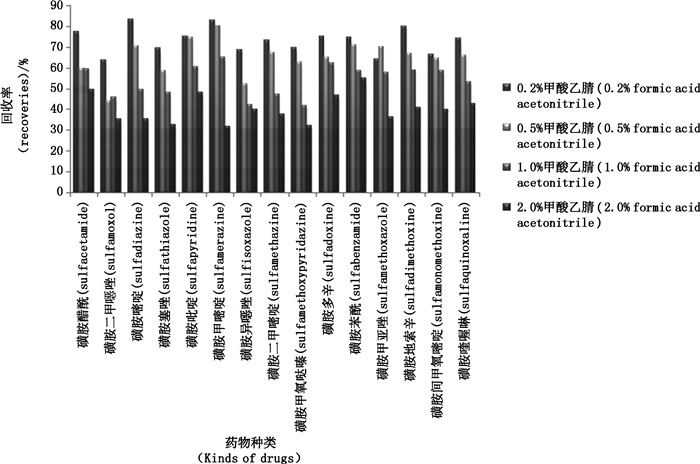
3.2 提取条件优化由于β-受体激动剂、磺胺、喹喏酮、大环内酯、苯并咪唑、镇静剂、抗病毒和截短侧耳素类共八大类药物极性及化学性质差别较大,同时提取时对提取条件要求较高,前处理专一性越强,处理方法环节越多,多种类同时提取的适应性越差,损失越严重,为了兼顾各种药物的提取回收率并结合文献方法[15-17],采用酸化有机相作为提取剂,通过空白羊奶样品添加10.0 μg·kg-1八大类混合标准溶液,比较0.2%、0.5%、1.0%、2.0%甲酸乙腈溶液为提取溶剂处理样品,经UPLC-MS/MS检测发现:酸性有机试剂提取条件下,大多数药物回收率出现先增大后减小的趋势(以β-受体激动剂为例见图 1),原因推测为随着加入甲酸量的加大,药物的离子化程度增大,其在高比例有机相中溶解性逐渐减弱,其中磺胺类药物回收率降低尤为明显(见图 2),综合各类药物回收率发现0.5%甲酸乙腈溶液提取效果较好,74种药物回收率均能达到60%以上。
|
图 1 不同提取溶剂下β-受体激动剂类药物提取回收率 Figure 1 Recoveries of β-agonists were obtained by different extraction conditions |
|
图 2 不同提取溶剂下磺胺类药物提取回收率 Figure 2 Recoveries of sulfonamides were obtained by different extraction conditions |
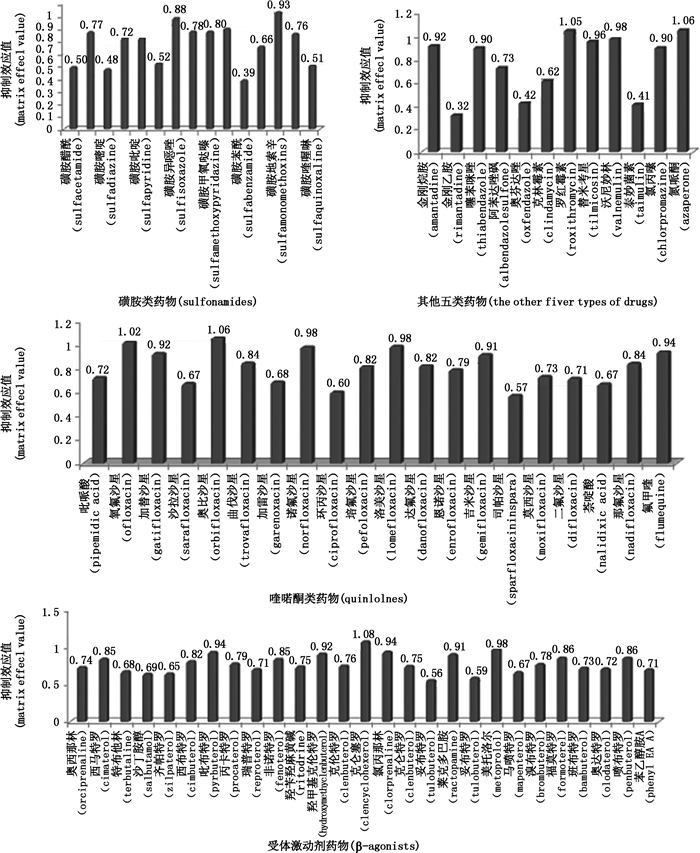
动物源性基质采用质谱进行定量分析时会存在不同程度和来源的基质效应[18-19],为评估基质效应的影响,一般会设计基质效应对照实验。本实验采取提取后添加法[20],通过测定基质效应系数(ME)来判断基质效应影响大小,若ME小于1.0,说明基质对待测物的响应产生抑制作用;若大于1.0,说明基质的存在增强效果。实验结果发现八大类药物在羊奶基质中均有不同程度的基质效应存在,其中β-受体激动剂ME在0.56~1.08之间,磺胺ME在0.39~0.93之间,喹喏酮ME在0.57~1.06之间,大环内酯、苯并咪唑、镇静剂、抗病毒和截短侧耳素类ME在0.32~1.06之间,因此在检测过程中应采用基质加标溶液,消除基质效应的影响,不同药物基质抑制程度见图 3。
|
图 3 基质效应图 Figure 3 The figure of matrix effect in goat milk |
实验采用空白羊奶样品经“2.1”项方法处理,在1.0~80.0 μg·L-1浓度范围内分别添加药物混标溶液,配制1.0、5.0、10.0、40.0、80.0 μg·L-1基质加标溶液,依次进样,以色谱峰面积为纵坐标,化合物质量浓度为横坐标做标准曲线,实验结果表明所有药物1.0~40.0 μg·L-1范围内线性良好,相关系数均大于0.991,结果见表 2。
|
|
表 2 羊奶中八大类74种药物线性范围、相关系数及定量限值 Table 2 Linear ranges, linear coefficients and the limits of quantitation of eight categories of seventy four kinds of forbidden and restricted drugs in goat milk |
将处理好的空白羊奶样品逐级添加标准溶液,按10倍信噪比确定方法的定量下限(LOQ),结果表明74种药物定量下限均小于0.5 μg·kg-1,具体见表 2。
3.5 回收率和精密度试验取空白羊奶样品,添加浓度为0.5、5.0、10.0 μg·kg-1 3个水平混标溶液,批内6次平行,不同时间重复测定3个批次,进行添加回收试验。平均回收率在61.9%~119.7%,批内RSD为1.1%~17.6%,批间RSD为2.1%~18.5%,方法的准确度及精密度满足GB/T 27404—2008技术要求。同时实验还发现当添加浓度增加到40.0 μg·kg-1时,大部分药物的回收率会出现大幅减低,推测原因为八大类药物同时添加时,前处理方法规定的提取溶剂提取不完全,造成目标化合物损失;其次添加浓度超出对应药物的线性范围造成定量不准确。
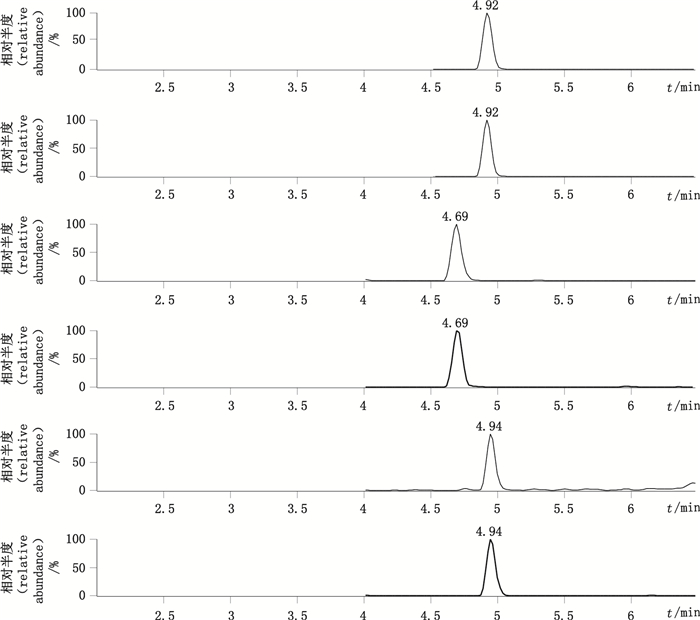
3.6 实际样品检测应用该方法对超市购买的10份羊奶样品和3份实验室盲样添加阳性羊奶样本进行测定,实验结果显示,购买的羊奶及奶粉样本中未检测到8大类药物残留,3份盲样阳性样本中,分别检出克仑特罗含量为6.3 μg·kg-1、环丙沙星15.4 μg·kg-1、金刚烷胺8.2 μg·kg-1(阳性样本图谱见图 4),与原添加浓度(克仑特罗8.0 μg·kg-1、环丙沙星20.0 μg·kg-1、金刚烷胺10.0 μg·kg-1)相比较,回收率分别为78.8%、77.0%和82.0%,符合国标中对回收率范围的要求,进一步表明该方法适用于羊奶中各类药物检测。
|
图 4 阳性样本色谱图 Figure 4 The chromatograms obtained from positive samples |
本实验通过对质谱条件和前处理过程进行优化,建立了同时检测羊奶八大类74种药物的超高效液相色谱-串联质谱方法,并对羊奶样本的基质效应的影响进行研究,并对所建方法进行了方法学验证和实际样本、盲样考核检测,验证该方法满足羊奶中多种类药物同时检测要求。该方法前处理简单高效,结果准确,适用于大批量样本中多种禁限用药物残留检测的需要,对应对动物源性产品中非法添加和保障畜产品安全具有参考作用。
| [1] |
李慕扬. 羊奶营养价值及羊奶奶酪生产研究状况[J]. 中国乳业, 2013, 133(1): 65. LI MY. Research on the nutritional value of goat milk and the production of goat cheese[J]. China Dairy, 2013, 133(1): 65. |
| [2] |
汪玉松, 邹思湘. 乳生物化学[M]. 长春: 吉林大学出版社, 1995, 3. WANG YS, ZOU SX. Milk Biochemistry[M]. Changchun: Jilin University Press, 1995, 3. |
| [3] |
厉曙光, 陈莉莉, 陈波. 我国2004-2012年媒体曝光食品安全事件分析[J]. 中国食品学报, 2014, 14(3): 1. LI SG, CHEN LL, CHEN B. The analysis of food safety incidents exposed by the media from 2004 to 2012 in China[J]. J Chin Inst Food Sci Technol, 2014, 14(3): 1. |
| [4] |
MU PQ, XU NN, CHAI TT, et al. Simultaneous determination of 14 antiviral drugs and relevant metabolites in chicken muscle by UPLC-MS/MS after QuEChERS preparation[J]. J Chromatogr B, 2016, 1023-1024: 17. DOI:10.1016/j.jchromb.2016.04.036 |
| [5] |
卢剑, 车文军, 张岩, 等. 凝胶净化色谱-固相萃取-超快速液相色谱-串联质谱法检测猪肉中9种β2-受体激动剂激素残留[J]. 食品科学, 2012, 33(24): 311. LU J, CHE WJ, ZHANG Y, et al. Determination of nine β2-agonist hormones residues in pork by GPC-SPE-RRLC-MS/MS[J]. Food Sci, 2012, 33(24): 311. DOI:10.7506/spkx1002-6630-201224068 |
| [6] |
刘洪斌, 姚喜梅, 蔡英华, 等. UPLC-MS/MS检测鸡蛋中16种磺胺类药物残留[J]. 分析试验室, 2015, 34(10): 1141. LIU HB, YAO XM, CAI YH, et al. Simultaneous determination of sixteen sulfonamides residues in eggs using liquid chromatography coupled with electrospray ionization tandem mass spectrometry[J]. Chin J Anal Lab, 2015, 34(10): 1141. |
| [7] |
LOUISE J, MAGDA TM, JULIANA BA, et al.High-throughput method for macrolides and lincosamides antibiotics residues analysis in milk and muscle using a simple liquid-liquid[J].2015, 144(1):686 http://europepmc.org/abstract/MED/26452878
|
| [8] |
GB/T 22286-2008动物源性食品中多种β-受体激动剂残留量的测定液相色谱串联质谱法[S]. 2008 GB/T 22286-2008 Determiantion of β-Agonists residues in food stuff of Animal Originby Liquid Chromatography with Tandem-Mass Spectrometric Method[S]. 2008 |
| [9] |
GB 29694-2013食品安全国家标准动物性食品中13种磺胺类药物多残留的测定高效液相色谱法[S]. 2013 GB 29694-2013 Determination of Sulfonamides Residues in Animal Derived Food by High Performance Liquid Chromatographic method[S]. 2013 |
| [10] |
GB/T 21312-2007动物源性食品中14种喹诺酮药物残留检测方法液相色谱-质谱/质谱法[S].2007 GB/T 21312-2007 Analysis of Fourteen Quinolones in Food of Animal Origin by High Performance Liquid Chromatography Tandem Mass Spectrometry[S]. 2007 |
| [11] |
JOSEPH MS, SUSAN BC, AARON S, et al. Analysis of sulfonamides, trimethoprim, fluoroquinolones, quinolones, triphenylmethane dyes and methyltestosterone in fish and shrimp using liquid chromatography-mass spectrometry[J]. J Chromatogr B, 2014, 972: 38. DOI:10.1016/j.jchromb.2014.09.009 |
| [12] |
ZHANG ZW, LI XW, DING SY, et al. Multiresidue analysis of sulfonamides, quinolones, and tetracyclines in animal tissues by ultra-high performance liquid chromatography-tandem mass spectrometry[J]. Food Chem, 2016, 204(1): 252. |
| [13] |
HOU XL, CHEN G, ZHU L, et al. Development and validation of an ultra high performance liquid chromatography tandem mass spectrometry method for simultaneous determination of sulfonamides, quinolones and benzimidazoles in bovine milk[J]. J Chromatogr B, 2014, 962: 20. DOI:10.1016/j.jchromb.2014.05.005 |
| [14] |
刘正才, 杨方, 余孔捷, 等. 超高效液相色谱-串联质谱法快速检测鳗鱼中磺胺类、喹诺酮类、四环素族抗生素药物残留[J]. 食品科学, 2009, 30(14): 167. LIU ZC, YANG F, YU KJ, et al. Simultaneous determination of qunolones, sulfonamides and tetracyclines residues in eel using solid phase extraction(SPE)and ultra-performance liquid chromatography-electrospray tandem mass spectrometry(UPLC-MS-MS)[J]. Food Sci, 2009, 30(14): 167. DOI:10.3321/j.issn:1002-6630.2009.14.031 |
| [15] |
云环, 崔凤云, 严华, 等. 超高效液相色谱-串联质谱法测定鸡肉中的利巴韦林和金刚烷胺[J]. 色谱, 2013, 31(8): 724. YUN H, CUI FY, YAN H, et al. Determiantion of ribavirin and amantadine in chicken by ultra performance liquid chromatography-tandem mass spectrometry[J]. Chin J Chromatogr, 2013, 31(8): 724. |
| [16] |
曲斌. QuEChERS在动物源性食品兽药残留检测中的研究进展[J]. 食品科学, 2013, 34(5): 327. QU B. Advances in application of QuEChERS for detection of veterinary drug residues in animal-derived foods[J]. Food Sci, 2013, 34(5): 327. |
| [17] |
李锋格, 苏敏, 李晓岩, 等. 分散固相萃取-超高效液相色谱-串联质谱法测定鸡肝中磺胺类、喹诺酮类和苯并咪唑类药物及其代谢物的残留量[J]. 色谱, 2011, 29(2): 120. LI FG, SU M, LI XY, et al. Determination of sulfonamides, quinolones, benzimidazoles and the metabolites of benzimidazoles in chicken livers by dispersive solid-phase extraction and ultra performance liquid chromatography-tandem mass spectrometry[J]. Chin J Chromatogr, 2011, 29(2): 120. |
| [18] |
王立琦, 贺利民, 曾振灵, 等. 液相色谱-串联质谱检测兽药残留中的基质效应研究进展[J]. 质谱学报, 2011, 32(6): 322. WANG LQ, HE LM, ZENG ZL, et al. Progress in matrix effect of veterinary drug residues analysis by high-performance liquid chromatography tandem mass spectrometry[J]. J Chin Mass Spectrom Soc, 2011, 32(6): 322. |
| [19] |
向平, 沈敏, 卓先义. 液相色谱-质谱分析中的基质效应[J]. 分析测试学报, 2009, 28(6): 753. XIANG P, SHEN M, ZHUO XY. Matrix effects in liquid chromatographic-mass spectrometric Analysis[J]. J Instrum Anal, 2009, 28(6): 753. |
| [20] |
MATUSZEWKI BK, CONSTANZER ML, CHAVEZ-ENG CM. Strategies for the assessment of matrix effect in quantitative bioanalytical methods based on HPLC-MS/MS[J]. Anal Chem, 2003, 75(1): 3019. |
 2018, Vol. 38
2018, Vol. 38 

 唑
唑