2. 河北省药品检验研究院, 石家庄 050011
2. Hebei Institute for Drug Control, Shijiazhuang 050011, China
麻杏止咳糖浆来源于后汉名医张仲景《伤寒论》中的麻杏石甘汤方剂,是由麻黄、苦杏仁、石膏、甘草(炙)4味药材加工而成的复方制剂,具有镇咳、平喘、祛痰的功效,主要用于治疗支气管炎咳嗽及喘息等症[1-3]。其现行质量标准有2个,分别收载于《卫生部药品标准》中药成方制剂第20册[4]和《国家药品监督管理局药品标准》(内科肺系二)[5]。前者无含量测定项,仅有盐酸麻黄碱的薄层色谱鉴别,后者虽然设定了盐酸麻黄碱的含量测定项,但供试品溶液的制备方法复杂,2个标准内容过于简单,均不能达到对麻杏止咳糖浆制剂质量进行有效控制的目的。本文在文献报道方法[6-8]的基础上建立了简单易行,准确度高的测定方法,可同时测定麻杏止咳糖浆中盐酸麻黄碱、盐酸伪麻黄碱、苦杏仁苷、甘草苷、甘草酸的含量,为麻杏止咳糖浆的质量控制提供技术支持。
1 仪器与试药 1.1 仪器Waters e2695高效液相色谱仪,四元泵,2998检测器(Waters公司);UPLC-XevoTM TQ-S液质联用仪,Masslynx数据处理系统(Waters公司);AE-240电子分析天平(METTLER TOLEDO公司);超纯水仪(Millipore公司)。
1.2 试药盐酸麻黄碱(批号171241-201007)、盐酸伪麻黄碱(批号171237-201208)、苦杏仁苷(批号110820-201607)、甘草苷(批号111610-201607)、甘草酸铵(批号110731-201619)均购自中国食品药品检定研究院,含量均在98%以上;甲醇、乙腈(色谱纯,Merck公司),水为超纯水,磷酸、磷酸二氢钾(分析纯,国药集团化学试剂有限公司);麻杏止咳糖浆样品为河北康芝制药有限公司生产。
2 方法与结果 2.1 色谱条件色谱柱:Thermo C18(250 mm×4.6 mm,5 μm);流动相:以乙腈为流动相A,以0.02 mol·L-1磷酸二氢钾溶液(含0.1%三乙胺+0.1%磷酸)为流动相B,梯度洗脱,洗脱程序见表 1;流速:1.0 mL·min-1;柱温:25 ℃;检测波长:210 nm(麻黄碱、伪麻黄碱、苦杏仁苷)、237 nm(甘草苷、甘草酸);进样量:10 μL。
|
|
表 1 梯度洗脱条件 Table 1 Conditions of gradient elution |
精密称取盐酸麻黄碱、盐酸伪麻黄碱、苦杏仁苷、甘草苷、甘草酸铵的对照品适量,分别置于50 mL量瓶中,用甲醇溶解并定容,制得盐酸麻黄碱质量浓度为0.999 0 mg·mL-1,盐酸伪麻黄碱质量浓度为0.439 1 mg·mL-1,苦杏仁苷质量浓度为1.199 mg·mL-1,甘草苷质量浓度为0.327 2mg·mL-1,甘草酸铵质量浓度为0.679 1 mg·mL-1的单一成分对照品储备液,低温保存。分别精密吸取上述5个化合物储备液依次为10、10、10、15、10 mL至同一100 mL量瓶中,用甲醇定容至刻度,配制成质量浓度分别为99.9、43.9、119.9、49.0、67.9 μg·mL-1的混合对照品溶液。
2.2.2 供试品溶液精密量取样品10 mL,置50 mL量瓶中,加80%甲醇水稀释至刻度,摇匀,滤过,取续滤液,即得。
2.2.3 阴性样品溶液按照《中药成方制剂》第20册麻杏止咳糖浆质量标准中规定的处方工艺,分别制备不含麻黄药材的阴性样品、不含苦杏仁药材的阴性样品、不含甘草药材的阴性样品。按“2.2.2”项下方法制备阴性样品溶液。
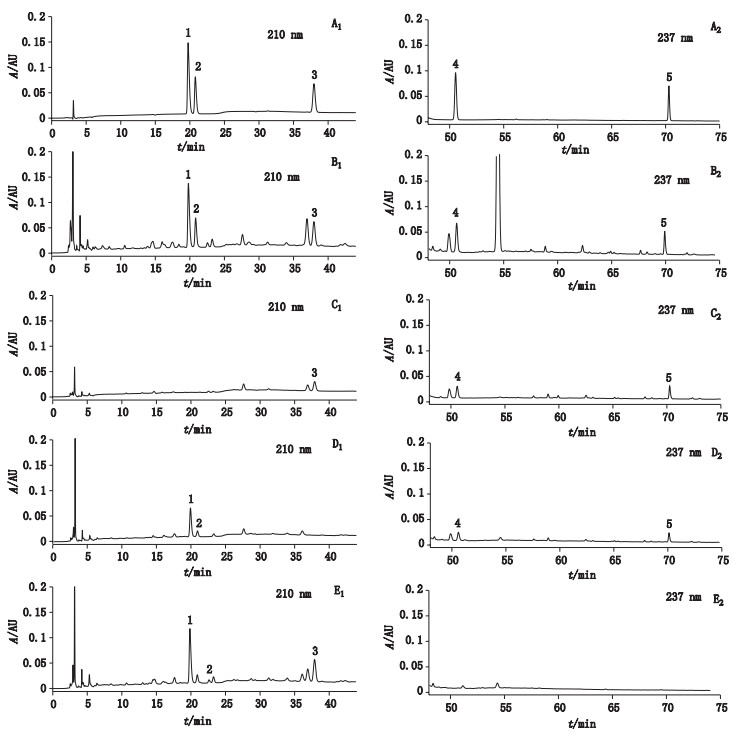
2.3 专属性试验分别取“2.2”项下混合对照品溶液、供试品溶液、阴性对照溶液各10 μL,按“2.1”项下色谱条件进样测定,色谱图见图 1。由图可知,其分离度较好;阴性样品色谱图中,在与对照品色谱峰相应的位置上无色谱峰出现,表明处方中的其他药味对测定成分无干扰,专属性良好。
|
1.麻黄碱(ephedrine) 2.伪麻黄碱(pseudo ephedrine) 3.苦杏仁苷(amygdalin) 4.甘草苷(glycyrrhizin) 5.甘草酸(glycyrrhizic acid) A1、A2.混合对照品(mixed reference substances) B1、B2.麻杏止咳糖浆(Maxing Zhike syrup) C1、C2.缺麻黄阴性样品(negative samples without Ephedrae Herba) D1、D2.缺苦杏仁阴性样品(negative samples without Armeniacae Semen Amarum) E1、E2.缺甘草阴性样品(negative samples without Glycyrrhizae Radix et Rhizoma) 图 1 麻杏止咳糖浆HPLC图谱 Figure 1 HPLC chromatograms of Maxing Zhike syrup |
分别精密吸取各对照品储备液稀释10倍后的溶液1、2、5、10 μL和各对照品储备液1、2、5、10 μL,按“2.1”项下色谱条件进样测定。以进样量(X,μg)为横坐标,峰面积值(Y)为纵坐标绘制标准曲线,进行线性回归,结果见表 2,表明各成分线性关系良好。
|
|
表 2 线性关系考察结果 Table 2 Results of linear relationship |
精密吸取麻杏止咳糖浆供试品溶液10 μL,按照“2.1”项下色谱条件连续进样6次,结果麻黄碱、伪麻黄碱、苦杏仁苷、甘草苷、甘草酸峰面积的RSD分别为0.68%、0.50%、0.65%、0.39%、0.38%,表明本方法具有良好的精密度。
2.6 稳定性试验取麻杏止咳糖浆供试品溶液按“2.1”项下色谱条件,分别在0、3、6、9、15、21、24 h进样测定,结果麻黄碱、伪麻黄碱、苦杏仁苷、甘草苷、甘草酸峰面积的RSD分别为0.31%、1.4%、0.96%、0.41%、1.0%,表明供试品溶液在24 h内稳定。
2.7 重复性试验取同一批样品5、10、15 mL各3份,制备供试溶液,按“2.1”项下色谱条件进行测定,盐酸麻黄碱、盐酸伪麻黄碱、苦杏仁苷、甘草苷、甘草酸平均含量分别为0.497、0.218、0.539、0.150、0.309 mg·mL-1,RSD分别为0.24%、0.37%、1.2%、0.33%、0.59%。结果表明,本方法重复性良好。
2.8 回收率试验精密量取已知含量的样品(盐酸麻黄碱0.497 mg·mL-1,盐酸伪麻黄碱0.218 mg·mL-1,苦杏仁苷含量为0.539 mg·mL-1,甘草苷含量为0.150 mg·mL-1,甘草酸含量为0.309 mg·mL-1)5 mL共9份,每3份为一组,分别加入低、中、高3个浓度的混合对照品溶液一定量,按“2.2.2”项下方法制备供试溶液。按“2.1”项下色谱条件进样测定,计算回收率。结果见表 3,表明回收率良好。
|
|
表 3 加样回收率结果 Table 3 Results of recovery |
取3批麻杏止咳糖浆各2份,分别按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件进行测定,并用外标法计算样品中5个成分的含量,结果见表 4。
|
|
表 4 麻杏止咳糖浆中5个成分的测定结果(mg·mL-1) Table 4 Determination of five components in Maxing Zhike syrup |
本研究建立了麻杏止咳糖浆中5个成分的HPLC测定方法,该方法高效,分离度好,结果准确,阴性无干扰,具有良好的精密度、稳定性和重复性。
3.1 检测波长的确定对盐酸麻黄碱、盐酸伪麻黄碱、苦杏仁苷、甘草苷、甘草酸5个成分的甲醇溶液进行全波长扫描,结果显示麻黄碱、伪麻黄碱、苦杏仁苷检测波长集中在210 nm附近,所以选择在210 nm波长下测定;甘草苷、甘草酸的检测波长参照《中华人民共和国药典》2015年版一部甘草项下的含量测定方法,最终选择237 nm。
3.2 流动相的选择实验中遇到麻黄碱、伪麻黄碱峰形拖尾的问题,且苦杏仁苷与其紧邻未知物的峰分离度难以达到要求,本文参考文献[9-14],首先尝试了采用甲醇-水、乙腈-水、乙腈-0.1%磷酸水、甲醇-乙腈-0.1%磷酸水等流动相进行试验,效果不理想。其次改用乙腈-0.1%磷酸(0.1%三乙胺),结果麻黄碱、伪麻黄碱峰形拖尾现象有改善,但是苦杏仁苷的峰依旧没有分开;之后又尝试乙腈-0.02 mol·L-1磷酸二氢钾溶液(0.1%三乙胺)作为流动相,结果分离效果明显改善。在上述基础上经过多次试验,发现加入0.1%磷酸调节pH,可以得到理想的分离效果。
3.3 技术难点分析本实验难点在于苦杏仁苷峰与其相邻未知峰的分离,因此通过UPLC-MS/MS对该未知峰进行了分析,结果表明,此未知峰和苦杏仁苷的一级和二级碎片图谱完全相同,推测此未知物可能为苦杏仁苷的同分异构体。
3.4 小结运用本文方法对麻杏止咳方其他剂型(麻杏止咳片、麻杏止咳胶囊、麻杏止咳颗粒)进行检测,结果盐酸麻黄碱、盐酸伪麻黄碱、苦杏仁苷、甘草苷、甘草酸5个成分都能达到很好分离;经过方法学验证,结果表明该方法也适用于上述剂型的质量控制。本文制订的方法可有效提高麻杏止咳系列制剂的质量控制水平,为其质量标准的进一步修订提供了依据。
| [1] |
翟文生. 从儿科麻杏石甘汤的临床应用看《伤寒论》的方证特点[J]. 中国中西医结合儿科学, 2009, 1(1): 27. QU WS. Study on the syndrome characteristics of treatise on febrile diseases from the clinical application of Maxing Shigan decoction[J]. Chin Pediatr Integr Tradit West Med, 2009, 1(1): 27. |
| [2] |
刘威, 何晓红, 张晓宇, 等. 麻杏石甘汤现代药理研究[J]. 中国实用医药, 2007, 2(6): 7. LIU W, HE XH, ZHANG XY, et al. Modern pharmacological research of Maxing Shigan decoction[J]. China Pract Med, 2007, 2(6): 7. |
| [3] |
马以泉, 王仁忠, 曹灵勇. 麻杏石甘汤药理作用研究[J]. 中国药业, 2005, 14(4): 32. MA YQ, WANG RZ, CAO LY, et al. Study on the pharmacological action of Maxing Shigan decoction[J]. China Pharm, 2005, 14(4): 32. |
| [4] |
国家药品标准. 中药成方制剂. 第二十册[S]. 2004 Drug Specifications Promulgated by Ministry of Public Health, P. R. China. Chinese Medicines Formula Preparation. Vol 20[S]. 2004 |
| [5] |
国家药品监督管理局. 国家中成药标准汇编内科肺系(二)分册[M]. 北京: 人民卫生出版社, 2002, 263. State Drug Administration. Proprietary Chinese Medicine Standards of the State Assembly the Archies of Internal Medicine Lung Department (2) the Intern[M]. Beijing: People's Medical Publishing House, 2002, 263. |
| [6] |
李冬梅, 庄爱爱, 苏建, 等. 麻杏止咳糖浆含量测定方法研究[J]. 中国药业, 2017, 26(12): 27. LI DM, ZHUANG AA, SU J, et al. Content determination of Maxing Zhike syrup[J]. China Pharm, 2017, 26(12): 27. DOI:10.3969/j.issn.1006-4931.2017.12.007 |
| [7] |
李焕丹, 陈哲琼, 宋粉云. HPLC法测定小儿清热止咳口服液中苦杏仁苷的含量[J]. 齐鲁药事, 2011, 30(9): 503. LI HD, CHEN ZQ, SONG FY. Determination of amygdalin in Xiaoer Qingre Zhike oral liquid by HPLC[J]. Qilu Pharm Aff, 2011, 30(9): 503. |
| [8] |
郭明晔, 张燕玲, 李洋, 等. HPLC法同时测定甘草及甘草头中4种成分的含量[J]. 世界科学技术-中医药现代化, 2014, 16(2): 358. GUO MY, ZHANG YL, LI Y, et al. Simultaneous determination of four constituents in roots and knotty rhizome of Glycyrrhiza uralensis by HPLC[J]. Mod Tradit Chin Med Mater Med World Sci Technol, 2014, 16(2): 358. DOI:10.11842/wst.2014.02.026 |
| [9] |
吕建豪, 张海平, 高小川, 等. HPLC法测定麻杏止咳片中盐酸麻黄碱和盐酸伪麻黄碱的含量[J]. 中药材, 2015, 38(12): 2626. LÜ JH, ZHANG HP, GAO XC, et al. Determination of ephedrine and pseudo ephedrine in Maxing Zhike syrup by HPLC[J]. J Chin Med Mater, 2015, 38(12): 2626. |
| [10] |
贺颖, 王志萍. HPLC法同时测定麻杏石甘汤剂中盐酸麻黄碱和苦杏仁苷含量[J]. 中华中医药杂志, 2013, 28(9): 2778. HE Y, WANG ZP. HPLC simultaneous determinations of ephedrine hydrocholoride and amygdalin in Maxing Shigan decoction[J]. China J Tradit Chin Med Pharm, 2013, 28(9): 2778. |
| [11] |
李翔, 刘皈阳, 马建丽, 等. HPLC法测定麻杏口服液中盐酸麻黄碱和盐酸伪麻黄碱的含量[J]. 药物分析杂志, 2014, 34(1): 190. LI X, LIU GY, MA JL, et al. HPLC determination of ephedrine hydrochloride and pseudoephedrine hydrochloride in the Maxing oral solution[J]. Chin J Pharm Anal, 2014, 34(1): 190. |
| [12] |
刘孝峰. HPLC法同时测定定喘止咳糖浆中5种成分的含量[J]. 实用药物与临床, 2016, 19(2): 219. LIU XF. Simultaneous determination of amygdalin, honokiol, magnolol, hesperidin and nobi-letin in Dingchuan Zhike syrups by HPLC[J]. Pract Pharm Clin Rem, 2016, 19(2): 219. |
| [13] |
罗培和, 朱其琼. HPLC法测定麻杏止咳糖浆中苦杏仁苷的含量[J]. 化工技术与开发, 2014, 43(2): 42. LUO PH, ZHU QQ. Determination of amygdalin in Maxing cough syrup by HPLC[J]. Chem Technol Dev, 2014, 43(2): 42. |
| [14] |
杨德斌, 仝燕, 马振山, 等. HPLC法同时测定小儿平喘祛痰颗粒中盐酸麻黄碱、盐酸伪麻黄碱、苦杏仁苷含量[J]. 中国中药杂志, 2013, 38(5): 687. YANG DB, TONG Y, MA ZS, et al. Simultaneous determination of ephedrine hydrochloride, pseudoephedrine hydrochloride and amygdalin in Xiao'er Pingchuan Qutan granules by HPLC[J]. China J Chin Mater Med, 2013, 38(5): 687. |
 2018, Vol. 38
2018, Vol. 38 
