2. 广东药科大学医药化工学院, 中山 528458
2. Medical Institute of Chemical Industry, Guangdong Pharmaceutical University, Zhongshan 528458, China
麝香心脑乐片是由红花、葛根、丹参、三七、淫羊藿、郁金、冰片、麝香、人参茎叶总皂甙9味中药合理组方制成的糖衣片,具有改善血管内皮功能、延缓动脉粥样硬化进程、抑制内膜增殖及再狭窄、缓解血管痉挛、保护再灌后微血管结构和功能完整性、抑制心室重构、缩小心肌梗死面积、改善心功能的作用,可活血化瘀、开窍止痛,主要用于冠心病、心绞痛、心肌梗塞、脑血栓等疾病的治疗。宋春华等[1]观察麝香心脑乐片治疗冠心病心绞痛的临床疗效,423例患者随机按照3:1的比例分为治疗组和对照组,以心可舒片为对照药物,采用随机、仿盲、多中心的方法进行对比研究,数据结果显示治疗组对胸痛、胸闷、心悸、痛引肩背症状疗效优于对照组;王琳等[2]通过结扎犬冠状动脉前降支制备急性心肌梗死模型,采用心外膜电图标测法、定量组织学法、血液生化学法、电镜法等方法,观察麝香心脑乐片对犬急性心肌缺血的影响,实验结果显示麝香心脑乐片可明显减轻缺血程度、减少缺血范围、缩小心肌梗死面积、显著降低血清乳酸脱氢酶和肌酸磷酸激酶含量。
该制剂收载于中药成方制剂第十三册,麝香心脑乐片标准中仅规定了性状及简单的理化鉴别,未对方中的任何成分进行定量研究[3]。本文采用HPLC波长切换法,同时对方中红花[4]、葛根[4]和丹参[4]中的羟基红花黄色素A、3′-羟基葛根素、葛根素、3′-甲氧基葛根素、丹参素、丹酚酸B和丹参酮ⅡA进行同时测定,样品处理方法简便,测定结果准确,为麝香心脑乐片质量的全面评价提供了科学依据。
1 材料 1.1 仪器Agilent 1200高效液相色谱仪(含真空脱气单元、泵、进样器、柱温箱、检测器、电脑工作站)(美国安捷伦公司);AUW220D型电子天平(日本岛津);KQ-250DB型超声波清洗器(昆山市超声仪器有限公司)。Hypersil BDS C18色谱柱(250 mm×4.6 mm,5 μm;填料:十八烷基硅烷键合硅胶;生产厂家:大连依利特分析仪器有限公司)。
1.2 药品与试剂羟基红花黄色素A对照品(111637-201609,含量91.9%,冷冻保存,本品具有引湿性,打开后一次性使用完毕)、葛根素对照品(110752-201514,含量95.5%,2~10 ℃冷处保存)、丹酚酸B对照品(111562-2016153,含量96.2%,冷冻保存,本品极具引湿性,建议打开包装一次性使用完毕)、丹参酮ⅡA对照品(110766-201520,含量98.9%)均购自中国食品药品检定研究院;3′-羟基葛根素对照品(117076-54-5,2-8 ℃避光保存)、3′-甲氧基葛根素对照品(117047-07-1,含量98.0%,2~8 ℃密闭避光保存)购自成都瑞芬思生物科技有限公司;丹参素对照品(76822-21-4,含量98.0%)购自宝鸡市辰光生物有限公司;麝香心脑乐片(批号见表 3)购于吉林亚泰明星制药有限公司;乙腈为色谱纯,甲醇、磷酸为分析纯。
2 方法与结果 2.1 色谱条件采用Hypersil BDS C18色谱柱(250 mm×4.6 mm,5 μm);体积流量:0.9 mL·min-1;柱温:35 ℃;进样量为10 μL;流动相A:乙腈,流动相B:0.4%磷酸溶液,梯度洗脱(洗脱程序见表 1);检测波长:403 nm[5-6](0~20 min检测羟基红花黄色素A)、250 nm[7-9](20~33 min检测3′-羟基葛根素、葛根素和3′-甲氧基葛根素)、280 nm[10-11](33~55 min检测丹参素、丹酚酸B和丹参酮ⅡA)。
|
|
表 1 梯度洗脱程序 Table 1 Gradient elution program |
分别精密称取对照品羟基红花黄色素A、3′-羟基葛根素、葛根素、3′-甲氧基葛根素、丹参素、丹酚酸B和丹参酮ⅡA各适量,用70%甲醇分别制成含羟基红花黄色素A 0.396 mg·mL-1、3′-羟基葛根素0.572 mg·mL-1、葛根素1.228 mg·mL-1、3′-甲氧基葛根素0.434 mg·mL-1、丹参素0.410 mg·mL-1、丹酚酸B 2.136 mg·mL-1、丹参酮ⅡA 0.424 mg·mL-1的单一成分对照品储备液。
2.2.2 混合对照品溶液分别依次量取单一成分对照品储备液适量,用70%甲醇制成含羟基红花黄色素A 0.019 8 mg·mL-1、3′-羟基葛根素0.028 6 mg·mL-1、葛根素0.061 4 mg·mL-1、3′-甲氧基葛根素0.021 7 mg·mL-1、丹参素0.008 2 mg·mL-1、丹酚酸B 0.106 8 mg·mL-1、丹参酮ⅡA 0.021 2 mg·mL-1的混合对照品溶液。
2.3 供试品溶液的制备取麝香心脑乐片适量,除去糖衣后,研成细粉,取约0.3 g,精密称定,精密加70%甲醇50 mL,密塞,称量,超声提取30 min,放冷至室温,用70%甲醇补足减失的量,振摇均匀,过滤,即得麝香心脑乐片供试品溶液。
2.4 阴性样品溶液的制备按中药成方制剂第十三册麝香心脑乐片质量标准项下处方比例,分别称取除红花、葛根和丹参外的其他8味药材各1份,按照麝香心脑乐片制备工艺和麝香心脑乐片供试品溶液的配制方法,制备红花阴性样品溶液、葛根阴性样品溶液和丹参阴性样品溶液。
2.5 方法学验证 2.5.1 线性关系考察精密吸取上述对照品储备液0.1、0.2、0.5、1.0、1.5、2.0 mL,分别用甲醇稀释至20 mL,振摇均匀,得20倍浓度差的6个系列浓度的混合对照品溶液,依法测定,以所测成分羟基红花黄色素A、3′-羟基葛根素、葛根素、3′-甲氧基葛根素、丹参素、丹酚酸B和丹参酮ⅡA的质量浓度X为横坐标,峰面积Y为纵坐标,绘制标准曲线,得回归方程,结果见表 2。
|
|
表 2 线性关系实验结果 Table 2 The results of the linear relationship test |
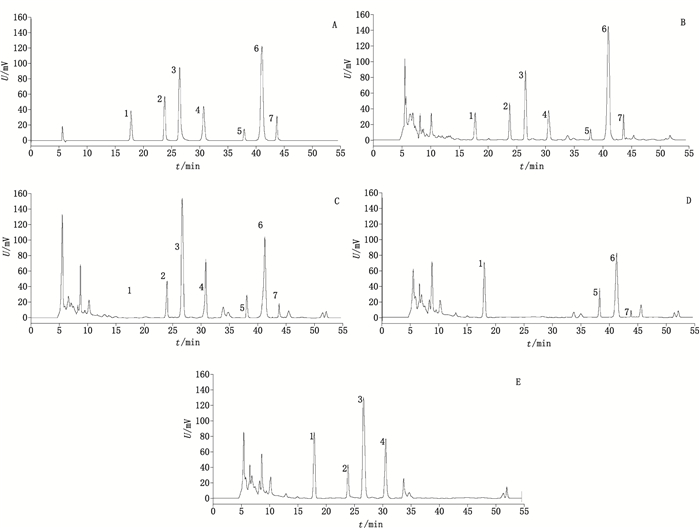
分别取上述3种阴性样品溶液、混合对照品溶液和供试品溶液,依法测定。试验结果显示,阴性样品溶液的色谱图中,在所测羟基红花黄色素A、3′-羟基葛根素、葛根素、3′-甲氧基葛根素、丹参素、丹酚酸B和丹参酮ⅡA 7个成分对应的位置无干扰,色谱图见图 1。
|
1.羟基红花黄色素A(hydroxysafflor yellow A)2.3′-羟基葛根素(3′-hydroxy puerarin)3.葛根素(puerarin)4.3′-甲氧基葛根素(3′-methoxy puerarin)5.丹参素(danshensu)6.丹酚酸B(salvianolic acid B)7.丹参酮ⅡA(tanshinone ⅡA) A.混合对照品未释出(reference substance)B.样品未释出(samples)C.红花阴性样品未释出(negative sample of Carthami Flos)D.葛根阴性样品未释出(negative sample of Puerariae Lobatae Radix)E.丹参阴性样品未释出(negative sample of Salviae Miltiorrhizae Radix et Rhizoma) 图 1 HPLC波长切换色谱图 Figure 1 Chromatogram of HPLC wavelength switching method |
取上述混合对照品溶液,依法连续进样6次,记录羟基红花黄色素A、3′-羟基葛根素、葛根素、3′-甲氧基葛根素、丹参素、丹酚酸B和丹参酮ⅡA的峰面积,分别计算这7个组分峰面积的RSD,其RSD依次为0.96%、0.83%、0.65%、1.0%、1.1%、0.58%和1.1%。
2.5.4 重复性试验取麝香心脑乐片(批号:20150801),按上述供试品溶液制备方法制备供试品溶液6份,依法测定,分别计算羟基红花黄色素A、3′-羟基葛根素、葛根素、3′-甲氧基葛根素、丹参素、丹酚酸B和丹参酮ⅡA的含量,并计算所测7个组分含量的RSD,结果7个组分的平均含量分别为2.98、4.16、12.02、3.27、1.62、21.19、3.11 mg·g-1,RSD依次为1.5%、0.68%、1.1%、1.4%、0.75%、1.0%和0.60%。
2.5.5 稳定性考察取麝香心脑乐片同一供试品溶液,在室温下放置0、2、4、6、8、12 h后依法进样测定,记录羟基红花黄色素A、3′-羟基葛根素、葛根素、3′-甲氧基葛根素、丹参素、丹酚酸B和丹参酮ⅡA的峰面积,并求得这7个组分峰面积的RSD分别为1.0%、0.92%、0.70%、1.0%、1.1%、0.62%和0.91%。结果显示麝香心脑乐片供试品溶液在室温下放置12 h内稳定。
2.5.6 加样回收率试验分别精密称取对照品羟基红花黄色素A、3′-羟基葛根素、葛根素、3′-甲氧基葛根素、丹参素、丹酚酸B和丹参酮ⅡA适量,用70%甲醇分别溶解并稀释制成含羟基红花黄色素A、3′-羟基葛根素、葛根素、3′-甲氧基葛根素、丹参素、丹酚酸B和丹参酮ⅡA为0.441、0.625、0.601、0.487、0.246、0.642、0.464 mg·mL-1单一成分对照品溶液,备用。取麝香心脑乐片(批号:20150801)6份,除去糖衣,研成细粉,每份约0.15 g,精密称定,精密加入上述各备用对照品溶液适量,再按照上述供试品溶液制备方法制备加样回收样品溶液。依法测定羟基红花黄色素A、3′-羟基葛根素、葛根素、3′-甲氧基葛根素、丹参素、丹酚酸B和丹参酮ⅡA的含量,计算这7个组分的回收率及RSD,结果见表 3。
|
|
表 3 回收率实验结果 Table 3 Results of recovery test |
取3批麝香心脑乐片,按“2.3”项下方法制备供试品溶液,在上述色谱条件下分别进样测定羟基红花黄色素A、3′-羟基葛根素、葛根素、3′-甲氧基葛根素、丹参素、丹酚酸B和丹参酮ⅡA的含量,结果见表 4。
|
|
表 4 含量测定结果(n=3,mg·g-1) Table 4 Results of content determination |
采用HPLC波长切换法对3批麝香心脑乐片中的羟基红花黄色素A、3′-羟基葛根素、葛根素、3′-甲氧基葛根素、丹参素、丹酚酸B和丹参酮ⅡA同时进行了定量测定。3批含量结果及方法学验证结果表明,结果采用HPLC波长切换方法对3批麝香心脑乐片中的羟基红花黄色素A、3′-羟基葛根素、葛根素、3′-甲氧基葛根素、丹参素、丹酚酸B和丹参酮ⅡA是科学可行的,且操作简便,准确度高,专属性强。
3.2 提取方式、提取溶剂及提取时间的确定分别考察了不同的提取方式(超声处理提取、水浴加热回流提取)、提取溶剂(甲醇、70%甲醇、40%甲醇、乙醇)及提取时间(20、30、40 min)对麝香心脑乐片中羟基红花黄色素A、3′-羟基葛根素、葛根素、3′-甲氧基葛根素、丹参素、丹酚酸B和丹参酮ⅡA提取率的影响,实验结果表明,采用超声提取和加热回流提取效果相当,但超声提取更加便捷;70%甲醇提取效果最好;30 min和40 min的提取效果相当,但部分所测成分明显高于20 min的提取效果。综合考虑,最终确定麝香心脑乐片供试品溶液制备方法为70%甲醇超声提取30 min。
3.3 流动相的考察分别考察了甲醇-水相、乙腈-水、甲醇-0.1%甲酸溶液[8, 12]、乙腈-0.1%甲酸溶液[10, 13]、乙腈-0.4%甲酸溶液[6]、乙腈-0.4%磷酸溶液等流动相体系[5],以色谱峰的基线平稳情况、所测各成分的峰形和分离效果为指标,优选出最佳的流动相体系为:乙腈-0.4%磷酸溶液,按照文中的梯度洗脱比例分离效果好,峰形也较好。
3.4 小结中成药复方制剂所含组分复杂,各成分的最大吸收波长不同,当采用某一固定波长时,难以确保所测各成分被检出或获得最大吸收,影响定量测定结果。波长切换技术能够满足不同最大吸收波长的物质同时检测,使得不能在同一波长下测定的物质在一次检测分析中同时出峰,提高了检测灵敏度,减少了干扰,缩短了分析时间。本文采用HPLC波长切换技术实现了对麝香心脑乐片中7个主要成分含量的同时测定,所测各成分达到了有效分离,方法专属性强,样品溶液稳定性好,为麝香心脑乐片质量的全面评价提供了科学依据。
| [1] |
宋春华, 刘爱东, 邓悦. 麝香心脑乐片治疗冠心病心绞痛423例[J]. 辽宁中医杂志, 2008, 35(4): 567. SONG CH, LIU AD, DENG Y. Effect of Shexiang Xinnaole tablets in treating 423 patients with coronary heart disease angina pectoris[J]. Liaoning J Tradit Chin Med, 2008, 35(4): 567. |
| [2] |
王琳, 李伟, 付萍, 等. 麝香心脑乐片对犬急性心肌缺血影响的实验研究[J]. 中国老年学杂志, 2009, 29(6): 688. WANG L, LI W, FU P, et al. Experimental study on effect of Shexiang Xinnaole tablets on acute myocardial ischemia in dogs[J]. Chin J Gerontol, 2009, 29(6): 688. |
| [3] |
卫生部药品标准. 中药成方制剂第十三册[S]. 1997: 229 Drug Specifications Promulgated by The Ministry of Public Health. PR China. Traditional Chinese Medicine Drugs Preparation Vol 13[S]. 1997: 229 |
| [4] |
中国药典2015年版一部[S]. 2015: 76, 151, 333 ChP 2015. Vo l[S]. 2015: 76, 151, 333 |
| [5] |
姚苗苗, 任爱农, 董仲才. RP-HPLC法同时测定红花中羟基红花黄色素A与红花黄色素A的含量[J]. 药物分析杂志, 2010, 30(2): 263. YAO MM, REN AN, DONG ZC. RP-HPLC determination of safflomin A and safflower yellow A in Carthamus tinctorius L.[J]. Chin J Pharm Anal, 2010, 30(2): 263. |
| [6] |
周思多, 王晓, 杨洪军, 等. 红花药材中四种化学成分的高效液相色谱双波长法同时测定[J]. 时珍国医国药, 2014, 25(11): 2595. ZHOU SD, WANG X, YANG HJ, et al. Simultaneous determination of four chemical components in Carthamus tinctorius L.by HPLC double wavelength method[J]. Lishizhen Med Mater Med Res, 2014, 25(11): 2595. |
| [7] |
姜兰芳, 周光明, 李艳艳. 胶束萃取-高效液相色谱法同时测定葛根粉中5种异黄酮[J]. 食品科学, 2011, 32(6): 186. JIANG LF, ZHOU GM, LI YY. Simultaneous determination of isoflavonoids in Kudzu powder by high performance liquid chromatography coupled with micelle-mediated extraction[J]. Food Scie, 2011, 32(6): 186. |
| [8] |
赵路, 路丽, 王淑美, 等. UPLC法同时测定不同产地葛根中5种活性成分的含量[J]. 中药材, 2015, 38(3): 473. ZHAO L, LU L, WANG SM, et al. Simultaneous determination of five active components in Puerariae Lobatae Radix from different habitats by UPLC[J]. J Chin Med Mater, 2015, 38(3): 473. |
| [9] |
李丽莉, 吕轶峰, 朱雪妍. 葛根芩连片多成分含量测定的研究[J]. 药物分析杂志, 2017, 37(9): 1607. LI LL, LÜ YF, ZHU XY. Determination of multiple components in Gegen Qinlian tablets[J]. Chin J Pharm Anal, 2017, 37(9): 1607. |
| [10] |
翟学佳, 徐锦凤. 丹参药材水溶性和脂溶性成分的含量[J]. 医药导报, 2009, 28(10): 1345. ZHAI XJ, XU JF. Simultaneous determination of hydrophilic and hipophilic compounds in Radix Salviae Miltiorrhizae by HPLC[J]. Her Med, 2009, 28(10): 1345. DOI:10.3870/yydb.2009.10.045 |
| [11] |
周国军, 李焱, 秦民坚, 等. 高效液相色谱法快速测定丹参中5种活性成分的含量[J]. 药物分析杂志, 2012, 32(8): 1357. ZHOU GJ, LI Y, QIN MJ, et al. Fast determination of 5 constituents in Radix et Rhizoma Salviae Miltiorrhizae by HPLC[J]. Chin J Pharm Anal, 2012, 32(8): 1357. |
| [12] |
支旭然, 刘洪涛, 吴茵, 等. UPLC-MS/MS法同时测定肾康注射液中7个有效成分[J]. 药物分析杂志, 2017, 37(1): 37. ZHI XR, LIU HT, WU Y, et al. Simultaneous determination of 7 active constituents in Shenkang injection by UPLC-MS/MS[J]. Chin J Pharm Anal, 2017, 37(1): 37. |
| [13] |
周霖, 姜晓芳, 左莉华, 等. 基于质谱-主成分分析法的冠心丹参胶囊中10个活性成分含量测定及质量评价研究[J]. 药物分析杂志, 2017, 37(10): 1824. ZHOU L, JIANG XF, ZUO LH, et al. Quantitative and quality evaluation research of principal active components in Guanxi Danshen capsules by MS-principal component analysis[J]. Chin J Pharm Anal, 2017, 37(10): 1824. |
 2018, Vol. 38
2018, Vol. 38 