利多卡因具有较强的组织弥漫性能和粘膜穿透力[1],通过抑制产生和传导兴奋波所需的离子流,稳定神经膜,从而产生局部麻醉作用,同时对局部组织无刺激,局部血管扩张不明显[2]。利多卡因气雾剂临床上常用于皮肤和粘膜的局部麻醉,在包皮扩张粘连分离[3]、声带[4]等手术中镇痛效果明显。
中国药典2015年版、欧洲药典与美国药典[5-7]均收载了利多卡因原料药和注射液的质量标准,利多卡因气雾剂的质量标准仅收载于美国药典。参考标准还发现,各国药典中对于利多卡因制剂均没有较好的杂质研究与评价方法,这对于利多卡因这一常用麻醉药物的安全性是一种严重的缺失。
建立药品标准的过程中,是否能够准确地控制有关物质将直接关系到药品的质量可控与安全性[8],其中对遗传毒性物质的研究更应给予足够的重视[9]。英国药典2013年版利多卡因原料药项下共收载10个已知杂质(结构见图 1),其中杂质A为遗传毒性杂质,具有基因毒性和致癌作用[10]。因此在利多卡因气雾剂质量标准的研制过程中,以英国药典2013年版中利多卡因原料的质量标准为研究依据[11],开发并优化了利多卡因杂质研究的分析方法,可同时测定利多卡因气雾剂中主成分、基因毒性杂质及其他已知杂质,方法快速简单,准确可靠,为利多卡因气雾剂的产业化及质量管控提供了重要的依据。
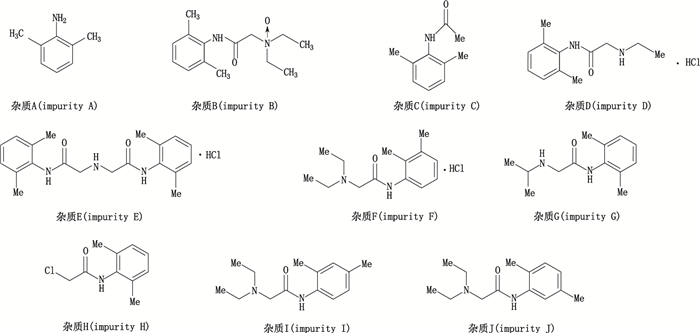
|
图 1 杂质A~J的化学结构式 Figure 1 Structures of impurity A-J |
Agilent 1100型高效液相色谱仪,包括G1322A脱气机、G1311A四元泵,G1313A自动进样器、G1315DAD检测器和HP化学工作站;Waters Symmetry-末端封尾十八烷基硅烷键合球形硅胶色谱柱(150 mm×3.9 mm,5 μm,Waters公司)。
1.2 试药利多卡因原料(国药准字H20059049,江苏济川制药有限公司),对照品利多卡因杂质A(批号100868-201202,中国食品药品检定研究院)、杂质B(批号2-PLL-5-4,TRC公司)、杂质C(批号LA70N02,J & K公司)、杂质D(批号3-MNZ-61-1,TRC公司)、杂质E(批号102.09.08.01,LGC公司)、杂质F(批号1490-031A4,TLC公司)、杂质G(批号1462-052A3,TLC公司)、杂质H(批号13-XJZ-32-1,TRC公司)、杂质I(批号11319,LGC公司)、杂质J(批号9893,LGC公司),乙腈为德国Merck色谱纯,水为纯净水,磷酸二氢钾和氢氧化钠均为分析纯(国药集团化学试剂有限公司)。
2 方法与结果 2.1 溶液制备 2.1.1 供试品溶液取本品1瓶,含利多卡因450 mg,除去帽盖,充分振摇,试喷5揿,用流动相洗净阀门及驱动器,充分干燥后,样品倒置于已加入30 mL流动相的适宜烧杯中,将驱动器前端浸入吸收液面下(至少15 mm),揿压喷射20揿(每次喷射间隔5 s,并取出充分振摇),取出供试品,用适量流动相洗净驱动器,合并洗液和吸收液至50 mL量瓶中,用流动相稀释至刻度,摇匀。即得9 mg·mL-1的有关物质供试品溶液。
2.1.2 对照溶液精密量取供试品溶液1 mL至100 mL量瓶,并用流动相稀释至刻度,作为自身对照溶液。
2.1.3 杂质对照品储备液精密称取已知杂质对照品A、B、C、D、E、F、G、H、I、J适量,用流动相稀释成质量浓度分别为0.18 mg·mL-1的溶液,以此溶液作为各杂质对照品储备液,根据各检测项下要求分别稀释配制溶液。
2.1.4 系统适用性溶液取上述杂质对照品储备液适量,于供试品溶液中,制成含有各已知杂质约为0.1%的利多卡因混合对照品溶液。
2.2 色谱条件与系统适用性试验色谱柱:Waters Symmetry-末端封尾十八烷基硅烷键合球形硅胶色谱柱(150 mm×3.9 mm,5μm);流动相:磷酸二氢钾缓冲液(精密称取4.85 g磷酸二氢钾,置于1 L水中,用2 mol·L-1的氢氧化钠溶液调节pH至8.0)-乙腈(65 :35);检测波长:230 nm;流速:1.0 mL·min-1;柱温:30 ℃;进样量:20 μL。
取系统适用性溶液注入液相色谱仪,进样测定,记录色谱图见图 2。在上述色谱条件下,利多卡因主峰与其他相邻杂质峰的分离度大于1.5,且各杂质之间分离度大于1.2,可保证杂质峰与主峰以及各杂质之间完全分离,保证有关物质定量的专属性与准确性。
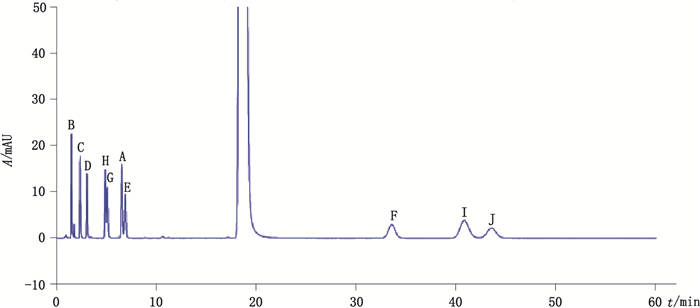
|
A. 2,6-二甲基苯胺(2,6-dimethylalanine)B. N-(2,6-二甲苯基)-2-(N-氧代-N,N-二乙基)-乙酰胺[2-(diethylazinoyl)-N-(2,6-dimethylphenyl)acetamide]C. N-(2,6-二甲苯基)乙酰胺[N-(2,6-dimethylphenyl)acetamide]D. N-(2,6-二甲苯基)-2-(乙氨基)乙酰胺盐酸盐[N-(2,6-dimethylphenyl)-2-(ethylamino)acetamide]E. 2,2’-亚氨基双[N-(2,6-二甲基苯基)]乙酰胺盐酸盐[2,2’-iminobis(N-(2,6-dimethylphenyl))acetiamide hydrochloride]F. 2-(二乙基氨基)-N-(2,3-二甲基苯基)乙酰胺盐酸(2-(diethylamino)-N-(2,3-dimethylphenyl)acetamide hydrochloride)G. N-(2,6-二甲苯基)-2-(异丙氨基)乙酰胺盐酸盐[N-(2,6-dimethylphenyl)-2-((1-methylethyl)amino)acetamide]H. N-(2,6-二甲苯基)-2-氯乙酰胺[2-chloro-N-(2,6-dimethyl phenyl)acetamide]I. N-(2,4-二甲苯基)-2-(二乙氨基)乙酰胺[2-(diethylamino)-N-(2,4-dimethylphenyl)acetamide]J. N-(2,5-二甲苯基)-2-(二乙氨基)乙酰胺[2-(diethylamino)-N-(2,5-dimethylphenyl)acetamide] 图 2 系统适用性试验色谱图 Figure 2 Chromatograms of system suitability test |
另取利多卡因气雾剂共6瓶,开盖后分别转移至50 mL量瓶中,在不同条件下进行强制降解实验,实验条件如下:
(1)未经破坏样品;(2)酸破坏:加2 mol·L-1盐酸1 mL,室温放置24 h后,以2 mol·L-1氢氧化钠溶液1 mL中和;(3)碱破坏:加2 mol·L-1氢氧化钠1 mL,室温放置24 h后,以2 mol·L-1盐酸溶液1 mL中和;(4)紫外光照破坏:4 500 lx紫外光照条件下放置7 d;(5)热破坏:105 ℃环境下放置24 h;(6)氧化破坏:加3%的过氧化氢溶液1 mL,放置5 min。
6种条件下的样品均用流动相定容至刻度,注入液相色谱仪测定,所得色谱图及空白溶剂、空白过氧化氢谱图如图 4所示,不同条件破坏后杂质含量如表 1所示。
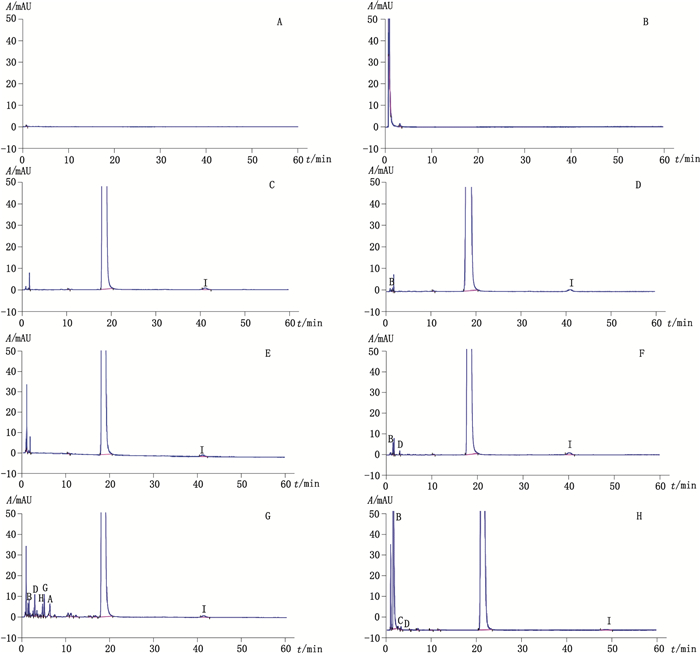
|
A.空白溶剂(blank solvent)B.过氧化氢(hydrogen peroxide)C.未破坏(no destruction)D.酸破坏(degradation by aci)E.碱破坏(degradation by base)F.光照破坏(degradation by UV light)G.高温破坏(degradation by high temperature)H.氧化破坏(degradation by hydrogen peroxide) 图 3 专属性试验图谱 Figure 3 Chromatogram of specificity test |
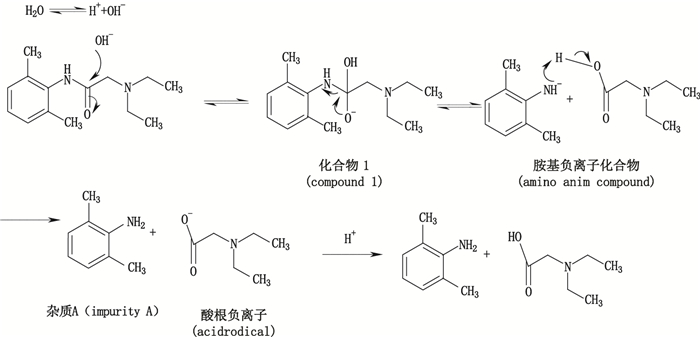
|
图 4 杂质A的反应机理 Figure 4 Generating mechanism of impurity A |
|
|
表 1 不同条件破坏后杂质含量(%) Table 1 The content of impurity after destruction test under different conditions |
结果表明本品在酸、碱和光照环境下较稳定,杂质个数和总量无显著变化。在酸破坏条件下,有关物质总含量为0.12%,主峰纯度因子为999.285;在碱破坏条件下,有关物质总含量为0.4%,主峰纯度因子为996.420;在光照破坏条件下,有关物质总含量为0.33%,主峰纯度因子为995.550;在105 ℃加热条件和3%的过氧化氢氧化条件下,均有不同程度的降解,在高温条件下伴有杂质A(0.17%)、B(0.08%)、D(0.21%)、H(0.15%)、G(0.22%)I(0.12%)的产生,主峰峰面积明显下降,有关物质总含量为1.77%,主峰纯度因子为995.820;在氧化破坏条件下,本品主要降解产生杂质B(34.69%),有关物质总含量为35.41%,说明在氧化条件下更不稳定,主峰纯度因子为999.661。
在上述条件下,各杂质峰与主峰均能分离完全,主峰纯度高,物料保持平衡,表明该方法具有良好的专属性。
2.4 检测下限与定量下限按“2.1”项下杂质对照品供试溶液配制方法平行制备各已知杂质对照品溶液,逐步稀释后依法进样,记录峰面积,选取信噪比约为3 :1时对应各杂质的浓度作为样品的检测下限,结果见表 2。
|
|
表 2 杂质检测下限和定量下限 Table 2 Impurity detection limit and quantitative limit |
按“2.1”项下杂质对照品供试溶液配制方法平行制备各已知杂质对照品溶液,逐步稀释后依法进样,记录峰面积,选取信噪比约为10 :1时对应各杂质的浓度作为样品的定量下限,结果见表 2。
2.5 线性试验和校正因子分别精密取“2.1”项下杂质对照品储备液适量,配制成浓度分别为0.1%杂质限度溶液浓度的20%、40%、80%、100%、150%、200%。将线性溶液注入液相色谱仪,记录峰面积,根据峰面积计算,以杂质浓度C为横坐标,峰面积A为纵坐标,在定量下限至一定浓度内以峰面积对溶液浓度进行线性回归,得线性方程,根据回归方程计算相对校正因子,结果如表 3所示。
|
|
表 3 杂质回归方程 Table 3 Regression equations of impurity |
按“2.1”项下方法配制杂质对照品溶液,连续进样6次,记录峰面积,测定系统精密度。杂质A~J峰面积的RSD均小于10%,表明各杂质的系统精密度良好。
2.7 重复性试验按“2.1.3”项下方法平行制备6份溶液,每份测定1次,记录峰面积,测定已知杂质重复性。结果显示杂质A~J的平均含量分别为99.95%、98.80%、99.51%、101.14%、98.58%、99.70%、98.48%、99.74%、99.88%、99.60%。各杂质平均含量的RSD均小于10%,重复性良好。
2.8 稳定性试验按“2.1.3”项下方法配制溶液,分别在0、6、12、18、24 h进样分析,以考察供试品溶液的稳定性。结果杂质A~J在24 h内的杂质含量的绝对值在±0.1%以内,且没有出现新的大于报告限度的杂质,表明溶液的稳定性良好。
2.9 样品测定取对照溶液和供试品溶液各20 μL,注入液相色谱仪,调节检测灵敏度,使对照溶液中主成分色谱峰高约为满量程的20%~25%,记录色谱图至60 min。供试品溶液的色谱图中若显杂质峰,其中杂质A(2.6-二甲基苯胺,相对保留时间为0.35)不得超过0.04%,其他单个杂质不得超过0.2%。杂质总量不得超过1.0%。36个月稳定性样品检测结果见表 4,其中D、E、G和H均未检出。
|
|
表 4 样品测定结果(%) Table 4 Determination results of samples |
根据Liu等[12-14]对酰胺水解反应机理的研究,推断利多卡因基因毒性杂质A产生的反应机理,见图 4。对基因毒性杂质A产生的原因进行分析:水分子部分解离为氢离子和氢氧根离子,氢氧根离子进攻利多卡因的羰基碳,使得碳氧双键上的1对电子向氧原子转移,形成中间体化合物1,随后O原子上的一对孤对电子转移形成C=O,此时可能会发生3种断裂方式:第1种是C-C键断裂,得到碳负离子,该碳负离子能量很高,故反应不会按照此途径进行;第2种是C-O键断裂,形成羟基离子,回到原来的状态;第3种是C-N键断裂,形成胺基负离子,虽然胺基负离子的离去能力较羟基离子弱,但胺基负离子N上的孤对电子可与苯环大π电子结构发生共轭,使得该中间体可以较稳定地存在,随后胺基负离子与羧酸发生质子交换形成杂质A,酸根负离子进行质子化形成羧酸分子。
3.2 校正因子研究中同时测定了各杂质的校正因子,结果显示:杂质A、B、C的相对校正因子为0.992、1.114、1.024,杂质F、I、J相对于利多卡因的校正因子分别为0.747、0.502、0.821(见表 3),故杂质A、B、C采用不加校正因子的自身对照法,而杂质F、I、J采用加校正因子的自身对照法[15]。杂质D、E、G、H在样品测定中均未检出,不做校正,即所有杂质均可采用自身对照法进行测定,并按照最大单一杂质限度计算,极大简化了操作步骤,降低了检验成本,更有利于利多卡因气雾剂产业化控制。
3.3 小结本文采用HPLC法测定利多卡因气雾剂有关物质,结果显示以英国药典2013年版为基础而建立的高效液相色谱法专属性强,灵敏度高,选择性好,用1套分析方法快速、便捷地完成了10个有关物质的定量研究,同时能够精确地控制遗传毒性杂质A,为该类产品的产业化质量控制和遗传毒性杂质含量测定提供了方法。
| [1] |
郭美宝, 张晓霞. 利多卡因气雾剂在局麻清创手术中的应用效果[J]. 福建医药杂志, 2013, 35(5): 106. GUO MB, ZHANG XX. The application effect of lidocaine aerosol in the local anesthesia debridement surgery[J]. Fujian Med J, 2013, 35(5): 106. |
| [2] |
刘红芸, 蔡雁卿, 刘华, 等. 利多卡因气雾剂在学龄前儿童无痛静脉穿刺中的应用研究[J]. 国际医药卫生导报, 2016, 22(12): 1693. LIU HY, CAI YQ, LIU H, et al. Applying aerosol inhalation of lidoeaine in pain less in travenous puncture in preschool children[J]. Int Med Health Guid News, 2016, 22(12): 1693. DOI:10.3760/cma.j.issn.1007-1245.2016.12.009 |
| [3] |
杨清清, 陆文辉, 陈芳芳, 等. 利多卡因气雾剂用于小儿包皮扩张分粘连术的镇痛效果[J]. 广东医学, 2011, 32(23): 3130. YANG QQ, LU WH, CHEN FF, et al. Lidocaine aerosol for pediatric prepuce expansion by adhesion of analgesic effect[J]. Guangdong Med J, 2011, 32(23): 3130. DOI:10.3969/j.issn.1001-9448.2011.23.044 |
| [4] |
刘静, 杨春艳, 李婷. 全身麻醉联合7%的利多卡因气雾剂在支撑喉镜下声带手术中的应用[J]. 中国医药科学, 2015, 5(17): 152. LIU J, YANG CY, LI T. The application of 7%lidocaine aerosol in general anesthesia of laryngoscope vocal surgery[J]. China Med Pharm, 2015, 5(17): 152. |
| [5] |
中国药典2015年版. 二部[S]. 2015: 978 ChP 2015.Vol Ⅱ[S].2015:978 |
| [6] |
EP 8.0[S].2621
|
| [7] |
USP 35-NF 30[S].2012:3683
|
| [8] |
张哲峰. 我国药物研发中杂质研究面临的挑战与思考[J]. 药品评价, 2010, 18(7): 12. ZHANG ZF. Challenge and consideration of related subtance research in drug research and development in China[J]. Drug Eval, 2010, 18(7): 12. |
| [9] |
TGA.Guidelines for the Registration of Drugsa[S].1994, 1(1). Appendix 10
|
| [10] |
高雪, 盖薇, 顾朝康. 超高效液相色谱-四极杆飞行时间质谱法测定血液与尿中赛拉嗪及代谢产物2, 6-二甲基苯胺[J]. 分析测试学报, 2015, 34(6): 646. GAO X, GAI W, GU CK. Simultaneous determination of xylazine and 2, 6-dimethylaniline in blood and urine by ultra high performance liquid chromatography coupled with quadrupole-time of flight mass spectrometry[J]. J Instrum Anal, 2015, 34(6): 646. |
| [11] |
BP 2013.Vol Ⅰ[S].2013:1332
|
| [12] |
LIU P, HAN J, CHEN CP, et al. Palladium-catalyzed oxygenation of C(sp2)-H and C(sp3)-H bonds under the assistance of oxalyl amide[J]. Roy Soc Chem, 2015, 5: 28430. |
| [13] |
LAVROV KV, ZALUNIN IA, KOTLOVA EK, et al. A new acylamidase from rhodococcus erythropolis TA37 can hydrolyze substituted amides[J]. Biochemistry, 2010, 75(8): 1111. |
| [14] |
SVENSSON F, ENGEN K, LUNDBACK T, et al. Virtual screening for transition state analogue inhibitors of IRAP based on quantum mechanically derived reaction coordinates[J]. J Chem Inf Model, 2015, 55: 1984. DOI:10.1021/acs.jcim.5b00359 |
| [15] |
张哲峰. HPLC法校正因子研究中的几个问题[J/OL]. [2011-12-07]. http://www.cde.org.cn/dzkw.do?method=largePage&id=312552 ZHANG ZF.Several problems in the research of the correction factor in HPLC method[J/OL].[2011-12-07].http://www.cde.org.cn/dzkw.do?method=largePage&id=312552 |
 2018, Vol. 38
2018, Vol. 38 
