参芍胶囊是由人参茎叶总皂苷和白芍制成的复方制剂,具有活血化瘀、益气止痛的功效,临床上适用于气虚血瘀所致的胸闷、胸痛、心悸、气短,以及冠心病心绞痛见上述证侯者[1]。参芍胶囊以人参茎叶总皂苷为君药,用于补气;白芍为臣药,行瘀止痛,养阴和血;两药合用,共奏活血化瘀,益气止痛之功效[2]。本研究参考相关文献,采用高效液相色谱-质谱(LC-MS/MS)联用技术,通过多反应离子监测对参芍胶囊中的人参皂苷Rb2、Rd、Re、Rg1和芍药苷5个成分同时进行测定。本方法的建立可为参芍胶囊的质量控制提供参考,并大大提高现行标准(中国药典2015年版一部参芍胶囊)常规液相色谱方法的检测效率,缩短检测时间。
1 仪器与试药 1.1 仪器U-3000高效液相色谱仪(Thermofisher公司),TSQ Quantum ACCESS MAX三重四极杆质谱仪,配有电喷雾离子源(ESI) (Thermofisher公司);Hypersil Gold C18色谱柱(2.1 mm×100 mm,3 μm;填料:十八烷基硅烷键合硅胶;Thermofisher公司);AE240电子天平(Mettler Toledo公司);Milli-Q Integral超纯水仪(Millipore公司)。
1.2 试药对照品人参皂苷Rb2(批号111715-200802,含量以94.8%计)、人参皂苷Rd(批号111828-201603,含量以92.1%计)、人参皂苷Re(批号110754-201626,供含量测定用)、人参皂苷Rg1(批号110703-201128,含量以93.4%计)、芍药苷(批号110736-201640,含量以95.2%计)均购于中国食品药品检定研究院。样品参芍胶囊(每粒装0.25 g)购于山东华源天宏药业有限公司。甲醇、乙腈和甲酸(Thermo Fisher公司)为色谱纯,水为超纯水,其他试剂(天津大茂化学试剂厂)均为分析纯。
2 方法与结果 2.1 溶液的制备 2.1.1 混合对照品储备液分别精密称取人参皂苷Rg1、Rb2、Re、Rd和芍药苷的对照品适量,用70%甲醇水制成含人参皂苷Rg1 172.9 μg·mL-1,人参皂苷Rb2 126.6 μg·mL-1,人参皂苷Re 174.4 μg·mL-1,人参皂苷Rd 103.4 μg·mL-1和芍药苷123.6 μg·mL-1的混合溶液,即得。
2.1.2 供试品溶液取样品内容物适量,混匀,取约0.2 g,精密称定,置100 mL量瓶中,加70%甲醇水适量,超声处理(功率400 W,频率40 kHz)30 min,放冷至室温,用70%甲醇水稀释至刻度,摇匀,滤过,精密量取5 mL,置100 mL量瓶中,用70%甲醇水稀释至刻度,用0.22 μm微孔滤膜过滤,即得。
2.1.3 阴性样品溶液按参芍胶囊制法,取辅料分别制备缺白芍和人参茎叶总皂苷的阴性样品。按照“2.1.2”项下方法制备溶液,即得。
2.2 色谱-质谱条件色谱条件:采用Hypersil Gold C18色谱柱(2.1 mm× 100 mm,3 μm),柱温40 ℃,以乙腈-0.1%甲酸水溶液为流动相,梯度洗脱(0~10 min,15%乙腈→40%乙腈;10~13 min,40%乙腈→70%乙腈),流速0.3 mL·min-1,进样量10 μL。
质谱条件:采用电喷雾离子源(ESI),蒸发温度为400 ℃,离子传输毛细管温度为350 ℃,鞘气压力276 kPa,辅助气压力34 kPa,电压为3 kV。选择负离子扫描方式,多反应监测(MRM)模式,5个分析物的质谱参数见表 1。
|
|
表 1 5个分析物的质谱参数 Table 1 The MS/MS parameters of 5 analytes |
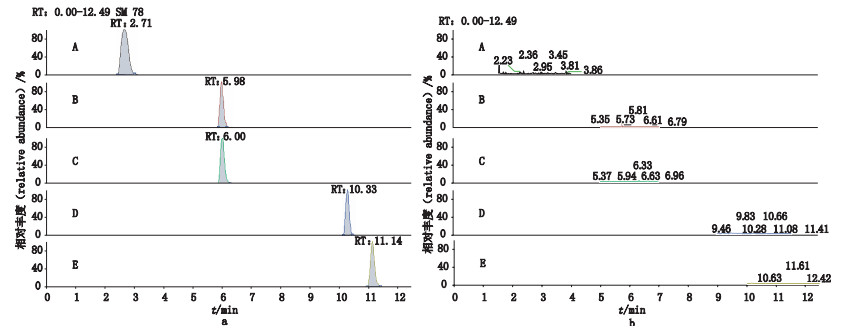
在上述试验条件下,样品及阴性样品的提取离子流图谱见图 1-a、b。
|
A.芍药苷(paeoniflorin) B.人参皂苷Rg1(ginsenoside Rg1) C.人参皂苷Re(ginsenoside Re) D.人参皂苷Rb2(ginsenoside Rb2) E.人参皂苷Rd(ginsenoside Rd) 图 1 样品(a)及阴性样品(b)中5个分析物提取离子流图 Figure 1 Extracted ion chromatograms of 5 analytes in sample(a)and negative sample(b) |
取混合对照品储备液适量,加70%甲醇水稀释制备成5个浓度的系列混合对照品溶液,按照“2.2”项下的条件进行测定。以对照品质量浓度(X)为横坐标,待测物质峰面积(Y)为纵坐标,进行线性回归计算,得到线性回归方程及相关系数,结果表明5个分析物在相应的范围内线性关系良好。采用混合对照品溶液逐级稀释,进样测定,以S/N=10时的对照品质量浓度为5个分析物各自的定量限,结果见表 2。
|
|
表 2 线性关系结果及定量限 Table 2 Linearity and quantitation limits |
取混合对照品溶液,连续进样6次,测得人参皂苷Rg1、Rb2、Re、Rd和芍药苷峰面积的RSD分别为2.2%、1.5%、1.8%、2.0%、1.7%,表明仪器的精密度良好。
2.5 重复性试验按“2.1.2”项下方法制备同一批样品(批号160701)的供试品溶液6份,进样测定。结果人参皂苷Rg1、Rb2、Re、Rd和芍药苷的平均含量分别为8.38、3.99、11.58、6.70、86.90 mg·g-1,RSD分别为1.7%、2.7%、2.5%、1.8%、2.2%,表明本方法的重复性良好。
2.6 稳定性试验取“2.1.2”项下同一份供试品溶液,分别于0、2、4、8、12、24 h进样测定,测得人参皂苷Rg1、Rb2、Re、Rd和芍药苷峰面积的RSD分别为2.5%、1.9%、1.8%、2.9%、2.4%,表明供试品溶液在24 h内稳定性良好。
2.7 加样回收率试验精密称取已知含量的参芍胶囊(批号160701)6份,每份0.1 g,分别置100 mL量瓶中,精密加入混合对照品储备液适量,按“2.1.2”项下方法制备供试溶液,进样测定,计算回收率。结果见表 3。
|
|
表 3 回收率结果(n=6) Table 3 Recoveries |
取3批次参芍胶囊样品,按照“2.1.2”项下方法制备供试品溶液,进样测定,通过回归方程计算含量,结果见表 4。
|
|
表 4 样品测定结果(X±SD,mg·g-1,n=3) Table 4 Results of sample analysis |
人参皂苷Rg1与人参皂苷Re分离困难,用常规液相色谱方法实现分离造成每次进样时间很长。LC-MS/MS法表现出的高选择性、高灵敏度,不要求人参皂苷Rg1与人参皂苷Re完全分离,大大缩短分析时间。另外人参皂苷类成分没有生色团,用紫外检测器测定时只能取末端吸收,干扰较大,采用质谱检测器,用MRM方式测定,可以有效避免干扰,专属性更强,可以准确测定样品中人参皂苷的含量。
3.2 提取条件的选择实验中分别考察了50%甲醇水、70%甲醇水和100%甲醇作为提取溶剂,超声与回流2种提取方式,结果发现选用70%甲醇水超声提取30 min,各被测成分峰形较好,提取率较高。
3.3 流动相的选择实验中分别考察了甲醇-0.1%甲酸水溶液、乙腈-0.1%甲酸水溶液等流动相体系。结果显示,采用乙腈-0.1%甲酸水溶液作为流动相,检测灵敏度较高。故选用乙腈-0.1%甲酸水溶液作为本实验的流动相。采用梯度洗脱方式,可有效缩短分析时间,改善峰形,提高灵敏度和分离能力等。
3.4 质谱条件的考察质谱分析中,对各被测成分的质谱参数进行了优化,人参皂苷类成分在负离子模式下有较高的响应和较好的峰形[4]。芍药苷在负离子检测模式下易产生加合离子峰[M+HCOO]-[5],以m/z 525.1作为母离子进行优化,确定以m/z 525.1→327.0为芍药苷的定量离子对,故本实验选择负离子模式进行测定。
3.5 小结本实验建立了LC-MS/MS法同时测定参芍胶囊中人参皂苷Rb2、Rd、Re、Rg1和芍药苷5个有效成分的含量,该方法简便、快速,灵敏度高,专属性好,可用于参芍胶囊的质量控制。相较于现行标准(中国药典2015年版一部参芍胶囊),能很大程度提高检测效率。LC-MS/MS法具有高准确性、高灵敏度、高专属性以及检测限和定量限更低的优点,已逐渐成为中药多成分测定的有效方法。
| [1] |
中国药典2015年版. 一部[S]. 2015: 1127 ChP 2015.Vol Ⅰ[S].2015:1127 |
| [2] |
郝朝霞, 柳青. 参芍胶囊治疗冠心病心绞痛40例临床观察[J]. 中西医结合心脑血管病杂志, 2005, 3(9): 841. HAO ZX, LIU Q. Clinical observation of 40 cases of Shenshao capsules in treatment of angina pectoris[J]. Chin J Integr Med Cardio/Cerebrovasc Dis, 2005, 3(9): 841. |
| [3] |
覃莎, 王锦, 朱平川, 等. UPLC-MS/MS法同时测定灯盏生脉胶囊中的11个活性成分的含量[J]. 药物分析杂志, 2013, 33(8): 1336. QIN S, WANG J, ZHU PC, et al. Simultaneous determination of eleven active components in Dengzhanshengmai capsules by ultra performance liquid chromatography with tandem mass spectrometry[J]. Chin J Pharm Anal, 2013, 33(8): 1336. |
| [4] |
赵振霞, 王敏, 王钰宁, 等. UPLC-MS/MS法测定心可舒胶囊中5种皂苷类成分的含量[J]. 药物分析杂志, 2016, 36(3): 494. ZHAO ZX, WANG M, WANG YN, et al. Simultaneous determination of five saponins in Xinkeshu capsules by UPLC-MS/MS[J]. Chin J Pharm Anal, 2016, 36(3): 494. |
| [5] |
周芙琼, 夏崇才, 朱维娜, 等. UPLC-MS/MS法同时测定止痒乳膏中10个成分的含量[J]. 药物分析杂志, 2016, 36(7): 1207. ZHOU FQ, XIA CC, ZHU WN, et al. Simultaneous determination of ten compounds in Zhiyang cream by UPLC-MS/MS method[J]. Chin J Pharm Anal, 2016, 36(7): 1207. |
| [6] |
闫寒, 赵松岩, 刘运嘉, 等. LC-MS-MS法测定参体和参须中人参皂苷Rb1、Rb2和Rc含量[J]. 中国实验方剂学杂志, 2013, 19(6): 105. YAN H, ZHAO YS, LIU JY, et al. Simultaneous quantitation of Rb1, Rb2 and Rc in Ginseng tail and the main root of Ginseng by LC-MS-MS[J]. Chin J Exp Tradit Med Form, 2013, 19(6): 105. |
| [7] |
杨钊, 张燕, 朱韵洁, 等. UPLC-MS/MS测定康艾注射液中5种主要成分含量[J]. 中国药学杂志, 2011, 46(4): 297. YANG Z, ZHANG Y, ZHU YJ, et al. Determination of 5 components in Kangai injecton by UPLC-MS/MS[J]. Chin Pharm J, 2011, 46(4): 297. |
| [8] |
蔡博, 董林毅, 王静, 等. 超高效液相色谱联用技术同时测定小金丸中7种成分的含量[J]. 中国药学杂志, 2015, 50(8): 718. CAI B, DONG LY, WANG J, et al. Simultaneous determination of seven components in Xiaojin pills by UPLC-MS[J]. Chin Pharm J, 2015, 50(8): 718. |
| [9] |
傅俊曾, 宋生有, 姜民, 等. 液相色谱-质谱联用同时测定芪参益气滴丸中黄芪甲苷、丹参素、原儿茶醛、人参皂苷Rg1和Rb1含量[J]. 中国药学杂志, 2012, 47(1): 61. FU JZ, SONG SY, JIANG M, et al. Simultaneous determination of the content of astragaloside Ⅳ, Danshensu, protocatechualdehyde, ginsenosides Rg1 and Rb1 in Qishenyiqi dropping pills by LC-MS[J]. Chin Pharm J, 2012, 47(1): 61. |
| [10] |
余健, 徐晓珍, 顾利强, 等. 高效液相色谱-串联质谱法同时测定参麦注射液中9种皂苷[J]. 中华中医药学刊, 2014, 32(1): 71. YU J, XU XZ, GU LQ, et al. Simultaneous quantification of ginsenosides Rg1, Re, Rf, Rd, Rc, Rb2, Rb1, Ro and ophiopogonin D in Shenmai injection by liquid chromatography-tandem mass spectrometry[J]. Chin Arch Tradit Chin Med, 2014, 32(1): 71. |
| [11] |
郑敏霞, 陈喆, 刘培, 等. 白芍中芍药苷及其衍生物的UPLC-MS/MS分析[J]. 中国中药杂志, 2011, 36(12): 1641. ZHENG MX, CHENG Z, LIU P, et al. Analysis and identification of glycosides in Paeonia lactiflora by UPLC-MS/MS[J]. China J Chin Mater Med, 2011, 36(12): 1641. |
| [12] |
刘颖, 欧阳玥, 李松, 等. 芪苈强心胶囊中12种成分的UPLC-MS测定[J]. 中国中药杂志, 2014, 39(10): 1822. LIU Y, OU YY, LI S, et al. Determination of twelve active compounds in Qili Qiangxin capsules by UPLC-MS[J]. China J Chin Mater Med, 2014, 39(10): 1822. |
| [13] |
方昱, 万丽丽, 朱金辉, 等. UPLC-MS/MS测定同济2号颗粒剂中黄芪甲苷、绿原酸、人参皂苷Rg1、人参皂苷Rb1和三七皂苷R1[J]. 药物评价研究, 2015, 38(4): 394. FANG Y, WAN LL, ZHU JH, et al. Determination of astragaloside Ⅳ, chlorogenic acid, ginsenosides Rg1, Rb1 and notoginsenoside R1 in Tongji No.2 granules by HPLC-MS/MS[J]. Drug Eval Res, 2015, 38(4): 394. |
| [14] |
张毅, 周慧. HPLC-MS/MS法同时测定参乌健脑胶囊中8种成分[J]. 中草药, 2016, 47(14): 2470. ZHANG Y, ZHOU H. Simultaneous determination of eight components in Shenwu Jiannao capsules by HPLC-MS/MS[J]. Chin Tradit Herb Drugs, 2016, 47(14): 2470. DOI:10.7501/j.issn.0253-2670.2016.14.013 |
| [15] |
乔晓莉, 肖学凤, 周大铮, 等. UPLC-MS/MS法同时测定注射用益气复脉(冻干)中13种成分[J]. 中草药, 2014, 45(23): 3402. QIAO XL, XIAO XF, ZHOU DZ, et al. Simultaneous analysis of 13 components in Yiqi Fumai injection(freeze-dried)by UPLC-MS/MS method[J]. Chin Tradit Herb Drugs, 2014, 45(23): 3402. DOI:10.7501/j.issn.0253-2670.2014.23.009 |
 2018, Vol. 38
2018, Vol. 38 