海马(Hippocampus)是海龙科(Syngnathiclae)海马属(Hippocampus)动物,是中国传统的强壮补益中药,性温味甘,入肝、肾经,具有补肾壮阳、消肿散结的功效,临床上用于治疗阳痿、遗尿、虚喘、症积、疗疮肿毒等症[1]。海马主要含有微量元素、氨基酸、脂肪酸、磷脂和甾体成分等[2],蛋白质是其主要成分,含量高达70%[3]。近代药理研究表明海马有强壮、抗血栓、抗肿瘤、抗衰老、抗疲劳、增强记忆力等药理活性[4]。目前对于海马的研究主要集中在传统的分离鉴定和药理研究等方面,而对提取的海马蛋白进行系统分析目前未见报道[5]。
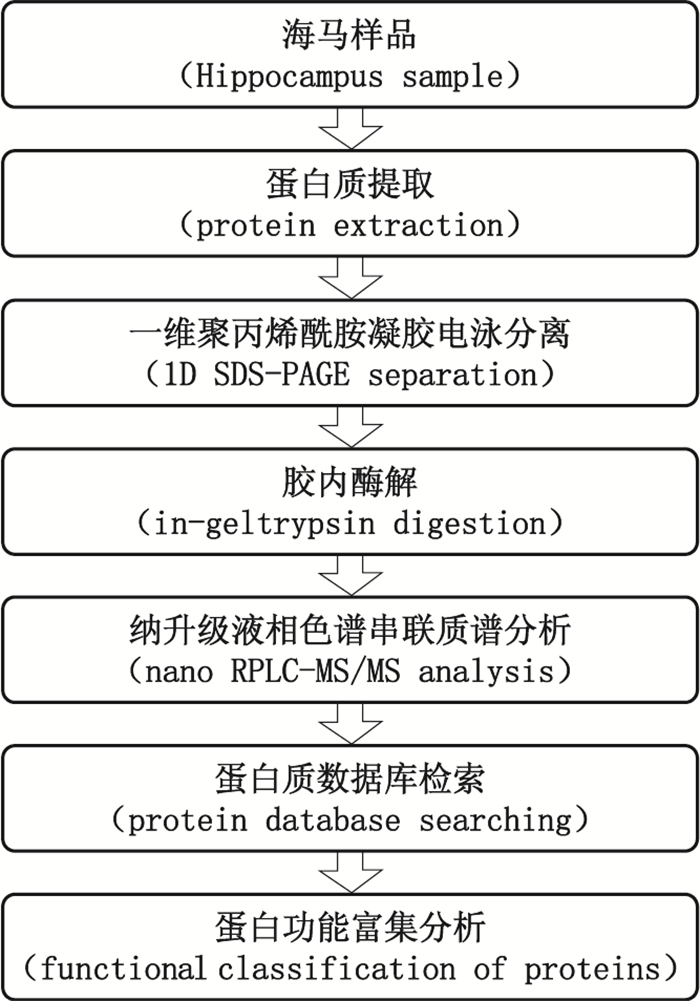
纳升级反相液相色谱-串联质谱法(nanoRPLC-MS/MS)具有高通量高灵敏度的特征,已被广泛应用于蛋白质组学分析中[6-9]。本研究引入蛋白质组学研究策略,实验设计如图 1所示,应用聚丙烯酰胺凝胶电泳技术对海马提取蛋白质进行分离,经胶内酶解处理后采用高灵敏、高通量的纳升级反相液相色谱-串联质谱方法分析,并对鉴别到的蛋白质进行基因本体(gene ontology,GO)功能富集分析[10],较系统地研究了海马的提取蛋白质,为中药海马的蛋白质成分研究奠定基础。
|
图 1 海马蛋白质分析实验设计流程图 Figure 1 Flow chart of experimental design for Hippocampus protein analysis |
纳升级液相色谱系统:Thermo Scientific EASY-nLC 1000(Thermo Scientific,Odense,Denmark)液相色谱系统;高分辨质谱系统:Thermo Scientific™ Q Exactive™组合型四极杆Orbitrap质谱仪(Thermo Scientific,Bremen,Germany),配有纳升电喷雾离子源(nano-electrospray ion source)、Mascot蛋白质分析软件(Version 1.2)。酶标仪Genios(Tecan公司)、垂直凝胶电泳仪(Bio-rad公司);离心浓缩仪(Labconco公司)。
二硫苏糖醇(DTT)购于Sigma-Aldrich(USA)公司,十二烷基磺酸钠(SDS)、尿素(UREA)购于Thermo Fisher Scientific(USA)公司,碘乙酰胺(IAA)购于Aladdin公司,丙酮、三氯乙酸(TCA)、β-巯基乙醇、丙烯酰胺、甲叉双丙烯酰胺、三羟甲基氨基甲烷(Tris)、NP-40、琼脂糖、溴酚蓝、乙酸钠、丙三醇、氯化钠、聚乙二醇辛基苯基醚、脱氧胆酸盐、SDS、乙二胺四乙酸购于上海生工生物工程有限公司,测序级胰蛋白酶购于Promega(Germany)公司,乙腈、甲醇、甲酸等质谱用试剂(质谱级)购于Merck公司。海马药材由中国海洋大学李国强教授友情赠送并鉴定为线纹海马(Hippocampus kelloggi Jordan et Snyder)的干燥体,产自广西壮族自治区,购买于青岛同仁堂药店(2013-11-23)。
2 试验方法 2.1 溶液的配制Bradford储存液:称取考马斯亮蓝G-250 350 mg,依次加入95%乙醇100 mL,88%磷酸200 mL,待考马斯亮蓝G250完全溶解后置于棕色瓶中保存。Bradford工作液:量取Bradford储存液30 mL,依次加入去离子水425 mL,95%乙醇15 mL,88%磷酸30 mL,搅拌混匀,滤纸过滤后保存于棕色瓶中,室温放置,使用时需再次过滤,即得。Tris-Gly SDS-PAGE浓缩胶(6%,15 mL):依次加入30%聚丙烯酰胺溶液3 mL,1.5 mol·L-1 Tris-HCl(pH 8.8)3.8 mL,10% SDS 0.15 mL,10%过硫酸铵(AP)0.15 mL,TEMED 12 μL及水7.9 mL至烧杯中,混匀,即得。Tris-Gly SDS-PAGE分离胶(12%,45 mL):依次加入30%聚丙烯酰胺溶液18 mL,1.5 mol·L-1 Tris-HCl(pH 8.8)11.4 mL,10% SDS 0.45 mL,10%过硫酸铵(AP)0.45 mL,N,N,N’,N’-四甲基乙二胺(TEMED)18 μL及水14.7 mL至烧杯中,混匀,即得。考马斯亮蓝R-250染色液:称取考马斯亮蓝R-250 0.25 g,依次加入甲醇45 mL,冰醋酸10 mL,待其完全溶解后加去离子水定容至100 mL,即得。考马斯亮蓝脱色液:量取甲醇250 mL,冰醋酸80 mL,加入去离子水定容至1 L,即得。10×SDS电泳缓冲液:分别称取Tris 30.3 g,甘氨酸187.7 g,SDS 10 g,加去离子水溶解,定容至1 L,室温保存,使用时加9倍的去离子水稀释至1×SDS电泳缓冲液。碳酸氢铵溶液(100 mmol·L-1):称取1.58 g碳酸氢铵溶于200 mL超纯水中,搅拌溶解,即得。二硫苏糖醇溶液(100 mmol·L-1):称取二硫苏糖醇0.0154 g溶于1 mL碳酸氢铵溶液(100 mmol·L-1)中,震荡使之溶解,即得。碘乙酰胺溶液(200 mmol·L-1):称取碘乙酰胺0.037 g溶于1 mL碳酸氢铵溶液(100 mmol·L-1)中,震荡使之溶解,即得。测序级胰蛋白酶(10 ng·μL-1):Promega公司试剂盒成品质量浓度为0.5 μg·μL-1,使用时用50 mmol·L-1的碳酸氢铵溶液稀释50倍使用。
2.2 海马总蛋白的提取海马蛋白质提取采用三氯乙酸/丙酮沉淀法[11]。干燥海马药材粉碎后,取粗粉100 mg,加入丙酮(含10%三氯乙酸,0.07%β巯基乙醇)5 mL,放入-20 ℃冰箱过夜,4 ℃ 13 000 r·min-1离心20 min,弃去上清,沉淀物用含0.07%巯基乙醇的丙酮溶液清洗3遍,冻干,将此干燥粉末中加入[RIPA]裂解缓冲液(三(羟甲基)氨基甲烷,50 mmol·L-1,pH 7.4;氯化钠150 mmol·L-1;1%聚乙二醇辛基苯基醚;脱氧胆酸盐,1%;SDS,0.1%;乙二胺四乙酸)5 mL裂解1 h,4 ℃ 13 000 r·min-1离心30 min,取上清即得海马总蛋白,应用Bradford法测定[12]蛋白浓度,具体实验方法:首先用去离子水配制2 mg·mL-1的牛血清白蛋白(BSA)的溶液,然后根据表 1加入考马斯亮蓝工作液,去离子水,BSA溶液或者样品。当加入BSA溶液或者样品后,需立即在涡旋振荡仪上混合,使蛋白和考马斯亮蓝G250染料充分结合。室温放置2~3 min后,从每个离心管中吸取200 μL加入到96孔板中,每组设4个复孔,然后用酶标仪测定570 nm处的吸收值,然后根据BSA溶液的浓度和相对应的吸收值绘制标准曲线。最后借助于标准曲线,将样品组的吸收值代入其中得到样品中的蛋白浓度。-80 ℃保存备用。
|
|
表 1 Bradford法测定蛋白浓度 Table 1 Bradford method for concentration determination |
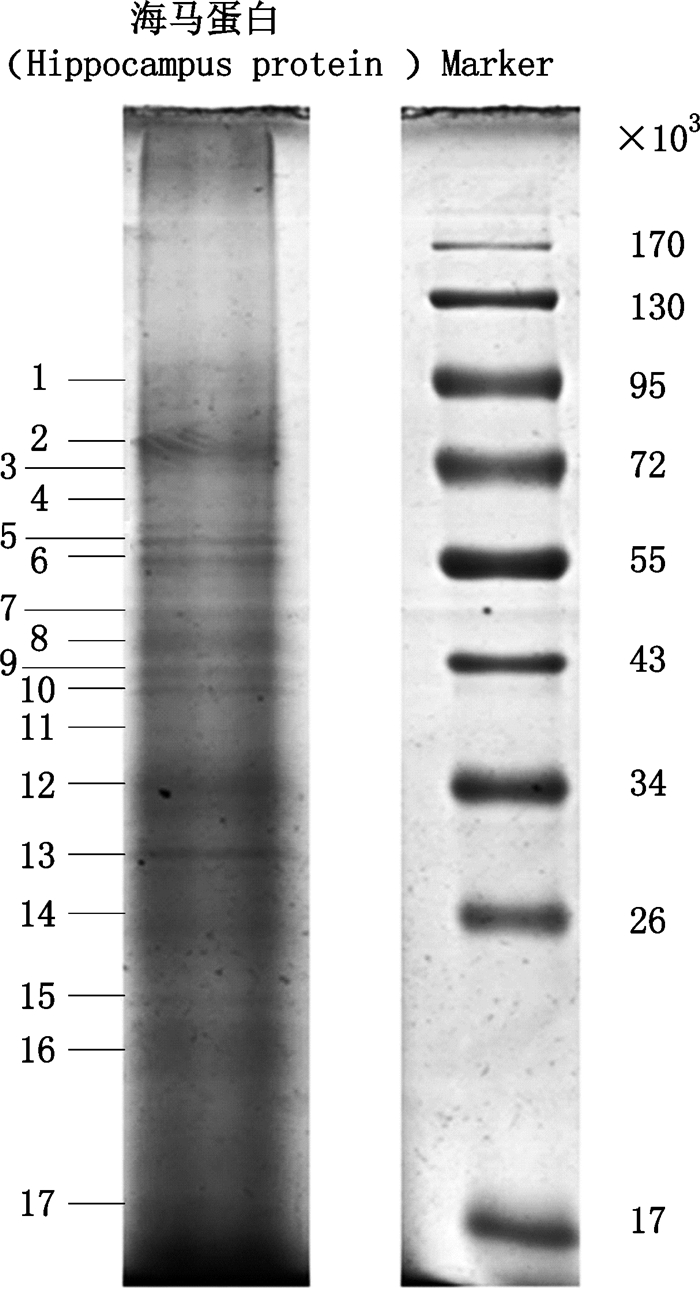
将海马总蛋白100 μg经上样液(SDS,2%;溴酚蓝,0.02%;Tris-HCl,0.08 mol·L-1,pH 8.0;丙三醇40%)溶解,煮沸5 min后上样到配好的凝胶(分离胶浓度12%,浓缩胶6%),上样量为20 μg总蛋白量,应用垂直凝胶电泳仪跑胶,先恒压60 V电泳30 min,使样品跑完浓缩胶;然后90 V恒压跑分离胶,距凝胶边缘约5 mm时,停止电泳,分离胶分子筛的作用使得蛋白质根据其各自分子量的大小而被分离。取出凝胶,放入100 mL考马斯亮蓝染色液中,置于水平摇床上缓慢摇动室温染色2 h,取出凝胶放入200 mL考马斯亮蓝脱色液中,置于水平摇床上缓慢摇动室温脱色12 h,直至蓝色背景被全部脱去,即得SDS-PAGE条带(图 2)。
|
图 2 海马提取蛋白SDS-PAGE Figure 2 The SDS-PAGE images of protein extracted from Hippocampus |
将图 2中SDS-PAGE标注的条带切下,共切得17个条带,分别放入离心管中,将条带切成约1 mm3大小的小块,用100 mmol·L-1碳酸氢铵溶液[含30%(v/v)乙腈]溶液洗涤至无色,去除上清液,冻干,每管加入100 mmol·L-1碳酸氢铵溶液90 μL和100 mmol·L-1二硫苏糖醇溶液10 μL,在56 ℃孵育30 min,去上清,加入50 μL乙腈洗涤2次,冻干,每管加入100 mmol·L-1碳酸氢铵溶液70 μL和200 mmol·L-1碘乙酰胺溶液30 μL,室温避光孵育20 min,去上清,加入50 μL乙腈洗涤2次,冻干,加入测序级胰蛋白酶(10 ng·μL-1)5 μL,放入4 ℃冰箱30 min,再加入50 mmol·L-1碳酸氢铵溶液30 μL,放入37 ℃恒温培养箱中过夜消化得酶解液,吸取酶解液到新的离心管中,原管加入含0.1%(v/v)甲酸和60%(v/v)乙腈的水溶液100 μL,超声15 min,吸出溶液并入前次溶液,此步骤重复3次,合并,冻干,得海马蛋白质胶内酶解物。
2.4 纳升级反相液相色谱串联质谱分析将上述胶内酶解物用30 μL 0.1%甲酸溶液复溶,13 000 r·min-1离心20 min后取上清液注入nanoLC-MS/MS仪器分析。EASY-nLC system液相系统色谱条件:采用Easy-spray C18毛细管柱(75 μm×50 mm,2 μm,120 Å),流动相A为3%乙腈(0.1%甲酸),流动相B为97%乙腈(0.1%甲酸),梯度洗脱(0~5 min,3%B→8%B; 5~195 min,8%B→20%B; 195~220 min,20%B→30%B; 220~225 min,30%B→90%B; 225~240 min,90%B),流速300 nL·min-1,自动进样,上样5 μL,分析时间240 min。质谱检测条件:采用正离子扫描方式,典型的质谱参数设置为离子喷雾电压2 kV,加热毛细管温度250 ℃;一级质谱扫描范围m/z 300~1 750;动态排除设置为30 s;高能碰撞解离(HCD)设置为60 ms 17 500分辨率;碰撞能量为27% 250 ms;应用数据依赖模式选择一级图谱峰进行二级扫描。
2.5 海马蛋白质数据库搜索对实验得到的质谱数据结果应用蛋白质发现软件在Uniprot中辐鳍鱼纲(Actinopterygii Group)蛋白质数据库(Actinopterygii(ray-finned fishes).fasta)中进行检索,数据库下载于NCBI Taxonomy:Actinopterygii(ray-finned fishes)database。数据库检索软件为Mascot search engines of proteome discoverer(Thermo Scientific,Version 1.2),设置参数如下:蛋白质以及多肽的假阳性率小于1%,酶为胰蛋白酶,固定修饰为酰胺甲基化,可变修饰为N端甲基化和甲硫氨酸氧化,最大允许1个错切,母离子质量偏差小于10,二级碎片离子偏差小于0.25个单位。
2.6 鉴定蛋白质功能分析采用DAVID Bioinformatics Resources 6.8(National Institute of Allergy and Infectious Diseases,NIH,USA)在线工具分别对鉴定到的海马蛋白质进行基因本体功能富集分析,探索鉴定到蛋白质的分子功能。
3 结果与讨论 3.1 干燥海马蛋白质的提取对干燥海马药材的蛋白质提取,是本研究的重点和难点,本研究应用三氯乙酸/丙酮沉淀法和RIPA试剂盒提取干燥海马蛋白质,提取蛋白使用Bradford法[12],测定蛋白质的浓度测定体系如表 1所示,测得蛋白质质量浓度为10 mg·mL-1,100 mg干燥海马蛋白共提取到45 mg蛋白质,提取效率是45%。蛋白提取液应用SDS-PAGE电泳分离,上样量为0.1 mg,电泳结果见图 2。如图所示海马蛋白质相对分子质量覆盖范围为1.7×104~1.3×105。
3.2 干燥海马蛋白质组学分析将海马的SDS-PAGE蛋白质条带经胶内酶解处理和nano-RPLC-MS/MS系统进行分析后,将质谱分析的数据应用Mascot搜索软件,在辐鳍鱼纲蛋白质数据库中进行检索比对,共检索得到假阳性率小于1%而置信度大于95%的蛋白192种,等电点范围为4.06~12.18,相对分子质量范围为3.06×103~3.52×106(如附表1所示),共检测到10 680条多肽。然而目前尚缺乏海马的蛋白质组数据库,海马的基因组数据尚未检测,所以质谱检测到的图谱在现有辐鳍鱼纲数据库中无法完全比对,有效图谱利用率仅为20%,也就是说还有80%的二级质谱图谱没有得到有效利用,对海马蛋白质组学的进一步研究还依赖于海马蛋白质组学数据库和基因组数据的完善。以往对于海马的研究主要集中在传统的分离鉴定和药理研究等方面,而对提取的海马蛋白进行系统分析目前未见报道。应用高通量蛋白质组学方法即应用液质方法结合数据库比对的策略,研究海马蛋白质组对海马有效成分的分析和海马药材的鉴定具有重要意义。
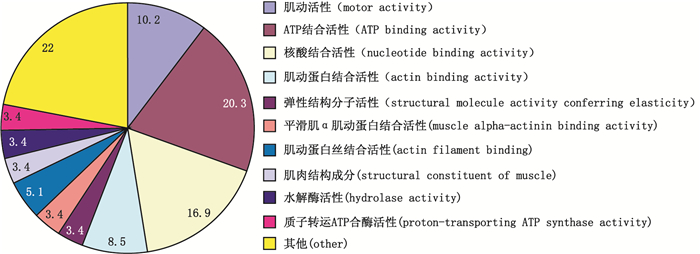
3.3 提取海马蛋白质组功能分析对鉴定到的192种蛋白质在DAVID Bioinformatics Resources 6.8数据库中搜索分析,考察了海马蛋白质的分子功能,具体分布见图 3。由图 3可见,在所鉴定的蛋白质中,具有结合活性的蛋白质占较大比例(54.2%),进一步分析结合活性蛋白,ATP结合活性蛋白含量最高(20.3%),嘌呤核苷酸结合活性次之(16.9%),此外还包括肌动结合蛋白活性、微丝结合蛋白活性、平滑肌a肌动蛋白结合蛋白活性(如表 2所示),这些功能都参与人体重要的代谢过程[13]。除了有结合活性功能的蛋白质外,海马提取物中的蛋白质主要有以下几大生物功能:肌动活性(motor activity)10.2%,肌动蛋白(actin)具有ATP酶活性,促使ATP发生水解而释放自由能,为肌肉收缩和细胞运动提供能量[14]。弹性结构分子活性3.4%,肌肉结构成分3.4%,水解酶活性3.4%,质子转运ATP合酶活性3.4%[15-17],通过对鉴定蛋白功能的分析,主要参与能量代谢过程以及结构成分,这些功能可能与海马药材的强壮补益功效有关。
|
图 3 海马提取蛋白质功能分布饼图 Figure 3 Pie chart of functional classification of proteins extracted from Hippocampus |
|
|
表 2 海马提取蛋白质组功能分析结果 Table 2 Results of functional classification of proteins extracted from Hippocampus by proteomic analysis |
本研究以重要海马干燥体为原料,经三氯乙酸/丙酮沉淀法得到海马蛋白提取物,利用蛋白质组学的研究思路,应用高通量、高灵敏度的nanoRPLC-MS/MS技术结合聚丙烯酰胺凝胶电泳方法,系统分析了海马提取蛋白质胶内酶解产物,并进行数据库检索鉴定蛋白质,对部分蛋白质的功能进行了分析,为海马蛋白质的生物活性以及海马药材的鉴别和有效成分研究奠定了基础。
| [1] |
中国药典2015年版. 一部[S]. 2015: 275 ChP 2015. Vol Ⅰ[S]. 2015: 275 |
| [2] |
朱苗, 谢勇, 卢忠英, 等. 海马活性成分提取技术研究进展[J]. 广州化工, 2015, 43(10): 19. ZHU M, XIE Y, LU ZY, et al. Research progress of active ingredient extraction technology from seahorses[J]. Guangzhou Chem Ind, 2015, 43(10): 19. |
| [3] |
王斌, 任西杰, 王燕, 等. 基于聚类、主成分和判别分析的海马醇提物红外指纹图谱研究[J]. 中国药学杂志, 2013, 48(4): 253. WANG B, REN XJ, WANG Y, et al. Fingerprint analysis of Hippocampus's ethanol extracts coupled with cluster analysis, principal component analysis and discriminant analysis[J]. Chin Pharm J, 2013, 48(4): 253. |
| [4] |
严家彬, 马润娣, 于立坚. 海马的药用价值[J]. 中国海洋药物, 2002, 21(6): 48. YAN JB, MA RD, YU LJ. Medicinal values of Hippocampus[J]. Chin J Mar Drugs, 2002, 21(6): 48. |
| [5] |
KUMARAVEL K, RAVICHANDRAN S, BALASUBRAMANIAN T, et al. Seahorses-a source of traditional medicine[J]. Nat Prod Res, 2012, 26(24): 2330. DOI:10.1080/14786419.2012.662650 |
| [6] |
NYNCA J, ARNOLD GJ, FROHLICH T, et al. Proteomic identification of rainbow trout sperm proteins[J]. Proteomics, 2014, 14(12): 1569. DOI:10.1002/pmic.v14.12 |
| [7] |
SKIPP P, ROBINSON J, O'CONNOR CD, et al. Shotgun proteomic analysis of Chlamydia trachomatis[J]. Proteomics, 2005, 5(6): 1558. DOI:10.1002/(ISSN)1615-9861 |
| [8] |
LAGRAIN B, BRUNNBAUER M, ROMBOUTS I, et al. Identification of intact high molecular weight glutenin subunits from the wheat proteome using combined liquid chromatography-electrospray ionization mass spectrometry[J]. PLoS One, 2013, 8(3): e58682. DOI:10.1371/journal.pone.0058682 |
| [9] |
POSSENTI A, FRATINI F, FANTOZZI L, et al. Global proteomic analysis of the oocyst/sporozoite of Toxoplasma gondii reveals commitment to a host-independent lifestyle[J]. BMC Genomics, 2013, 14: 183. DOI:10.1186/1471-2164-14-183 |
| [10] |
FORNÉ I, ABIÁN J, CERDÀ J. Fish proteome analysis:model organisms and non-sequenced species[J]. Proteomics, 2010, 10(4): 858. DOI:10.1002/pmic.v10:4 |
| [11] |
NATARAJAN S, XU C, CAPERNA TJ, et al. Comparison of protein solubilization methods suitable for proteomic analysis of soy-bean seed proteins[J]. Anal Biochem, 2005, 342(2): 214. DOI:10.1016/j.ab.2005.04.046 |
| [12] |
JIN MY, DONG L, DAI JD, et al. Determination of the content of protein in pilose antler processed by different methods with bradford method[J]. Chin Arch Tradit Chin Med, 2015, 33: 592. |
| [13] |
Liu S, Cerione RA, Clardy J. Structural basis for the guanine nucleotide-binding activity of tissue transglutaminase and its regulation of transamidation activity[J]. Proc Natl Acad Sci USA, 2002, 99(5): 2743. DOI:10.1073/pnas.042454899 |
| [14] |
Corner MA, Schenck CH. Perchance to dream? Primordial motor activity patterns in vertebrates from fish to mammals:their prenatal origin, postnatal persistence during sleep, and pathological reemergence during REM sleep behavior disorder[J]. Neurosci Bull, 2015, 31(6): 649. DOI:10.1007/s12264-015-1557-1 |
| [15] |
Chaterji S, Kim P, Choe SH, et al. Synergistic effects of matrix nanotopography and stiffness on vascular smooth muscle cell function[J]. Tissue Eng, 2014, 20(15-16): 2115. DOI:10.1089/ten.tea.2013.0455 |
| [16] |
Honecker F, Rohlfing T, Harder S, et al. Proteome analysis of the effects of all-trans retinoic acid on human germ cell tumor cell lines[J]. J Proteomics, 2014, 96(2): 300. |
| [17] |
Owen A, Sener A, Malaisse WJ. Stimulus-secretion coupling of glucose-induced insulin release.LI.Divalent cations and ATPase activity in pancreatic islets[J]. Enzyme, 1983, 29(1): 2. DOI:10.1159/000469598 |
 2018, Vol. 38
2018, Vol. 38 
