地龙为我国常用动物类中药,来源于钜蚓科动物参环毛蚓Pheretima aspergillum(E.Perrier)、通俗环毛蚓Pheretima vulgaris Chen、威廉环毛蚓Pheretima guillelmi(Michaelsen)或栉盲环毛蚓Pheretima pectinifera Michaelsen的干燥体。前1种习称“广地龙”,后3种习称“沪地龙”[1]。沪地龙味咸性寒,归肝、脾、膀胱经,具有清热止痉、平肝熄风、通经活络、平喘利尿的功效,用于高热神昏、惊痫抽搐、关节痹痛、肢体麻木、半身不遂、肺热喘咳、尿少水肿、高血压等症[2-3]。临床研究表明,核苷类成分是沪地龙舒张支气管、抗组胺、平喘的重要药用物质基础[4-8];其中次黄嘌呤、黄嘌呤的含量与地龙药材止咳化痰平喘的药效作用成正相关[9]。
目前关于中药中核苷类成分的含量测定方法已有较多文献报道[10-12],而以沪地龙为考察对象的研究尚不多见。吴文如等[13]采用Symmetry C18色谱柱,以10 mmol·L-1磷酸二氢钾溶液和甲醇为流动相,梯度洗脱,测定了地龙药材中尿嘧啶、次黄嘌呤、尿苷和肌苷的含量;季倩等[14]采用SORBAX SB-Aq色谱柱,以5 mmol·L-1磷酸二氢钾溶液为流动相,测定了地龙药材中次黄嘌呤、黄嘌呤、尿嘧啶和尿苷的含量;基于黄帅等[15]对地龙核苷类成分的特征图谱研究以及本课题组前期的物质基础研究工作,本实验以尿嘧啶、次黄嘌呤、黄嘌呤、尿苷、肌苷、鸟苷和2’-脱氧鸟苷为指标成分,建立同时评价该7个指标成分的高效液相色谱法,并对前处理方法进行优化。该方法可为沪地龙药材的质量评价提供依据。
1 仪器与试药 1.1 仪器Agilent 1260高效液相色谱仪,配Agilent G4212B紫外检测器和OpenLAB CDS版本C.01.07色谱工作站(Agilent公司);Phenomenex Gemini C18(250 mm×4.6 mm,5 μm,填料:十八烷基硅烷键合硅胶;Phenomenex公司);BP211D型和CP224S型电子分析天平(Sartorius公司);CENRIFUGE 5810R离心机(Eppendorf公司);Elmasonic E300H超声波清洗仪(Elma公司)。
1.2 试药甲醇,色谱纯(美国MERCK公司);5 mol·L-1乙酸铵水溶液,色谱纯(美国SIGMA-ALDRICH公司);浓盐酸,分析纯(含氯化氢36%~38%的水溶液,国药集团化学试剂有限公司);浓氨水,分析纯(含氨25%~28%的的水溶液,上海凌峰化学试剂有限公司);冰乙酸,分析纯(上海凌峰化学试剂有限公司);氯化钠,分析纯(上海凌峰化学试剂有限公司);去离子水(美国Millipore公司);尿嘧啶(批号100469-201302,含量99.6%)、次黄嘌呤(批号140661-200903,含量99.6%)的对照品购自中国食品药品检定研究院;黄嘌呤(批号WXBC0529V,含量99.0%)、尿苷(批号054K1280,含量99.0%)、肌苷(批号043K0079,含量99.0%)、鸟苷(批号BCBM5446V,含量98.0%)、2’-脱氧鸟苷(批号MKBS7406V,含量99.0%)的对照品购自美国SIGMA-ALDRICH公司;沪地龙药材由上海康桥中药饮片有限公司提供,药材产地及规格见表 1。
|
|
表 1 药材产地及规格 Table 1 Origins and specifications of Shanghai Pheretima |
0.9%生理盐水:取氯化钠9 g,加水1 000 mL,摇匀,即得。1%氨水:取20 mL浓氨水(含氨25%~28%的水溶液)置于500 mL量瓶中,用水定容至刻度,摇匀,即得。0.1%氨水:取2 mL浓氨水(含氨25%~28%的的水溶液)置于500 mL量瓶中,用水定容至刻度,摇匀,即得。4%盐酸:取10 mL浓盐酸(含氯化氢36%~38%的水溶液)置于100 mL量瓶中,用水定容至刻度,摇匀,即得。0.4%盐酸:取10 mL浓盐酸(含氯化氢36%~38%的水溶液)置于1 000 mL量瓶中,用水定容至刻度,摇匀,即得。1%醋酸:取1 mL冰醋酸置于100 mL量瓶中,用水定容至刻度,摇匀,即得。0.1%醋酸:取1 mL冰醋酸置于1 000 mL量瓶中,用水定容至刻度,摇匀,即得。
2.1.2 对照品储备液精密称取尿嘧啶、次黄嘌呤、黄嘌呤、鸟苷的对照品各20 mg,分别置于20 mL量瓶中,用0.1%氨水溶解并定容至刻度,分别作为尿嘧啶、次黄嘌呤、黄嘌呤、鸟苷的对照品储备液;精密称取尿苷、肌苷、2’-脱氧鸟苷的对照品各20 mg,分别置于20 mL量瓶中,用水溶解并定容至刻度,分别作为尿苷、肌苷、2’-脱氧鸟苷的对照品储备液。
2.1.3 混合对照品溶液精密吸取对照品储备液各1 mL于10 mL量瓶中,加4%盐酸约1.6 mL调pH至中性,用水稀释至刻度,即得质量浓度均为100 μg·mL-1的混合对照品溶液;精密吸取100 μg·mL-1混合对照品溶液5 mL至10 mL量瓶中,加水稀释至刻度,得50 μg·mL-1混合对照品溶液;精密吸取50 μg·mL-1混合对照品溶液2 mL至10 mL量瓶中,加水稀释至刻度,得10 μg·mL-1混合对照品溶液;精密吸取50 μg·mL-1混合对照品溶液1 mL至10 mL量瓶中,加水稀释至刻度,得5 μg·mL-1混合对照品溶液;精密吸取10 μg·mL-1混合对照品溶液1 mL至10 mL量瓶中,加水稀释至刻度,得1 μg·mL-1混合对照品溶液;精密吸取5 μg·mL-1混合对照品溶液1 mL至10 mL量瓶中,加水稀释至刻度,得0.5 μg·mL-1混合对照品溶液。
2.1.4 供试品溶液取样品粉末(过24目筛)约2.5 g,精密称定,置具塞锥形瓶中,精密加入0.1%氨水50 mL,密塞,摇匀,称量,浸泡30 min。然后超声处理(功率250 W,频率40 kHz)30 min,放冷,再称量,用0.1%氨水补足减失的量,摇匀,移至50 mL离心管中,4 000 r·min-1离心5 min;精密量取上清液5 mL,移至10 mL量瓶中,加0.4%盐酸约2 mL调pH至中性,加水定容至刻度,摇匀,移至15 mL离心管中,4 000 r·min-1离心5 min。取上清液,用微孔滤膜滤过,取续滤液,即得。
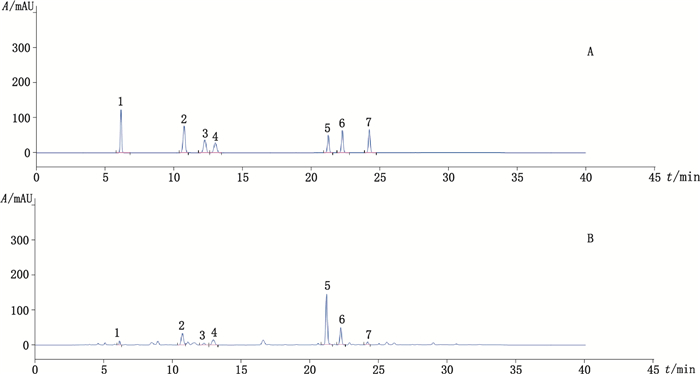
2.2 色谱条件色谱柱:Phenomenex Gemini C18(250 mm×4.6 mm,5 μm);流动相:以甲醇(A)-5 mmol·L-1乙酸铵溶液(B),按表 2程序进行梯度洗脱,流速1.0 mL·min-1;检测波长:254 nm;柱温:30 ℃;进样量:10 μL。在上述色谱条件下,对照品与样品色谱图见图 1。
|
|
表 2 梯度洗脱程序 Table 2 Gradient elution program |
|
1.尿嘧啶(uracil)2.次黄嘌呤(hypoxanthine)3.黄嘌呤(xanthine)4.尿苷(uridine)5.肌苷(inosine)6.鸟苷(guanosine)7.2’-脱氧鸟苷(2’-deoxyguanosine) 图 1 混合对照品(A)与5号样品(B)HPLC色谱图 Figure 1 HPLC chromatograms of mixed reference substances(A) and sample No. 5(B) |
精密吸取“2.1.3”项下系列混合对照品溶液各10 μL,注入液相色谱仪,分别测定。以对照品质量浓度(X)为横坐标,以峰面积值(Y)为纵坐标,绘制标准曲线,计算回归方程,测定结果见表 3。
|
|
表 3 线性关系考察 Table 3 Linearity of 7 nucleoside components |
精密吸取10 μg·mL-1混合对照品溶液10 μL,连续进样分析6次,记录各对照品色谱峰面积,计算RSD。结果显示尿嘧啶、次黄嘌呤、黄嘌呤、尿苷、肌苷、鸟苷、2’-脱氧鸟苷峰面积的RSD(n=6)分别为0.075%、0.064%、0.057%、0.066%、0.032%、0.081%、0.072%,表明方法的精密度良好。
2.3.3 稳定性取5号样品,按“2.1.4”项下方法制备供试品溶液1份。精密吸取供试品溶液10 μL,分别于0、1、2、3、6、9、12、18、24 h进样分析,记录峰面积,计算RSD;结果尿嘧啶、次黄嘌呤、黄嘌呤、尿苷、肌苷、鸟苷、2’-脱氧鸟苷峰面积的RSD(n=9)分别为2.3%、1.0%、0.99%、2.2%、0.60%、0.23%、1.1%,表明供试品溶液在24 h内稳定。
2.3.4 重复性取5号样品,按“2.1.4”项下方法同时制备供试品溶液6份,进样测定,记录峰面积,按标准曲线法计算各成分含量;结果样品中尿嘧啶、次黄嘌呤、黄嘌呤、尿苷、肌苷、鸟苷、2’-脱氧鸟苷平均含量(n=6)分别为0.079、0.383、0.109、0.407、2.337、0.710、0.100 mg·g-1,RSD分别为1.9%、2.5%、3.7%、3.0%、1.4%、3.2%、2.2%,表明方法的重复性较好。
2.3.5 加样回收率精密称取5号样品约1.25 g,一式6份,分别精密加入质量浓度为1 mg·mL-1的各对照品储备液适量(尿嘧啶储备液0.1 mL,次黄嘌呤储备液0.5 mL,黄嘌呤储备液0.2 mL,尿苷储备液0.5 mL,肌苷储备液3 mL,鸟苷储备液0.75 mL,2’-脱氧鸟苷储备液0.125 mL),按“2.1.4”项下方法制备供试溶液,记录峰面积,计算加样回收率;结果尿嘧啶、次黄嘌呤、黄嘌呤、尿苷、肌苷、鸟苷、2’-脱氧鸟苷平均回收率(n=6)分别为98.6%、104.6%、105.3%、96.2%、91.0%、88.1%、106.5%,RSD分别为2.6%、1.8%、1.4%、2.6%、0.42%、2.1%、2.1%,表明方法的准确度较好。
2.4 样品含量测定取不同产地规格的沪地龙样品12批,一式2份,按“2.1.4”项下方法制备供试品溶液,进样测定,按标准曲线法计算7个核苷类成分的含量,结果见表 4。不同样品的尿嘧啶、黄嘌呤的含量差异较大,原因有待分析。
|
|
表 4 样品含量测定结果(mg·g-1,n=2) Table 4 Determination of 7 nucleoside components in Shanghai Pheretima |
在建立本方法之初,曾对Agilent公司ZORBAX SB-C18(250 mm×4.6 mm,5 μm)、Waters公司XBridge C18(250 mm×4.6 mm,5 μm)、Phenomenex公司Synergi C18(250 mm×4.6 mm,5 μm)、Phenomenex公司Luna C18(250 mm×4.6 mm,5 μm)、Phenomenex公司Kinetex C18(250 mm×4.6 mm,5 μm)和Phenomenex公司Gemini C18(250 mm×4.6 mm,5 μm)6种不同品牌的液相色谱柱进行了比较。对照品溶液测定结果显示,采用ZORBAX SB-C18和Synergi C18色谱柱时次黄嘌呤和黄嘌呤色谱峰都存在明显的拖尾现象,同时采用Synergi C18色谱柱时黄嘌呤和尿苷色谱峰有较严重的重叠,而采用其他色谱柱时的分离效果相对较好。供试品溶液测定结果显示,采用XBridge C18色谱柱时尿嘧啶和次黄嘌呤色谱峰与样品基质色谱峰存在较严重的重叠现象,采用Kinetex C18色谱柱时次黄嘌呤色谱峰与样品基质色谱峰存在较严重的重叠现象,采用Luna C18和Gemini C18色谱柱时对供试品溶液各色谱峰的分离效果相对较好,但采用Luna C18色谱柱时不适合长时间用纯水相洗脱,故最终选择采用Gemini C18色谱柱建立沪地龙中7个核苷类成分的含量测定方法。
根据文献报道,供试品溶液制备方式考察了超声提取法和回流提取法[15-16]。与回流提取法相比,超声提取法对待测物的提取效率相对较高,且待测物被药材基质色谱峰干扰的程度小。改变超声提取时间从30 min到60 min,对待测物的提取效率没有显著影响。因此,采用超声提取30 min的方法作为沪地龙中核苷类化合物的前处理方法。由于尿嘧啶、次黄嘌呤、黄嘌呤和鸟苷对照品在水中的溶解度较差,在碱性溶剂中溶解度较好,所以提取溶剂也尝试了不同pH的溶剂,包括水、生理盐水、0.1%氨水、1%氨水、0.1%醋酸、1%醋酸、0.4%盐酸、4%盐酸等;提取效果由好至差顺序为0.1%氨水、生理盐水、水、1%氨水、0.1%醋酸、1%醋酸、0.4%盐酸、4%盐酸,故最终采用0.1%氨水作为提取溶剂。
另有一个问题值得注意,采用水或生理盐水作为提取溶剂,所得供试品溶液放置过夜后,有沉淀析出,稳定性较差,这与季倩等[14]的研究结果相符。经分析,沉淀析出的原因可能是:沪地龙药材富含蛋白质,采用水或生理盐水超声提取,所得溶液中蛋白质浓度过高,放置过程中可能随温度改变或缓慢盐析作用,造成蛋白质析出现象。将沉淀后的供试品溶液再次离心,上清液经液相色谱分析,次黄嘌呤、尿嘧啶含量显著上升,黄嘌呤含量上升,尿苷、肌苷、鸟苷、2’-脱氧鸟苷色谱峰消失。该原因可能是由于提取溶液里仍含有活性酶,在室温、水或生理盐水环境下,将核苷的糖苷键水解,所以色谱分析结果显示碱基含量上升,核苷含量下降。而采用0.1%氨水超声提取,可能在超声提取过程中就已导致大部分酶变性,并且在后续调pH至中性的过程中,加大了溶液的盐浓度,会使得蛋白质直接大量析出,相当于提前去除蛋白质杂质。因此,其所得最终供试品溶液可以稳定放置24 h。
本实验建立了HPLC法同时测定沪地龙药材中7个核苷类成分的含量,该方法简单、有效、准确,可以考虑作为沪地龙药材的质量控制标准。
| [1] |
中国药典2015年版. 一部[S]. 2015: 122 ChP 2015. Vol Ⅰ[S]. 2015: 122 |
| [2] |
刘亚明, 郭继龙, 刘必旺, 等. 中药地龙的活性成分及药理作用研究进展[J]. 山西中医, 2011, 27(3): 44. LIU YM, GUO JL, LIU BW, et al. Research progress in the active ingredients and pharmacological effects of Pheretima[J]. Shanxi J TCM, 2011, 27(3): 44. |
| [3] |
殷书梅, 储益平, 吴鹏. 地龙活性提取物的主要药效学试验[J]. 中草药, 2002, 33(10): 926. YIN SM, CHU YP, WU P. Pharmacodynamic test of active extract of Lumbricus[J]. Chin Tradit Herb Drugs, 2002, 33(10): 926. DOI:10.3321/j.issn:0253-2670.2002.10.029 |
| [4] |
张晓晨. 地龙药理与临床研究进展[J]. 中成药, 2011, 33(9): 1574. ZHANG XC. Pharmacological and clinical research progress of Pheretima[J]. Chin Tradit Pat Med, 2011, 33(9): 1574. |
| [5] |
HUANG CQ, LI W, WU B, et al. Pheretima aspergillum decoction suppresses inflammation and relieves asthma in a mouse model of bronchial asthma by NF-κB inhibition[J]. J Ethnopharmacol, 2016, 189: 22. DOI:10.1016/j.jep.2016.05.028 |
| [6] |
CHU XP, XU ZH, WU DZ, et al. In vitro and in vivo evaluation of the anti-asthmatic activities of fractions from Pheretima[J]. J Ethnopharmacol, 2007, 111(3): 490. DOI:10.1016/j.jep.2006.12.013 |
| [7] |
杜航, 孙佳明, 郭晓庆, 等. 地龙的化学成分及药理作用[J]. 吉林中医药, 2014, 34(7): 707. DU H, SUN JM, GUO XQ, et al. Chemical constituents and pharmacological effects of Pheretima[J]. Jilin J Tradit Chin Med, 2014, 34(7): 707. |
| [8] |
木海鸥, 苏孝共. 地龙的药理研究概要[J]. 中国药业, 2007, 16(1): 61. MU HO, SU XG. Overview of pharmacological research on Pheretima[J]. China Pharm, 2007, 16(1): 61. |
| [9] |
利红宇, 李钟, 黄艳玲, 等. 不同炮制的广地龙平喘化痰止咳药效比较[J]. 时珍国医国药, 2010, 21(6): 1464. LI HY, LI Z, HUANG YL, et al. Comparison of the expectorant, antitussive and antiasthmatic effects of Pheretima aspergillum prepared by different processing methods[J]. Lishizhen Med Mater Med Res, 2010, 21(6): 1464. |
| [10] |
毛坤军, 李富强, 白钢钢, 等. HPLC同时测定虎力散片剂中10个核苷和碱基类成分含量[J]. 药物分析杂志, 2014, 34(11): 1959. MAO KJ, LI FQ, BAI GG, et al. Simultaneous determination of ten nucleoside and nuclebase components in Hulisan tablets by HPLC[J]. Chin J Pharm Anal, 2014, 34(11): 1959. |
| [11] |
肖平, 陈建伟, 李祥. 高效毛细管电泳法同时测定板蓝根药材中7种核苷类成分的含量[J]. 中国药学杂志, 2014, 49(7): 604. XIAO P, CHEN JW, LI X. Simultaneous determination of seven nucleosides in Isatidis Radix by HPCE[J]. Chin Pharm J, 2014, 49(7): 604. |
| [12] |
张文萌, 贾玉荣, 付锦楠, 等. RP-HPLC法同时测定熟地黄中5个核苷类成分的含量[J]. 药物分析杂志, 2013, 33(1): 94. ZHANG WM, JIA YR, FU JN, et al. RP-HPLC simultaneous determination of five nucleosides in Radix Rehmanniae Preparata[J]. Chin J Pharm Anal, 2013, 33(1): 94. |
| [13] |
吴文茹, 李薇, 赖小平. HPLC法测定不同产地地龙中尿嘧啶、次黄嘌呤、尿苷、肌苷的含量[J]. 中国药师, 2011, 14(7): 914. WU WR, LI W, LAI XP. Determination of uracil, hypoxantine, uridine and inosine in Earthworm from different habitats by HPLC[J]. China Pharm, 2011, 14(7): 914. |
| [14] |
季倩, 高守红, 张汉明, 等. HPLC法测定各沪产地龙和广地龙中次黄嘌呤、黄嘌呤、尿嘧啶和尿苷的含量[J]. 第二军医大学学报, 2015, 36(4): 443. JI Q, GAO SH, ZHANG HM, et al. HPLC in determination of hypoxanthine, xanthine, uridine and uracil in Shanghai Pheretima and Pheretima aspergillum (E.Perrier)[J]. Acad J Second Mil Med Univ, 2015, 36(4): 443. |
| [15] |
黄帅, 徐风, 杨平, 等. 地龙的HPLC特征图谱研究[J]. 中国药房, 2015, 26(21): 2971. HUANG S, XU F, YANG P, et al. Study on the HPLC characteristic chromatogram of Pheretima[J]. J China Pharm, 2015, 26(21): 2971. DOI:10.6039/j.issn.1001-0408.2015.21.33 |
| [16] |
刘丽芳, 金蓉鸾, 徐国钧. HPLC法测定10种动物药中尿嘧啶、黄嘌呤、次黄嘌呤、脲苷的含量[J]. 中国中药杂志, 1999, 24(2): 73. LIU LF, JIN RL, XU GJ. HPLC determination of uracil xanthine, hypoxanthine and uridine in ten species of animal drugs[J]. China J Chin Mater Med, 1999, 24(2): 73. |
 2018, Vol. 38
2018, Vol. 38 
