2. 湖南省中医药研究院, 长沙 410013;
3. 湖南中医药大学, 长沙 410208
2. Hunan Academy of TCM, Changsha 410013, China;
3. Hunan University of Chinese Medicine, Changsha 410208, China
活血促愈胶囊由三七、积雪草、丹参、槐米4味中药组成,具有活血散瘀、消肿止痛之功效,用于急性软组织损伤、骨折早期瘀血阻滞所致的肿胀,疼痛,肢体功能障碍[1-3]。三七为方中君药,积雪草为臣药,三七中所含人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1是活血、止痛、抗炎与止血的主要有效成分[4]。积雪草所含积雪草苷、羟基积雪草苷能够在创伤愈合过程中促进成纤维细胞增生,细胞处基质的合成,抑制胶原的生成,干预瘢痕形成及抗炎作用[5]。经查阅文献,在质量控制方面,单独测定三七、积雪草中1种或几种有效成分的方法比较多[7-16],同时测定2味药的成分未见报道。根据本制剂的功能主治,为了能整体性地评价其质量,本试验采用HPLC法同时测定人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1、积雪草苷、羟基积雪草苷5个有效成分的含量,为活血促愈胶囊的质量控制提供依据。
1 仪器与试药 1.1 仪器岛津公司LC-20AT高效液相色谱仪,岛津公司SPD-20A紫外检测器,AKZO NOBEL公司kromsil 100-5-C18色谱柱(250 mm×4.6 mm,5 μm;填料:十八烷基硅烷键合硅胶),梅特勒-托利多公司Mettler Toledo XPE105电子分析天平(十万分之一),武汉恒信世纪科技有限公司HX-06超声波清洗器。
1.2 试药对照品人参皂苷Rg1(批号110703-201530)、人参皂苷Rb1(批号110704-201424)、三七皂苷R1(批号110745-201318)、积雪草苷(批号110892-201505)、羟基积雪草苷(批号110893-201403)均购自中国食品药品检定研究院。活血促愈胶囊(本课题组自制,批号20150811、20150817、20150822)。实验用所有原药材均购自湖南上药九旺医药有限公司,经湖南省中医药研究院生药室鉴定,均为相应原药材。乙腈为色谱纯(购自Tedia公司),正丁醇、氨水、甲醇均为分析纯(购自长沙市汇虹化玻仪器设备有限公司),水为怡宝纯净水。
2 方法与结果 2.1 色谱条件采用Kromsil 100-5-C18色谱柱(250 mm×4.6 mm,5 μm),以乙腈(A)-水(B)为流动相,梯度洗脱(0~20 min,19%A→35%A;20~35 min,35%A→40%A),流速1 mL·min-1,检测波长203 nm,柱温30 ℃,进样量10 μL(对照品溶液)、20 μL(供试品溶液及阴性样品溶液)。在上述色谱条件下,人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1、积雪草苷、羟基积雪草苷理论板数均不少于4 000。
2.2 溶液的制备 2.2.1 混合对照品溶液精密称取对照品人参皂苷Rg1 17.55 mg,人参皂苷Rb1 15.96 mg,三七皂苷R1 16.95 mg,积雪草苷13.87 mg,羟基积雪草苷16.38 mg,分别加甲醇制成每1 mL含人参皂苷Rg1 3.51 mg、人参皂苷Rb1 3.192 mg、三七皂苷R1 0.678 mg、积雪草苷1.387 mg、羟基积雪草苷3.276 mg的对照品储备液。
分别精密量取上述对照品储备液各1 mL,置同一10 mL量瓶中,加甲醇制成每1 mL含人参皂苷Rg1 0.351 mg,人参皂苷Rb1 0.319 2 mg,三七皂苷R1 0.067 8 mg,积雪草苷0.138 7 mg,羟基积雪草苷0.327 6 mg的混合对照品溶液。
2.2.2 供试品溶液取活血促愈胶囊内容物适量,研细,混匀,精密称取约0.4 g,置带塞锥形瓶中,精密加入甲醇20 mL,超声(功率250 W,频率40 kHz)处理30 min,滤过,容器及滤渣用甲醇10 mL洗涤,洗液与滤液合并,蒸干,残渣加水15 mL使溶解,用正丁醇(水饱和)振摇提取3次,每次15 mL,合并正丁醇液,用氨试液25 mL洗涤1次,取正丁醇液,用水饱和的正丁醇50 mL洗涤2次,取正丁醇液,分液漏斗用适量正丁醇洗涤,合并洗液与正丁醇液,蒸干,加甲醇溶解残渣,移至10 mL量瓶中,加甲醇至刻度,摇匀,过滤(0.45 μm的微孔滤膜),初滤液弃去,取续滤液,即得。
2.2.3 阴性样品溶液按照活血促愈胶囊处方及工艺制备缺积雪草、缺三七的阴性样品,再按“2.2.2”项下方法制成缺积雪草、缺三七的阴性样品溶液。
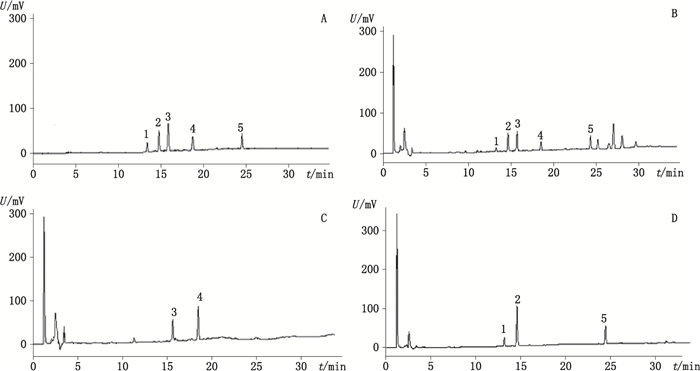
2.3 专属性试验分别取混合对照品溶液10 μL,供试品溶液与阴性样品溶液各20 μL,按上述设定的色谱条件进样测定,高效液相色谱图见图 1。阴性样品在与样品中人参皂苷Rg1、人参皂Rb1、三七皂苷R1、积雪草苷、羟基积雪草苷相应的保留时间处无色谱峰干扰,说明本方法专属性好。
|
1.三七皂苷R1(notoginsenoside R1)2.人参皂苷Rg1(ginsenoside Rg1)3.羟基积雪草苷(madecassoside)4.积雪草苷(asiaticoside)5.人参皂苷Rb1(ginsenoside Rb1) A.混合对照品(mixed reference substances)B.活血促愈胶囊供试品(sample of Huoxue Cuyu capsules)C.缺三七的阴性样品(negative sample without Notoginseng Radix et Rhizoma)D.缺积雪草的阴性样品(negative sample without Centellae Herba) 图 1 活血促愈胶囊HPLC图 Figure 1 HPLC chromatograms of Huoxue Cuyu capsules |
取混合对照品溶液2、5、10、15、20 μL,分别进样测定,将进样X(μg)与峰面积Y进行线性回归,人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1、积雪草苷和羟基积雪草苷的回归方程:
Y=230 416X-3 515.3 r=0.999 6
Y=151 912X+6 088.8 r=0.999 8
Y=303 729X+94.463 r=0.999 9
Y=317 603X+16 245 r=0.999 9
Y=307 109X-8 375.1 r=0.999 9
线性范围分别为0.702~7.02、0.655 2~6.552、0.135 6~1.356、0.277 4~2.774和0.638 4~6.384 μg。
2.5 精密度试验取混合对照品溶液连续进样测定6次,以人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1、积雪草苷、羟基积雪草苷峰面积计,结果RSD分别为0.89%、1.0%、1.8%、1.4%、0.92%,表明仪器精密度良好。
2.6 稳定性试验取批号为20150811的活血促愈胶囊,制备供试品溶液后于室温下分别放置0、2、4、8、12、24 h后进样测定,以人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1、积雪草苷、羟基积雪草苷峰面积计,结果RSD分别为1.1%、1.0%、1.7%、0.98%、1.3%,表明室温条件下供试品溶液24 h内稳定。
2.7 重复性试验取批号为20150811的活血促愈胶囊,按“2.2.2”项下方法平行制备供试品溶液6份,进样测定,记录峰面积,计算含量。结果人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1、积雪草苷、羟基积雪草苷含量平均值分别为4.20、3.82、0.78、1.80和3.16 mg·g-1,RSD分别为1.7%、2.0%、2.2%、2.0%、1.9%,表明本方法重复性良好。
2.8 加样回收率试验精密称取已知含量的活血促愈胶囊样品(批号为20150811)0.2 g共6份,每份分别加入与0.2 g样品中人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1、积雪草苷、羟基积雪草苷含有量相当的对照品,按“2.2.2”项下方法制备供试溶液,进样测定,计算各成分的量,并计算加样回收率,结果见表 1。
|
|
表 1 5个皂苷加样回收率试验结果 Table 1 Results of recovery test of 5 saponins |
取3批活血促愈胶囊,分别按“2.2.2”项下方法制备供试品溶液,进样测定,以外标法计算样品中人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1、积雪草苷、羟基积雪草苷含量,结果见表 2。
|
|
表 2 样品中5种有效成分的含量(mg·g-1,n=3) Table 2 Determination results of the five effective components in different batch number of samples |
本品由4味中药制成,其制备工艺是三七醇提,积雪草、丹参、槐米水提,所以对醇提部分以人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1为指标进行含量测定,水提部分以积雪草苷、羟基积雪草苷为指标进行含量测定,建立的方法能较全面地控制本品的质量。
3.2 供试品溶液制备方法的选择参照《中华人民共和国药典》2015年版一部,比较了直接用甲醇超声处理、甲醇超声处理后再用正丁醇提取以及甲醇超声处理后再用大孔树脂吸附3种方法,结果甲醇超声处理与甲醇超声处理后再用大孔树脂吸附2种方法制备的供试品溶液进行色谱分离时杂质峰多,人参皂苷Rg1峰与后面峰未分开,分离效果不好;甲醇超声处理后再用正丁醇提取制备的供试品溶液杂质峰较少,分离效果好,因此选择此方法作为本品供试品溶液的制备方法。
3.3 检测波长的选择人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1的最大吸收波长为203 nm,积雪草苷、羟基积雪草苷的最大吸收波长为205 nm,考虑到波长选择可以参考最大吸收波长的±2 nm,因此,5个成分均采用203 nm作为测定波长。
3.4 流动相的选择参照《中华人民共和国药典》2015年版一部三七含量测定项下的流动相,结果人参皂苷Rg1、羟基积雪草苷以及积雪草苷三者不能得到较好的分离,经过试验摸索,增加1个梯度程序,则5个成分均能得到较好的分离。
3.5 小结中药复方制剂具有多成分、多靶点、多功效的特点,因此,建立多指标含量测定的质量标准体系,能更好地控制中药制剂的整体质量。本文建立了同时测定活血促愈胶囊中人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1、积雪草苷、羟基积雪草苷含量的方法。经方法学验证,所建立的测定方法符合定量分析要求,测定结果准确,重复性好,可用于活血促愈胶囊的质量控制,同时也为相关有类似组方的复方制剂质量研究提供了参考。
| [1] |
徐琳本, 陈丽萍, 肖梅英. 活血促愈胶囊对外伤血瘀证大鼠模型的影响[J]. 中国实验方剂学杂志, 2013, 19(4): 270. XU LB, CHEN LP, XIAO MY. Effects of Huoxue Cuyu capsules on rats with acute blood stasis[J]. Chin J Exp Tradit Med Form, 2013, 19(4): 270. |
| [2] |
邹旦, 彭六明, 肖放军, 等. 活血促愈胶囊治疗骨折早期软组织损伤30例[J]. 湖南中医杂志, 2012, 28(2): 32. ZOU D, PENG LM, XIAO FJ, et al. Treatment of 30 cases of soft tissue injury in the early stage of the fracture by Huoxue Cuyu capsules[J]. Hunan J Tradit Chin Med, 2012, 28(2): 32. |
| [3] |
陈莉萍, 徐琳本, 肖梅英, 等. 促骨方对家兔实验性骨折愈合的影响及镇痛作用研究[J]. 中药材, 2015, 38(1): 147. CHEN LP, XU LB, XIAO MY, et al. Study on the effect and analgesic effect of promoting bone recipe on experimental fracture healing in rabbits[J]. J Chin Med Mater, 2015, 38(1): 147. |
| [4] |
王莹, 禇杨, 李伟, 等. 三七皂苷成分及药理作用的研究进展[J]. 中草药, 2015, 46(9): 1381. WANG Y, CHU Y, LI W, et al. Advances in study on saponins in Panax notoginseng and their pharmacological activities[J]. Chin Tradit Herb Drugs, 2015, 46(9): 1381. DOI:10.7501/j.issn.0253-2670.2015.09.023 |
| [5] |
丁元, 张翥, 王锁刚. 积雪草苷研究进展[J]. 时珍国医国药, 2016, 27(3): 697. DING Y, ZHANG Z, WANG SG. Research progress of asiaticoside[J]. Lishizhen Med Mater Med Res, 2016, 27(3): 697. |
| [6] |
中国药典2015年版. 一部[S]. 2015: 11, 283 ChP 2015.Vol Ⅰ[S].2015:11, 283 |
| [7] |
覃洁萍, 姚蓉, 苏倩, 等. 高效液相色谱法同时测定复方扶芳藤合剂中人参皂苷Rb1和黄芪甲苷的含量[J]. 中国医院药学杂志, 2012, 32(5): 353. QIN JP, YAO R, SU Q, et al. Determination of ginsenoside Rb1 and astragaloside Ⅳ in compound Fufang mixture by HPLC[J]. Chin J Hosp Pharm, 2012, 32(5): 353. |
| [8] |
徐鹏, 冯素香, 赵迪, 等. HPLC-ELSD法测定血塞通注射液中三七皂苷R1、人参皂苷Rg1、Re、Rb1、Rd[J]. 中成药, 2013, 35(3): 521. XU P, FENG SX, ZHAO D, et al. Determination of notoginsenoside R11 and ginsenoside Rg1, Re, Rb1, Rd in Xue-saitong injection by HPLC-ELSD[J]. Chin Tradit Pat Med, 2013, 35(3): 521. |
| [9] |
柳小亚, 李继平, 陈心悦, 等. HPLC同时测定红芪中8个活性成分的含量及聚类分析[J]. 药学学报, 2016, 51(5): 786. LIU XY, LI JP, CHEN XR, et al. Determination of eight active components in Radix Hedysari by HPLC and its cluster analysis[J]. Acta Pharm Sin, 2016, 51(5): 786. |
| [10] |
郭琪, 程利娟, 雷虹, 等. HPLC法同时测定麻仁润肠丸中9个成分的含量[J]. 药物分析杂志, 2013, 33(10): 1677. GUO Q, CHENG LJ, LEI H, et al. Determination of nine components in Maren Runchang pills by HPLC[J]. Chin J Pharm Anal, 2013, 33(10): 1677. |
| [11] |
韩杰, 孔祥文, 李东辉. HPLC法测定活血止痛胶囊中三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1及阿魏酸[J]. 中成药, 2011, 33(7): 1186. HAN J, KONG XW, LI DH. HPLC determination of four active components in Huoxue Zhitong capsules[J]. Chin Tradit Pat Med, 2011, 33(7): 1186. |
| [12] |
梁李广, 马维. HPLC测定不同产地和不同时间的积雪草中的积雪草苷和羟基积雪草苷[J]. 华西药学杂志, 2009, 24(2): 186. LIANG LG, MA W. Determination of asiaticoside and madecassoside in Centella asiatica urban collected from different seasons and different habitats by HPLC[J]. West China J Pharm Sci, 2009, 24(2): 186. |
| [13] |
蒋平, 髙惠, 王晓梅, 等. 用HPLC法测定积雪草苷涂膜剂中积雪草苷和羟基积雪草苷的含量[J]. 药学服务与研究, 2013, 13(4): 282. JIANG P, GAO H, WANG XM, et al. Determination of contents of asiaticoside and madecassoside in asiaticoside film coating by HPLC method[J]. Pharm Care Res, 2013, 13(4): 282. |
| [14] |
张高菊, 沈勇, 孟珍贵, 等. HPLC法测定姜状三七5种皂苷含量[J]. 药物分析杂志, 2016, 36(3): 500. ZHANG GJ, SHEN Y, MEMG ZG, et al. Determination of 5 saponins in Panax zingiberensis by HPLC[J]. Chin J Pharm Anal, 2016, 36(3): 500. |
| [15] |
吴其国, 符德欢, 王丽, 等. HPLC法测定姜状三七根茎中的人参皂苷Rg1、人参皂苷Rb1及三七皂苷R1[J]. 云南大学学报(自然科学版), 2012, 34(2): 202. WU QG, FU DH, WANG L, et al. Determination of notoginsenoside R1, ginsenoside Rg1 and ginsenoside Rb1 in Panax zingiberensis by HPLC[J]. J Yunnan Univ(Nat Sci Ed), 2012, 34(2): 202. |
| [16] |
张崇禧, 鲍建才, 李向高, 等. HPLC法测定人参、西洋参和三七不同部位中人参皂苷的含量[J]. 药物分析杂志, 2005, 25(10): 1190. ZHANG CX, BAO JC, LI XG, et al. HPLC determination of the amount of ginsenosides in different part of Panax ginseng C.A.Mey.and P.quinquefolius L.and P.notoginseng(Burk)F.H.Chen[J]. Chin J Pharm Anal, 2005, 25(10): 1190. |
 2017, Vol. 37
2017, Vol. 37 
