冠心丹参胶囊是由丹参、三七、降香3味中药材组成的中药成方制剂,已被中国药典2015年版一部收载[1],具有活血化瘀、理气止痛之功效,主要用于气滞血瘀所致心悸气短、胸闷刺痛等,该药单用或联合用药疗效确切,临床上作为冠心病、心绞痛的常用药物[2]。本课题组前期采用质谱定性技术研究了冠心丹参胶囊中的化学成分,结合化学成分研究相关文献,确定了冠心丹参胶囊中含有脂溶性的二萜醌类化合物如隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA和水溶性的酚酸类化合物如丹参素、咖啡酸、迷迭香酸、丹酚酸B、丹酚酸A以及三萜类化合物如熊果酸等[3]。药理学实验研究表明丹参酮类脂溶性物质具有抗肿瘤,保护心肌,抗炎的作用;酚酸类水溶性物质具有抗脂质过氧化,清除自由基,抗肝损伤、肝纤维化和防治动脉粥样硬化的功效;熊果酸还能够显著提高机体的免疫力[4-12]。推测这些成分应该是冠心丹参胶囊发挥临床疗效的物质基础,因此对这些成分进行定量研究对于提高冠心丹参胶囊质量标准和保障其药物稳定性具有重要的意义,近年来已有关于冠心丹参胶囊活性成分含量测定的研究报道,但其测定成分较少,且基本上都是采用HPLC-UV方法测定[13-14],这些方法测定时间较长,且检测灵敏度较差。本研究采用灵敏度、选择性和精确度更高的UPLC-MS技术,通过正、负离子切换扫描,MRM和SIR采集模式同时进行的方式建立了测定冠心丹参胶囊中丹参素、原儿茶醛、咖啡酸、迷迭香酸、丹酚酸B、丹酚酸A、丹参酮Ⅰ、隐丹参酮、丹参酮ⅡA、熊果酸共10个主要活性成分含量的方法,可更加快速、高效和全面地对冠心丹参胶囊进行质量分析和控制。
中药化学成分复杂多样,采用UPLC-MS技术虽然可以在短时间内得到大量的化学成分含量数据,但如何对这些多变量数据进行分析,继而得到中药的质量信息和评价多批次样品的内在质量差异是目前中药质量控制研究中存在的难点问题。主成分分析(principal component analysis,PCA)技术具有从海量数据中抽提出有用数据信息的功能,将该技术应用于复杂的中药成分数据分析中,可系统、准确地提取数据信息和研究中药质量,并使中药质量评价更加数字化、信息化、科学化[15]。SIMCA14.0是一款专业处理多元变量数据的模式识别统计分析软件,该功能中的主成分分析法可对中药的原始多成分变量进行快速提取,重新组合并生成几个综合变量,经数学投影处理后,样本落在主成分平面上的具体位置,即可反映各个样本的总体信息特征,以达到综合评价药物质量的目的。本实验采用的液质联用结合主成分分析法,可更好地表征冠心丹参胶囊的质量,同时为深入研究冠心丹参胶囊质量和提高其质量控制方法奠定基础。
1 仪器和试剂ACQUITY UPLC超高效液相色谱仪(Waters公司);Xevo TQD三重四极杆质谱(Waters公司);ACQUITY UPLC® BEH C18色谱柱(2.1 mm×50 mm,1.7 μm;填料:十八烷基键合硅胶-亚乙基桥杂化颗粒;Waters公司);AL104型万分之一分析天平(METTLER TOLEDO上海有限公司);BX7200HP台式超声波清洗器(上海新苗医疗器械制造有限公司)。
丹参素(A1,批号15082714)、原儿茶醛(A2,批号15091608)咖啡酸(A3,批号15090803)、迷迭香酸(A4,批号15082904)、丹酚酸B(A5,批号15081916)、丹酚酸A(A6,批号16012810)、丹参酮Ⅰ(A7,批号16030210)隐丹参酮(A8,批号16022403)、丹参酮ⅡA(A9,批号15092512)、熊果酸(A10,批号15082905)的对照品均购于成都曼思特生物科技有限公司,均经面积归一法测定,纯度均大于99%。甲醇、乙腈、甲酸为色谱纯,水为超纯水,其他试剂均为分析纯。冠心丹参胶囊胶囊共10个批次(国药控股深圳中药有限公司,批号分别为15115001、151202、140803、15115002、15115003、140802、160102、150705、150301、131104)。
2 方法与结果 2.1 色谱及质谱条件 2.1.1 色谱条件采用ACQUITY UPLCR BEH C18色谱柱(2.1 mm×50 mm,1.7 μm),流动相为乙腈(A)-0.1%甲酸水(B),梯度洗脱(0~2 min,5%A→20%A;2~4 min,20%A→60%A;4~7 min,60%A→95%A),流速0.2 mL·min-1,柱温40 ℃,进样量5 μL。
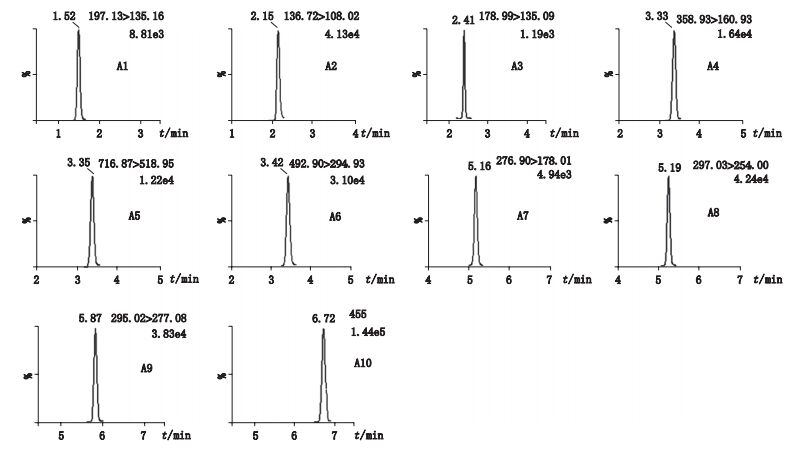
2.1.2 质谱条件离子源为电喷雾离子源(ESI),离子源温度150 ℃,毛细管电压3.5 kV,脱溶剂气和辅助气为氮气,脱溶剂气(氮气)流速650 L·h-1,脱溶剂气温度350 ℃,锥孔气(氮气)流速50 L·h-1,碰撞气(氩气)压力2.85×10−1 Pa,其他主要质谱参数见表 1;在优化的质谱条件下10个待测成分的提取离子流色谱图,见图 1。
|
|
表 1 10种成分的质谱相关参数 Table 1 MS parameters of ten components |
2.2 溶液的制备 2.2.1 混合对照品储备液
取丹参素、原儿茶醛、咖啡酸、迷迭香酸、丹酚酸B、丹酚酸A、丹参酮Ⅰ、隐丹参酮、丹参酮ⅡA、熊果酸的对照品适量,精密称定,以50%甲醇水溶液制备成质量浓度分别为丹参素500.0 μg·mL-1,原儿茶醛24.0 μg·mL-1,咖啡酸2.0 μg·mL-1,迷迭香酸80.0 μg·mL-1,丹酚酸B 60.0 μg·mL-1,丹酚酸A 10.0 μg·mL-1,丹参酮Ⅰ 80.0 μg·mL-1,隐丹参酮120.0 μg·mL-1,丹参酮ⅡA 100.0 μg·mL-1,熊果酸10.0 μg·mL-1的混合对照品储备液。
2.2.2 供试品溶液取冠心丹参胶囊粉末约1.0 g,精密称定,置具塞锥形瓶中,精密加入50%甲醇水溶液20 mL,密塞,称量,超声(200 W,40 kHz)处理30 min,放冷,再称量,用50%甲醇水溶液补足减失的量,摇匀,滤过,续滤液经0.22 μm微孔滤膜滤后即得供试品溶液。
2.3 方法学考察 2.3.1 线性和范围分别精密量取混合对照品储备液适量,50%甲醇水溶液稀释并定容,依次配制成6个浓度的系列梯度溶液,详见表 2。在“2.1”项色谱质谱条件下进样分析,记录峰面积,以各待测物的质量浓度(C,μg·mL-1)为横坐标,以峰面积(Y)为纵坐标,进行线性回归,标准曲线方程及相关系数由Masslynx 4.1计算。以S/N=3计算检测限(LOD),以S/N=10计算定量限(LOQ),结果见表 3。结果表明,10个待测化合物线性关系均良好,r≥0.999 6。
|
|
表 2 10个成分的系列梯度溶液浓度 Table 2 The concentration series of the ten components |
|
|
表 3 10个成分的回归方程、线性范围、相关系数、检测限和定量限 Table 3 The regression equation, liner range, correlation coefficient, LOD and LOQ of ten components |
取中浓度的混合对照品溶液,连续进样6次及连续进样3 d(每天连续进样6次),记录各成分的峰面积并计算相应RSD,结果见表 4,其日内精密度和日间精密度RSD均小于3%。结果表明,仪器精密度良好。
|
|
表 4 10种待测物的精密度、稳定性及重复性考察 Table 4 The results of precision, stability and repeatability of ten components |
取同一供试品溶液(样品批号15115001)和同一混合对照品溶液,分别于0、2、6、10、12、24 h进样分析,记录各成分的峰面积并计算相应RSD,结果见表 4,样品和混合对照品的各峰面积的RSD均小于4%。结果表明,供试品溶液及混合对照品溶液在24 h内基本稳定。
2.3.4 重复性试验取同一批次的冠心丹参胶囊(批号15115001)6份,按“2.2.2”项下方法平行制备供试品溶液,分别进样测定含量并计算RSD。结果见表 4,各待测成分含量的RSD均小于3%,表明该方法重复性良好。
2.3.5 加样回收率试验取同一批次冠心丹参胶囊(批号15115001)粉末约0.5 g共9份,精密称定,分别加入低、中、高3个质量浓度的对照品混合溶液适量,使加入各成分的量分别为冠心丹参胶囊中相应成分含有量的80%、100%和120%;按“2.2.2”项下方法平行制备供试溶液,分别进样测定各成分的量,计算平均回收率及RSD,结果见表 5,各成分平均回收率均在98%~101%之间,RSD均小于3%。结果表明,该方法下10个待测成分的测定准确度较好。
|
|
表 5 加样回收率结果 Table 5 The results of recovery |
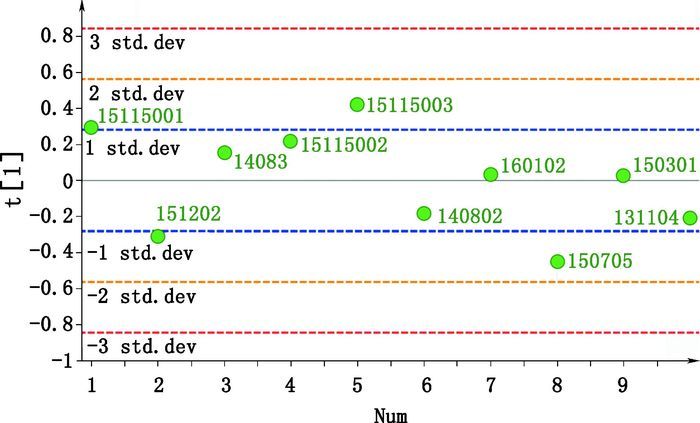
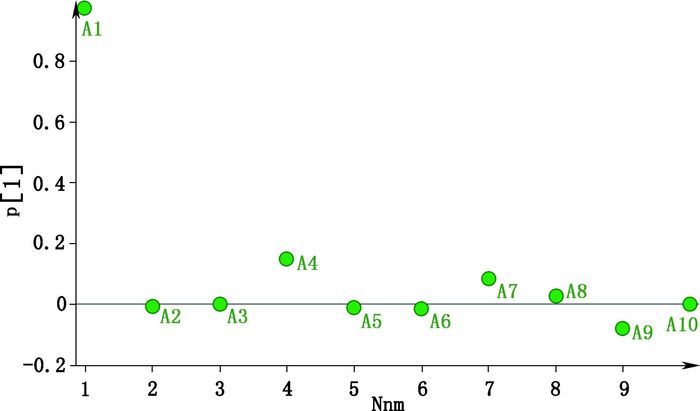
取10个批次的冠心丹参胶囊,按“2.2.2”项下方法平行制备供试品溶液,在“2.1”项色谱质谱条件下进样分析,记录峰面积并计算10个活性成分在冠心丹参胶囊中的含量,结果见表 6,各成分含量在不同批次之间RSD均小于10%。为从整体上比较冠心丹参胶囊不同批次之间的质量稳定性,本实验采用多元数据处理软件SIMCA 14.0对不同批次之间数据进行主成分分析,如图 2,图 2显示不同样品批次的质量偏差均控制在2 SD(standard deviation,标准偏差)内,表明批次之间差异较小,总体质量较为稳定;但批次15115003、150705质量偏差在1 SD-2 SD之间,较其他批次稍有差异,通过载荷图(图 3)分析导致质量差异的主要因素,可知A1(丹参素)及A4(迷迭香酸)对15115003和150705批次的质量偏差贡献最大,提示在以后的生产及质控中可对该2个成分进行重点控制,以减少样品批次之间的质量差异。
|
|
表 6 10批冠心丹参胶囊中10个活性成分的含量测定(mg·g-1) Table 6 The contents of ten active components in ten batches of Guanxin Danshen capsules |
|
图 2 10批冠心丹参胶囊质量得分散点图 Figure 2 The score scatter plot of ten batches of Guanxin Danshen capsules |
|
图 3 10个活性成分载荷图 Figure 3 The loading plot of ten active components |
由于样品检测成分复杂,为使所有成分均具有良好的溶解性,本实验分别考察了提取溶剂(纯甲醇、80%甲醇-水、50%甲醇-水、30%甲醇-水),超声时间(20、30、45、60 min)及溶剂效应对提取成分的影响。结果发现,选择50%甲醇-水作为提取溶剂,超声提取30 min的方法作为提取条件时,10个检测成分的响应好,提取较为完全,无重复析出现象,且溶剂效应不明显。
3.2 色谱质谱条件的确定色谱条件的选择:考察不同比例的甲醇-水、甲醇-甲酸水和乙腈-甲酸水作为流动相系统的分离效果,发现乙腈-0.1%甲酸水作为流动相梯度洗脱时,各个成分的分离效果最佳,色谱峰峰形较好,相邻峰之间均能达到基线分离,适用于该药品中上述组分的检测分析。
质谱条件的选择:实验发现,选择的10个活性成分在不同离子状态和检测模式下采集,响应灵敏度有很大差异,因此研究中采用了正负离子结合多模式检测的方式进行采集。其中A7(丹参酮Ⅰ)、A8(隐丹参酮)、A9(丹参酮ⅡA)采用正离子模式,其他采用负离子模式;A10(熊果酸)采用SIR检测,其他采用MRM检测。通过Mass Tune对主要质谱参数进行优化,确定了最佳的毛细管电压、锥孔电压、碰撞能量和定量离子对。在本实验条件下,A10(熊果酸)的碰撞能过高,且不易得到特征子离子,通过比对熊果酸标准对照品的保留时间和检测离子,采用SIR模式,从而实现对样品中熊果酸成分的定性和定量。
3.3 含量测定含量测定结果表明,10批冠心丹参胶囊中的10个活性成分在含量差异上较小,RSD均在10%范围以内;相关数据经多元数据处理软件SIMCA 14.0进行主成分分析,分析结果表明10批冠心丹参胶囊总体质量较为稳定,质量偏差均在2 SD范围内,但个别批次之间仍有少许差异,可通过对批次质量差异影响较大的样品活性成分进行质控,以使样品批次质量更加稳定。中药中的活性成分复杂多样,且常因采集季节、产地、入药部位的不同而使不同批次之间的含量差异显著,复方制剂的含量更是难以稳定控制。本实验所建立的UPLC-MS/MS方法专属,准确可靠,可对冠心丹参胶囊中的多组分化合物进行测定;同时结合主成分分析技术,可更加全面地评价药物质量,为今后冠心丹参胶囊的质量控制提供了客观的科学依据和参考标准。
| [1] |
中国药典2015年版. 一部[S]. 2015 ChP 2015.Vol Ⅰ[S]. 2015 |
| [2] |
谭巨涛. 冠心丹参胶囊联合阿司匹林治疗急性冠脉综合征[J]. 山西中医, 2010, 26(S1): 3. TAN JT. The acute coronary syndrome cured by Guanxin Danshen capsule combined with aspirin[J]. Shanxi J Tradit Chin Med, 2010, 26(S1): 3. |
| [3] |
刘超. 冠心丹参制剂质量标准研究[D]. 天津: 天津大学, 2008 LIU C. The Quality Standard Investigation of Guanxin Danshen[D]. Tianjin:Tianjin University, 2008 http://cdmd.cnki.com.cn/Article/CDMD-10056-2009073979.htm |
| [4] |
曾金, 张志荣, 廖萍, 等. 隐丹参酮的药理作用研究进展[J]. 中成药, 2015, 37(6): 1309. ZENG J, ZHANG ZR, LIAO P, et al. Research progress on pharmacological activities of cryptotanshinone[J]. Chin Tradit Pat Med, 2015, 37(6): 1309. |
| [5] |
王艳. 丹参酮Ⅰ抗血管生成作用和机制研究[D]. 南昌: 南昌大学, 2015 WANG Y. Studies on the Antiangiogenic Activity and Mechanism of Tanshinone I[D]. Nanchang:Nanchang University, 2015 http://cdmd.cnki.com.cn/Article/CDMD-10411-1015966391.htm |
| [6] |
闫俊, 冯娟, 杨雪, 等. 丹参酮ⅡA的药理作用及疾病治疗的最新进展[J]. 实用药物与临床, 2015, 18(8): 972. YAN J, FENG J, YANG X, et al. Recent progress on pharmacological effects and therapeutic use of tanshinone ⅡA[J]. Pract Pharm Clin Rem, 2015, 18(8): 972. |
| [7] |
王冰瑶, 吴晓燕, 樊官伟. 丹参素保护心血管系统的药理作用机制研究进展[J]. 中草药, 2014, 45(17): 2571. WANG BY, WU XY, FAN GW. Pharmacologic mechanism for protective effects of danshensu on cardiovascular system[J]. Chin Tradit Herb Drugs, 2014, 45(17): 2571. DOI:10.7501/j.issn.0253-2670.2014.17.027 |
| [8] |
杨九凌, 祝晓玲, 李成文, 等. 咖啡酸及其衍生物咖啡酸苯乙酯药理作用研究进展[J]. 中国药学杂志, 2013, 48(8): 577. YANG JL, ZHU XL, LI CW, et al. Pharmacological research progress on caffeic acid and the ramification caffeic acid phenethyl ester[J]. China Pharm J, 2013, 48(8): 577. |
| [9] |
周丹, 刘艾林, 杜冠华. 迷迭香酸的药理学研究进展[J]. 中国新药杂志, 2011, 20(7): 594. ZHOU D, LIU AL, DU GH. Advance in pharmacological research of rosmarinic acid[J]. Chin J New Drugs, 2011, 20(7): 594. |
| [10] |
林超, 刘兆国, 钱星, 等. 丹酚酸B在心血管疾病中药理作用进展[J]. 中国药理学通报, 2015, 31(4): 449. LIN C, LIU ZG, QIAN X, et al. Research progress of salvianolic acid B in cardiovascular diseases[J]. Chin Pharmacol Bull, 2015, 31(4): 449. |
| [11] |
张莉, 张维库, 赵莹, 等. 丹酚酸A的研究与进展[J]. 中国中药杂志, 2011, 36(19): 2603. ZHANG L, ZHANG WK, ZHAO Y, et al. Research progress of salvianolic acid A[J]. China J Chin Mater Med, 2011, 36(19): 2603. |
| [12] |
张明发, 沈雅琴. 齐墩果酸和熊果酸调节血脂、抗肥胖药理作用研究进展[J]. 药物评价研究, 2015, 38(1): 90. ZHANG MF, SHEN YQ. Research progress on lipidemic regulation and antiobesity effects of oleanolic acid and ursolic acid[J]. Drug Eval Res, 2015, 38(1): 90. |
| [13] |
魏惠珍, 王跃生, 吴有根, 等. HPLC同时测定冠心丹参胶囊中丹参素、原儿茶醛、丹酚酸B、和丹参酮ⅡA的含量[J]. 中成药, 2009, 31(1): 64. WEI HZ, WANG YS, WU YG, et al. Simultaneous determination of tanshinol natrium, protocatechuic aldehyde, salvianolic acid B and tanshinone ⅡA in Guanxin Danshen capsule by HPLC[J]. Chin Tradit Pat Med, 2009, 31(1): 64. |
| [14] |
汤杰, 宋冰娜, 郑盼, 等. HPLC测定冠心丹参胶囊中主成分的含量[J]. 中国现代中药, 2015, 17(10): 1078. TANG J, SONG BN, ZHENG P, et al. Determination of main components in Guanxin Danshen capsules by HPLC[J]. Mod Chin Med, 2015, 17(10): 1078. |
| [15] |
张爱华, 陈长宝, 张连学. 化学模式识别在中药质量评价中的应用进展[C]//第六届全国药用植物与植物学术研讨会论文集. 北京: 中国植物学会, 2006: 360 ZHANG AH, CHEN CB, ZHANG LX. Application of Pattern Recognition to Quality Assessment of the Traditional Chinese Medicine[C]//The Academic Symposium Proceedings of the Sixth National Conference on Medicinal Plants and Plant. Beijing:Botanical Society of China, 2006:360 |
 2017, Vol. 37
2017, Vol. 37