2. 内蒙古宇航人药业有限责任公司, 呼和浩特 024000
2. Inner Mongolia Yuhangren Pharmaceutical Limited Liability Company, Huhehaote 024000, China
中药复方制剂中所含的多种化学成分以“整体”的形式作用于机体,其疗效是众多化学成分协同作用的结果,具有多药味多靶点的特点,因此对中药复方制剂质量进行评价和控制的方法应能客观、全面地反映其所含的化学成分。中药色谱指纹图谱能表征中药成分整体特性,是评价中药复方制剂质量的有效手段[1-3]。将色谱指纹图谱技术对中药的定性分析和多指标成分的定量分析有机结合起来,可实现中药质量的全面有效控制[4]。
五味沙棘方始载于《医法海鉴》,又名达尔布班扎,由沙棘、木香、白葡萄干、甘草、栀子5味药材组成。方中沙棘为君药,木香为臣药,白葡萄干、甘草、栀子为佐使药[5]。该方以散剂为主,其他尚有颗粒剂、口服液、胶囊剂,临床上常用于治疗感冒咳嗽、慢性支气管炎、肺脓痈、咯痰不利,疗效可靠,作用机制较为明确[6]。目前对五味沙棘颗粒质量控制的研究主要集中在异鼠李素、栀子苷等成分的含量测定方面,测定成分比较单一,不能全面反映五味沙棘颗粒的质量[7-10]。本文采用HPLC法建立五味沙棘颗粒的特征图谱,并同时测定异鼠李素、栀子苷、甘草酸苷、甘草酸铵的含量,以期为五味沙棘颗粒整体质量控制提供参考。
1 仪器与试药 1.1 仪器日本岛津LC-2010高效液相色谱仪(四元低压梯度,自动进样装置,紫外检测器)、LCsolution工作站,日本岛津公司;溶剂过滤器,天津津腾实验设备有限公司;KQ-500DV型数控超声波清洗器,昆山市超声仪器有限公司;FA2204B型电子天平,上海精密科学仪器有限公司。
1.2 试剂乙腈为色谱纯,磷酸、甲醇为分析纯,试验用水娃哈哈纯净水。
1.3 对照品及药品异鼠李素、栀子苷、甘草苷、甘草酸铵的对照品均购自中国食品药品检定研究院,批号分别为110860-201109、110731-201316、110753-201415、110731-201418;五味沙棘颗粒(批号分别为20131101、20131201、20140201、20140801、20141001、20141101、20150601、20150701、20151001、20151101)均来源于内蒙古宇航人药业有限责任公司。
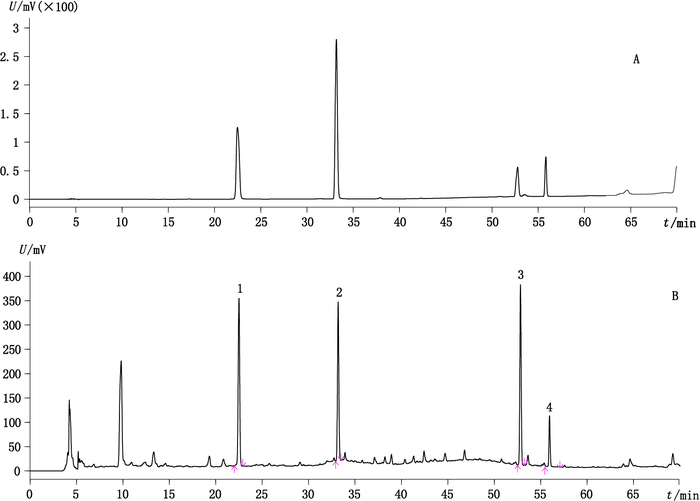
2 方法与结果 2.1 色谱条件岛津公司InertsustainswiftTM C18色谱柱(250 mm×4.6 mm,5 μm;填料:十八烷基硅烷键合硅胶),以乙腈(A)-0.1%磷酸水溶液(B)为流动相,梯度洗脱(0~25 min,5%A→19%A;25~28 min,19%A→23%A;28~34 min,23%A→26%A;34~40 min,26%A→32%A;40~65 min,32%A→58%A),流速1 mL·min-1,检测波长240 nm,柱温35 ℃,进样量20 μL。见图 1。
|
A.混合对照品(mixed reference substances)B.样品(sample,lot:20141101)1.栀子苷(gardenoside)2.甘草苷(liquiritin)3.异鼠李素(isorhamnetin)4.甘草酸(glycyrrhizic acid) 图 1 五味沙棘颗粒高效液相色谱图 Figure 1 HPLC chromatograms of Wuwei Shaji granules |
精密称取栀子苷、甘草苷、异鼠李素、甘草酸铵的对照品适量,加甲醇分别制成对照品储备液(栀子苷1.920 mg·mL-1,甘草苷0.108 mg·mL-1,异鼠李素0.124 mg·mL-1,甘草酸0.200 mg·mL-1);再分别精密量取上述储备液适量,置10 mL量瓶中,用甲醇稀释至刻度,摇匀,得系列浓度混合对照品溶液(质量浓度分别为0.058、0.009、0.006、0.030 mg·mL-1;0.077、0.013、0.008、0.040 mg·mL-1;0.096、0.016、0.010、0.050 mg·mL-1;0.115、0.019、0.012、0.060 mg·mL-1;0.134、0.023、0.014、0.070 mg·mL-1)。
2.2.2 供试品溶液取五味沙棘颗粒粉末约4 g,精密称定,置100 mL具塞锥形瓶中,精密加入80%甲醇水溶液40 mL,称量,超声(40 kHz,200 W)40 min,放冷,用80%甲醇水溶液补足减失的量,摇匀,过滤,续滤液用0.45 μm微孔滤膜过滤,即得。
2.3 特征图谱 2.3.1 精密度试验精密吸取同一供试品溶液(样品批号20141101)20 μL,按“2.1”项色谱条件连续进样测定6次,记录色谱图;以甘草苷为参照峰,计算共有峰的相对保留时间和相对峰面积,RSD均小于3.0%,说明仪器精密度良好。
2.3.2 稳定性试验精密量取同一供试品溶液(样品批号20141101)20 μL,按“2.1”项色谱条件分别于0、2、4、8、12、16、20、24 h进样测定,记录色谱图;以甘草苷为参照峰,计算共有峰的相对保留时间和相对峰面积,RSD均小于3.0%。结果表明,供试品溶液在24 h内稳定。
2.3.3 重复性试验取五味沙棘颗粒粉末(样品批号20141101)约4 g共6份,按“2.2.2”项方法制备供试品溶液,按“2.1”项色谱条件分别进样测定,记录色谱图。以甘草苷为参照峰,计算共有峰的相对保留时间和相对峰面积,RSD均小于3.0%,表明该方法重复性好。
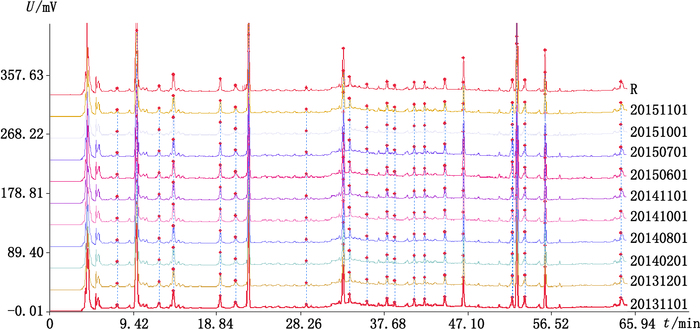
2.3.4 建立特征图谱取10批五味沙棘颗粒粉末,按“2.2.2”项方法制备供试品溶液,分别进样测定,记录65 min液相色谱图。根据结果,采用国家药典委员会“中国色谱指纹图谱相似度评价系统(2004A)”进行数据分析,设定批号20131101的样品为参照图谱,将其他样品的色谱峰与参照图谱进行自动匹配,生成五味沙棘颗粒特征图谱,见图 2。计算10批样品与特征图谱的相似度在0.92~0.99之间。
|
图 2 10批五味沙棘颗粒特征图谱 Figure 2 The characteristic chromatograms of Wuwei Shaji granules |
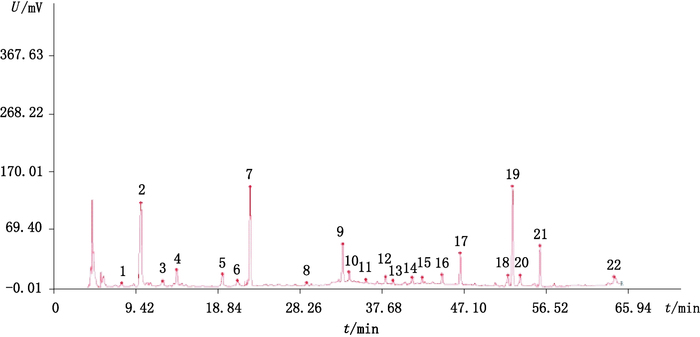
根据10批五味沙棘颗粒的特征图谱检测结果,共标定了4个特征峰。经过与对照品比对,可知7号峰为栀子苷,9号峰为甘草苷,19号峰为异鼠李素,21号峰为甘草酸,见图 3。
|
图 3 五味沙棘颗粒的共有模式图谱 Figure 3 Common pattern of the characteristic chromatogram of Wuwei Shaji granules |
取“2.2.1”项下系列浓度混合对照品溶液,按“2.1”项色谱条件进样测定,以峰面积Y为纵坐标,质量浓度X(mg·mL-1)为横坐标,绘制标准曲线,计算回归方程,结果见表 1。
|
|
表 1 4种成分的线性回归方程、相关系数(r)及线性范围 Table 1 The regression equations, correlation coefficients (r) and linear ranges of 4 components |
精密量取混合对照品溶液20 μL,按上述色谱条件连续进样测定6次,分别记录4个指标成分的峰面积。以栀子苷、甘草苷、异鼠李素、甘草酸的峰面积计算,RSD分别为0.88%、0.55%、1.0%、0.86%。
2.4.3 稳定性试验精密量取同一供试品溶液20 μL,按上述色谱条件分别于0、2、4、8、12、24 h注入液相色谱仪进行测定,记录峰面积,结果栀子苷、甘草苷、异鼠李素、甘草酸峰面积的RSD分别为0.65%、0.87%、0.79%、0.73%,表明供试品溶液在24 h内稳定。
2.4.4 重复性试验取同一批号五味沙棘颗粒6份,按“2.2.2”项下方法制备供试品溶液,分别取20 μL注入液相色谱仪进行测定,记录峰面积,计算含量及RSD。结果栀子苷平均含量为0.61 mg·g-1,RSD为0.88%;甘草苷平均含量为0.19 mg·g-1,RSD为1.6%;异鼠李素平均含量为0.09 mg·g-1,RSD为1.1%;甘草酸平均含量为0.39 mg·g-1,RSD为0.83%。表明该方法的重复性良好。
2.4.5 加样回收试验取已知含量的五味沙棘颗粒(批号20151001)共6份,每份约2.0 g,精密称定,分别置具塞锥形瓶中,分别精密加入各对照品溶液适量,按“2.2.2”项方法制成供试溶液,分别取20 μL按上述色谱条件进行测定,记录色谱图,计算回收率,结果表明方法的准确度良好,见表 2。
|
|
表 2 4种成分的加样回收率(n=6) Table 2 The recoveries of the 4 components |
取3批五味沙棘颗粒样品,按“2.2.2”项下方法制备供试品溶液,按“2.1”项色谱条件进样测定,采用外标法计算,测定结果见表 3。
|
|
表 3 3批样品中4种成分含量测定结果(mg·g-1,n=3) Table 3 Contents of four constituents in three batches of samples |
本实验曾分别采用甲醇、80%甲醇水制备供试品溶液,分别以甲醇-水、甲醇-水-磷酸系统、乙腈-水及乙腈-水-磷酸系统为流动相,对五味沙棘颗粒中待测成分的分离情况进行了考察,结果以乙腈-水-磷酸系统分离效果较好[11-12]。对五味沙棘颗粒中的待测成分栀子苷、甘草酸铵、甘草苷、异鼠李素进行了全波长扫描,结果各成分在240 nm处均有较大吸收,且该波长处待测成分无干扰,因此选用240 nm作为检测波长。为了建立一种准确、可行且具备普遍适用性的五味沙棘颗粒中多种指标性成分的含量测定方法,本文进行了较为全面的实验研究,并进行了方法学验证,结果表明该法准确可靠,可作为该制剂的质控方法。
| [1] |
LI Y, WU T, ZHU J, et al. Combinative method using HPLC fingerprint and quantitative analyses for quality consistency evaluation of a herbal medicinal preparation produced by different manufacturers[J]. J Pharm Biomed Anal, 2010, 52(4): 597. DOI:10.1016/j.jpba.2010.01.018 |
| [2] |
易伦朝, 吴海, 梁逸曾. 色谱指纹图谱与中药质量控制[J]. 色谱, 2008, 26(2): 166. YI LC, WU H, LIANG YZ. Chromatogrphic fingerprint and quality control of traditional Chinese medicines[J]. Chin J Chromatogr, 2008, 26(2): 166. |
| [3] |
胡晓茹, 杨思广, 戴忠, 等. 葛根芩连片特征图谱及含量测定方法研究[J]. 药物分析杂志, 2014, 34(9): 1590. HU XR, YANG SG, DAI Z, et al. Study on characteristic fingerpringts and quantitative analysis of Gegen Qinlian tablets[J]. Chin J Pharm Anal, 2014, 34(9): 1590. |
| [4] |
耿怡玮. 基于HPLC特征图谱的清肝化瘀方质量标准研究及医院临床中药学服务模式探讨[D]. 北京: 北京中医药大学, 2015 GENG YW. Based on HPLC Feature Maps of Liver Blood Quality Standard Research and Clinical TCM Service Mode[D]. Beijing:Beijing University of Chinese Medicine, 2015 http://cdmd.cnki.com.cn/Article/CDMD-10026-1015386230.htm |
| [5] |
苏日娜. 五味沙棘散研究进展[J]. 北方药学, 2012, 9(5): 103. SU RN. Advances in studies on Wuwei Shaji powder[J]. J North Pharm, 2012, 9(5): 103. |
| [6] |
杨阿敏. 蒙药使用指南[M]. 呼和浩特: 内蒙古教育出版社, 2001, 33. YANG AM. Mongolian medication guide[M]. Huhehaote: Inner Mongolia Education Publishing House, 2001, 33. |
| [7] |
耿婕, 薛培凤, 赵子龙, 等. 高效液相色谱法测定五味沙棘颗粒中异鼠李素含量[J]. 中国药业, 2013, 22(21): 27. GENG J, XUE PF, ZHAO ZL, et al. Determination of isorhamnetin in Wuwei Shaji granules by HPLC[J]. China Pharm, 2013, 22(21): 27. |
| [8] |
樊精辉, 曾月宁, 丛丽华, 等. 五味沙棘颗粒含量测定的方法学研究[J]. 大家健康, 2013, 7(9): 22. FAN QH, ZENG YN, CONG LH, et al. Study on methodology for determination of Wuwei Shaji granules[J]. For All Health, 2013, 7(9): 22. |
| [9] |
韩峰超, 沈君, 赵霓, 等. 测定五味沙棘颗粒剂中异鼠李素的含量[J]. 中成药, 2000, 22(9): 651. HAN FC, SHEN J, ZHAO N, et al. Determination of isorhamnetine in Wuwei Shaji granules by RP-HPLC[J]. Chin Tradit Pat Med, 2000, 22(9): 651. |
| [10] |
薛培凤, 朝可图, 耿婕, 等. HPLC法测定五味沙棘颗粒中栀子苷的含量[C]//中华中医药学会第七次中药分析学术交流论文集. 广州: 中华中医药学会, 2014: 246 XUE PF, CHAO KT, GENG J, et al. Determination of geniposide in Wuwei Shaji granules by high performance liquid chromatography[C]//The Seventh of China Association of Chinese Medicine Academic Exchanges on Traditional Chinese Medicine Analysis. Guangzhou:China Association of Chinese Medicine, 2014:246 |
| [11] |
中国药典2015年版. 一部[S]. 2015: 616 ChP 2015. Vol Ⅰ[S]. 2015:616 |
| [12] |
刘建群, 韩晋, 袁海龙, 等. 吸附小柱-高效液相色谱法测定五味沙棘散中栀子苷的含量[J]. 中草药, 2001, 32(3): 218. LIU JQ, HAN J, YUAN HL, et al. Determination of gardenoside in Wuwei Shaji powder by mini adsorption column-HPLC[J]. Chin Tradit Herb Drugs, 2001, 32(3): 218. |
 2017, Vol. 37
2017, Vol. 37 
