麦味地黄胶囊由麦冬、醋五味子、熟地黄、酒萸肉、牡丹皮、山药、茯苓、泽泻八味药组成,具有滋肾养肺的功效,用于肺肾阴亏,潮热盗汗,咽干咳血,眩晕耳鸣,腰膝酸软,消渴。现代药学研究表明,熟地黄含有环烯醚萜及其苷类、糖类、氨基酸类等成分[1]。其中5-羟甲基糠醛具有抗心肌缺血、抗氧化、Ca2+拮抗、改善血液流变学、保护肝组织、保护血管内皮细胞等作用,是补益肝肾作用的物质基础之一[2-3]。山茱萸含有环烯醚萜苷类、五环三萜酸及其酯类、鞣质类、多糖类等成分,其中马钱苷有抗休克、保护心肌细胞、保护血管内皮细胞、调节免疫反应等作用,莫诺苷有保护心肌细胞、保护血管内皮细胞、保护神经细胞、促进缺血性脑损伤后血管新生等作用[4-10]。牡丹皮含有酚及酚苷类、单萜及其苷类、三萜、甾醇及其苷类等成分,其中丹皮酚有抗炎、抗菌,抗血栓形成和抗动脉粥样硬化,抗心律失常,降压,镇痛、降温、解热,调节免疫功能等作用[11]。五味子含有木脂素类、多糖类、挥发油类等成分,其中五味子醇甲有保护肝细胞,保护神经细胞,改善神经系统功能,防治老年性痴呆,逆转肿瘤的耐药性等作用[12-17]。因此,控制麦味地黄胶囊中5-羟甲基糠醛、莫诺苷、马钱苷、丹皮酚、五味子醇甲的含量,对保证产品质量具有重要意义。本研究建立了同时测定麦味地黄胶囊中5种有效成分的含量测定方法,为其质量控制提供参考。
1 仪器与试药Agilent 1260高效液相色谱仪、Agilent 1260 DAD检测器(安捷伦仪器公司);Precisa XR 205SM-DR分析天平,KQ-250型超声波清洗器(昆山市超声仪器有限公司)。Agela Venusil MP C18(2)色谱柱(4.6 mm×250 mm,5 μm;艾杰尔科技公司)。
莫诺苷对照品(批号140301)购自成都普菲德生物技术有限公司;马钱苷对照品(批号111640-201005)、五味子醇甲对照品(批号110857-200507)、5-羟甲基糠醛对照品(批号111626-201509)、丹皮酚对照品(批号110708-201407)均购自中国食品药品检定研究院;麦味地黄胶囊(A、B 2家生产企业提供,共10批);甲醇、乙腈为色谱纯(Merck公司),水为超纯水,其他试剂均为分析纯。
2 方法与结果 2.1 色谱条件与系统适用性试验[18-19]色谱柱为Venusil MP C18(2)(4.6 mm×250 mm,5 μm);以乙腈为流动相A,0.2%磷酸溶液为流动相B,按表 1中的配比进行梯度洗脱;0~30 min 5-羟甲基糠醛检测波长为284 nm,30~70 min莫诺苷和马钱苷检测波长为240 nm,70~80 min丹皮酚检测波长为274 nm,80~90 min五味子醇甲检测波长为216 nm;流量1.0 mL·min-1;柱温40 ℃。理论板数按莫诺苷、马钱苷峰计算均应不低于4 000。
|
|
表 1 流动相梯度洗脱程序 Table 1 Gradient elution program of the mobile phase |
取5-羟甲基糠醛对照品、莫诺苷对照品、马钱苷对照品、丹皮酚对照品和五味子醇甲对照品适量,精密称定,加70%甲醇制成每1 mL中含5-羟甲基糠醛75.18 μg,莫诺苷21.15 μg,马钱苷20.72 μg,丹皮酚49.75 μg,五味子醇甲8.14 μg的混合溶液,作为对照品溶液。
2.2.2 供试品溶液取装量差异项下本品内容物,研细,取约1 g,精密称定,置具塞锥形瓶中,精密加入70%甲醇25 mL,密塞,称量,加热回流1 h,放冷,再称量,用70%甲醇补足减失的量,摇匀,滤过,取续滤液,即得。
2.2.3 阴性对照溶液按照处方比例和工艺制备缺熟地黄、酒萸肉、牡丹皮、醋五味子的阴性样品,同供试品溶液制备方法制成阴性对照溶液。
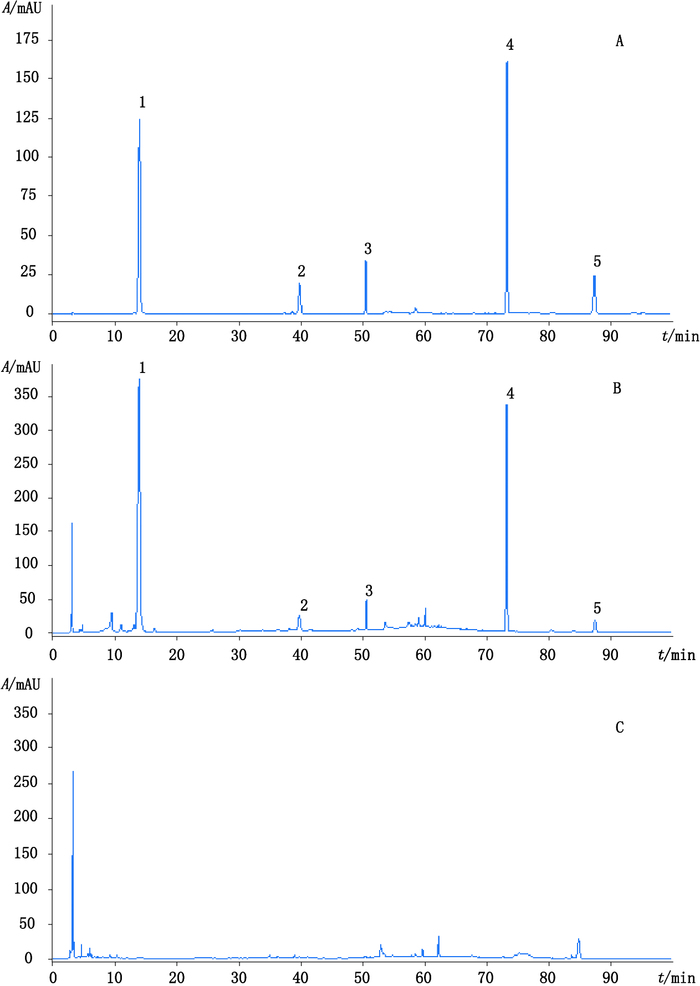
2.3 专属性试验取混合对照品溶液、供试品溶液及阴性对照溶液,依法测定。结果供试品色谱中呈现与对照品色谱峰保留时间相应的色谱峰,阴性对照无干扰。见图 1。
|
1. 5-羟甲基糠醛(5-hydroxymethyl-2 furaldehyde)2.莫诺苷(morroniside)3.马钱苷(loganin)4.丹皮酚(paeonol)5.五味子醇甲(schisandrin) 图 1 混合对照品(A)、供试品(B)、阴性样品(C)HPLC色谱图 Figure 1 HPLC chromatograms of mixed reference substances(A), sample(B)and negative sample(C) |
精密吸取混合对照品溶液1、2、6、10、15、20、30 μL,注入液相色谱仪,依法测定。以色谱峰面积(Y)对进样量(X)进行线性回归,得5-羟甲基糠醛、莫诺苷、马钱苷、丹皮酚、五味子醇甲的线性回归方程。见表 2。
|
|
表 2 线性回归方程 Table 2 Linear regression equation |
取混合对照品溶液10 μL,重复进样6次,测定5-羟甲基糠醛、莫诺苷、马钱苷、丹皮酚、五味子醇甲的峰面积,结果5-羟甲基糠醛、莫诺苷、马钱苷、丹皮酚、五味子醇甲峰面积的RSD分别为0.05%、0.1%、0.7%、0.2%、0.4%,表明仪器进样精密度良好。
2.6 稳定性试验取同一供试品溶液(批号130501),分别在制备后第0、2、4、6、8、10、12 h依法测定。结果5-羟甲基糠醛、莫诺苷、马钱苷、丹皮酚、五味子醇甲峰面积的RSD分别为0.2%、0.3%、1.8%、0.1%、0.4%,表明供试品溶液在12 h内稳定。
2.7 重复性试验取同一批供试品(批号130501)6份,按“2.6.2”项下方法制备供试品溶液。按上述色谱条件依法测定,按外标法计算供试品中5-羟甲基糠醛、莫诺苷、马钱苷、丹皮酚、五味子醇甲的含量。结果5-羟甲基糠醛、莫诺苷、马钱苷、丹皮酚、五味子醇甲的平均含量分别为3.366 7、0.776 8、0.742 6、2.052 8、0.143 7 mg·g-1,其RSD分别为1.1%、2.3%、1.3%、1.2%、1.7%。
2.8 加样回收率试验取已知含量的供试品(批号130501,5-羟甲基糠醛含量3.366 7 mg·g-1,莫诺苷含量0.776 8 mg·g-1,马钱苷含量0.742 6 mg·g-1,丹皮酚含量2.052 8 mg·g-1,五味子醇甲含量0.143 7 mg·g-1)6份,每份约0.5 g,精密称定,精密加入混合对照品溶液(5-羟甲基糠醛质量浓度65.47 μg·mL-1,莫诺苷质量浓度16.92 μg·mL-1,马钱苷质量浓度12.43 μg·mL-1,丹皮酚质量浓度39 μg·mL-1,五味子醇甲质量浓度3.26 μg·mL-1)25 mL,按“2.2.2”项下方法制备供试品溶液。依法测定,结果5-羟甲基糠醛、莫诺苷、马钱苷、丹皮酚、五味子醇甲的平均加样回收率分别为96.8%(RSD=0.65%)、96.3%(RSD=0.61%)、97.7%(RSD=0.32%)、97.7%(RSD=1.4%)、100.6%(RSD=1.9%)。
2.9 样品测定按上述色谱条件和样品制备方法,测定10批样品中5-羟甲基糠醛、莫诺苷、马钱苷、丹皮酚、五味子醇甲的含量,结果见表 3。
|
|
表 3 样品测定结果(mg·g-1,n=2) Table 3 Determination results of samples |
试验分别用50%甲醇、70%甲醇、甲醇为提取溶剂制备供试品溶液,测定供试品中5-羟甲基糠醛、莫诺苷、马钱苷、丹皮酚、五味子醇甲的含量,结果使用70%甲醇提取含量最高,故选择70%甲醇提取。
3.2 提取方式的选择试验以70%甲醇为溶剂,分别考察超声提取(功率250 W,频率50 kHz)和加热回流提取30、60、90 min的提取效果。结果加热回流提取60 min,供试品中5-羟甲基糠醛、莫诺苷、马钱苷、丹皮酚、五味子醇甲的含量最高,故选择加热回流提取60 min。
3.3 检测波长的选择5-羟甲基糠醛、莫诺苷、马钱苷、丹皮酚、五味子醇甲在200~400 nm内最大吸收波长分别为284、240、236、274、216 nm,莫诺苷和马钱苷的最大吸收波长接近,故选择240 nm测定莫诺苷和马钱苷,284 nm测定5-羟甲基糠醛,274 nm测定丹皮酚,216 nm测定五味子醇甲。
4 小结麦味地黄胶囊为国家食品药品监督管理局标准YBZ08032009、YBZ00072009收载品种。原标准仅有显微鉴别和薄层鉴别项,无含量测定项,不能全面控制产品质量。现代药理学研究表明,麦味地黄胶囊发挥药效的物质基础是方中多味药材中含有的多种成分,测定多种有效成分是控制复方质量的发展方向。10批样品的含量测定结果表明,同一厂家样品中的5-羟甲基糠醛、莫诺苷、马钱苷、丹皮酚和五味子醇甲含量接近,不同厂家样品中的含量差异较大,反映了不同厂家在原料药材控制和生产工艺上的差异,表明在麦味地黄胶囊质量标准中增加5-羟甲基糠醛、莫诺苷、马钱苷、丹皮酚和五味子醇甲等多有效成分的含量测定项目,有利于控制产品质量的稳定性,保证产品的有效性。
| [1] |
李更生, 于震, 王慧森. 地黄化学成分与药理研究进展[J]. 国外医学中医中药分册, 2004, 26(2): 74. LI GS, YU Z, WANG HS. Research progress in chemical constituents and pharmacology of Rehmannia glutinosa[J]. Foreign Med Sci:Tradit Chin Med, 2004, 26(2): 74. |
| [2] |
傅紫琴, 王明艳, 蔡宝昌. 5-羟甲基糠醛(5-HMF)在中药中的研究现状探讨[J]. 中华中医药学刊, 2008, 26(3): 508. FU ZQ, WANG MY, CAI BC. Discussion of 5-hydroxymethylfurfural (5-HMF)in Chinese native medicine research present situation[J]. Chin Arch Tradit Chin Med, 2008, 26(3): 508. |
| [3] |
丁霞, 王明艳, 余宗亮, 等. 山茱萸中5-羟甲基糠醛的分离鉴定及生物活性研究[J]. 中国中药杂志, 2008, 33(4): 392. DING X, WANG MY, YU ZL, et al. Studies on separation, appraisal and the biological activity of 5-HMF in Cornus officinalis[J]. China J Chin Mater Med, 2008, 33(4): 392. |
| [4] |
张程荣, 曹岗, 张云, 等. 山茱萸的化学、药理与炮制研究进展[J]. 中华中医药学刊, 2011, 29(9): 2002. ZHANG CR, CAO G, ZHANG Y, et al. Research progress on chemical constituents, pharmacological activities and processing history of Fructus Corni[J]. Chin Arch Tradit Chin Med, 2011, 29(9): 2002. |
| [5] |
王天山, 潘扬, 殷飞, 等. 马钱素与辛弗林对家兔重症失血性休克模型的作用[J]. 南京中医药大学学报, 1999, 15(6): 345. WANG TS, PAN Y, YIN F, et al. Effect of loganin and synephrine on rabbit model with Severe Hemorrhagic Shock[J]. J Nangjing Univ Tradit Chin Med, 1999, 15(6): 345. |
| [6] |
赵武述, 张玉琴, 赵世萍, 等. 山茱萸成分的免疫活性研究[J]. 中草药, 1990, 21(3): 17. ZHAO WS, ZHANG YQ, ZHAO SP, et al. Study on immunological activity of chemical constituents in Fructus corni[J]. China Tradit Herb Drugs, 1990, 21(3): 17. |
| [7] |
魏仁平, 孙芳玲, 刘婷婷, 等. 莫诺苷对脑缺血再灌注大鼠皮层肝细胞生长因子及血管性血友病因子表达的影响[J]. 中国比较医学杂志, 2016, 26(3): 24. WEI RP, SUN FL, LIU TT, et al. Effects of morroniside on the expression of the HGF and vWF in peri-infarct cortex after cerebral ischemia-reperfusion in rats[J]. Chin J Comp Med, 2016, 26(3): 24. |
| [8] |
赵文望, 皮文霞, 蔡宝昌, 等. 马钱苷、莫诺苷对高糖致心肌细胞损伤的保护机制研究[J]. 中成药, 2016, 38(1): 160. ZHAO WW, PI WX, CAI BC, et al. The study of the protection mechanism of loganin and morronside on myocardial cell injury induced by hyperglycemia[J]. Chin Tradit Pat Med, 2016, 38(1): 160. |
| [9] |
艾厚喜, 王文, 孙芳玲, 等. 莫诺苷抑制H2O2诱导的神经细胞凋亡[J]. 中国中药杂志, 2008, 33(18): 2109. AI HX, WANG W, SUN FL, et al. Morroniside inhibits H2O2 induced apoptosis in cultured nerve cells[J]. China J Chin Mater Med, 2008, 33(18): 2109. DOI:10.3321/j.issn:1001-5302.2008.18.025 |
| [10] |
刘凯, 许惠琴, 吴佳蕾, 等. 马钱苷、莫诺苷对AGEs损伤HUVEC的增殖的影响[J]. 中药药理与临床, 2014, 30(3): 53. LIU K, XU HQ, WU JL, et al. The study of loganin and morronside from effective ingredients of Cornus officinalis protecting HUVEC damaged by AGEs[J]. Pharmacol Clin Chin Mater Clin Med, 2014, 30(3): 53. |
| [11] |
王祝举, 唐力英, 赫炎. 牡丹皮的化学成分和药理作用[J]. 国外医药·植物药分册, 2006, 21(4): 155. WANG ZJ, TANG LY, HE Y. The chemical constituents and pharmacological effects of Cortex Moutan[J]. World Notes Plant Med, 2006, 21(4): 155. |
| [12] |
王楠, 全吉淑, 吕士杰. 五味子有效成分及药理作用研究进展[J]. 吉林医药学院学报, 2016, 37(3): 213. WANG N, QUAN JS, LÜ SJ. The research progress of chemical constituents in Schisandra Chinensis and pharmacological actions[J]. J Jilin Med Coll, 2016, 37(3): 213. |
| [13] |
王莹, 刘莹, 李全, 等. 五味子醇甲改善果蝇攀爬能力的量效与时效关系研究[J]. 中医药学报, 2014, 42(4): 45. WANG Y, LIU Y, LI Q, et al. The time and dose effect relationship of schisandrin improving the climbing ability of drosophila melanogaster[J]. Acta Chin Med Pharm, 2014, 42(4): 45. |
| [14] |
周妍妍, 刘艳丽, 董春雪, 等. 五味子醇甲对APP/PS1双转基因痴呆模型小鼠脑组织突触素、α-突触核蛋白表达的影响[J]. 中国药理学通报, 2013, 29(8): 1076. ZHOU YY, LIU YL, DONG CX, et al. Effect of schisandrin on expression of both SYP and α-syn in brain tissue of the APP/PS1 double transgenic dementia mice[J]. Chin Pharmacol Bull, 2013, 29(8): 1076. |
| [15] |
肖飞, 翁文, 罗焕敏. 五味子醇甲对β-淀粉样蛋白损伤PC12细胞的预保护及治疗作用[J]. 中药材, 2010, 33(3): 397. XIAO F, WENG W, LUO HM. Protective and therapeutic effects of schisandrol A on amyloid β-protein damaged PC12 cells[J]. J Chin Med Mater, 2010, 33(3): 397. |
| [16] |
李玲, 路太英, 樊青霞. 五味子醇甲逆转MRP1多药耐药机制的研究[J]. 医药论坛杂志, 2009, 30(18): 102. LI L, LU TY, FANG QX. The mechanism of schizandrin reverse MRP1 mediated multidrug resistance[J]. J Med Forum, 2009, 30(18): 102. |
| [17] |
张明华, 陈虹, 李灵芝, 等. 五味子甲素和五味子醇甲对四氯化碳所致肝脏损伤的保护作用[J]. 武警医学, 2002, 13(7): 395. ZHANG MH, CHEN H, LI LZ, et al. Deoxyschizandrin and schizandrin protect liver against carbon tetrachloride induced damage[J]. Med J Chin PAPF, 2002, 13(7): 395. |
| [18] |
李桂本, 王海波, 李振国. HPLC波长切换技术同时测定知柏地黄丸(浓缩丸)中莫诺苷、芒果苷、马钱苷和丹皮酚的含量[J]. 药物分析杂志, 2015, 35(1): 125. LI GB, WANG HB, LI ZG. Simultaneous determination of the content of morroniside, chimonin, loganin and paeonol in Zhibai Dihuang pills(concentrated pills)by HPLC wavelength switching technology[J]. Chin J Pharm Anal, 2015, 35(1): 125. |
| [19] |
李桂本, 王海波, 李振国. HPLC波长切换同时测定知柏地黄丸中莫诺苷、马钱苷和丹皮酚的含量[J]. 中国实验方剂学杂志, 2015, 21(16): 48. LI GB, WANG HB, LI ZG. Simultaneous determination of morroniside, loganin and paeonol in Zhibai Dihuang pills by HPLC wavelength switching technology[J]. Chin J Exp Tradit Med Form, 2015, 21(16): 48. |
 2017, Vol. 37
2017, Vol. 37 